Способ получения алифатических карбоновых кислот
Иллюстрации
Показать всеИзобретение относится к области органического синтеза, а именно к способу получения алифатических карбоновых кислот С7 (н-С6Н13СООН, н-гептановая (энантовая) кислота), С9 (н-C8H17COOH, н-нонановая (пеларгоновая) кислота) и С11 (н-C10H21COOH, н-ундекановая (ундециловая) кислота) каталитическим окислением соответствующих альфа-алкенов. Способ получения алифатических карбоновых кислот осуществляют окислением соответствующего алкена раствором пероксида водорода в двухфазной системе в присутствии катализатора. Процесс проводят в присутствии металлокомплексного катализатора с общей формулой Q3{PO4[W(O)(O2)2]4}, где: Q - четвертичный аммониевый катион - [(R1)3NR2]+, где: R1, R2 содержат от 1 до 16 атомов углерода, либо с формулой [C5H5N(n-C16H33)]3{PO4[W(O)(O2)2]4}. Технический результат - высокие выход и селективность целевой алифатической карбоновой кислоты. 5 з.п. ф-лы, 12 пр., 1 табл.
Реферат
Изобретение относится к области органического синтеза, а именно к способу получения алифатических карбоновых кислот С7 (н-С6Н13СООН, н-гептановая (энантовая) кислота), С9 (н-C8H17COOH, н-нонановая (пеларгоновая) кислота) и С11 (н-С10Н21СООН, н-ундекановая (ундециловая) кислота) каталитическим окислением соответствующих альфа-алкенов раствором пероксида водорода.
В пищевой промышленности применяют сложные эфиры гептановой кислоты в качестве ароматизаторов и вкусовых добавок (метиловый, этиловый), а также для маркировки таких продуктов, как мясо (глицеролтригептаноат) и масла. В парфюмерной промышленности гептановая кислота используется для производства синтетических ароматизаторов. В химической и нефтехимической промышленности гептановую кислоту используют в качестве сомономера алкидных смол, производства смазочных материалов для летательных аппаратов и гидравлических жидкостей. В фармацевтической промышленности гептановую кислоту используют для производства гормональных препаратов (энантаты тестостерона, тренболона, дростанолона, метенолона).
Нонановую кислоту применяют в производстве лаков, пластиков, гидротропных солей, фармацевтических препаратов, синтетических ароматизаторов и вкусовых добавок, флотореагентов, смазочных материалов, пластификаторов, добавок к бензину. В агрохимической промышленности нонановую кислоту используют в производстве гербицидов (нонаноат аммония) и регуляторов цветения растений. В пищевой промышленности нонановую кислоту применяют в качестве пищевой добавки, а также в качестве компонента раствора для чистки овощей и фруктов. В фармацевтической промышленности нонановую кислоту для модификации антибиотиков (например, фениколов) с целью усиления их эффекта. Морфолид пеларгоновой кислоты является боевым отравляющим веществом и входит в состав перцовых спреев.
Ундекановую кислоту также применяют в парфюмерной (производство ароматических веществ), химической (производство эмульгаторов, ПАВ) и пищевой промышленности (пищевые добавки и маскирующие агенты).
В середине XX столетия алифатические карбоновые кислоты получали окислением непредельных жирных кислот, входящих в состав природных животных и растительных жиров. Нонановую и азелаиновую кислоты получали в смеси окислением олеиновой кислоты концентрированной (>80%) азотной кислотой в присутствии соединений ванадия при атмосферном давлении и повышенной температуре (до 100°C) [US 2,203,680, C07C 51/275, 1940; GB 524,163, C07C 51/275, 1940] (1):
После разделения карбоновых кислот выход нонановой кислоты достигал 20-57%.
С тех пор предложены десятки способов по улучшению процесса получения карбоновых кислот путем окислительного расщепления непредельных жирных. Основные направления модификации метода сводились к:
- повышению эффективности метода очистки и разделения образующихся карбоновых кислот [US 2,560,156, C07C 51/493, 1951; US 2,862,942, C07C 51/27, 1958];
- снижению концентрации используемой азотной кислоты за счет повышения температуры и давления [US 2,773,095, 1956];
- поиску новых катализаторов, позволяющих проводить реакцию в более мягких условиях [US 2,847,431, C07C 51/25, 1958];
- проведению окисления сильными минеральными кислотами в комбинации с другими окислителями, например, пероксидом водорода [US 5,864,049, B01J 27/13, 1999; US 2012/0302778, C07C 51/16, 2012].
Параллельно с целью создания эффективного процесса получения карбоновых кислот из непредельных кислот были разработаны способы окисления кислородом с использованием: различных катализаторов - соединений Co, Mn, Cu, Cr [GB 813,842,
С07С 51/25; С07С 51/27, 1959], Се [US 3,407,221, С07С 51/25, 1968], а также использованию в качестве окислителя озона или озон-содержащих смесей [GB 809,451, С07С 51/215; C11С 3/00, 1959; GB 841,653, С07С 51/34, 1960].
Однако использование в качестве исходного сырья непредельных карбоновых кислот растительного происхождения в большей степени доступно для стран с теплым климатом. Поэтому в качестве альтернативного исходного сырья с 50-х годов рассматриваются продукты нефтехимического производства - углеводороды.
В результате парциального окисления углеводородного сырья смешанного состава кислородом воздуха образуется смесь кислородсодержащих органических соединений [US 2288769, С10М 1/08, 1942; US 2810739, С07С 1/04, 1954]. Выделение карбоновых кислот из смеси продуктов достаточно трудоемко, в связи с чем в промышленности этот процесс на сегодняшний день не используется.
С 1970-х годов широко исследуемым методом переработки алкенов в карбоновые кислоты является карбоксилирование - присоединение молекул монооксида углерода и воды по двойной связи алкенов. Развитие метода заключается преимущественно в варьировании методов активирования реакции - предлагают применение HF [US 3,005,846, С07С 51/14, 1961], соли Pb [GB 1,066,772, B01J 31/16, 1967], воздействие УФ-излучения [GB 1,267,273, С07С 51/00, 1972]. Наилучшие результаты в реакции карбонилирования алкенов с целью получения карбоновых кислот показали фосфиновые комлексы Rh, Pd [US 4,257,973, С07С 51/14, 1981; US 4,273,936, C07C 51/145, 1981]. Однако реакцию карбоксилирования необходимо проводить в достаточно жестких условиях - при давлении до 8 МПа и температуре до 200°C.
Окисление органических соединений при атмосферном давлении и температуре до 100°C возможно с использованием экологически благоприятного окислителя - раствора пероксида водорода. Окисление алкенов пероксидом водорода в присутствии металлокомплексных катализаторов было предложено Милласом (Nicolas A. Milas) [US 2,437,648, С07С 45/27, С07С 45/28, 1948]. В ходе реакции образуются гликоли, которые в дальнейшем могут быть окислены до карбоновых кислот. Прямое окисление алкенов до карбоновых кислот возможно, но требует большого избытка пероксида водорода. Получение карбоновых кислот окислением ненасыщенных соединений в одном реакторе провел Сиби [US 5,939,572, С07С2 33/05, 1999]. Реакция протекает в присутствии оксидов металлов (W, Mo, Nb, Yt и др.). Однако для окисления промежуточных гликолей до карбоновых кислот метод также требует введения в зону реакции дополнительного окислителя - молекулярного кислорода. Несмотря на то, что вышеописанные процессы могут быть отнесены к экологически безопасным, многостадийность делает их менее привлекательными для реализации в промышленности. Прямое окисление алкенов в карбоновые кислоты раствором пероксида водорода возможно с применением каталитических систем на основе пероксополиоксометаллатов.
Наиболее близким является способ получения моно- или дикарбоновых кислот (гептановой и нонановой кислот) окислительным расщеплением алкенов [US 4,532,079, С07С 51/285, 1985]. В качестве катализатора используют комплексное соединение с общей формулой Q3XW4O24-2n, где: Q - «ониевый» катион (R5R6R7R8)M+, Μ - из ряда Ν, Р, As, Sb; R5, R6, R7, R8 содержат от 20 до 70 углеродных атомов и могут быть как одинакового, так и разного строения; X - атом Ρ или As; n - 0, 1, 2.
Реакцию окисления органических субстратов проводят в двухфазной системе: водная фаза, содержащая пероксид водорода до 70%, и органическая фаза, содержащая органический растворитель (ароматический или хлорсодержащий углеводород, например бензол или дихлорэтан) при температуре от 20 до 120°C и атмосферном давлении (для поддержания газообразных алкенов в жидком состоянии давление может быть увеличено вплоть до 100 атм). Реагенты берутся в стехиометрических количествах или с небольшим избытком пероксида водорода. Количества катализатора берутся из расчета 0,01-1 г-атом W на 1 моль субстрата (т.е. [Sub]/[Cat]=4-400). Выход гептановой кислоты при каталитическом окислении октена-1 составляет 65% за 6,5 ч при [H2O2]/[Sub]=5,5; ундекановой кислоты - 49% при окислении додецена-1 в тех же условиях.
Основными, существенными недостатками известного способа являются: проведение реакции окисления в присутствии органического растворителя, низкий выход целевых карбоновых кислот, длительное время проведения реакции, а также использование для приготовления катализатора экологически опасных As, Sb, WCl6, WOCl4, хлорсодержащих углеводородов.
Изобретение решает задачу увеличения эффективности процесса получения алифатических карбоновых кислот, таких как гептановая или нонановая, или ундекановая.
Задача решается способом получения алифатических карбоновых кислот, а именно гептановой, нонановой и ундекановой окислением соответствующего алкена раствором пероксида водорода в двухфазной системе в присутствии металлокомплексного катализатора с общей формулой Q3{PO4[W(O)(O2)2]4}, где: Q - четвертичный аммониевый катион - [(R1)3NR2]+, где: R1, R2 содержат от 1 до 16 атомов углерода, либо с формулой [C5H5N(n-C16H33)]3{PO4[W(O)(O2)2]4}.
Каталитический комплекс синтезируется по известной методике [РФ 2,335,341, B01J 31/18.2008].
В качестве алкена - субстрата используют октен-1 или децен-1, или додецен-1. Используют разбавленные растворы пероксида водорода с концентрацией 25-35%.
Процесс осуществляют в двухфазной системе «органическая фаза - водная фаза», где роль органической фазы выполняет субстрат (алкен) при температуре 60-95°C и общем давлении 1 атм при следующих соотношениях компонентов: [Sub]/[Cat]=100-500: [H2O2]/|Sub]=4-6.
Сущность изобретения иллюстрируется следующими примерами.
Получение карбоновых кислот осуществляют следующим способом.
Реакцию селективного каталитического окисления алкенов (1) проводят в термостатированной конической колбе с использованием магнитной мешалки (500-750 об./мин). Реактор снабжен обратным холодильником.
Последовательность приготовления реакционной смеси: в реактор помещают навеску катализатора, добавляют рассчитанный объем алкена, перемешивают, вводят раствор пероксида водорода в соответствии со стехиометрией реакции (2) и включают нагрев. Температуру поддерживают с помощью водяного термостата с точностью ±0,1°C.
Для определения конверсии исходного алкена и выхода целевого продукта полученную смесь продуктов анализировали с помощью метода газовой
хроматографии. По полученным значениям рассчитывали полную селективность процесса.
Пример 1.
К навеске катализатора [(n-C8H17)3NCH3]3{PO4[WO(O2)2]4} (1,2177 г, 0,5397 ммоль) добавляют октен-1 (16,94 мл, 107,94 ммоль) и 30%-ный раствор H2O2 (54,63 мл, 539,70 ммоль), что соответствует соотношению исходных компонентов: [Sub]/[Cat]=200, [Ox]/[Sub]=5. Подключают предварительно разогретый до 90°C термостат. Перемешивают смесь в течение 4 ч, после чего фазы разделяют.
Содержание гептановой кислоты в органической фазе, определенное с помощью метода ГХ, соответствует выходу 94,7%. Содержание октена-1 в органической фазе, определенное с помощью метода ГХ, соответствует конверсии 98,0%. Полная селективность реакции равна 96,6%.
Пример 2.
К навеске катализатора [(n-C8H17)3NCH3]3{PO4[WO(O2)2]4} (0,6232 г, 0,2762 ммоль) добавляют октен-1 (21,67 мл, 138,10 ммоль) и 30%-ный раствор H2O2 (69,89 мл, 690,50 ммоль), что соответствует соотношению исходных компонентов: [Sub]/[Cat]=500, [Ox]/[Sub]=6. Подключают предварительно разогретый до 95°C термостат. Перемешивают смесь в течение 3 ч, после чего фазы разделяют.
Содержание гептановой кислоты в органической фазе, определенное с помощью метода ГХ, соответствует выходу 88,0%. Содержание октена-1 в органической фазе, определенное с помощью метода ГХ, соответствует конверсии 95,2%. Полная селективность реакции равна 92,5%.
Пример 3.
К навеске катализатора [(n-C8H17)3NCH3]3{PO4[WO(O2)2]4} (1,2211 г, 0,5412 ммоль) добавляют октен-1 (16,99 мл, 108,24 ммоль) и 35%-ный раствор H2O2 (46,95 мл, 541,20 ммоль), что соответствует соотношению исходных компонентов: [Sub]/[Cat]=200, [Ox]/[Sub]=5. Подключают предварительно разогретый до 90°C термостат. Перемешивают смесь в течение 4 ч, после чего фазы разделяют.
Содержание гептановой кислоты в органической фазе, определенное с помощью метода ГХ, соответствует выходу 92,8%. Содержание октена-1 в
органической фазе, определенное с помощью метода ГХ, соответствует конверсии 96,4%. Полная селективность реакции равна 96,3%.
Пример 4.
К навеске катализатора [(n-C8H17)3NCH3]3{PO4[WO(O2)2]4} (1,1683 г, 0,5178 ммоль) добавляют октен-1 (16,25 мл, 103,56 ммоль) и 30%-ный раствор H2O2 (52,41 мл, 517,18 ммоль), что соответствует соотношению исходных компонентов: [Sub]/[Cat]=200, [Ox]/[Sub]=5. Подключают предварительно разогретый до 60°C термостат. Перемешивают смесь в течение 6 ч, после чего фазы разделяют.
Содержание гептановой кислоты в органической фазе, определенное с помощью метода ГХ, соответствует выходу 56,4%. Содержание октена-1 в органической фазе, определенное с помощью метода ГХ, соответствует конверсии 61,9%. Полная селективность реакции равна 91,1%.
Пример 5.
К навеске катализатора [C5H5H(n-C16H33)]3{PO4[WO(O2)2]4} (1,5047 г, 0,7291 ммоль), предварительно растворенной в небольшом количестве 1,2-дихлорэтана (5 мл), добавляют октен-1 (17,16 мл, 109,37 ммоль) и 30%-ный раствор H2O2 (44,28 мл, 437,46 ммоль), что соответствует соотношению исходных компонентов: [Sub]/[Cat]=150, [Ox]/[Sub]=4. Подключают предварительно разогретый до 90°C термостат. Перемешивают смесь в течение 3 ч, после чего фазы разделяют.
Содержание гептановой кислоты в органической фазе, определенное с помощью метода ГХ, соответствует выходу 90,3%. Содержание октена-1 в органической фазе, определенное с помощью метода ГХ, соответствует конверсии 94,1%. Полная селективность реакции равна 95,9%.
Пример 6.
К навеске катализатора [C5H5H(n-C16H33)]3{PO4[WO(O2)2]4} (1,3798 г, 0,6686 ммоль), предварительно растворенной в небольшом количестве 1,2-дихлорэтана (5 мл), добавляют октен-1 (15,74 мл, 100,29 ммоль) и 25%-ный раствор H2O2 (60,91 мл, 501,45 ммоль), что соответствует соотношению исходных компонентов: [Sub]/[Cat]=150, [Ox]/[Sub]=5. Подключают предварительно разогретый до 90°C термостат. Перемешивают смесь в течение 4 ч, после чего фазы разделяют.
Содержание гептановой кислоты в органической фазе, определенное с помощью метода ГХ, соответствует выходу 89,9%. Содержание октена-1 в органической фазе, определенное с помощью метода ГХ, соответствует конверсии 97,1%. Полная селективность реакции равна 92,6%.
Пример 7.
К навеске катализатора [n-Bu4N]3{PO4[WO(O2)2]4} (2,0993 г, 1,1181 ммоль), предварительно растворенной в небольшом количестве 1,2-дихлорэтана (5 мл), добавляют октен-1 (17,55 мл, 111,81 ммоль) и 30%-ный раствор H2O2 (67,90 мл, 670,86 ммоль), что соответствует соотношению исходных компонентов: [Sub]/[Cat]=100, [Ox]/[Sub]=6. Подключают предварительно разогретый до 80°C термостат. Перемешивают смесь в течение 6 ч, после чего фазы разделяют.
Содержание гептановой кислоты в органической фазе, определенное с помощью метода ГХ, соответствует выходу 17,8%. Содержание октена-1 в органической фазе, определенное с помощью метода ГХ, соответствует конверсии 68,9%. Полная селективность реакции равна 25,9%.
Пример 8.
К навеске катализатора [(n-C8H17)3NCH3]3{PO4[WO(O2)2]4} (1,1527 г, 0,5109 ммоль) добавляют децен-1 (19,34 мл, 102,18 ммоль) и 30%-ный раствор H2O2 (51,71 мл, 510,90 ммоль), что соответствует соотношению исходных компонентов: [Sub]/[Cat]=200, [Ox]/[Sub]=5. Подключают предварительно разогретый до 90°C термостат. Перемешивают смесь в течение 5 ч, после чего фазы разделяют.
Содержание нонановой кислоты в органической фазе, определенное с помощью метода ГХ, соответствует выходу 89,4%. Содержание децена-1 в органической фазе, определенное с помощью метода ГХ, соответствует конверсии 96,6%. Полная селективность реакции равна 92,6%.
Пример 9.
К навеске катализатора [C5H5N(n-C16H33)]3{PO4[WO(O2)2]4} (1,4440 г, 0,6997 ммоль), предварительно растворенной в небольшом количестве 1,2-дихлорэтана (5 мл), добавляют децен-1 (19,87 мл, 104,96 ммоль) и 30%-ный раствор H2O2 (53,12 мл, 524,78 ммоль) ), что соответствует соотношению исходных компонентов: [Sub]/[Cat]=150,
[Ox]/[Sub]=5. Подключают предварительно разогретый до 95°C термостат. Перемешивают смесь в течение 3 ч, после чего фазы разделяют.
Содержание нонановой кислоты в органической фазе, определенное с помощью метода ГХ, соответствует выходу 86,9%. Содержание децена-1 в органической фазе, определенное с помощью метода ГХ, соответствует конверсии 96,8%. Полная селективность реакции равна 89,8%.
Пример 10.
К навеске катализатора [n-Bu4N]3{PO4[WO(O2)2]4} (1,9938 г, 1,0619 ммоль), предварительно растворенной в небольшом количестве 1,2-дихлорэтана (5 мл), добавляют децен-1 (20,10 мл, 106,19 ммоль) и 30%-ный раствор H2O2 (64,49 мл, 637,14 ммоль), что соответствует соотношению исходных компонентов: [Sub]/[Cat]=100, [Ox]/|Sub]=6. Подключают предварительно разогретый до 80°C термостат. Перемешивают смесь в течение 6 ч, после чего фазы разделяют.
Содержание нонановой кислоты в органической фазе, определенное с помощью метода ГХ, соответствует выходу 16,4%. Содержание децена-1 в органической фазе, определенное с помощью метода ГХ, соответствует конверсии 66,9%. Полная селективность реакции равна 24,5%.
Пример 11.
К навеске катализатора [(n-C8H17)3NCH3]3{PO4[WO(O2)2]4} (1,1297 г, 0,5007 ммоль) добавляют додецен-1 (22,47 мл, 100,14 ммоль) и 30%-ный раствор H2O2 (50,68 мл, 500,70 ммоль), что соответствует соотношению исходных компонентов: [Sub)/[Cat]=200, [Ox]/[Sub]=5. Подключают предварительно разогретый до 90°C термостат. Перемешивают смесь в течение 4 ч, после чего фазы разделяют.
Содержание ундекановой кислоты в органической фазе, определенное с помощью метода ГХ, соответствует выходу 82,2%. Содержание додецена-1 в органической фазе, определенное с помощью метода ГХ, соответствует конверсии 96,2%. Полная селективность реакции равна 85,4%.
Пример 12.
К навеске катализатора [C5H5N(n-C16H33)]3{PO4[WO(O2)2]4} (1,4647 г, 0,7097 ммоль), предварительно растворенной в небольшом количестве 1,2-дихлорэтана (5 мл),
добавляют додецен-1 (23,89 мл, 106,46 ммоль) и 30%-ный раствор H2O2 (53,88 мл, 532,28 ммоль), что соответствует соотношению исходных компонентов: [Sub]/[Cat]=150, [Ox]/[Sub]=5. Подключают предварительно разогретый до 90°C термостат. Перемешивают смесь в течение 4 ч, после чего фазы разделяют.
Содержание ундекановой кислоты в органической фазе, определенное с помощью метода ГХ, соответствует выходу 80,8%. Содержание додецена-1 в органической фазе, определенное с помощью метода ГХ, соответствует конверсии 97,4%. Полная селективность реакции равна 83,0%.
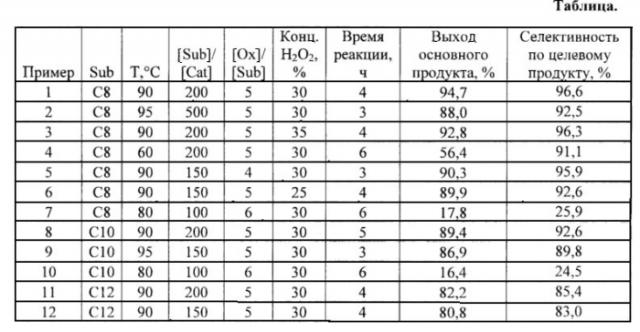
Примеры получения карбоновых кислот приведены в таблице.
Таким образом, как видно из приведенных примеров и таблицы, предлагаемый способ позволяет получать востребованные в промышленности карбоновые кислоты C7 и выше окислением доступных алкенов экологически безопасным и дешевым пероксидом водорода в мягких условиях с высокими выходами и селективностями.
1. Способ получения алифатических карбоновых кислот, а именно гептановой, нонановой и ундекановой, окислением соответствующего алкена раствором пероксида водорода в двухфазной системе в присутствии катализатора, отличающийся тем, что процесс проводят в присутствии металлокомплексного катализатора с общей формулой Q3{PO4[W(O)(O2)2]4}, где: Q - четвертичный аммониевый катион - [(R1)3NR2]+, где: R1, R2 содержат от 1 до 16 атомов углерода, либо с формулой [C5H5N(n-C16H33)]3{PO4[W(O)(O2)2]4}.
2. Способ по п. 1, отличающийся тем, что в качестве алкена - субстрата используют октен-1 или децен-1, или додецен-1.
3. Способ по п. 1, отличающийся тем, что процесс осуществляют при температуре 60-95°C и общем давлении 1 атм.
4. Способ по п. 1, отличающийся тем, что используют следующие соотношения компонентов: [Sub]/[Cat] = 100-500; [H2O2]/[Sub] = 4-6.
5. Способ по п. 1, отличающийся тем, что используют разбавленные растворы пероксида водорода с концентрацией 25-35%.
6. Способ по п. 1, отличающийся тем, что процесс осуществляют в присутствии 1,2-дихлорэтана.