N,n-бис(1-адамантил-1-этиламина) гидрохлорид и способ его получения
Иллюстрации
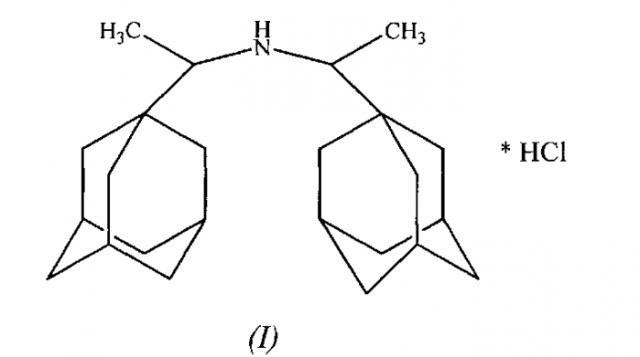
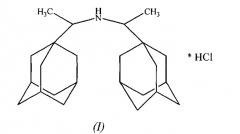
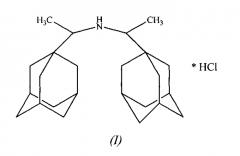
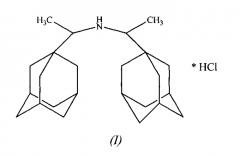
Показать всеИзобретение относится к новому соединению - гидрохлориду N,N-бис-(1-адамантил-1-этиламина) структурной формулы I и способу его получения. Соединение обладает биологической активностью и может быть использовано как компонент лекарственного средства или как маркер примеси лекарственного средства в качестве стандартного образца в аналитической химии фармацевтических препаратов.
Способ получения соединения формулы I включает а) получение 1-адамантил-1-этиламина из гидрохлорида 1-адамантил-1-этиламина, б) получение основания Шиффа структурной формулы III
обработкой соединения, полученного на стадии а) ацетиладамантаном в) обработкой основания Шиффа формулы III восстанавливающим агентом с получением бис(1-адамантил-1-этиламина) гидрохлорида формулы I. Соединение охарактеризовано температурой плавления, данными ИК, ЯМР и масс. спектра. 2 н.п. ф-лы, 8 ил., 1 табл., 3 пр.
Реферат
Заявленное изобретение относится к органической химии, а именно к способам получения N,N-бис(1-адамантил-1-этиламина) гидрохлорида общей формулы I:
Соединение формулы I может найти применение как компонент противовирусных средств, а также как маркер примеси в образце лекарственного средства.
Известен способ получения 1-аминоэтил-адамантана, формулы II, являющегося биологически активной основой субстанции противогриппозного препарата, широко применяемого в качестве лекарственного средства для борьбы с вирусами гриппа типа А [1, 2].
В результате анализа методики синтеза 1-аминоэтил-адамантана промышленным способом [3] было обнаружено, что в процессе синтеза 1- аминоэтил-адамантана возможно протекание побочной реакции с образованием основания Шиффа, а при дальнейшем воздействии восстанавливающих агентов образуется продукт структурной формулы I. Образование продукта структурной формулы I подтвердилось анализом ряда образцов субстанции 1-аминоэтил-адамантана гидрохлорида, полученных промышленным способом, с помощью методов хромато-масс-спектрометрии и ЯМР.
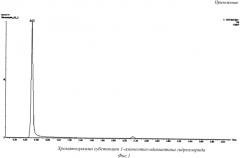
На хроматограмме субстанции 1-аминоэтил-адамантана гидрохлорида обнаружена примесь с Rt=2.35 (Фиг. 1), в масс-спектре примеси (Фиг. 2) присутствует ион с молекулярной массой 342,34 г/моль, который с погрешностью 0,03 г/моль может быть интерпретирован как квазимолекулярный ион с брутто-формулой C24H41N.
С целью обеспечения возможности количественного определения содержания соединения структурной формулы I в исследуемых образцах была разработана методика синтеза соединения структурной формулы I и проведен его встречный синтез.
Техническим результатом изобретения является способ получения нового соединения N,N-бис(1-адамантил-1-этиламина) гидрохлорида.
Краткое описание чертежей:
Фиг. 1. Хроматограмма субстанции 1-аминоэтил-адамантана гидрохлорида.
Фиг. 2. Масс-спектр примеси, обнаруженной в субстанции 1-аминоэтил адамантана гидрохлорида Rt=2,35.
Фиг. 3. Масс-спектр примеси, обнаруженной в субстанции 1-аминоэтил адамантана в режиме диссоциации активированной соударением (MS-MS по m/z 342+).
Фиг. 4. Спектр ЯМР 1Н бис(1-адамантил-1-этиламина) гидрохлорида в CDCl3.
Фиг. 5. Спектр ЯМР 13С бис(1-адамантил-1-этиламина) гидрохлорида в CDCl3.
Фиг. 6. Спектр ЯМР 1Н бис(1-адамантил-1-этиламина) гидрохлорида в D2O.
Фиг. 7. Спектр ИК бис(1-адамантил-1-этиламина) гидрохлорида.
Фиг. 8. Порядок нумерации атомов углерода в соединении формулы I для идентификации на спектрах ЯМР. Фиг. 8 носит только поясняющий характер для удобства чтения 1Н-ЯМР спектра.
Заявленное изобретение иллюстрируется следующими примерами:
Пример 1. Получение 1-адамантил-1-этиламина (промежуточная стадия)
10 г 1-адамантил-1-этиламина гидрохлорида растворяют в 40 мл воды, затем в полученный раствор вносят раствор 4,07 г едкого натра в 20 мл воды.
Реакционную массу выдерживают в течение 1 ч при температуре 65°С и интенсивном перемешивании на магнитной мешалке. Полученную эмульсию охлаждают в течение 0,5 ч до комнатной температуры. Затем экстрагируют двумя порциями по 30 мл хлористого метилена и отделяют органический слой на делительной воронке. Экстракт сушат над безводным сульфатом натрия в течение 0,5 ч. Для отделения осадка осушителя органический раствор отфильтровывают через фильтр Шотта под вакуумом. Хлористый метилен отгоняют на роторном испарителе. Получают 7,40 г 1-адамантил-1-этиламина, который без очистки вовлекают в следующую стадию.
Пример 2. Получение основания Шиффа структурной формулы III (промежуточная стадия)
Смесь 3,56 г (0,02 моль) ацетиладамантана и 3,58 г (0,02 моль) 1-адамантил-1-этиламина нагревают до кипения и выдерживают при этой температуре в течение 1 ч. Полученный сплав обрабатывают 60 мл метанола и полученный твердый осадок высушивают под вакуумом на фильтре Шотта. Получают 6,21 г основания Шиффа структурной формулы III, которое без очистки вовлекают в следующую стадию.
Пример 3. Получение бис(1-адамантил-1-этиламина) гидрохлорида (финальная стадия)
Полученное на предыдущей стадии основание Шиффа помещают в 100 мл метанола и при интенсивном перемешивании малыми порциями добавляют боргидрид натрия. Для инициации процесса на магнитной мешалке выставляют температуру рабочей поверхности 80°С. Реакционную массу выдерживают при этих условиях в течение 3 ч. Далее реакционную массу переносят в 500 мл воды. Выпавший осадок фильтруют на фильтре Шотта и сушат. Сухой остаток растворяют в 50 мл хлороформа и в течение 1 ч пропускают через хлороформный раствор сухой хлористый водород. Хлороформный раствор соединения формулы I упаривают досуха с получением продукта, который затем перекристаллизовывают из 5 мл хлористого метилена.
В результате получают 4,5 г N,N-бис(1-адамантил-1-этиламина) гидрохлорида. Итоговый выход соединения структурной формулы I, с учетом трех стадий, составляет 59%.
Полученный N,N-бис(1-адамантил-1-этиламина) гидрохлорид обладает следующими характеристиками:
1. температура плавления 276°C (с разложением);
2. спектр ЯМР 1Н в CDCl3 (1,413 (6Н, уш.с, С(24)Н3, С(25)Н3), 1,72 (12Н, уш.с, С(4)Н2, С(6)Н2, С(10)Н2, С(17)Н2, С(19)Н2, С(23)Н2), 1,79 (6Н, уш.с, С(2)Н, С(8)Н, С(9)Н, C(15)H, C(21)H, С(22)Н), 2,092 (6Н, уш.с, С(3)Н, С(5)Н, С(7)Н, С(16)Н, С(18)Н, С(20)Н), 2,708 (2Н, м., С(11)Н, С(13)Н), 7,31 (1Н, c., NH));
3. спектр ЯМР 13С в CDCl3 (11,946 (2С, С(24), С(25)), 28,159 (6С, С(3), С(5), С(7), C(16), С(18), С(20)), 35,936 (2С, С(1), С(14)), 36,373 (6С, С(4), С(6), С(10), С(17), C(19), С(23)), 38,496 (6С, С(2), С(8), С(9), С(15), С(21), С(22)), 67,421 (2С, С(11), С(13)));
4. спектр ЯМР 1Н в D2O;
5. масс-спектр с молекулярным ионом массой 342,34 г/моль;
6. ИК спектр.
| Таблица пиков к фиг. 7 | |
| Положение | Интенсивность |
| 459.17 | 88.640 |
| 600.89 | 85.889 |
| 668.68 | 87.591 |
| 752.06 | 91.711 |
| 812.87 | 90.802 |
| 850.77 | 90.485 |
| 933.64 | 88.254 |
| 970.06 | 89.506 |
| 983.47 | 89.361 |
| 1026.04 | 84.545 |
| 1049.73 | 81.943 |
| 1070.48 | 59.729 |
| 1094.34 | 84.531 |
| 1177.11 | 80.551 |
| 1198.76 | 86.298 |
| 1254.60 | 88.423 |
| 1317.58 | 81.187 |
| 1349.45 | 73.971 |
| 1375.14 | 70.414 |
| 1394.47 | 60.908 |
| 1419.19 | 67.208 |
| 1447.09 | 51.743 |
| 1598.25 | 58.742 |
| 2342.05 | 76.195 |
| 2360.66 | 70.788 |
| 2478.97 | 78.389 |
| 2681.59 | 64.633 |
| 2846.29 | 27.276 |
| 2901.37 | 17.156 |
| 3357.59 | 72.734 |
Ссылки на литературу
1. Ершов Ф.И., Чижов Н.П., Тазулахова Э.Б. Противовирусные средства. СПб.: Наука. 1993. 104 с.
2. Яхонтов Л.Н., Глушков Р.Г. Синтетические лекарственные средства. / М. Медицина. 1983. С. 54-57.
3. Макареев С.М., Калитеевский В.В., Шелудяков В.Д., Лебедев А.В., Лебедева А.Б., Устинова О.Л. Способ получения 1-(1′-адамантил)этиламина. Патент РФ №2118313 по Заявке №97106700 от 6 мая 1997 г.
1. Соединение структурной формулы I
2. Способ получения соединения структурной формулы I по п.1, включающий в себя 3 стадии, а именно: а) получение 1-адамантил-1-этиламина из гидрохлорида 1-адамантил-1-этиламина, б) обработкой соединения, полученного на стадии а) ацетиладамантаном с получением основания Шиффа структурной формулы III в) обработкой основания Шиффа формулы III восстанавливающим агентом с получением бис(1-адамантил-1-этиламина) гидрохлорида формулы I.