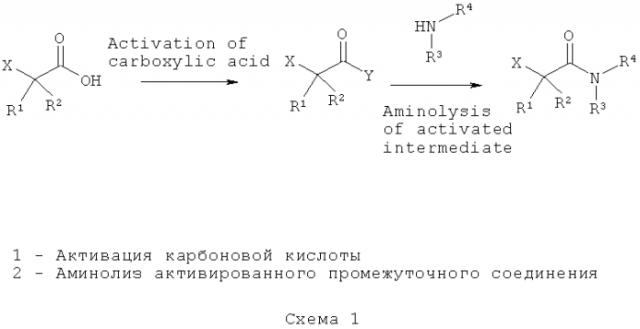
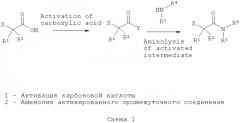
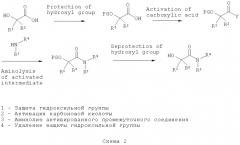
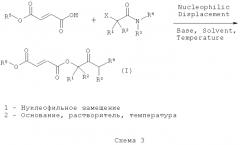
Пролекарства метилгидрофумарата, фармацевтические композиции с ними и способы применения
Иллюстрации
Показать всеИзобретение относится к соединению формулы (I), являющемуся пролекарством метилгидрофумарата (МHF). В формулы (I) радикалы и символы имеют значения, указанные в формуле изобретения. Изобретение также относится к фармацевтической композиции, включающей заявленные пролекарства метилгидрофумарата, к применению заявленных пролекарств метилгидрофумарата и фармацевтической композиции, включающих их, для лечения заболеваний, таких как псориаз, астма, рассеянный склероз, воспалительное заболевание кишечника и артрит, и к способам лечения указанных заболеваний. Технический результат - более высокая пероральная биодоступность и уровни в плазме МHF, диметилфумарата и/или других метаболитов. 10 н. и 37 з.п. ф-лы, 1 табл., 54 пр.
Реферат
Область техники, к которой относится изобретение
В данном описании раскрываются пролекарства метилгидрофумарата, фармацевтические композиции, включающие пролекарства метилгидрофумарата, и способы применения пролекарств метилгидрофумарата и фармацевтических композиций с ними для лечения таких заболеваний, как псориаз, астма, рассеянный склероз, воспалительное заболевание кишечника и артрит.
Уровень техники
Эфиры фумаровой кислоты (РАЕ), одобренные в Германии для лечения псориаза, проходят оценку в Соединенных Штатах для лечения псориаза и рассеянного склероза и предложены для применения при лечении широкого ряда иммунологических, аутоиммунных и воспалительных заболеваний и состояний.
FAE и другие производные фумаровой кислоты предложены для применения при лечении самых разных заболеваний и состояний, в том числе, иммунологических, аутоиммунных и воспалительных процессов, включая псориаз (Joshi and Strebel, WO 1999/49858; US 6277882; Mrowietz and Asadullah, Trends Mol. Med., 2005, 111(1), 43-48; и Yazdi and Mrowietz, Clinics Dermatology, 2008, 26, 522-526); астму и хронические обструктивные болезни легких (Joshi et al., WO 2005/023241 и US 2007/0027076); сердечную недостаточность, в том числе, левожелудочковую недостаточность, инфаркт миокарда и стенокардию (Joshi., WO 2005/023241; Joshi et al., US 2007/0027076); митохондриальные и нейродегенеративные заболевания, такие как болезнь Паркинсона, болезнь Альцгеймера, болезнь Гентингтона, пигментная ретинопатия и митохондриальная энцефаломиопатия (Joshi and Strebel, WO 2002/055063, US 2006/0205659. US 6509376, US 6858750 и US 7157423); трансплантацию (Joshi and Strebel, WO 2002/055063, US 2006/0205659, US 6359003, US 6509376 и US 7157423; и Lehmann et al.. Arch. Dermatol. Res., 2002, 294, 399-404); аутоиммунные заболевания (Joshi and Strebel, WO 2002/055063, US 6509376, US 7157423 и US 2006/0205659), включая рассеянный склероз (MS) (Joshi and Strebel, WO 1998/52549 и US 6436992; Went and Lieberburg, US 2008/008986; Schimrigk et al., Eur. J. Neurology, 2006, 13, 604-610; и Schilling et al., Clin. Experimental Immunology, 2006, 145, 101-107); ишемию и реперфузионное повреждение (Joshi et al., US 2007/0027076); AGE-индуцированное повреждение генома (Heidland, WO 2005/027899); воспалительные заболевания кишечника, такие как болезнь Крона и неспецифический язвенный колит; артрит и другие заболевания (Nilsson et al., WO 2006/037342, и Nilsson and Muller, WO 2007/042034).
Полагают, что механизм действия эфиров фумаровой кислоты опосредуется путями, связанными с иммунологической реакцией. Например, FAE вызывают смещение иммунной реакции от Th1 к Th2, благоприятно изменяя цитокиновый профиль; ингибируют вызванную цитокинами экспрессию факторов адгезии, таких как VCAM-1, ICAM-1 и Е-отбора, причем посредством этого уменьшается выхождение иммунных клеток; и снижают лимфоциты через апоптозные механизмы (Lehmann et al., J. Investigative Dermatology, 2007, 127, 835-845; Gesser et al., J. Investigative Dermatology, 2007, 127, 2129-2137; Vandermeeren et al., Biochem. Biophys. Res. Commun., 1997, 234, 19-23; и Treumer et al., J. Invest. Dermatol., 2003, 121, 1383-1388).
Последние исследования приводят к мысли, что FAE являются ингибиторами активации NF-κВ - фактора транскрипции, который регулирует индуцибельную экспрессию медиаторов провоспаления (D'Acquisto et al., Molecular Interventions, 2002, 2(1), 22-35). Соответственно, FAE предложены для применения при лечении NF-кВ-опосредуемых заболеваний (Joshi et al., WO 2002/055066; и Joshi and Strebel, WO 2002/055063, US 2006/0205659, US 7157423 и US 6509376). Также показано, что ингибиторы активации NF-κВ применимы в ангиостатической терапии (Tabruyn and Griffioen, Angiogenesis, 2008, 11, 101-106), при воспалительном заболевании кишечника (Atreya et al., J. Intern. Med., 2008, 263(6), 591-6); и, на животных моделях, заболеваний, включая воспаление, включая нейтрофильный альвеолит, астму, гепатит, воспалительное заболевание кишечника, нейродегенерации, ишемию/реперфузию, септический шок, гломерулонефрит и ревматоидный артрит (D'Acquisto et al., Molecular Interventions, 2002, 2(1), 22-35).
Исследования также предполагают, что ингибирование NF-κВ FAE может быть опосредовано взаимодействием с передачей сигнала фактора некроза опухоли (TNF). Диметилфумарат ингибирует индуцированную TNF экспрессию мРНК тканевого фактора и белка и индуцированное TNF связывание ДНК белков NF-κВ, и ингибирует индуцированное TNF поступление активированных белков NF-κВ, причем посредством этого ингибируется активация генов воспаления (Loewe et al., J. Immunology, 2002, 168, 4781-4787). Пути передачи сигналов TNF вовлечены в патогенез иммуноопосредуемых воспалительных заболеваний, таких как ревматоидный артрит, болезнь Крона, псориаз, псориатический артрит, ювенильный идиопатический артрит и анкилозирующий спондилит (Tracey et al., Pharmacology & Therapeutics, 2008, 117, 244-279).
Таблетка с энтеросолюбильным покрытием Fumaderm®, содержащая смесь солей моноэтилфумарата и диметилфумарата (DMF) (2), который быстро гидролизуется до монометилфумарата (МНР) (1), рассматриваемого как основной биоактивный метаболит, одобрена в Германии в 1994 для лечения псориаза.
Fumaderm® дозируют TID по 1-2 г/сутки, вводимых для лечения псориаза. Fumaderm® обнаруживает высокую степень изменчивости от пациента к пациенту в отношении абсорбции лекарственного средства, и пища сильно уменьшает биологическую доступность. Полагают, что абсорбция происходит в тонкой кишке с максимальными уровнями, достигаемыми через 5-6 часов после перорального введения. Существенное побочное действие имеет место у 70-90% пациентов (Brewer and Rogers, Clin. Expt'l Dermatology, 2007, 32, 246-49; и Hoefhagel et al., Br. J. Dermatology, 2003, 149, 363-369). Побочное действие современной терапии FAE включает желудочно-кишечные расстройства, включая тошноту, рвоту и диарею, и транзиторное покраснение кожи. Также DMF показывает плохую растворимость в воде.
В попытках преодолеть недостатки современной терапии FAE разработаны производные фумаровой кислоты (Joshi and Strebel, WO 2002/055063, US 2006/0205659 и US 7157423 (амиды и белковофумаратные конъюгаты); Joshi et al., WO 2002/055066, и Joshi and Strebel, US 6355676 (моно- и диалкилэфиры); Joshi and Strebel, WO 2003/087174 (карбоциклические и оксакарбоциклические соединения); Joshi et al., WO 2006/122652 (тиосукцинаты);); Joshi et al., US 2008/0233185 (диалкил- и диарилэфиры) и соли (Nilsson et al., US 2008/0004344). Фармацевтические композиции с регулируемым высвобождением, включающие эфиры фумаровой кислоты, раскрыты Nilsson and Muller, WO 2007/042034. Пролекарства циклоамидные эфиры описаны Nielsen and Bundgaard, J. Pharm. Sci, 1988, 77(4), 285-298.
Раскрытие изобретения
Необходимы Пролекарства МНР с высокой гастроинтестинальной просачиваемостью и/или абсорбцией, улучшенной растворимостью, упорядоченным гидролизом (т.е. предпочтительное отщепление прогрупп) и минимальным гидролизом в просвете кишки или энтероцитной цитоплазмы. Такие Пролекарства МНР, которые обеспечивают более высокую пероральную биодоступность и уровни в плазме MHF, DMF и/или других метаболитов, могут увеличить эффективность/пропорцию респондеров по сравнению с существующими эфирами фумаровой кислоты; облегчить использование меньших доз, пониженную частоту дозирования и стандартизованные схемы приема; уменьшить действие пищи; уменьшить желудочно-кишечное побочное действие/токсичность и уменьшить изменчивость лечения от пациента к пациенту. В первом аспекте изобретение относится к соединениям формулы (I)
или их фармацевтически приемлемым солям, где в указанной формуле
R1 и R2 выбирают независимо из водорода, C1-6-алкила и замещенного C1-6-алкила;
R3 и R4 выбирают независимо из водорода, C1-6-алкила, замещенного C1-6-алкила, C1-6-гетероалкила, замещенного C1-6-гетероалкила, С4-12-циклоалкилалкила, замещенного С4-12-циклоалкилалкила, С7-12-арилалкила и замещенного С7-12-арилалкила; или R3 и R4 вместе с атомом азота, с которым они связаны, образуют цикл, выбранный из C5-10-гетероарила, замещенного С5-10-гетероарила, С5-10-гетероциклоалкила и замещенного С5-10-гетероциклоалкила; и
R5 выбирают из метила, этила и С3-6-алкила;
где каждую группу-заместитель выбирают независимо из галогена, -ОН, -CN, -CF3, -О, - NO2, бензила, - C(O)NR11 2, - R11, - OR11, - C(O)R11, - COOR11 и -NR11 2, где каждый R11 выбирают независимо из водорода и С1-4-алкила;
при условии, что когда R5 представляет собой этил, тогда R3 и R4 выбирают независимо из водорода, C1-6-алкила и замещенного C1-6-алкила.
Во втором аспекте изобретение относится к соединениям формулы (II)
или их фармацевтически приемлемым солям, где в указанной формуле R6 выбирают из C1-6-алкила, замещенного C1-6-алкила, C1-6-гетероалкила, замещенного C1-6-гетероалкила, С3-8-циклоалкила, замещенного С3-8-циклоалкила, С6-8-арила, замещенного С6-8-арила и -OR10, где R10 выбирают из C1-6-алкила, замещенного C1-6-алкила, С3-10-циклоалкила, замещенного С3-10-циклоалкила, С6-10-арила и замещенного С6-10-арила;
R7 и R8 выбирают независимо из водорода, С1-6-алкила и замещенного С1-6-алкила;
и
R9 выбирают из С1-6-алкила и замещенного С1-6-алкила;
где каждую группу-заместитель выбирают независимо из галогена, -ОН, -CN, -CF3, -О, -NO2, бензила, -C(O)NR11 2, -R11, -OR11, -C(O)R11, -COOR11 и -NR11 2, где каждый R11 выбирают независимо из водорода и C1-4-алкила.
В третьем аспекте изобретение относится к соединениям формулы (III)
или их фармацевтически приемлемым солям, где в указанной формуле
R1 и R2 выбирают независимо из водорода, С1-6-алкила и замещенного С1-6-алкила;
и
R3 и R4 выбирают независимо из водорода, С1-6-алкила, замещенного С1-6-алкила, C1-6-гетероалкила, замещенного C1-6-гетероалкила, С4-12-циклоалкилалкила, замещенного С4-12-циклоалкилалкила, С7-12-арилалкила и замещенного С7-12-арилалкила; или R3 и R4 вместе с атомом азота, с которым они связаны, образуют цикл, выбранный из С5-10-гетероарила, замещенного С5-10-гетероарила, С5-10-гетероциклоалкила и замещенного C5-10-гетероциклоалкила;
где каждую группу-заместитель выбирают независимо из галогена, -ОН, -CN, -CF3,=O, -NO2, бензила, -C(O)NR11 2, -R11, -OR11, -C(O)R11, -COOR11 и -NR11 2, где каждый R11 выбирают независимо из водорода и C1-4-алкила.
В четвертом аспекте изобретение относится к соединениям формулы (IV)
или их фармацевтически приемлемым солям, где в указанной формуле R6 выбирают из С1-6-алкила, замещенного С1-6-алкила, C1-6-гетероалкила, замещенного C1-6-гетероалкила, С3-8-циклоалкила, замещенного С3-8-циклоалкила, С6-8-арила, замещенного С6-8-арила и -OR10, где R10 выбирают из С1-6-алкила, замещенного C1-6-алкила, С3-10-циклоалкила, замещенного С3-10-циклоалкила, С6-10-арила и замещенного С6-10-арила; и
R7 и R8 выбирают независимо из водорода, С1-6-алкила и замещенного С1-6-алкила;
где каждую группу-заместитель выбирают независимо из галогена, -ОН, -CN, -CF3,=O, -NO2, бензила, -C(O)NR11 2, -R11, -OR11, -C(O)R11, -COOR11 и -NR11 2, где каждый R11 выбирают независимо из водорода и C1-4-алкила;
при условии, что
когда один из R7 и R8 выбран из этила и метила, а другой из R7 и R8 представляет собой водород, тогда R не является -С(СН3)=СН2; и
когда каждый из R7 и R8 представляет собой водород, тогда R6 не выбирают из -СН=СН2 и 4-карбоксифенила.
В пятом аспекте изобретение относится к фармацевтическим композициям, включающим соединение формул (I)-(IV) и, по меньшей мере, один фармацевтически приемлемый носитель.
В шестом аспекте изобретение относится к способам лечения заболевания у пациента, включающим введение пациенту, нуждающемуся в таком лечении, фармацевтической композиции, включающей терапевтически эффективное количество соединения формул (I)-(IV). В некоторых воплощениях заболевание выбирают из псориаза, рассеянного склероза, воспалительного заболевания кишечника, астмы, хронической обструктивной болезни легких и артрита.
В седьмом аспекте изобретение относится к способам ингибирования активации NF-κВ у пациента, включающим введение пациенту фармацевтической композиции, включающей терапевтически эффективное количество соединения формул (I)-(IV).
В восьмом аспекте изобретение относится к способам ингибирования функции TNF у пациента, включающим введение пациенту фармацевтической композиции, включающей терапевтически эффективное количество соединения формул (I)-(IV).
Осуществление изобретения
Определения
Черточка («-»), которая не находится между двумя буквами или символами, используется для указания точки присоединения для группы-заместителя. Например, -CONH2 присоединяется через атом углерода.
Термин «алкил» относится к насыщенному или ненасыщенному разветвленному или линейному одновалентному углеводородному радикалу, полученному удалением одного атома водорода от одного атома углерода исходного алкана, алкена или алкина. Примеры алкильных групп включают, но не ограничиваются перечисленным, метил; этилы, такие как этанил, этенил и этинил; пропилы, такие как пропан-1-ил, пропан-2-ил, проп-1-ен-1-ил, проп-1-ен-2-ил, проп-2-ен-1-ил (аллил), проп-1-ин-1-ил, проп-2-ин-1-ил и т.д.; бутилы, такие как бутан-1-ил, бутан-2-ил, 2-метил-пропан-1-ил, 2-метил-пропан-2-ил, бут-1-ен-1-ил, бут-1-ен-2-ил, 2-метил-проп-1-ен-1-ил, бут-2-ен-1-ил, бут-2-ен-2-ил, бута-1,3-диен-1-ил, бута-1,3-диен-2-ил, бут-1-ин-1-ил, бут-1-ин-3-ил, бут-3-ин-1-ил и т.д., и подобные группы.
Термин «алкил» специфически предназначен для включения групп с любой степенью или уровнем замещения, т.е., групп с исключительно одинарными углерод-углеродными связями, групп с одной или несколькими двойными углерод-углеродными связями, групп с одной или несколькими тройными углерод-углеродными связями и групп с комбинациями одинарной, двойной и тройной углерод-углеродных связей. Когда предполагается определенный уровень насыщения, используют термины «алканил», «алкенил» и «алкинил». В некоторых воплощениях алкильная группа может иметь от 1 до 20 атомов углерода (C1-20), в некоторых воплощениях от 1 до 10 атомов углерода (С1-10), в некоторых воплощениях от 1 до 8 атомов углерода (C1-8), в некоторых воплощениях от 1 до 6 атомов углерода (C1-6), в некоторых воплощениях от 1 до 4 атомов углерода (C1-4) и в некоторых воплощениях от 1 до 3 атомов углерода (C1-3)
Термин «арил» относится к одновалентному ароматическому углеводородному радикалу, полученному удалением одного атома водорода от одного атома углерода исходной ароматической циклической системы. Арил включает моноциклические системы, например, бензол; бициклические системы, в которых, по меньшей мере, один цикл является карбоциклическим и ароматическим, например, нафталин, индан и тетралин; и трициклические системы, в которых, по меньшей мере, один цикл является карбоциклическим и ароматическим, например, флуорен. Арил охватывает полициклические системы с, по меньшей мере, одним карбоциклическим ароматическим циклом, конденсированным с, по меньшей мере, одним карбоциклическим ароматическим циклом, циклоалкильным циклом или гетероциклоалкильным циклом. Например, арил включает фенильный цикл, конденсированный с 5-7-членным гетероциклоалкильным циклом, содержащим один или несколько гетероатомов, выбранных из N, О и S. В случае таких конденсированных бициклических систем, в которых только один из циклов является карбоциклическим ароматическим циклом, атом углерода радикала может находиться в карбоциклическом ароматическом цикле или гетероциклоалкильном цикле. Примеры арильных групп включают, но не ограничиваются перечисленным, группы, образованные от ацеантрилена, аценафтилена, ацефенантрилена, антрацена, азулена, бензола, хризена, коронена, флуорантена, флуорена, гексацена, гексафена, гексалена, as-индацена, s-индацена, индана, индена, нафталина, октацена, октафена, окталена, овалена, пента-2,4-диена, пентацена, пенталена, пентафена, перилена, феналена, фенантрена, пицена, плейадена, пирена, пирантрена, рубицена, трифенилена, тринафталена и т.п.. В некоторых воплощениях арильная группа может иметь от 6 до 20 атомов углерода (С6-20), от 6 до 12 атомов углерода (С6-12), от 6 до 10 атомов углерода (С6-10), и в некоторых воплощениях от 6 до 8 атомов углерода (С6-8). Однако арил не охватывает и никоим образом не перекрывает гетероарил, имеющий в данном описании отдельное определение.
Термин «арилалкил» относится к ациклическому алкильному радикалу, в котором один из атомов водорода, связанных с атомом углерода, типично, концевого или sp3 атома углерода, заменен арильной группой. Примеры арилалкильных групп включают, но не ограничиваются перечисленным, бензил, 2-фенилэтан-1-ил, 2-фенилэтен-1-ил, нафтилметил, 2-нафтилэтан-1-ил, 2-нафтилэтен-1-ил, нафтобензил, 2-нафтофенилэтан-1-ил и подобные. Когда предполагаются определенные алкильные группы, используют номенклатуру арилалканил, арилалкенил или арилалкинил. В некоторых воплощениях арилалкильная группа представляет собой С7-30-арилалкил, например, алканильная, алкенильная или алкенильная часть арилалкильной группы является C1-10, и арильная часть является С6-20, в некоторых воплощениях арилалкильная группа представляет собой С6-18-арилалкил, например, алканильная, алкенильная или алкенильная часть арилалкильной группы является C1-8, и арильная часть является С6-10. В некоторых воплощениях арилалкильная группа представляет собой С7-12-арилалкил.
«Соединения» формул (I)-(IV), раскрытые в данном описании, включают любые специфические соединения в пределах указанных формул. Соединения можно идентифицировать или по их химической структуре и/или химическому названию. Соединения называют с использованием Chemistry 4-D Draw Pro, версия 7.01 с (Chemlnnovation Software, Inc., San Diego, CA). Когда химическая структура и химическое название вступают в противоречие, определяющей для идентификации соединения является химическая структура. Соединения, описанные в данном описании, могут включать один или несколько хиральных центров и/или двойных связей и поэтому могут существовать в виде стереоизомеров, таких как изомеры по двойной связи (т.е., геометрические изомеры), энантиомеры или диастереомеры. Соответственно, любые химические структуры в пределах объема представленного описания, в целом или в части с родственной конфигурацией, охватывают все возможные энантиомеры и стереоизомеры иллюстрированных соединений, включая стереохимически чистую форму (например, геометрически чистую, энантиомерно чистую или диастереомерно чистую) и энантиомерные и стереоизомерные смеси. Энантиомерные и стереоизомерные смеси можно разделить на составляющие их энантиомеры или стереоизомеры с использованием методов разделения или методов хирального синтеза, хорошо известных специалистам в данной области техники. Соединения формул (I)-(IV) включают, но не ограничиваются перечисленным, оптические изомеры соединений формул (I)-(IV), их рацематы и другие их смеси. В таких воплощениях отдельный энантиомер или диастереомер, т.е. оптически активную форму, можно получить асимметричным синтезом или расщеплением рацематов. Расщепление рацематов можно осуществить, например, обычными методами, такими как кристаллизация в присутствии расщепляющего агента или хроматография с использованием, например, хиральных неподвижных фаз. Безотносительно к вышеизложенному, в соединениях формул (I)-(IV) конфигурация у показанной двойной связи представляет собой только Е-конфигурацию (т.е., транс-конфигурацию).
Соединения формул (I)-(IV) также могут существовать в нескольких таутомерных формах, включая енольную форму, кетоформу и их смеси. Соответственно, химические структуры, отображенные в данном описании, охватывают все возможные таутомерные формы показанных соединений. Соединения формул (I)-(IV) также включают меченные изотопами соединения, когда один или несколько атомов имеют атомную массу, отличающуюся от атомной массы, обычно обнаруживаемой в природе. Примеры изотопов, которые могут быть введены в соединения, раскрытые в данном описании, включают, но не ограничиваются перечисленным, 2H, 3Н, 11С, 13С, 14С, 15N, 18О, 17О и т.д.. Соединения могут существовать в несольватированных формах, а также в сольватированных формах, включая гидратированные формы и N-оксиды. Вообще соединения, упоминаемые в данном описании, могут представлять собой свободные кислоты, могут быть гидратированными, сольватированными или N-оксидами. Некоторые соединения могут существовать в нескольких кристаллических, сокристаллических или аморфных формах. Соединения формул (I)-(IV) включают их фармацевтически приемлемые соли или фармацевтически приемлемые сольваты формы свободной кислоты любой из вышеуказанных форм, а также кристаллические формы любой из вышеуказанных форм.
Соединения формул (I)-(IV) также включают сольваты. Термин «сольват» относится к комплексу соединения с одной или несколькими молекулами растворителя в стехиометрическом или нестехиометрическом количестве. Такие молекулы растворителя представляют собой растворители, обычно используемые в области фармации, о которых известно как о безвредных для пациентов, например, воду, этанол и т.п.. Молекулярный комплекс соединения или части соединения и растворителя может быть стабилизирован нековалентными внутримолекулярными силами, такими как, например, электростатические силы, ван-дер-ваальсовы силы или водородные связи. Термин «гидрат» относится к сольвату, в котором одна или несколько молекул растворителя являются молекулами воды.
Кроме того, когда приводятся структуры соединений, звездочка (*) указывает точку присоединения части структуры к остальной молекуле.
Термин «циклоалкил» относится к насыщенному или частично ненасыщенному циклическому алкильному радикалу. Когда предполагается определенный уровень насыщения, используют номенклатуру «циклоалканил» или «циклоалкенил». Примеры циклоалкильных групп включают, но не ограничиваются перечисленным, группы, образованные от циклопропана, циклобутана, циклопентана, циклогексана и т.п.. В некоторых воплощениях циклоалкильная группа представляет собой С3-15-циклоалкил, С3-12-циклоалкил, и в некоторых воплощениях С3-8-циклоалкил.
Термин «циклоалкилалкил» относится к ациклическому алкильному радикалу, в котором один из атомов водорода, связанных с атомом углерода, типично, концевым или sp3 атомом углерода, заменен циклоалкильной группой. Когда предполагаются определенные алкильные части, используют номенклатуру «циклоалкилалканил», «циклоалкилалкенил» или «циклоалкилалкинил». В некоторых воплощениях циклоалкилалкильная группа представляет собой С4-30-циклоалкилалкил, например, алканильная, алкенильная или алкинильная группа циклоалкилалкильной группы представляет собой группу C1-10, а циклоалкильная группа представляет собой группу С3-20, и в некоторых воплощениях циклоалкилалкильная группа представляет собой С3-20-циклоалкилалкил, например, алканильная, алкенильная или алкинильная группа циклоалкилалкильной группы представляет собой группу C1-8, а циклоалкильная группа представляет собой группу С3-12. В некоторых воплощениях циклоалкилалкильная группа представляет собой С4-12-циклоалкилалкил.
Термин «заболевание» относится к заболеванию, расстройству, состоянию или симптому любого из вышеуказанных заболеваний.
Термин «лекарство», определенный в 21 U.S.С, § 321(g)(l), означает «(А) изделия, признанные в официальной фармакопеи Соединенных Штатов, официальной гомеопатической фармакопеи Соединенных Штатов или в официальном National Formulary или любом их приложении; и (В) изделия, предназначенные для применения при диагностике, излечивании, смягчении, лечении или предупреждении заболевания у людей или других животных; и (С) изделия (иные, чем пищевые продукты), предназначенные для воздействия на любую функцию организма людей или других животных…»
Термин «галоген» относится к атому фтора, хлора, брома или иода. В некоторых воплощениях термин «галоген» относится к атому хлора.
Термин «гетероалкил» сам по себе или как часть другого заместителя относится к алкильной группе, в которой один или несколько атомов углерода (и некоторые ассоциированные атомы водорода) заменены независимо одинаковыми или разными гетероатомными группами. Примеры гетероатомных групп включают, но не ограничиваются перечисленным, -O-, -S-,-O-O-, -S-S-, -O-S-, -NR13, =N-N=, -N=N-, -N=N-NR13, -PR13, -P(O)2-, -POR13, -OP(O)2-, -SO-, -SO2-,-Sn(R13)2- и т.п., где каждый R13 выбирают независимо из водорода, C1-6-алкила, замещенного C1-6-алкила, С6-12-арила, замещенного С6-12-арила, С7-18-арилалкила, замещенного С3-7-арилалкила, С3-7-циклоалкила, замещенного С3-7-циклоалкила, С3-7-гетероциклоалкила, замещенного С1-6гетероциклоалкила, C1-6-гетероалкила, замещенного C1-6-гетероалкила, С6-12-гетероарила, замещенного С6-12-гетероарила, С7-18-гетероарилалкила или замещенного C7-18-гетероарилалкила. Ссылка на, например, C1-6-гетероалкил означает C1-6-алкильную группу, в которой, по меньшей мере, один из атомов углерода (и некоторые ассоциированные атомы водорода) заменен гетероатомом. Например, С1-6-гетероалкил включает группы, имеющие пять атомов углерода и один гетероатом, группы, имеющие четыре атомов углерода и два гетероатома, и т.д.. В некоторых воплощениях каждый R13 выбирают независимо из водорода и C1-3-алкила. В некоторых воплощениях гетероатомную группу выбирают из -O-, -S-, -NH-,-Н(СН3)- и -SO2-; и в некоторых воплощениях гетероатомная группа представляет собой -О-.
Термин «гетероарил» относится к одновалентному гетероароматическому радикалу, образованному удалением одного атома водорода от одного атома исходной гетероароматической циклической системы. Гетероарил охватывает несколько циклических систем, имеющих, по меньшей мере, один гетероароматический цикл, конденсированный с, по меньшей мере, одним другим циклом, который может быть ароматическим или неароматическим. Например, гетероарил охватывает бициклические системы, в которых один цикл является ароматическим, и второй цикл является гетероциклоалкильным циклом. В случае таких конденсированных гетероарильных циклических систем, в которых только один из циклов содержит один или несколько гетероатомов, углерод радикала может находиться в ароматическом цикле или в гетероциклоалкильном цикле. В некоторых воплощениях, когда общее число атомов N, S и О в гетероарильной группе превышает единицу, гетероатомы не являются соседними друг для друга. В некоторых воплощениях общее число гетероатомов в гетероарильной группе составляет не более двух.
Примеры гетероарильных групп включают, но не ограничиваются перечисленным, группы, образованные от акридина, арсиндола, карбазола, β-карболина, хромана, хромена, циннолина, фурана, имидазола, индазола, индола, индолина, индолизина, изобензофурана, изохромена, изоиндола, изоиндолина, изохинолина, изотиазола, изоксазола, нафтиридина, оксадиазола, оксазола, перимидина, фенантридина, фенантролина, феназина, фталазина, птеридина, пурина, пирана, пиразина, пиразола, пиридазина, пиридина, пиримидина, пиррола, пирролизина, хиназолина, хинолина, хинолизина, хиноксалина, тетразола, тиадиазола, тиазола, тиофена, триазола, ксантена, тиазолидина, оксазолидина и т.п.. В некоторых воплощениях гетероарильная группа представляет собой 4-20-членный гетероарил (C4-20), и в некоторых воплощениях 4-12-членный гетероарил (C4-12). В некоторых воплощениях гетероарильные группы представляет собой группы, образованные от тиофена, пиррола, бензотиофена, бензофурана, индола, пиридина, хинолина, имидазола, оксазола или пиразина. Например, в некоторых воплощениях С5-гетероарил может представлять собой фурил, тиенил, пирролил, имидазолил, пиразолил, изотиазолил, изоксазолил.
Термин «гетероциклоалкил» относится к насыщенному или ненасыщенному циклическому алкильному радикалу, в котором один или несколько атомов углерода (и некоторых ассоциированных атомов водорода) заменены независимо одинаковыми или разными гетероатомами; или к исходной ароматической циклической системе, в которой один или несколько атомов углерода (и некоторых ассоциированных атомов водорода) заменены независимо одинаковыми или разными гетероатомами так, что циклическая система более не содержит, по меньшей мере, один ароматический цикл. Примеры гетероатомов для замены атома(ов) углерода включают, но не ограничиваются перечисленным, N, Р, О, S, Si и т.д. Примеры гетероциклоалкильных групп включают, но не ограничиваются перечисленным, группы, образованные от эпоксидов, азиринов, тииранов, имидазолидина, морфолина, пиперазина, пиперидина, пиразолидина, пирролидина, хинуклидина и т.п.. В некоторых воплощениях гетероциклоалкильная группа представляет собой С5-10-гетероциклоалкил, С5-8-гетероциклоалкил, и в некоторых воплощениях С5-6-гетероциклоалкил.
«Уходящая группа» имеет значение, обычно связанное с ней в синтетической органической химии, т.е., представляет собой атом или группу, способные заменяться нуклеофилом, и включает галоген, такой как хлор, бром, фтор и иод, ацилокси (алкоксикарбонил), такой как ацетокси и бензилокси, арилоксикарбонил, мезилокси, тозилокси, трифторметансульфонилокси, арилокси, такой как 2,4-динитрофенокси, метокси, N,O-диметилгидроксиламино, п-нитрофенолят, имидазолил и т.п..
Определение «исходная ароматическая циклическая система» относится к ненасыщенной циклической или полициклической системе с системой конъюгированных π-(пи)-электронов. В определение «исходная ароматическая циклическая система» включены конденсированные циклические системы, в которых один или несколько циклов являются ароматическими и один или несколько циклов являются насыщенными или ненасыщенными, такие как, например, флуорен, индан, инден, фенален и т.д.. Примеры исходных ароматических циклических систем включают, но не ограничиваются перечисленным, ацеантрилен, аценафтилен, ацефенантрилен, антрацен, азулен, бензол, хризен, коронен, флуорантен, флуорен, гексацен, гексафен, гексален, as-индацен, s-индацен, индан, инден, нафталин, октацен, октафен, октален, овален, пента-2,4-диен, пентацен, пентален, пентафен, перилен, фенален, фенантрен, пицен, плейаден, пирен, пирантрен, рубицин, трифенилен, тринафтален и т.п.
Определение «исходная гетероароматическая циклическая система» относится к ароматической циклической системе, в которой один или несколько атомов углерода (и любых ассоциированных атомов водорода) независимо заменены одинаковыми или различными гетероатомами таким образом, что сохраняется непрерывная система π-электронов, характеризующая ароматические системы, и ряд π-электронов вне плоскости, соответствующих правилу Хюккеля (4n+2). Примеры гетероатомов для замены атомов углерода включают, но не ограничиваются перечисленным, N, Р, О, S, Si и т.д.. В определение «исходная гетероароматическая циклическая система» конкретно включены конденсированные циклические системы, в которых один или несколько циклов являются ароматическими и один или несколько циклов являются насыщенными или ненасыщенными, такие как, например, арсиндол, бензодиоксан, бензофуран, хроман, хромен, индол, индолин, ксантен и т.д. Примеры исходных гетероароматических циклических систем включают, но не ограничиваются перечисленным, арсиндол, карбазол, β-карболин, хроман, хромен, циннолин, фуран, имидазол, индазол, индол, индолин, индолизин, изобензофуран, изохромен, изоиндол, изоиндолин, изохинолин, изотиазол, изоксазол, нафтиридин, оксадиазол, оксазол, перимидин, фенантридин, фенантролин, феназин, фталазин, птеридин, пурин, пиран, пиразин, пиразол, пиридазин, пиридин, пиримидин, пиррол, пирролизин, хиназолин, хинолин, хинолизин, хиноксалин, тетразол, тиадиазол, тиазол, тиофен, триазол, ксантен, тиазолидин, оксазолидин и т.п..
Термин «пациент» относится к млекопитающему, например, человеку.
Определение «фармацевтически приемлемый» относится к (материалу), одобренному или достойному одобрения регулирующим государственным органом или правительством или внесенному в фармакопею США или другую одобренную фармакопею для использования для животных, и в частности, для людей.
Определение «фармацевтически приемлемая соль» относится к соли соединения, которая обладает нужной фармакологической активностью исходного соединения. Такие соли включают соли присоединения кислот, образованные с неорганическими кислотами, такими как хлороводородная кислота, бромоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и т.п.; или образованные с органическими кислотами, такими как уксусная кислота, пропионовая кислота, гексановая кислота, циклопентанпропионовая кислота, гликолевая кислота, виноградная кислота, молочная кислота, малоновая кислота, янтарная кислота, яблочная кислота, малеиновая кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, 3-(4-гидроксибензоил)бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, 1,2-этандисульфоновая кислота, 2-гидроксиэтансульфоновая кислота, бензолсульфоновая кислота, 4-хлорбензолсульфоновая кислота, 2-нафталинсульфоновая кислота, 4-толуолсульфоновая кислота, камфорсульфоновая кислота, 4-метилбицикло[2,2,2]окт-2-ен-1-карбоновая кислота, глюкогептоновая кислота, 3-фенилпропионовая кислота, триметилуксусная кислота, трет-бутилуксусная кислота, лаурилсерная кислота, глюконовая кислота, глутамовая кислота, гидроксинафтойная кислота, салициловая кислота, стеариновая кислота, муконовая кислота и т.п.; и соли, образованные замещением кислотного протона, присутствующего в исходном соединении, ионом металла, например, ионом щелочного металла, ионом щелочноземельного металла или ионом алюминия; или координацией с органическим основанием, таким как этаноламин, диэтаноламин, триэтаноламин, N-метилглюкамин и т.п.. В некоторых воплощениях фармацевтически приемлемая соль представляет собой гидрохлорид. В некоторых воплощениях фармацевтически приемлемая соль представляет собой натриевую соль.
Термин «фармацевтически приемлемый носитель» относится к фармацевтически приемлемому разбавителю, фармацевтически приемлемому адъюванту, фармацевтически приемлемому эксципиенту, фармацевтически приемлемому носителю или сочетанию любых из вышеуказанных материалов, с которыми соединение по настоящему изобретению можно вводить пациенту, и которые не разрушают его фармакологическую активность, и которые являются нетоксичными при введении в дозах, достаточных для обеспечения терапевтически эффективного количества соединения.
Термин «фармацевтическая композиция» относится к соединению формул (I)-(IV) и, по меньшей мере, одному фармацевтически приемлемому носителю, с которым соединение формул (I)-(IV) вводят пациенту.
Определение «замещенный» относится к группе, в которой один или несколько атомов водорода независимо заменены одинаковыми или раличными группами-заместителями. В некоторых воплощениях каждую группу-заместитель выбирают независимо из галогена, -ОН, -CN, -CF3, =О, -NO2, бензила, -C(O)NH2, -R11, -OR11, -C(O)R11, -COOR11 и -NR11 2, где каждый R11 выбирают независимо из водорода и С1-4-алкила. В некоторых воплощениях каждую группу-заместитель выбирают независимо из галогена, -ОН, -CN, -CF3, -NO2, бензила, -R11, -OR11 и -NR11 2, где каждый R11 выбирают независимо из водорода и С1-4-алкила. В некоторых воплощениях каждую группу-заместитель выбирают независимо из галогена, -ОН, -CN, -CF3, =O, -NO2, бензила, -C(O)NR11 2, -R11, -OR11, -C(O)R11, -COOR11 и -NR11 2, где каждый R11 выбирают независимо из водорода и С1-4-алкила. В некоторых воплощениях каждую группу-заместитель выбирают независимо из -ОН, C1-4-алкила и -NH2.
Термин «лечить» или «