Способ реабилитации пожилых пациентов ишемической болезнью сердца с хронической сердечной недостаточностью, перенесших инфаркт миокарда
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к терапии и кардиологии, и касается реабилитации пожилых больных ишемической болезнью сердца (ИБС) с хронической сердечной недостаточностью (ХСН), перенесших инфаркт миокарда (ИМ). Для этого в отдаленные сроки - через 6 и более месяцев после перенесенного ИМ на фоне стандартной медикаментозной терапии за 60 минут до начала дозированной ходьбы вводят препарат омега-3-полиненасыщенных жирных кислот - Омакор. Такой комплекс лекарственных средств в сочетании с дозированной физической нагрузкой обеспечивает повышение толерантности к физическим нагрузкам, улучшение функции сердечно-сосудистой системы и нормализацию липидного обмена, что, в свою очередь, приводит к снижению количества неблагоприятных сердечно-сосудистых событий и замедлению прогрессирования ХСН. 2 пр., 5 табл.
Реферат
Изобретение относится к медицине и может быть использовано в кардиологии и реабилитологии для физической реабилитации пожилых больных, перенесших инфаркт миокарда (ИМ).
Современная тактика ведения больных ишемической болезнью сердца (ИБС), отягощенной хронической сердечной недостаточностью (ХСН), включает в себя физическую реабилитацию. По данным ряда клинических исследований, а также мета-анализа ЕхТrаМАТСН дозированные физические нагрузки оказывают положительное влияние на прогноз больных ХСН [1]. Согласно результатам мета-анализа ЕхТrаМАТСН среди пациентов, тренировавшихся в течение года, летальность снизилась на 35%, на основании чего физические тренировки были отнесены к I классу рекомендаций (уровень доказательности В) по диагностике и лечению ХСН [2].
Однако многие вопросы, касающиеся тренировок таких больных (сроки начала тренировок, продолжительность, фоновая медикаментозная терапия), остаются нерешенными; иными словами, до сих пор не определены оптимальные программы кардиореабилитации пожилых больных сердечной недостаточностью после перенесенного ИМ [3, 4]. В частности, по данным Николаевой Л.Ф., Аронова Д.М. к длительным физическим нагрузкам больным, перенесшим ИМ, разрешается приступать через 3-4 месяца после него [5], но в отношении сроков физической реабилитации у пожилых больных ИБС с ХСН, перенесших ИМ, единого мнения не существует. При этом прогрессирование ХСН определяется темпами постинфарктного ремоделирования миокарда, которое может продолжаться неделями или месяцами, но, по данным Перуцкого Д.Н. и соавт. (2011) к 6-му месяцу после перенесенного ИМ становится очевидным отсутствие прогрессирования ХСН, обусловленное закончившимися процессами ремоделирования, или в дальнейшем после перенесенного ИМ ХСН будет принимать быстро- или умереннопрогрессирующий характер [6].
В Российской Федерации в настоящее время около 25% населения имеют возраст старше 65 лет, которые, в соответствии с документами ООН и Международной организации труда, считаются пожилыми лицами [7]. Больные старших возрастных групп склонны к осложненному течению инфаркта миокарда и часто имеют отягощенную коморбидность. В качестве метода ранней реабилитации у больных ИБС, перенесших ИМ, в стационаре предлагаются схемы групповой и индивидуальной лечебной физкультуры, которые неоднократно показывали свою эффективность и положительное прогностическое влияние, однако в старших возрастных группах проведение групповой реабилитации малоприемлемо, а индивидуальные тренировки невозможны в силу организационных и экономических трудностей [7].
Известен способ реабилитации пожилых больных с ХСН, перенесших ИМ, на санаторном этапе реабилитации, в котором для снижения риска развития повторных сердечно-сосудистых катастроф и улучшения качества жизни пациентов применяют комплекс физических тренировок с использованием велотренажера и дозированной ходьбы под контролем показателей центральной гемодинамики [8].
Данный способ является наиболее близким к заявляемому по технической сущности и по достигаемому клиническому результату и выбран в качестве прототипа.
Недостатком данного способа является то, что эффективность контролируемых тренировок ограничивается наличием некорригированной циркуляторной гипоксии при ХСН после перенесенного ИМ, кроме того, также он применим только к короткому санаторному этапу реабилитации пациентов пожилого возраста, перенесших инфаркт миокарда, из-за необходимости использования специальных технических устройств, таких как велотренажер, что резко ограничивает применение данного метода пациентов в домашних условиях.
Задачей изобретения является повышение эффективности способа реабилитации пожилых больных в отдаленные сроки после перенесенного ИМ.
Поставленная задача решается путем назначения в отдаленные сроки (через 6 и более месяцев) после перенесенного ИМ больным ИБС, ассоциированной с хронической сердечной недостаточностью, на фоне стандартной медикаментозной терапии за 60 минут до начала контролируемых физических тренировок посредством дозированной ходьбы антиоксиданта - препарата омега-3-полиненасыщенных жирных кислот (ω-3 ПНЖК) - Омакор.
Новым в предлагаемом способе является назначение пожилым больным ИБС с ХСН через 6 и более месяцев после перенесенного ИМ препарата ω-3 ПНЖК Омакор за 60 минут до начала контролируемых физических тренировок в виде дозированной ходьбы.
Предложенный способ реабилитации основан на том, что в его основе лежит воздействие ω-3 ПНЖК на такие пусковые факторы развития хронической сердечной недостаточности у больных перенесших ИМ, как диастолическая и систолическая дисфункция миокарда и гипертензивная гипертрофия левого желудочка, что, в конечном итоге, обеспечивая регресс ишемической дисфункции миокарда, позволит уменьшить общее количество неблагоприятных сердечно-сосудистых событий [9]. В частности, в исследованиях Green Р. (2007) и Arena R. (2008) было показано, что у больных ИБС с ХСН снижение насосной функции сердца после перенесенного инфаркта миокарда ассоциируется со снижением пикового потребления кислорода миокардом сердца и организмом в целом, что является независимым предиктором сердечной смерти и неблагоприятных сердечно-сосудистых событий [10, 11]. По данным исследования GISSI-HF, установлено, что назначение у больных ИБС с ХСН препарата Омакор обеспечивало достоверное снижение общей смертности на 9% и частоты госпитализаций в связи с сердечно-сосудистыми причинами на 8% в течение 90 дней лечения, но в дальнейшем не влияло на прогноз пациентов, перенесших ОИМ [8, 12, 13]. При этом, в метаанализе Poole CD. и соавт. (2013) представлено, что назначение ω-3 ПНЖК в первые 14 сут. после ОИМ приводит к статистически значимому снижению риска смерти на 32%, в первые 90 сут. - на 22%, но начало терапии ω-3 ПНЖК более чем через 90 сут. после перенесенного ОИМ практически не влияет на прогноз [14]. Кроме того, Piepoli M.F. и соавт.(2004) выявили, что использование физических тренировок у больных ИБС, ассоциированной с тяжелыми функциональными классами сердечной недостаточности, позволяет снизить не только количество неблагоприятных сердечно-сосудистых событий, но и улучшить качество жизни пациентов [1]. Вместе с тем, данных по применению Омакора у пожилых пациентов с ИБС и ХСН, перенесших ИМ, недостаточно, а в длительные программы реабилитации, включающие физические тренировки, такие пациенты, как правило, не включались.
Техническим результатом предлагаемого изобретения является повышение эффективности способа реабилитации пожилых пациентов ИБС с хронической сердечной недостаточностью, перенесших ИМ, что позволит улучшить качество жизни и снизить риск развития неблагоприятных сердечно-сосудистых событий.
Технический результат достигается путем назначения в отдаленные сроки (через 6 и более месяцев) после перенесенного ИМ пожилым больным ИБС с хронической сердечной недостаточностью на фоне проведения контролируемых физических тренировок антиоксиданта Омакора в дополнение к основной терапии. Это дает возможность обеспечить более эффективные и безопасные подходы к проведению реабилитационных мероприятий у пожилых пациентов ИБС с ХСН, перенесших ИМ, за счет реализации: 1) защиты миокарда от токсического действия перекисного окисления, уменьшения гибели кардиомиоцитов (пути некроза и апоптоза); 2) антиишемического действия - улучшение как систолической, так и диастолической функции миокарда левого желудочка; 3) уменьшения повреждения эндотелия под воздействием стрессорных гемодинамических воздействий.
Отличительные признаки проявили в заявляемой совокупности новые свойства, явным образом не вытекающие из уровня техники в данной области и не очевидные для специалиста. Идентичной совокупности признаков в проанализированной литературе не обнаружено. Предлагаемое изобретение может быть использовано в здравоохранении.
Исходя из вышеизложенного, следует считать изобретение соответствующим условиям патентоспособности "Новизна", "Изобретательский уровень", "Промышленная применимость".
Способ осуществляют следующим образом.
Перед началом лечения определяют толерантность к физической нагрузке путем проведения велоэргометрической пробы (ВЭМ). Для этого пробу выполняют со скоростью педалирования 60 оборотов в 1 минуту, со ступенчатой, непрерывно возрастающей нагрузкой, начиная с 25 Вт с последующим ежеминутным увеличением нагрузки на 10 Вт до достижения критериев прекращения пробы, таких как:
- появление или усиление стенокардитической боли средней и выраженной интенсивности;
- бледность кожных покровов, цианоз (признаки гипоперфузии);
- устойчивая желудочковая тахикардия;
- подъем ST на 1 см и более (кроме VI и aVR);
- депрессия сегмента ST>=4 мм;
- нарастающая боль в груди;
- достижение расчетной максимальной или субмаксимальной ЧСС.
Через 6 месяцев после перенесенного ИМ, на фоне приема стандартной терапии, включающей прием аспирина в дозе 75 мг/сут, иАПФ (энап - в дозе от 5 до 40 мг/сут, подбирается индивидуально), диуретик (гипотиазид - в дозе от 12,5 до 75 мг/сут, подбирается индивидуально), α1β1β2-адреноблокатора (карведилол - в дозе от 6,25 до 50 мг/сут, подбирается индивидуально) за 60 минут до начала контролируемых физических тренировок (дозированной ходьбы) пациент принимает Омакор 1 раз в сутки на протяжении всей жизни.
Затем пациент выполняет дозированную ходьбу, начиная с 0,5 км в темпе ходьбы 70 шагов в минуту до 2 км в темпе 100-110 шагов в минуту на расстояние от 2 до 10 км, при этом пациент сам контролирует дальность и скорость ходьбы, исходя из своего удовлетворительного состояния, отсутствия ангинозных приступов, и того факта, что частота сердечных сокращений должна быть не более 60% от максимальной установленной по результатам ВЭМ. Каждые 3 месяца проводят контроль физического состояния пациента с использованием ВЭМ пробы, и при необходимости корригируют уровень физической нагрузки (исходя из полученных результатов ВЭМ).
Обследовано 68 больных ИБС с хронической сердечной недостаточностью через 6 и более месяцев после перенесенного ИМ в анамнезе (39 мужчин и 28 женщин) в возрасте от 60 до 77 лет (в среднем возрасте 65,3±6,8 лет). Методом простой рандомизации сформировано две группы: группа физических тренировок на фоне приема Омакора (согласно предложенному способу) - 35 больных (группа «Омакор+тренировки») на фоне приема аспирина в дозе 75 мг/сут, α1β1β2-адреноблокатора карведилола (в дозе, начиная с 6,125 мг/сут в два приема с последующим ее увеличением до максимально переносимой (в среднем 19,6±5,4 мг/сут), и АПФ энап (в дозе, начиная с 5 мг/сут до максимальной дозировки 40 мг/сут) и диуретик гипотиазид (в дозе, начиная с 12,5 мг/сут до максимальной дозировки 75 мг/сут) и группа сравнения без использования предложенного способа - 33 больных.
На каждого больного заполнялась специально разработанная клиническая карта. Все пациенты давали свое письменное информированное согласие для участия в исследовании. Состояние больных оценивали исходно и через 6 месяцев с анализом частоты комбинированной конечной точки, включавшей: летальность, инсульт, повторные госпитализации по поводу обострений ХСН, повторных ИМ. Кроме того, оценивалась систолическая функцию левого желудочка (по данным ЭХО КГ) и физическую толерантность по данным теста 6-минутной ходьбы. Дополнительно оценивали липидный спектр крови.
Критериями оценки хорошего антиишемического и гемодинамического эффектов предложенной методики считали: регресс симптомов ХСН, уменьшение частоты и тяжести стенокардии, снижение суточной потребности нитратов, повышение физической толерантности по результату теста 6-минутной ходьбы.
В исследование включили пациентов, состояние которых сохранялось стабильным в течение не менее 2-3-х недель на постоянной базовой терапии, включавшей дезагрегант, ингибитор АПФ, β-адреноблокатор, статин, диуретик и, при необходимости, антагонист альдостерона.
На момент включения в исследование пациенты обеих групп не различались по таким основным показателям, как возраст, пол, сопутствующая патология, тяжесть недостаточности кровообращения, получаемой медикаментозной терапии. После рандомизации, пациенты исследуемой группы в дополнении к стандартной терапии получали комплекс физической реабилитации по предложенной схеме и препарат Омакор.
Статистический анализ полученных цифровых данных проводили с использованием программы STATISTICA 6.0 (StatSoft, USA).
Результаты наблюдения пациентов исследуемых групп через 6 месяцев представлены в таблице 1. В группе пациентов, получавших препарат Омакор, на фоне контролируемых тренировок диагностировалось значительно меньше летальных исходов, инсультов и повторных инфарктов миокарда. При этом в исследуемой группе госпитализаций статистически значимо реже регистрировались повторные госпитализации по поводу декомпенсации ХСН и неблагоприятные сердечно-сосудистые события (11,4% vs 30,3%, р=0,029; 25,7% vs 57,6%, р=0,015 соответственно).
| Таблица 1Частота развития комбинированной конечной точки в исследуемых группах через 6 месяцев наблюдения | |||
| Показатели | Группа сравнения (n=33) | Группа «Омакор+тренировки» (n=35) | Р |
| Сердечно-сосудистая смерть | 3 (9,1%) | - | 0.217 |
| Инфаркт миокарда | 5 (15,2%) | 2 (5,7%) | 0.378 |
| Инсульт | 1 (3,0%) | - | 0.976 |
| Госпитализация с декомпенсацией ХСН | 10(30,3%) | 4(11,4%) | 0.029 |
| Общее число неблагоприятных сердечно-сосудистых событий | 19(57,6%) | 6(17,1%) | 0.001 |
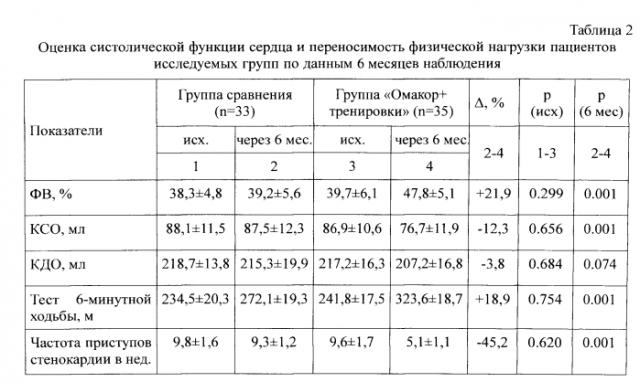
По данным ЭХО-КГ выявлено, что в группе физических тренировок на фоне приема Омакора достигнуто значительное (на 20,4%, р=0,001) увеличение фракции выброса ЛЖ и явное (на 11,7%, р=0,001) снижение конечного систолического объема ЛЖ. В этой же группе отмечалось значительное увеличение переносимости физических нагрузок и уменьшение количества приступов стенокардии в неделю - на 33,8% (р=0,001) (таблица 2).
Кроме того, выявлено существенное антиатерогенное действие предложенной методики, а именно: снижение уровня общего холестерина крови на 23% (р=0,001), снижение содержания атерогенных липопротеидов низкой плотности (ЛПНП) и триглицеридов на 23 и 28% (р=0,001) соответственно, увеличение содержания антиатерогенных липопротеидов высокой плотности (ЛПВП) - на 11,6% (р=0,001) (таблица 3).
Таким образом, через 6 и более месяцев после перенесенного ИМ, прием за 60 минут до начала контролируемых физических тренировок антиоксиданта - препарата ω-3 ПНЖК - Омакор на фоне стандартной медикаментозной терапии пожилыми пациентами ИБС с хронической сердечной недостаточностью, позволил обеспечить достоверное снижение частоты повторных госпитализаций по поводу прогрессирования ХСН и общего количества неблагоприятных сердечно-сосудистых событий. Кроме того, было зарегистрировано значительное улучшение клинического течения ИБС и ХСН: отмечено меньшее количество приступов стенокардии в неделю, улучшение переносимости физической нагрузки и улучшение систолической функции сердца. Каких-либо негативных коронарогенных или гемодинамических эффектов установлено не было.
Предлагаемый способ реабилитации пожилых больных ИБС с хронической сердечной недостаточностью, перенесших ИМ, иллюстрируется следующими клиническими примерами.
Пример 1 (2013 г.). Пациент К., 67 лет, поступил в плановом порядке в терапевтическое отделение с диагнозом: ИБС: стенокардия напряжения II ФК. Постинфарктный (2009) кардиосклероз. НК IIА. ХСН ФК III (NYHA).
При поступлении предъявлял жалобы на одышку по типу «нехватки воздуха» при незначительной физической нагрузке, общую слабость и учащенное сердцебиение.
Объективно: общее состояние больного средней степени тяжести за счет декомпенсации ХСН. Положение активное. Телосложение правильное. Конституция нормостеническая. Питание нормальное. Кожные покровы чистые, нормальной влажности, бледные, диффузный цианоз. Лимфоузлы не увеличены. Трофические изменения обеих голеней (индурация). Варикозное расширение вен н/конечностей. Костно-мышечный аппарат без видимых изменений Число дыхательных движений 20 в минуту. Ритм правильный. Дыхание через нос свободно. Вены шеи не расширены. Перкуторный звук над легкими ясный, легочный. Дыхание везикулярное с жестким оттенком. Выслушивалось небольшое количество сухих хрипов. Область сердца не изменена. Верхушечный толчок в V межреберье по средне-ключичной линии. Сердечный толчок не определяется. Тоны сердца глухие. Ритм сердечных сокращений правильный. ЧСС 85 ударов в 1 минуту. В клиническом анализе крови признаки анемии легкой степени тяжести (Нв 117 г/л, эр 3,98×109/л). В клиническом анализе мочи без патологических изменений. При ЭХО КГ исследовании небольшое расширение полости ЛЖ. Гипо- и акинез верхушки. ФВ ЛЖ 46%, Аорта уплотнена - 36 мм (табл.4).
| Таблица 4Показатели ЭХО КГ и липидного спектра пациента К. | ||
| Показатели | Госпитальный этап | 3 месяца |
| ЭХО-КГ | ||
| КДР ЛЖ (см) | 6,2 | 5,7 |
| КСР ЛЖ (см) | 4,67 | 4,2 |
| ЛП (см) | 4,1 | 4,1 |
| МЖП (см) | 1,2 | 1,1 |
| ЗСЛЖ (см) | 1,2 | 1,1 |
| ФВ (%) | 46 | 51 |
| Липидный спектр | ||
| ОХС (ммоль/л) | 6,7 | 5,4 |
| ТГ (ммоль/л) | 1,4 | 1,0 |
| ЛПНП (ммоль/л) | 4,63 | 3,8 |
| ЛПВП (ммоль/л) | 1,02 | 0,8 |
В условиях стационара была назначена терапия: бисопролол 5 мг, эналаприл 2,5 мг × 2 раза в сутки, утром и вечером; аспирин-кардио 100 мг в обед, плавике 75 мг утром, верошпирон 25 мг × 4 раза в сутки, аторвастатин 40 мг на ночь. К индивидуально подобранным дозам препаратов с первых суток госпитализации, был добавлен препарат омега-3-жирных кислот (Омакор) в дозе 1000 мг/сутки. К моменту выписки пациента из стационара по данным ЭХО КГ зарегистрирована положительная динамика в виде прироста показателя ФВ 51% (на 10,9%) Через 10 суток после выписки из стационара в плановом порядке была проведена ВЭМ проба: ТФН - 75 Вт, субмаксимальная частота сердечных сокращений - 98 ударов в минуту. В дальнейшем пациенту было рекомендовано проводить дозированную ходьбу с 0,5 км в темпе ходьбы 70 шагов в минуту до 2 км в темпе 100-110 шагов в минуту на расстояние от 2 до 10 км, при этом он сам должен контролировать дальность и скорость ходьбы исходя из своего удовлетворительного состояния, отсутствия ангинозных приступов, и того факта, что частота сердечных сокращений должна быть не более 60% от максимальной установленной. Через 3 месяца при повторном проведении ВЭМ выявлена положительная динамика в виде увеличения ТФН до 125 Вт и прироста субмаксмимальной ЧСС с 98 уд. в минуту до 116 уд. в минуту.
ПРИМЕР 2 (2013 г.). Пациент Д., 71 год, пенсионер. Поступил в терапевтическое отделение с диагнозом: ИБС: стенокардия напряжения II ФК. Постинфарктный (2012 г.) кардиосклероз. Пароксизмальная форма ФП. Редкая суправентрикулярная экстрасистолия. Пароксизмальная наджелудочковая тахикардия. НК II А, ХСН ФК III (NYHA). Гипертоническая болезнь III ст. Риск 4.
При поступлении жалобы на повышение АД до 170/90 мм рт.ст., сопровождавшееся головокружением, головной болью, шаткостью при ходьбе, снижением концентрации внимания; на одышку по типу "нехватки" воздуха при незначительной ФН - наклоны туловища, самообслуживание; кашель, без мокроты, "свисты" в груди, отеки голеней. Настоящее ухудшение в самочувствии в виде вышеописанных жалоб в течение недели.
Объективно: состояние средней степени тяжести, за счет декомпенсации ХСН. Положение активное. Телосложение правильное. Конституция нормостеническая. Питание повышенное. Сознание ясное. Кожные покровы чистые, нормальной влажности. Лимфатические узлы - б/о. Щитовидная железа не пальпируется. Костно-мышечная система - визуально не изменена. Перкуторно над всеми легочными полями ясный легочный звук. Дыхание в легких везикулярное, ослабленно по задней поверхности грудной клетки с двух сторон, хрипов нет. Частота дыхательных движений 19 в минуту. Органы пищеварения: язык влажный, чистый. Живот при пальпации мягкий, безболезненный. Печень пальпируется. (+) 4-5 см из-под реберной дуги, край гладкий, заострен, слабо болезненная, плотно-эластичная. Пузырные симптомы отрицательные. Стул - ежедневно, оформленный. Область сердца не изменена. Верхушечный толчок в V межреберье на 1 см кнутри от средне-ключичной линии. Сердечный толчок не определяется. Тоны сердца ритмичные, приглушенные. Шумов нет. АД 150/70 мм рт.ст; частота сердечных сокращений 80 в минуту. Мочеполовая система: поясничная область визуально не изменена. Почки не пальпируются. См поколачивания отрицательный с обеих сторон. Диурез не учащен, безболезненный. Пастозность стоп и нижней трети голеней. Варикозное расширение вен голеней. При ЭХО КГ исследовании выявлено незначительное расширение ЛП. Гипертрофии миокарда не выявлено. Сократительная способность ЛЖ снижена (ФВ - 50%). Гипо-акинезия заднего и задне-базального сегментов ЛЖ. Атеросклероз аорты, створок АоК. Створки МК уплотнены. МК и ТК недостаточность. Диастолическая дисфункция ЛЖ - 1 тип (табл.5).
| Таблица 5Показатели ЭХО КГ и липидного спектра пациента Д. | ||
| Показатели | Госпитальный этап | 3 месяца |
| ЭХО КГ | ||
| КДР ЛЖ (см) | 5,5 | 5,7 |
| КСР ЛЖ (см) | 4,06 | 4,1 |
| ЛП (см) | 4Д | 4,2 |
| МЖП (см) | 1,06 | 1,1 |
| ЗСЛЖ (см) | 1,06 | 1,1 |
| ФВ (%) | 50 | 52 |
| Липидный спектр | ||
| ОХС (ммоль/л) | 5,9 | 5,6 |
| ТГ (ммоль/л) | 2,5 | 2,2 |
| ЛПНП (ммоль/л) | 4,7 | 4,02 |
| ЛПВП (ммоль/л) | 0,8 | 1,01 |
В стационаре была назначена терапия: амлодипин 5 мг × 1 раз в день, аспирин-кардио 100 мг × 1 раз в день, диувер 10 мг × 1раз в сутки, зилт 75 мг × 1р/сутки, эналаприл 5 мг × 2раза в день, конкор 5 мг × 1 раз в день, аторвастатин 40 мг на ночь.
В условиях стационара физические тренировки не проводились в связи с декомпенсацией гипертонической болезни. Из стационара выписан на 11-е сутки с положительной динамикой в виде стабилизации АД в пределах целевых уровней, улучшения общего состояния, купирования головной боли, головокружения, отсутствия признаков нарастания сердечной недостаточности: уменьшения одышки при физической нагрузке, купирования отеков нижних конечностей. Через 14 суток после выписки из стационара в плановом порядке был проведен Тредмил - тест: ТФН - 50 Вт, субмаксимальная частота сердечных сокращений - 112 ударов в минуту.
Через 3 месяца при повторном проведении тредмил-теста была выявлена слабо положительная динамика в виде незначительного увеличения ТФН до 60 Вт и отсутствие статистически значимого прироста субмаксмимальной ЧСС с 112 уд. в минуту до 116 уд. в минуту. При контроле динамики липидограммы: уровень общего холестерина, уровень ЛПНП, ТГ достоверно значимо не изменился. По ЭХО КГ достоверного улучшения показателей внутрисердечной гемодинамики выявлено не было.
Таким образом, назначение препарата ω-3 ПНЖК Омакор за 60 минут до начала контролируемых физических тренировок в виде дозированной ходьбы на фоне стандартной медикаментозной терапии у пожилых больных ИБС с ХСН, в отдаленные сроки (через 6 и более месяцев) после перенесенного ИМ, увеличивает толерантность к физическим нагрузкам, обеспечивает положительные изменения показателей ЭХО КГ и липидного спектра крови и снижение общего количества неблагоприятных сердечно-сосудистых событий, способствует снижению темпов прогрессирования ХСН.
Предлагаемый способ применен у 33 пациентов и позволяет повысить эффективность реабилитации пожилых больных ИБС с хронической сердечной недостаточностью, перенесших ИМ, за счет реализации антиангинального, противоишемического и гемодинамического эффектов.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
1) Piepoli M.F., Davos С, Francis D.P. et al. Exercise training meta-analysis of trials in patients with chronic heart failure (ExTraMATCH) // BMJ. - 2004. - Vol.328. - P. 189.
2) Dickstein K, Cohen-Solal A, Filippatos G, McMurray JJ, Ponikowski P, Poole-Wilson PA, et al. ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2008: the Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2008 of the European Society of Cardiology. Eur Heart J. - 2008. - №29. - 2388-2442.
3) Catherine De Maeyer, Paul Beckers, et al. Exercise Training in Chronic Heart Failure // Ther Adv Chronic Dis. - 2013. - 4(3). - 105-117.
4) Кардиореабилитация: практическое руководство. Под ред. Дж. Ниебауэра. - пер. с англ., под ред. Ю.М.Позднякова. - М.: Логосфера, 2012. - 328 с (с.101).
5) Николаева Л.Ф., Аронов Д.М. ЛФК при инфаркте миокарда и хронической ишемической болезни сердца // Лечебная физическая культура / Под ред. В.А.Епифанова. - 2-е изд. - М., 2002.
6) Перуцкий Д.Н., Макеева Т.И., Константинов С.Л. Основные концепции постинфарктного ремоделирования миокарда левого желудочка. НАУЧНЫЕ ВЕДОМОСТИ. Серия Медицина. Фармация. - 2011. - 10(105). - Вып.14. - 51-59.
7) Безденежных А.В. Использование пассивных мышечных тренировок в комплексной реабилитации при инфаркте миокарда у пожилых больных. Автореферат канд. дисс. - 2011. - 23 с.
8) Патент на изобретение № RU 2329780 от 20.07.2006. Автор(ы): Баховудинова О.В., Зайцев Н.М., Авдонченко Т.С., Тарасов Н.И., Гзогян М.Н. Патентообладатель(и): ОАО Санаторий «Прокопьевский».
9) Национальные рекомендации ОССН, РКО и РНМОТ по диагностике и лечению ХСН (четвертый пересмотр). ISSN 1728-4651. Журнал Сердечная недостаточность. - Том 14. - №7(81). - 472 С.
10) Arena R., Myers J., Abella J. et al. The partial pressure of resting end-tidal carbon dioxide predict major cardiac events in patients with systolic heart failure. Am J Cardiol. - 2008. - Vol.156. - 982-988.
11) Green P., Lund L.H., Mancini D. Comparison of Peak Exercise Oxygen Consumption and the Heart Failure Survival Score for Predicting Prognosis in Women Versus Men. Am J Cardiol. -2007. - Vol.99. - 399 - 403.
12) Macchia A, Levantesi G, Franzosi MG, et al., for the GISSI-Prevenzione Investigators. Left ventricular systolic dysfunction, total mortality, and sudden death in patients with myocardial infarction treated with n-3 polyunsaturated fatty acids. EurJ Heart Fail. - 2005. - Vol.7. - 904-09.
13) Finzi, A. A. Effects of n-3 polyunsaturated fatty acids on malignant ventricular arrithmias in patients with chronic heart failure and implantable cardioverter-defibrillation: a Substady GISSI-HF / A. A Finzi, R. Latini, S. Barlera at al. Am. Heart J. - 2011. - Vol.161. - P. 338-343.
14) Poole CD., Halcox J.P., Jenkins-Jones S., Carr E.S., Schifflers M.G., Ray K.K., Currie C.J. Omega-3 Fatty acids and mortality outcome in patients with and without type 2 diabetes after myocardial infarction: a retrospective, matched-cohort study. Clin Ther. - 2013. - Vol.35(1). - 40-51. doi: 10.1016/j.clinthera.2012.11.008. Дата обращения 23.06.14 г.
Способ реабилитации пожилых пациентов ишемической болезнью сердца с хронической сердечной недостаточностью, перенесших инфаркт миокарда, заключающийся в проведении физических тренировок посредством дозированной ходьбы на фоне стандартной медикаментозной терапии дезагрегантами, β1-адреноблокаторами, диуретиками и ингибиторами АПФ, отличающийся тем, что при проведении дозированной ходьбы через 6 и более месяцев после перенесенного инфаркта миокарда за 60 минут до начала физических тренировок пациентам назначают препарат омега-3-полиненасыщенных жирных кислот (Омакор).