Способ определения вероятности сохранения миокарда от инфарктного повреждения у больных с острым коронарным синдромом
Иллюстрации
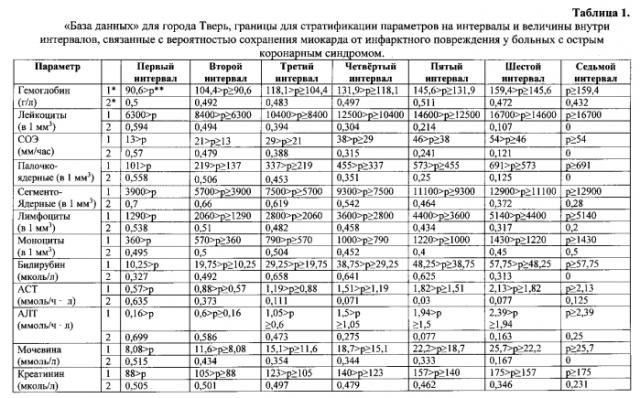
Показать всеИзобретение относится к кардиологии и представляет собой способ определения вероятности сохранения миокарда от инфарктного повреждения, для чего создается «база данных» на основе исследования на момент поступления 7 параметров периферической крови, 11 параметров биохимического анализа крови и 6 параметров стандартной 12-канальной электрокардиограммы у 200 больных с Q-инфарктом миокарда и 200 больных, у которых развитие инфаркта миокарда не происходило. Параметры стратифицируют соответственно 7 интервалам, в которых путем расчета отношения больных, у которых не развивается инфаркт миокарда, ко всем больным с острым коронарным синдромом находят величины, связанные с вероятностью сохранения миокарда от инфарктного повреждения. Расчет вероятности у конкретного больного осуществляют путем исследования указанных выше параметров, поиска в «базе данных» соответствующих интервалов и величин, связанных с вероятностью сохранения миокарда. Суммируя найденные величины, рассчитывают интегральный показатель, который нормализуют, приводят к размерности от 0 до 100%. Изобретение позволяет повысить точность прогноза сохранения миокарда у больных с острым коронарным синдромом. 1 табл., 2 пр.
Реферат
Изобретение относится к медицине, а именно к кардиологии.
Известен способ определения невысокого риска развития инфаркта миокарда при нестабильной стенокардии (Шамсеев М.Р., Бондарева З.Г., Аронов Е.А. и др. Острый коронарный синдром: диагностическая и прогностическая ценность тропонина I и кардиоспецифических ферментов. Бюллетень СО РАМН №3(109), 2003 г.) по регистрации уровня тропонина I ниже 2 ng/ml. Недостатком указанного способа является отсутствие числовой информации о величине риска инфарктного повреждения, что затрудняет разработку правильной лечебной тактики.
Также известен способ прогнозирования осложнений больного инфарктом миокарда (патент РФ №2197173), в котором по данным первых суток протекания инфаркта миокарда с учетом самого неблагоприятного признака, артериальной гипотонии, а также инсульта в анамнезе, одышки в 1-е сутки при частоте дыхания до 2-х в мин, менее или более 26 дыханий в мин, с учетом развития полной атриовентрикулярной и внутрижелудочковой блокады в 1-е сутки инфаркта миокарда, средней элевации сегмента ST после тромболитической терапии и величины постоянного члена регрессионного уравнения проводится анализ на персональном компьютере. Причем, если при решении полученных дискриминантных уравнений, достоверность или общий процент корректности которых составил 95,6%, значение первого уравнения для выживших пациентов будет больше, то с вероятностью 96,8% определяют, что данный больной переживет острый период заболевания, а если будет больше значение второго уравнения, то с вероятностью 78,6% прогнозируют, что наступит летальный исход в остром периоде инфаркта миокарда. Недостатками указанного способа являются трудность и недостаточная достоверность диагностики инфаркта миокарда в первые сутки наблюдения, а также приравнивание всех больных по вероятности благоприятного исхода в случае превышения значения первого уравнения над значением второго, что затрудняет подбор врачебной тактики.
Также известен способ диагностики у лиц с ишемической болезнью сердца возможного (субклинического) инфаркта миокарда или приверженности к нему (заявка на патент РФ №2004134078/14). Причем используются анамнестические величины, выраженные в баллах, и рассчитывается диагностический показатель на основе 20 величин. При значении диагностического показателя, равного 1 или меньше 1, судят об отсутствии инфаркта миокарда и отсутствии возможной перспективы его развития в ближайшем будущем. Недостатком указанного способа является приравнивание по вероятности сохранения сердечной стенки от инфарктного повреждения всех больных с диагностическим показателем менее 1 и равного 1, что затрудняет принятие решения о необходимости госпитализации в кардиологическое отделение при динамическом наблюдении за больным.
В качестве прототипа авторы предлагают способ определения риска развития инфаркта миокарда у больных с острым коронарным синдромом (патент РФ №2488111), в котором у больных с острым коронарным синдромом при исследовании 7 параметров периферической крови, 11 параметров биохимического анализа крови и 6 параметров стандартной 12-канальной электрокардиограммы с помощью «базы данных» находят величины, связанные с риском развития инфаркта миокарда. Далее, суммируя величины, связанные с риском, рассчитывают интегральный показатель. Интегральный показатель нормализуют, приводят к размерности от 0 до 100%.
Недостатком прототипа является отсутствие дублирующей прогностической системы, подтверждающей или опровергающей полученный прогноз.
Авторы предлагают способ определения вероятности сохранения миокарда от инфарктного повреждения у больных с острым коронарным синдромом на основании определения 7 показателей периферической крови: концентрации гемоглобина, содержания лейкоцитов, палочкоядерных нейтрофилов, сегментоядерных нейтрофилов, лимфоцитов и моноцитов в 1 мм3, скорости оседания эритроцитов, 11 параметров биохимического анализа: активности аспартатаминотрасферазы и активности аланинаминотрасферазы, протромбинового индекса, содержания в плазме крови билирубина, мочевины, креатинина, β-липопротеидов, общего белка, фибриногена, общего холестерина, глюкозы, и 6 показателей стандартной 12-канальной электрокардиограммы: разности квадратов максимального и минимального RR интервалов, угла альфа, длительности зубца Р, длительности интервала PQ, длительности комплекса QRS, длительности интервала QT.
Методика проведения исследования: определение уровня гемоглобина производится гемихромным методом по Пупковой В.И. и соавт. (1998); определение количества лейкоцитов в единице объема периферической крови - унифицированным методом подсчета в автоматическом счетчике, скорость оседания эритроцитов - капиллярным унифицированным микрометодом Панченкова (1972). Методика проведения исследования: изучение морфологического состава крови производится с помощью микроскопии мазков, окрашенных по Романовскому-Гимзе; определение количества палочкоядерных, сегментоядерных нейтрофилов, лимфоцитов и моноцитов при подсчете лейкоцитарной формулы по Гаркави Л.Х. и соавт. (1999). Определение концентрации билирубина в сыворотке крови проводили колориметрическим методом с диазореагентом. Для определения активности аспартатаминотрасферазы и аланинаминотрасферазы пользовались колориметрическим динитрофенилгидразиновым методом исследования активности аминотрасфераз в сыворотке крови (по Райтману, Френкелю, 1957). Определение концентрации мочевины и креатинина в сыворотке крови проводили по цветной реакции с диацетилмонооксимом и по цветной реакции Яффе (методом Поппера и соавт., 1937) соответственно (1972), содержание общего белка - колориметрическим методом с биуретовым реактивом. Уровень общего холестерина в сыворотке крови определяли унифицированным методом Илька по реакции с уксусным ангидридом (реакция Либермана-Бурхардта), содержание β-липопротеидов - при электрофоретическом разделении липопротеинов сыворотки крови в агаровом геле с использованием электрофоретической системы и наборов реагентов фирмы «Кормэй». Концентрация фибриногена определялась гравиметрическим методом по Рутбергу (1974). Концентрацию глюкозы в крови определяли унифицированным глюкозооксидазным методом по окислению о-толидина (1974), протромбиновый индекс - по Квику. Определение показателей 12-канальной ЭКГ производили при ее регистрации на аппаратно-программном комплексе «КАД-03» («ДНК и К», Тверь).
С помощью ПЭВМ ретроспективному анализу подвергают 7 параметров клинического анализа крови, 11 биохимических параметров и 6 параметров стандартной 12-канальной электрокардиограммы (ЭКГ) на момент поступления у 400 пациентов с острым коронарным синдромом (ОКС), у 200 из которых при последующем наблюдении в течение двух недель установлен диагноз Q-образующего инфаркта миокарда, а у других 200 - инфаркт миокарда не развивался и установлен диагноз прогрессирующей стенокардии. По каждому параметру показатели больных инфарктом миокарда (ИМ) и показатели больных нестабильной стенокардией (НС) объединяют в единые числовые ряды. Объединенные числовые ряды сортируют, в них определяют максимальные и минимальные числовые значения и разности между ними. Путем деления полученных разностей на число 4 рассчитывают шаги стратификации для каждого параметра. Путем последовательного суммирования с минимальным числовым значением или одного, или двух, или трех шагов стратификации рассчитывают начальные границы, отделяющие первый, второй, третий и четвертый начальные интервалы каждого параметра. Размер шага стратификации делят на число 4. Путем расчета разности начальной границы с одной четвертой шага стратификации, а также расчета суммы начальной границы с одной четвертой шага стратификации рассчитывают 6 окончательных границ каждого параметра, отделяющие первый, второй, третий, четвертый, пятый, шестой и седьмой окончательные интервалы параметров, включавших также и границу, отделяющую минимальное значение интервала. Число больных НС (больных с ОКС, у которых не развивался ИМ) найденное соответственно начальному интервалу, делят на число больных с острым коронарным синдромом (сумму больных с НС и ИМ), найденное в соответствующем интервале. Результат деления обозначают термином «величина, связанная с вероятностью сохранения миокарда от инфарктного повреждения у больных с ОКС» (величина, связанная с вероятностью СМИП). В первом, третьем, пятом и седьмом окончательных интервалах величины, связанные с вероятностью СМИП, приравнивают соответственно к таковым в первом, втором, третьем и четвертом начальных интервалах. Во втором окончательном интервале величину, связанную с вероятностью СМИП, рассчитывают как среднюю арифметическую величину первого и второго начальных интервалов, в четвертом окончательном - как среднюю арифметическую второго и третьего начальных интервалов, а в шестом окончательном - третьего и четвертого начальных интервалов. Тем самым формируют «базу данных» для конкретного региона. «База данных» для города Тверь, т.е. границы интервалов и величин внутри интервалов, связанных с вероятностью СМИП, представлена в таблице 1.
В «базе данных» у всех 400 больных с ОКС независимо от дальнейшей его трансформации рассчитывают суммы величин, связанных с вероятностью СМИП, т.е. интегральные показатели вероятности. Определяют максимальное и минимальное значения интегрального показателя. Максимальное значение интегрального показателя, найденное в «базе данных», - 12,996; минимальное - 9,063.
Расчет вероятности СМИП строят на отслеживании доли случаев, в которых не развивалось инфарктное повреждение стенки сердца за 2 недели, среди больных ОКС, аналогичных по симптоматике. Т.к. накопление информации о сохранении миокарда от инфарктного поражения среди аналогичных по симптоматике больных ОКС связано со значительными трудностями, для расчета вероятности применяют суммирование долей случаев, определяемых на основе сопоставления числа больных, у которых не развился ИМ, ко всем больным с ОКС внутри интервала параметра. Таким образом, достигалось возникновение действия закона больших чисел и появления закономерной величины в результате суммирования большого числа случайных величин.
Поэтому алгоритм определения вероятности СМИП у конкретного больного в способе заключается в следующих действиях. Во-первых, определяют величины, связанные с вероятностью СМИП, т.е. на основе результата клинического и биохимического анализа крови, стандартной 12-канальной ЭКГ у конкретного больного осуществляют поиск в «базе данных» соответствующего интервала и соответствующего числового значения величины, связанной с вероятностью СМИП. Во-вторых, проводят суммирование величин, связанных с вероятностью СМИП, и определение суммированием интегрального показателя. В-третьих, осуществляют нормализацию интегрального показателя, т.е. перевод в шкалу измерения от 0% до 100% с учетом максимально разрешаемой медицинской погрешности в 5%. Считают, что минимальному значению интегрального показателя соответствует 5% вероятность, а максимальному значению - 95% вероятность. Числовой массив между 5% и 95% риском используют как шкалу оценки вероятности, причем, 1% вероятности соответствует величина 1:
где max - максимальное значение интегрального показателя в «базе данных», a min - минимальное его значение.
Для перевода значения интегрального показателя в вероятность сохранения миокарда у конкретного пациента с ОКС используют формулу 2:
где max - максимальное значение интегрального показателя в «базе данных», min - минимальное его значение, вероятность - вероятность СМИП у конкретного больного, а инт. пок. - числовое значение интегрального показателя у конкретного пациента.
При невозможности проведения какого-либо исследования, например при отсутствии реактивов, «база данных» редуцируют, т.е. для названного, неосуществленного исследования все величины, связанные с вероятностью СМИП, приравнивают к нулю. После этого в редуцированной «базе данных» находят значения максимальной и минимальной величины интегрального показателя. Например, при невозможности исследования протромбинового индекса максимальное значение интегрального показателя в редуцированной «базе данных» составляет 12,488, минимальное значение - 8,555. При невозможности исследования уровня содержания β-липопротеидов в сыворотке крови максимальное значение интегрального показателя в редуцированной «базе данных» составляет 12,451, минимальное значение - 8,569. Найденные в редуцированной «базе данных» максимальное и минимальное значения интегрального показателя и редуцированный интегральный показатель конкретного больного подставляют в формулу 2, при этом результат расчета в редуцированной «базе данных» незначительно, в пределах 5% погрешности, отличается от результата расчета по полной «базе данных».
В проведенном исследовании у больных, у которых в последующем не развивался инфаркт миокарда (первая группа), средняя величина вероятности СМИП на момент поступления составила величину 79,7±0,69%, у больных, у которых развивался инфаркт миокарда (вторая группа), средняя вероятность СМИП составила величину 56,7±1,15% (при сравнении с первой группой t=17,1). В первой группе у 114 пациентов (57% от входящих в группу) величина вероятности СМИП была больше или равнялась 80%), во второй группе только у 11 пациентов (5,5% от входящих в группу) вероятность СМИП была больше или равнялась 80%).
Далее проводят сопоставление вероятности СМИП и риска развития ИМ, определяемого по алгоритму патента №2488111, причем если вероятность СМИП определялась по редуцированной «базе данных», то редуцируют и «базу данных» из патента 2488111, находят максимальное и минимальное значения интегрального показателя редуцированной «базы данных» и для расчета используют формулу 2 описания изобретения. Для сопоставления первоначально суммируют величины вероятности СМИП и риска ИМ. Далее рассчитывают отличие суммы от 100%. Если отличие меньше 5%, величины погрешности, максимально разрешенной в медицине, то величину вероятности СМИП можно оставить без изменения. Если отличие составляет 5 и более процентов, то высчитывается средняя величина вероятности СМИП и результата расчета разности 100% и риска развития ИМ. Средняя величина в последующем используется как значение уточненного прогноза.
Заключительный этап сопоставления направлен на улучшение диагностики. Повышение риска развития инфаркта миокарда со снижением вероятности СМИП, при близости их суммы к 100% будет косвенно свидетельствовать об инфаркте миокарда. Снижение риска развития инфаркта миокарда с повышением вероятности СМИП при близости их суммы к 100%, будет косвенно свидетельствовать о нестабильной стенокардии. В то же время одновременное повышение риска развития ИМ и вероятности СМИП или их одновременное снижение, когда отличие их суммы от 100% составляет величину больше 10%, может заставить усомниться в правильности диагноза и, в частности, подвергнуть диагноз повторному анализу, а также предположить развитие заболеваний иной природы, имеющих сходную с острым коронарным синдромом клиническую картину, например, таких, как перикардит, аортоартериит или поражение аорты атеросклеротического генеза.
Пример 1. Больной Л., 66 лет. При двухнедельном наблюдении и лечении в кардиологическом отделении у больного выявлена ИБС: впервые возникшая стенокардия напряжения ЗФК, осложненная сердечной недостаточностью IIA степени
На момент поступления у исследуемого:
уровень гемоглобина - 70 г/л; интервал 1; величина, связанная с вероятностью СМИП - 0,5;
содержание лейкоцитов - 4600 в 1 мм3; интервал 1; величина, связанная с вероятностью СМИП - 0,601;
скорость оседания эритроцитов - 5 мм/ч; интервал 1; величина, связанная с вероятностью СМИП - 0,57;
содержание палочкоядерных нейтрофилов - 230 в 1 мм3; интервал 3; величина, связанная с вероятностью СМИП - 0,453;
содержание сегментоядерных нейтрофилов - 2484 в 1 мм3; интервал 1; величина, связанная с вероятностью СМИП - 0,7;
содержание лимфоцитов - 1472 в 1 мм3; интервал 2; величина, связанная с вероятностью СМИП - 0,51;
содержание моноцитов - 368 в 1 мм3; интервал 2; величина, связанная с вероятностью СМИП - 0,5;
содержание в плазме крови общего билирубина - 19 ммоль/л; интервал 2; величина, связанная с вероятностью СМИП - 0,492;
активность аспартатаминотрасферазы - 0,33 ммоль/ч·л; интервал 1; величина, связанная с вероятностью СМИП - 0,635;
активность аланинаминотрасферазы - 0,41 ммоль/ч·л; интервал 2; величина, связанная с вероятностью СМИП - 0,586;
содержание в плазме крови мочевины - 5,6 ммоль/л; интервал 1; величина, связанная с вероятностью СМИП - 0,515;
содержание в плазме крови креатинина - 102 мкмоль/л; интервал 2; величина, связанная с вероятностью СМИП - 0,501;
содержание в плазме крови β-липопротеидов - 2700 мг/л; интервал 1; величина, связанная с вероятностью СМИП - 0,5;
содержание в плазме крови белка - 64 г/л; интервал 3; величина, связанная с вероятностью СМИП - 0,546;
протромбиновый индекс - 84%; интервал 5; величина, связанная с вероятностью СМИП - 0,529;
концентрация фибриногена - 2 г/л; интервал 1; величина, связанная с вероятностью СМИП - 0,511;
уровень общего холестерина - 5,1 ммоль/л; интервал 3; величина, связанная с вероятностью СМИП - 0,483;
концентрация в плазме крови глюкозы - 4 ммоль/л; интервал 1; величина, связанная с вероятностью СМИП - 0,488;
разность квадратов максимального и минимального RR-интервалов - 0 с2; интервал 1; величина, связанная с вероятностью СМИП - 0,567;
угол альфа - «плюс» 58°; интервал 5; величина, связанная с вероятностью СМИП - 0,599;
длительность зубца Р - 0,11 с; интервал 6; величина, связанная с вероятностью СМИП - 0,296;
длительность интервала PQ - 0,15 с; интервал 3; величина, связанная с вероятностью СМИП - 0,511;
длительность комплекса QRS - 0,09 с; интервал 2; величина, связанная с вероятностью СМИП - 0,507;
длительность интервала QT - 0,39 с; интервал 4; величина, связанная с вероятностью СМИП - 0,511.
Интегральный показатель, сумма величин, связанных с вероятностью СМИП, у больного Л. составляет величину 12,604. Подставив значение интегрального показателя в формулу 2, получаем величину вероятности СМИП в течение 2 недель:
вероятность=5+(12,604-9,063):(12,996-9,063)*90=86,0(%).
Проведем расчет риска развития ИМ у больного Л., 66 лет по алгоритму патента №2488111.
На момент поступления у исследуемого:
уровень гемоглобина - 70 г/л; интервал 1; величина, связанная с риском развития ИМ - 0,5;
содержание лейкоцитов - 4600 в 1 мм3; интервал 1; величина, связанная с риском развития ИМ - 0,399;
скорость оседания эритроцитов - 5 мм/ч; интервал 1; величина, связанная с риском развития ИМ - 0,425;
содержание палочкоядерных нейтрофилов - 230 в 1 мм3; интервал 1; величина, связанная с риском развития ИМ - 0,495;
содержание сегментоядерных нейтрофилов - 2484 в 1 мм3; интервал 1; величина, связанная с риском развития ИМ - 0,3;
содержание лимфоцитов - 1472 в 1 мм3; интервал 2; величина, связанная с риском развития ИМ - 0,479;
содержание моноцитов - 368 в 1 мм3; интервал 2; величина, связанная с риском развития ИМ - 0,488;
содержание в плазме крови общего билирубина - 19 ммоль/л; интервал 1; величина, связанная с риском развития ИМ - 0,521;
активность аспартатаминотрасферазы - 0,33 ммоль/ч·л; интервал 1; величина, связанная с риском развития ИМ - 0,355;
активность аланинаминотрасферазы - 0,41 ммоль/ч·л; интервал 1; величина, связанная с риском развития ИМ - 0,429;
содержание в плазме крови мочевины - 5,6 ммоль/л; интервал 1; величина, связанная с риском развития ИМ - 0,475;
содержание в плазме крови креатинина - 102 мкмоль/л; интервал 2; величина, связанная с риском развития ИМ - 0,516;
содержание в плазме крови β-липопротеидов - 2700 мг/л; интервал 1; величина, связанная с риском развития ИМ - 0,489;
содержание в плазме крови белка - 64 г/л; интервал 3; величина, связанная с риском развития ИМ - 0,448;
протромбиновый индекс - 84%; интервал 5; величина, связанная с риском развития ИМ - 0,462;
концентрация фибриногена - 2 г/л; интервал 1; величина, связанная с риском развития ИМ - 0,479;
уровень общего холестерина - 5,1 ммоль/л; интервал 3; величина, связанная с риском развития ИМ - 0,497;
концентрация в плазме крови глюкозы - 4 ммоль/л; интервал 1; величина, связанная с риском развития ИМ - 0,499;
разность квадратов максимального и минимального RR-интервалов - 0 с2; интервал 1; величина, связанная с риском развития ИМ - 0,458;
угол альфа - «плюс» 58°; интервал 5; величина, связанная с риском развития ИМ - 0,391;
длительность зубца Р - 0,11 с; интервал 6; величина, связанная с риском развития ИМ - 0,699;
длительность интервала PQ - 0,15 с; интервал 3; величина, связанная с риском развития ИМ - 0,476;
длительность комплекса QRS - 0,09 с; интервал 2; величина, связанная с риском развития ИМ - 0,482;
длительность интервала QT - 0,39 с; интервал 4; величина, связанная с риском развития ИМ - 0,478.
Интегральный показатель, сумма величин, связанных с риском развития ИМ, у больного Л. составляет величину 11,236. Подставив значение интегрального показателя в соответствующую формулу патента №2488111, получают величину риска развития ИМ в течение 2 недель:
Риск=5+(инт. пок.-10,927)*23,112=5+(11,236-10,927)*23,112=12,1%.
Далее сопоставляют вероятность СМИП и риск ИМ и суммируют указанные величины. 86+12,1=98,1%. Отличие суммы от 100% составляет 1,9% и меньше 5%. Поэтому величину вероятности СМИП оставляют без изменения, и она составляет 86%.
Допустим, что у больного Л. возникла невозможность проведения исследования протромбинового индекса. Тогда редуцированный интегральный показатель у больного Л. составит (см. 5 интервал для ПТИ) 12,604-0,529=12,075. Используя формулу 2 и подставив в нее значения максимального и минимального значений интегрального показателя из редуцированной «базы данных» (12,488 и 8,555), получают величину вероятности СМИП в течение 2 недель, незначительно отличающуюся от вероятности, рассчитанной по полной «базе данных»:
вероятность=5+(12,075-8,555):(12,488-8,555)*90=85,5(%).
Аналогично рассчитывают риск развития ИМ из редуцированной «базы данных» патента №2488111. Используя формулу 2 патента и подставив в нее значения максимального и минимального значения интегрального показателя из редуцированной «базы данных» (14,371 и 10,389), получают величину вероятности СМИП в течение 2 недель, незначительно отличающуюся от вероятности, рассчитанной по полной «базе данных»:
риск=5+(10,774-10,389):(14,381-10,389)*90=13,7(%).
Далее сопоставляют вероятность СМИП и риск ИМ и суммируют указанные величины. 85,5+13,7=99,2%. Отличие суммы от 100% составляет 0,8%, поэтому используют значение вероятности СМИП, равное 85,5%.
При невозможности проведения исследования уровня содержания β-липопротеидов в сыворотке крови редуцированный интегральный показатель у больного Л. составит (см. 1 интервал для β-липопротеидов) 12,604-0,5=12,104. Используя формулу 2, получают величину вероятности СМИП:
вероятность=5+(12,104-8,569):(12,451-8,569)*90=87,0(%).
Аналогично рассчитывают риск развития ИМ из редуцированной «базы данных» патента №2488111. Используя формулу 2 патента, получают риск ИМ:
риск=5+(10,747-10,432):(14,331-10,432)*90=13,3(%).
Далее сопоставляют вероятность СМИП и риск ИМ и суммируют указанные величины. 87,0+13,3=100,3%. Отличие суммы от 100% составляет 0,3%, поэтому используют значение вероятности СМИП, равное 87,0%.
У больного Л. сопоставление подтверждает диагноз нестабильной стенокардии.
Пример 2. Больной С., 55 лет. При двухнедельном наблюдении и лечении в кардиологическом отделении у больного выявлен инфаркт миокарда передне-перегородочной области левого желудочка с переходом на верхушку сердца, осложненный сердечной недостаточностью 3 ФК по Killip.
На момент поступления у исследуемого:
уровень гемоглобина - 158 г/л; интервал 6; величина, связанная с вероятностью СМИП - 0,472;
содержание лейкоцитов - 19800 в 1 мм3; интервал 7; величина, связанная с вероятностью СМИП - 0;
скорость оседания эритроцитов - 2 мм/ч; интервал 1; величина, связанная с вероятностью СМИП - 0,57;
содержание палочкоядерных нейтрофилов - 990 в 1 мм3; интервал 7; величина, связанная с вероятностью СМИП - 0;
содержание сегментоядерных нейтрофилов - 15642 в 1 мм3; интервал 7; величина, связанная с вероятностью СМИП - 0,28;
содержание лимфоцитов - 2178 в 1 мм3; интервал 3; величина, связанная с вероятностью СМИП - 0,482;
содержание моноцитов - 792 в 1 мм3; интервал 4; величина, связанная с вероятностью СМИП - 0,452;
содержание в плазме крови общего билирубина - 11 ммоль/л; интервал 2; величина, связанная с вероятностью СМИП - 0,492;
активность аспартатаминотрасферазы - 2,45 ммоль/ч·л; интервал 7; величина, связанная с вероятностью СМИП - 0,125;
активность аланинаминотрасферазы - 1,44 ммоль/ч·л; интервал 4; величина, связанная с вероятностью СМИП - 0,275;
содержание в плазме крови мочевины - 11,3 ммоль/л; интервал 2; величина, связанная с вероятностью СМИП - 0,434;
содержание в плазме крови креатинина - 88 мкмоль/л; интервал 2; величина, связанная с вероятностью СМИП - 0,501;
содержание в плазме крови β-липопротеидов - 4400 мг/л; интервал 2; величина, связанная с вероятностью СМИП - 0,495;
содержание в плазме крови белка - 71 г/л; интервал 4; величина, связанная с вероятностью СМИП - 0,494;
протромбиновый индекс - 95%; интервал 6; величина, связанная с вероятностью СМИП - 0,491;
концентрация фибриногена - 5,75 г/л; интервал 6; величина, связанная с вероятностью СМИП - 0,142;
уровень общего холестерина - 6,2 ммоль/л; интервал 4; величина, связанная с вероятностью СМИП - 0,522;
концентрация в плазме крови глюкозы - 5 ммоль/л; интервал 1; величина, связанная с вероятностью СМИП - 0,488;
разность квадратов максимального и минимального RR-интервалов - 0,682 с2; интервал 3; величина, связанная с вероятностью СМИП - 0,182;
угол альфа - «плюс» 30°; интервал 4; величина, связанная с вероятностью СМИП - 0,56;
длительность зубца Р - 0,08 с; интервал 2; величина, связанная с вероятностью СМИП - 0,474;
длительность интервала PQ - 0,17 с; интервал 4; величина, связанная с вероятностью СМИП - 0,478;
длительность комплекса QRS - 0,09 с; интервал 2; величина, связанная с вероятностью СМИП - 0,507;
длительность интервала QT - 0,39 с; интервал 4; величина, связанная с вероятностью СМИП - 0,511.
Интегральный показатель, сумма величин, связанных с вероятностью СМИП, у больного С. составляет величину 9,427. Подставив значение интегрального показателя в формулу 2, получаем величину вероятности СМИП в течение 2 недель:
вероятность=5+(9,427-9,063):(12,996-9,063)*90=13,3(%).
Далее проводят расчет риска развития ИМ у больного С., 55 лет по алгоритму патента №2488111.
На момент поступления у исследуемого:
уровень гемоглобина - 158 г/л; интервал 6; величина, связанная с риском развития ИМ - 0,534;
содержание лейкоцитов - 19800 в 1 мм3; интервал 7; величина, связанная с риском развития ИМ - 1;
скорость оседания эритроцитов - 2 мм/ч; интервал 1; величина, связанная с риском развития ИМ - 0,425;
содержание палочкоядерных нейтрофилов - 990 в 1 мм3; интервал 1; величина, связанная с риском развития ИМ - 0,495;
содержание сегментоядерных нейтрофилов - 15642 в 1 мм3; интервал 7; величина, связанная с риском развития ИМ - 0,711;
содержание лимфоцитов - 2178 в 1 мм3; интервал 3; величина, связанная с риском развития ИМ - 0,509;
содержание моноцитов - 792 в 1 мм3; интервал 4; величина, связанная с риском развития ИМ - 0,538;
содержание в плазме крови общего билирубина - 11 ммоль/л; интервал 1; величина, связанная с риском развития ИМ - 0,521;
активность аспартатаминотрасферазы - 2,45 ммоль/ч·л; интервал 7; величина, связанная с риском развития ИМ - 0,875;
активность аланинаминотрасферазы - 1,44 ммоль/ч·л; интервал 3; величина, связанная с риском развития ИМ - 0,845;
содержание в плазме крови мочевины - 11,3 ммоль/л; интервал 2; величина, связанная с риском развития ИМ - 0,554;
содержание в плазме крови креатинина - 88 мкмоль/л; интервал 1; величина, связанная с риском развития ИМ - 0,47;
содержание в плазме крови β-липопротеидов - 4400 мг/л; интервал 2; величина, связанная с риском развития ИМ - 0,495;
содержание в плазме крови белка - 71 г/л; интервал 4; величина, связанная с риском развития ИМ - 0,496;
протромбиновый индекс - 95%; интервал 6; величина, связанная с риском развития ИМ - 0,498;
концентрация фибриногена - 5,75 г/л; интервал 6; величина, связанная с риском развития ИМ - 0,845;
уровень общего холестерина - 6,2 ммоль/л; интервал 4; величина, связанная с риском развития ИМ - 0,468;
концентрация в плазме крови глюкозы - 5 ммоль/л; интервал 1; величина, связанная с риском развития ИМ - 0,499;
разность квадратов максимального и минимального RR-интервалов - 0,682 с2; интервал 2; величина, связанная с риском развития ИМ - 0,608;
угол альфа - «плюс» 30°; интервал 4; величина, связанная с риском развития ИМ - 0,428;
длительность зубца Р - 0,08 с; интервал 2; величина, связанная с риском развития ИМ - 0,511;
длительность интервала PQ - 0,17 с; интервал 4; величина, связанная с риском развития ИМ - 0,516;
длительность комплекса QRS - 0,09 с; интервал 2; величина, связанная с риском развития ИМ - 0,482;
длительность интервала QT - 0,39 с; интервал 4; величина, связанная с риском развития ИМ - 0,478.
Интегральный показатель, сумма величин, связанных с риском развития ИМ, у больного С. составляет величину 13,801. Подставив значение интегрального показателя в соответствующую формулу патента №2488111, получают величину риска развития ИМ в течение 2 недель у больного С.:
Риск=5+(инт. пок.-10,927)*23,112=5+(13,801-10,927)*23,112=71,4%ю
Далее сопоставляют вероятность СМИП и риск ИМ, суммируют указанные величины: 13,3+71,4=84,7%. Далее рассчитывают отличие суммы от 100%. Отличие составляет у больного С. 15,3% и больше чем 5%. Поэтому высчитывается средняя величина вероятности СМИП и разности 100% и риска развития ИМ: (13,3+100-71,4)/2=21,0%. Уточненное значение вероятности сохранения миокарда от инфарктного повреждения составляет у больного С. 21%.
Допустим, что у больного С. возникла невозможность проведения исследования протромбинового индекса. Тогда редуцированный интегральный показатель у больного С. составит 9,427-0,491=8,936. Используя формулу 2 и подставив в нее значения максимального и минимального значения интегрального показателя из редуцированной «базы данных» (12,488 и 8,555), получают величину вероятности СМИП:
вероятность=5+(8,936-8,555):(12,488-8,555)*90=13,7(%)
Аналогично рассчитывают риск развития ИМ из редуцированной «базы данных» патента №2488111. Используя формулу 2 патента и подставив в нее значения максимального и минимального значения интегрального показателя из редуцированной «базы данных» (14,371 и 10,389), получают величину риска развития ИМ:
риск=5+(13,303-10,389):(14,381-10,389)*90=70,9(%).
Далее сопоставляют вероятность СМИП и риск ИМ и суммируют указанные величины. 13,7+70,9=84,6%. Отличие суммы от 100% составляет 15,4%, поэтому используют среднее значение вероятности СМИП и разности 100% и риска ИМ, равное 21,4%.
При невозможности проведения исследования уровня содержания β-липопротеидов в сыворотке крови редуцированный интегральный показатель у больного С. составит 9,427-0,495=8,932. Используя формулу 2, получают величину вероятности СМИП:
вероятность=5+(8,932-8,569):(12,451-8,569)*90=13,4(%).
Аналогично рассчитывают риск развития ИМ из редуцированной «базы данных» патента №2488111. Используя формулу патента, получают риск ИМ:
риск=5+(13,306-10,432):(14,331-10,432)*90=71,3(%)
Далее сопоставляют вероятность СМИП и риск ИМ и суммируют указанные величины. 13,4+71,3=84,7%. Отличие суммы от 100% составляет 15,3%, поэтому используют среднее значение вероятности СМИП и разности 100% и риска ИМ, равное 21,1%.
У больного С. диагноз инфаркта миокарда должен быть подвергнут сомнению и повторному анализу.
Таким образом, по сравнению с прототипом заявленный способ обладает следующими преимуществами:
1. Сопоставление вероятности СМИП с риском развития инфаркта миокарда (патент №2488111) в случае раздельного формирования «баз данных» позволяет уточнять прогноз ОКС.
2. Способ позволяет рассчитать вероятность сохранения миокарда от инфарктного повреждения у каждого конкретного больного с острым коронарным синдромом и отслеживать ее в динамике даже в случае невозможности проведения у больного исследования какого-либо параметра, входящего в «базу данных».
Способ определения вероятности сохранения миокарда от инфарктного повреждения у больных с острым коронарным синдромом, включающий формирование «базы данных» на основе исследования у 200 больных с острым коронарным синдромом, у которых за двухнедельный срок не происходило развитие инфарктного повреждения миокарда, и исследования у 200 больных с острым коронарным синдромом, трансформирующимся за двухнедельный срок в Q-инфаркт миокарда, 7 показателей периферической крови: концентрации гемоглобина, содержания лейкоцитов, палочкоядерных нейтрофилов, сегментоядерных нейтрофилов, лимфоцитов и моноцитов в 1 мм3, скорости оседания эритроцитов, 11 параметров биохимического анализа: активности аспартатаминотрасферазы и активности аланинаминотрасферазы, протромбинового индекса, содержания в плазме крови билирубина, мочевины, креатинина, β-липопротеидов, общего белка, фибриногена, общего холестерина, глюкозы, и 6 показателей стандартной 12-канальной электрокардиограммы: разности квадратов максимального и минимального RR интервалов, угла альфа, длительности зубца Р, длительности интервала PQ, длительности комплекса QRS, длительности интервала QT; их стратификации соответственно 7 интервалам и расчета величин, связанных с вероятностью сохранения миокарда от инфарктного повреждения, определение максимального и минимального значений интегрального показателя в «базе данных», а также нахождение вероятности сохранения миокарда у конкретного больного с острым коронарным синдромом, для чего исследуют указанные выше 7 параметров периферической крови, 11 параметров биохимического анализа крови и 6 параметров стандартной 12-канальной электрокардиограммы, определяют по «базе данных» величины, связанные с вероятностью сохранения миокарда от инфарктного повреждения, суммируют их, т.е. рассчитывают интегральный показатель, и далее нормализуют интегральный показатель путем расчета суммы 5 и произведения 90 на отношение разности интегрального показателя у конкретного больного и минимального его значения в «базе данных» к разности максимального и минимального значений интегрального показателя в «базе данных»; отличающийся тем, что для нахождения в интервалах величин, связанных с вероятностью сохранения миокарда от инфарктного повреждения, рассчитывают отношение больных, входящих в интервал, у которых не развивался инфаркт миокарда, ко всем больным с острым коронарным синдромом, входящим в интервал; в случае невозможности проведения какого-либо исследования «базу данных» редуцируют, то есть для неисследованных параметров все величины, связанные с вероятностью сохранения миокарда, приравнивают к нулю, после этого в редуцированной «базе данных» находят значения максимальной и минимальной величин интегрального показателя, которые используют для нормализации.