Антагонисты пуринорецепторов на основе новых производных пиридоксина
Иллюстрации
Показать всеИзобретение относится к синтетическим биологически активным веществам гетероциклического ряда, обладающим антагонистической активностью по отношению к пуринорецепторам и представляющим собой продукты модификации пиридоксина, а именно n-(1,5-дигидро-3-R-8-метил-9-гидрокси-[1,3]диоксепино[5,6-c]пиридинил-6-азо)фенилсульфокислоты и их солевые формы общей формулы I, где R выбран из группы: атом водорода, этил, гептил или октил. Соединения формулы (I) обладают высокой антагонистической активностью по отношению к пуринорецепторам и могут найти применение в медицине и ветеринарии. 2 табл., 5 пр.
Реферат
Изобретение относится к синтетическим биологически активным веществам гетероциклического ряда, обладающим антагонистической активностью по отношению к пуринорецепторам и представляющим собой продукты модификации пиридоксина, а именно n-(1,5-дигидро-3-R-8-метил-9-гидрокси-[1,3]диоксепино[5,6-c]пиридинил-6-азо)фенилсульфокислоты и их солевые формы общей формулы I:
,
где R выбран из группы: атом водорода, этил, гептил или октил.
Соединения формулы (I) обладают высокой антагонистической активностью по отношению к пуринорецепторам (P2-рецепторы) и могут найти применение в медицине и ветеринарии.
P2 рецепторы представляют собой мишень для фармакологического воздействия и разработки новых лекарственных средств для лечения различных заболеваний. Разработка антагонистов P2-рецепторов является перспективным направлением современной химии и фармакологии. Наиболее важным доказательством огромного значения пуринергической нейротрансмиссии является внедрение в клиническую практику лекарственных средств, воздействующих на P2-рецепторы и успешно применяемых для лечения патологий сердечно-сосудистой системы [А.У. Зиганшин, P2-рецепторы: перспективная мишень для будущих лекарств / Зиганшин А.У., Зиганшина Л.Е. // Гэотар-Медиа, Москва - 2009].
Наиболее близким по химической структуре и назначению аналогом заявляемых веществ является PPADS (пиридоксальфосфат-6-азофенил-2′,4′-дисульфоновая кислота) - известный антагонист пуринорецепторов [J.B. Schachter, Second messenger cascade specificity and pharmacological selectivity of the human P2Y1-purinoreceptor / J.B. Schachter, Q. Li, J.L. Boyer, et al. // Br. J. PharmacoL, 118, 167-173 (1996).]. PPADS послужил основой для создания целого ряда антагонистов пуринорецепторов [N. Syed, Pharmacology of P2X receptors / N. Syed, Ch. Kennedy // WIREs Membr Transp Signal, - 2012, - V. 1, - c. 16-30.], при этом модификации затрагивали, в основном, бензольное кольцо, а в третьем-четвертом положениях пиридинового цикла присутствовали фосфатные, фосфонатные, амино- и альдегидные группы. Несмотря на значительное количество синтезированных производных PPADS, все они обладают целым рядом значительных недостатков, в том числе сложностью получения, связанной с необходимостью введения в структуру пиридоксина фосфатного фрагмента и альдегидной группы, вследствие чего задача по созданию новых эффективных антагонистов пуринорецепторов остается актуальной.
Следует отметить, что описанные выше соединения, по мнению заявителя, не могут рассматриваться в качестве аналогов к заявленному техническому решению вследствие того, что они не совпадают с заявляемыми соединениями по химической структуре. Заявителем не выявлены источники, содержащие информацию о технических решениях, идентичных настоящему изобретению, что позволяет сделать вывод о его соответствии критерию «новизна».
Задача заявленного технического решения состоит в создании новых биологически активных соединений с высокой антагонистической активностью в отношении пуринорецепторов.
Поставленная задача решается путем синтеза антагонистов пуринорецепторов общей формулы (I):
,
где R выбран из группы: атом водорода, этил, гептил или октил.
Заявляемые вещества общей формулы (I) могут применяться в виде нейтральных форм или в виде солей с катионами натрия, калия, лития, аммония, магния, кальция или другими фармакологически приемлемыми катионами.
В отличие от PPADS в заявляемых соединениях применяется ацетальная защита гидроксиметильных групп, что значительно упрощает их получение.
Наиболее близким по химическому строению и назначению к заявленным веществам является PPADS, который был выбран в качестве реперного соединения для сравнения антагонистической активности.
Заявляемые вещества проявили высокую антагонистическую активность в отношении P2X-рецепторов на гладкомышечных клетках мочевого пузыря и семявыносящего протока и могут найти применение в медицине и ветеринарии.
Заявителем не выявлены источники, в которых содержались бы сведения о влиянии отличительных признаков изобретения на достигаемый технический результат. Указанное новое свойство объекта - создание соединений с высокой антагонистической активностью в отношении пуринорецепторов обусловливает, по мнению заявителя, соответствие изобретения критерию «изобретательский уровень».
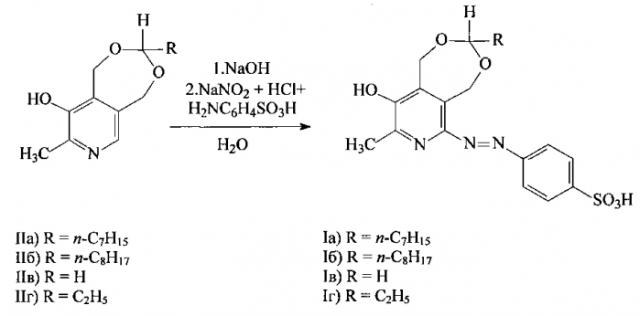
Предлагаемые в заявленном техническом решении соединения формулы (I) получали согласно нижеприведенным схемам:
Ацетали пиридоксина II(а-г) были получены по описанным в литературе методикам [Пат. РФ 2501801, МПК C07D 491/056. Производные пиридоксина с нелинейными оптическими свойствами. [Текст] / Штырлин Ю.Г., Петухов А.С., Стрельник. А.Д., Штырлин Н.В., Гарипов М.Р., Лодочникова О.А., Литвинов И.А., Морозов О.А., Ловчев А.В.; ВГАОУ ВПО К(П)ФУ. - Опубл. 20.12.2013].
Характеристики новых соединений и результаты исследования антагонистической активности в отношении пуринорецепторов (табл. 1, 2) приведены в примерах конкретного выполнения.
Примеры конкретного выполнения заявленного технического решения
Пример 1. Синтез n-(1,5-дигидро-3-гептил-8-метил-9-гидрокси-[1,3]диоксепино[5,6-c]пиридинил-6-азо)фенилсульфоновой кислоты (Ia)
В колбе на 50 мл готовили раствор диазосоединения из 0.005 моль сульфаниловой кислоты, 0.35 г (0,005 моль) нитрита натрия в 50 мл (0,01 моль) 0.2 н соляной кислоты при температуре 0-5°C. Отдельно готовили раствор 0.005 моль ацеталя IIa и 0.6 г (0,015 моль) гидроокиси натрия в 15 мл воды. К раствору натриевой соли ацеталя по каплям при перемешивании и охлаждении до 0-5°C добавили раствор диазосоединения. Реакционную смесь перемешивали при комнатной температуре 30 минут и нейтрализовали разбавленной соляной кислотой до pH 7.5. Реакционную массу сушили в вакууме досуха, продукт перекристаллизовывали из этилового спирта. Выход 40%. Т.разл. 225-226°C. ЯМР 1H (400 Мгц, ДМСО-d6): δ 0.87 (т, 3J=6.8 Гц, CH3, 3H); 1.23-1.37 (м, 5CH2, 10H); 1.58-1.63 (м, CH2, 2H); 2.19 (с, CH3, 3H); 4.54, 5.06 (AB-квартет, 2J=-15.0 Гц, CH2, 2H); 4.87 (т, 3J=5.5 Гц, CH, 1H); 4.98, 5.56 (AB-квартет, 2J=-14.8 Гц, CH2, 2H); 7.63 (с, C6H4, 4H). ESI-HRMS m/z 462.1700 [(M-H)-] (рассчитано для C22H28N3O6S - 462.1699).
Пример 2. Синтез n-(1,5-дигидро-3-октил-8-метил-9-гидрокси-[1,3]диоксепино[5,6-c]пиридинил-6-азо)фенилсульфоновой кислоты (Iб)
Синтезируют и разрабатывают аналогично соединению (Iа), используя ацеталь (IIб) вместо ацеталя (IIа). Выход 40%. Т.разл. 225-226°C. ЯМР 1H (400 МГц, DMSO-d6): δ 0.86 (т, 3J=6.7 Гц, CH3, 3H); 1.2-1.38 (м, 6CH2, 12H); 1.57-1.62 (м, CH2, 2H); 2.16 (с, CH3, 3H); 4.51, 5.05 (AB-квартет, 2J=-14.8 Гц, CH2, 2H); 4.88 (т, 3J=5.6 Гц, CH, 1H); 5.00, 5.56 (AB-квартет, 2J=-14.6 Гц, CH2, 2H); 7.63 (с, C6H4, 4H). ESI-HRMS m/z 476.1855 [(M-H)-] (рассчитано для C23H30N3O6S - 476.1855).
Пример 3. Синтез n-(1,5-дигидро-8-метил-9-гидрокси-[1,3]диоксепино[5,6-c]пиридинил-6-азо)фенилсульфоновой кислоты (Iв)
Синтезируют и разрабатывают аналогично соединению (Iа), используя ацеталь (IIв) вместо ацеталя (IIа). Выход 65%. Т.разл. 239-240°C. ЯМР 1H (400 МГц, DMSO-d6): δ 2.44 (с, CH3, 3H); 4.93 (с, CH2, 2H); 4.98 (с, CH2, 2H); 5.31 (с, CH2, 2H); 7.75, 7.82 (AB-квартет, 3J=8.4 Гц, C6H4, 4H). ESI-HRMS m/z 364.0603 [(M-H)-] (рассчитано для C15H14N3O6S - 364.0603).
Пример 4. Синтез n-(1,5-дигидро-3-этил-8-метил-9-гидрокси-[1,3]диоксепино[5,6-c]пиридинил-6-азо)фенилсульфоновой кислоты (Iг)
Синтезируют и разрабатывают аналогично соединению (Iа), используя ацеталь (IIг) вместо ацеталя (IIа). Выход 45%. Т.разл. 225-226°C. ЯМР 1H ЯМР 1H (400 МГц, DMSO-d6): δ 0.91 (т, 3J=7.2 Гц, CH3, 3H); 1.66 (м, CH2, 2H); 2.39 (с, CH3, 3H); 4.73, 5.09 (AB-квартет, 2J=-15.6 Гц, CH2, 2H); 4.91 (т, 3J=5.7 Гц, CH, 1H); 5.10, 5.51 (AB-квартет, 2J=-15.2 Гц, CH2, 2H); 7.72, 7.78 (AB-квартет, 3J=8.4 Гц, C6H4, 4H). ESI-HRMS m/z 392.0916 [(M-H)-] (рассчитано для C17H18N3O6S - 392.0916).
Пример 5. Исследование антагонистической активности синтезированных соединений по отношению к P2-рецепторам
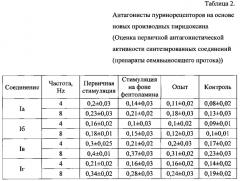
Исследование антагонистической активности синтезированных соединений по отношению к P2-рецепторам в концентрации 10-2 М изучали in vitro на самцах крыс линии Wistar массой 150-200 г (питомник «Пущино», Московская область). Все эксперименты выполнены в соответствии с правилами проведения работ с использованием экспериментальных животных. Применяли метод исследования механической активности изолированных органов [Зиганшин А.У., Зиганшина Л.Е. Фармакология рецепторов АТФ. - М.: Гэотар-Медицина, 1999. - 210 с]. Для изучения P2X-рецептор-опосредуемых сокращений объектами исследования являлись препараты мочевого пузыря и семявыносящего протока. Для сравнения активности исследуемых соединений в одних условиях во всех экспериментах оценивалась активность известного антагониста P2-рецепторов - PPADS (Tocris, Великобритания). Для исключения влияния холино- и адренорецепторов эксперименты проводились в присутствии M-холиноблокатора атропина и α-адреноблокатора фентоламина (Sigma, США). Проводилась стимуляция электрическим полем частотой 0,5-32 Гц. О величине антагонистической активности веществ судили по величинам сократительного ответа. Приведены результаты экспериментов, полученные при стимуляции частотой 4 и 8 Гц.
Изучение антагонистического действия синтезированных соединений показало наличие значительной активности в отношении пуринорецепторов у заявляемых веществ (см. Табл. 1, 2), не уступающей эффекту известного антагониста PPADS.
Заявителем не выявлены источники, содержащие информацию о технических решениях, идентичных настоящему изобретению, что позволяет сделать вывод о его соответствии критерию «новизна».
Производные пиридоксина, а именно n-(1,5-дигидро-3-R-8-метил-9-гидрокси-[1,3]диоксепино[5,6-c]пиридинил-6-азо)фенилсульфокислоты и их солевые формы, обладающие антагонистической активностью в отношении пуринорецепторов, общей формулы I: ,где R выбран из группы: атом водорода, этил, гептил или октил.