Новые вакцинные составы, включающие сапонинсодержащие адъюванты
Иллюстрации
Показать всеНастоящее изобретение раскрывает стабильную вакцинную композицию, включающую по меньшей мере один иммуноген, выбранный из инактивированного цирковируса свиней типа 2 (PCV-2), вируса ящура (FMDV) и бактерий; сапонин, гидроксид алюминия, неионные поверхностно-активные вещества с конечным ГЛБ эмульсии от около 9 до около 12. Изобретение сохраняет стабильность в течение коммерчески полезного периода времени. 10 з.п. ф-лы, 9 ил., 16 табл., 7 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к эмульсиям масло-в-воде, их применению в качестве адъювантов и к фармацевтическим, иммунологическим или вакцинным композициям, которые содержат данные эмульсии.
Включение ссылкой
Настоящей заявкой заявляется приоритет предварительной патентной заявки США №61/241171 от 10 сентября 2009 года, и дополнительно дается ссылка на следующие патентные заявки: патентная заявка США №12/027776 от 7 февраля 2008 года, патентная заявка США №10/899181 от 26 июля 2004 года, теперь является выданным патентом США 7371395, и предварительная патентная заявка США №60/490345 от 24 июля 2003 года. Вышеупомянутые заявки и все документы, процитированные в них или в ходе их рассмотрения («документы, процитированные в заявке») и все документы или ссылки в документах, процитированных в заявке, и все документы, процитированные или упоминаемые в данном документе («документы, процитированные в данном документе»), и все документы, процитированные или упомянутые в документах, процитированных в данном документе, вместе с какими-либо инструкциями производителя, описаниями, техническими описаниями изделия и технологическими картами для любых продуктов, упомянутых в данном документе, или в любом документе, включенном ссылкой в данный документ, настоящим включены в данный документ ссылкой, и могут быть использованы при практическом осуществлении изобретения.
Предшествующий уровень техники
Применение адъювантов в вакцинах хорошо известно. Адъювант представляет собой соединение, которое при объединении с вакцинным антигеном повышает иммунный ответ на вакцинный антиген по сравнению с ответом, индуцированным вакцинным антигеном отдельно. Среди стратегий, которые стимулируют иммуногенность антигена, есть те, в которых придают вакцинным антигенам дисперсную форму, те, в которых вакцинные антигены полимеризуют или эмульгируют, есть способы инкапсуляции вакцинных антигенов, есть пути улучшения ответа собственных цитокинов хозяина, и есть способы, которые направляют вакцинные антигены к антиген-презентирующим клеткам (Nossal, 1999, In: Fundamental Immunology. Paul (Ed.), Lippincott-Raven Publishers, Philadelphia, Pa.; Vogel and Powell, 1995, In: Vaccine Design. The Subunit and Adjuvant Approach. Powell and Newman (Eds.), Plenum Press, NY, N.Y. p.141). Так как адъюванты играют существенную роль в улучшении иммуногенности вакцинных антигенов, то применение адъювантов в составе вакцин является по существу повсеместным (Nossal, 1999, выше; Vogel and Powell, 1995, выше; см. также заявку РСТ WO 97/18837, раскрытие которой включено в данный документ ссылкой). Подходящие адъюванты, хорошо известные в данной области, различаются по своей природе. Они могут, например, состоять из нерастворимых в воде неорганических солей, липосом, мицелл или эмульсий, как например, адъювант Фрейнда. Другие адъюванты можно найти в публикации Vogel and Powell, 1995, упомянутой выше. Хотя не существует единого механизма действия адъювантов, существенной характеристикой является их способность значительно повышать иммунный ответ на вакцинный антиген по сравнению с ответом, индуцированным вакцинным антигеном отдельно (Nossal, 1999, выше; Vogel and Powell, 1995, выше). В связи с этим, некоторые адъюванты являются более эффективными по части усиления гуморального иммунного ответа; другие адъюванты более эффективны в увеличении клеточно-опосредованного иммунного ответа (Vogel and Powell, 1995, выше); и еще другая группа адъювантов увеличивает оба типа иммунного ответа против вакцинных антигенов, гуморальный и клеточно-опосредованный (Vogel and Powell, 1995, выше).
Как правило, эмульсии, используемые в вакцинном составе, включают смесь масла, водного раствора и поверхностно-активных веществ. Некоторые эмульсии включают липофильное поверхностно-активное вещество, такое как «SPAN 80®» и гидрофильное поверхностно-активное вещество, такое как «TWEEN 80®».
Однако могут наблюдаться проблемы стабильности с эмульсиями, используемыми в качестве вакцинных адъювантов, в частности, во время хранения и транспортировки. Это в особенности верно, когда эти композиции содержат концентрированные иммуногены, особенно неочищенные концентрированные иммуногены. Как правило, это происходит с адъювантами, используемыми в инактивированных (убитых) вакцинах. Данная проблема еще более значима для мультивалентных вакцинных композиций, поскольку иммуногены сильнее сконцентрированы в том же объеме разбавителя.
Другая проблема, касающаяся адъюванта, связана с риском побочных эффектов, таких как токсичность или локальное воспаление в месте инъекции. Например, после инъекции может возникнуть локальный воспалительный ответ и/или гранулема. С целью ограничения таких побочных реакций, количество поверхностно-активных веществ и других компонентов в эмульсии может быть уменьшено; однако это уменьшение в результате может привести к снижению стабильности вакцинной композиции. Таким образом, существует необходимость получения новых адъювантов и вакцинных композиций, содержащих такие адъюванты, с повышенной безопасностью и стабильностью.
Сущность изобретения
В первом воплощении, в настоящем изобретении предлагается новая эмульсия масло-в-воде (М/В) с повышенной стабильностью в присутствии бактериальных или вирусных суспензий, особенно концентрированных и не очищенных или слабо очищенных.
Другое воплощение настоящего изобретения обеспечивает стабильную, безопасную и легко вводимую, в частности, инъецируемую, М/В эмульсию в качестве носителя для доставки фармацевтической композиции, включающей, по меньшей мере, один активный ингредиент, который, более конкретно, может представлять собой иммуноген.
Еще одно воплощение настоящего изобретения обеспечивает стабильную, безопасную и инъецируемую М/В эмульсию, действующую в качестве адъюванта для повышения иммунного ответа, индуцированного иммуногеном. Конкретно, в настоящем изобретении предлагается новый адъювант, который при использовании в вакцинной композиции, содержащей иммуноген, повышает клеточный иммунный ответ вакцинированного на иммуноген, гуморальный иммунный ответ или, предпочтительно, повышает оба иммунных ответа.
Еще в одном воплощении настоящего изобретения предлагается стабильная, безопасная и иммуногенная композиция или вакцина, включающая М/В эмульсию.
В следующем воплощении настоящего изобретения предлагается способ получения вакцинной композиции с использованием адъюванта по настоящему изобретению; полученная вакцинная композиция; и способы ее применения.
Еще в одном воплощении настоящего изобретения предлагается набор реагентов, включающий один или несколько флаконов. В одном воплощении, набор реагентов включает один флакон, содержащий адъювант по настоящему изобретению и иммуноген или другой фармацевтический продукт. Еще в одном воплощении, набор реагентов включает иммуноген или другой фармацевтический продукт в первом флаконе, и адъювант, полученный согласно настоящему изобретению, во втором флаконе, при этом адъювант разработан так, чтобы перед применением его необходимо было смешивать с иммуногеном или другим вакцинным продуктом.
В одном воплощении, в настоящем изобретении предлагается инъецируемая эмульсия масло-в-воде (М/В), включающая:
(1) водный раствор, включающий иммуноген;
(2) водный раствор, включающий гидрофильное ионное поверхностно-активное вещество, такое как сапонин
(3) необязательный водный раствор, включающий гидроксид алюминия;
(4) минеральное масло;
(5) неионное липофильное поверхностно-активное вещество;
(6) неионное гидрофильное поверхностно-активное вещество с низким значением ГЛБ, которое включает этоксилированные диэфиры сорбита и жирных кислот (как правило, имеющие значение от 11 до 13).
В другом воплощении, в настоящем изобретении предлагается инъецируемая эмульсия масло-в-воде (М/В), включающая:
(1) водный раствор, включающий иммуноген;
(2) водный раствор, включающий гидрофильное ионное поверхностно-активное вещество, такое как сапонин
(3) минеральное масло;
(4) неионное липофильное поверхностно-активное вещество;
(5) неионное гидрофильное поверхностно-активное вещество с низким значением ГЛБ, которое включает этоксилированные диэфиры сорбита и жирных кислот (как правило, имеющие значение от 11 до 13).
В другом воплощении, в настоящем изобретении предлагается инъецируемая эмульсия масло-в-воде (М/В), включающая:
(1) водный раствор, включающий иммуноген;
(2) водный раствор, включающий гидрофильное ионное поверхностно-активное вещество, такое как сапонин
(3) необязательный водный раствор, включающий гидроксид алюминия;
(4) неионное гидрофильное поверхностно-активное вещество с высоким значением гидрофильно-липофильного баланса (ГЛБ) более чем 13 и менее чем 40, конкретно, с ГЛБ>13,5, и предпочтительно с ГЛБ>14;
(5) минеральное масло;
(6) неионное липофильное поверхностно-активное вещество;
(7) неионное гидрофильное поверхностно-активное вещество с низким значением ГЛБ (значение ГЛБ от около 9 до около 13).
В другом воплощении, в настоящем изобретении предлагается инъецируемая эмульсия масло-в-воде (М/В), включающая:
(1) водный раствор, включающий иммуноген;
(2) водный раствор, включающий гидрофильное ионное поверхностно-активное вещество, такое как сапонин
(3) неионное гидрофильное поверхностно-активное вещество с высоким значением гидрофильно-липофильного баланса (ГЛБ) более чем 13 и менее чем 40, конкретно, с ГЛБ≥13,5, и предпочтительно с ГЛБ≥14;
(4) минеральное масло;
(5) неионное липофильное поверхностно-активное вещество;
(6) неионное гидрофильное поверхностно-активное вещество с низким значением ГЛБ (значение ГЛБ от около 9 до около 13).
Еще в одном воплощении, в настоящем изобретении предлагается вакцинная композиция, включающая новую эмульсию, содержащую, по меньшей мере, один иммуноген, подходящий для вызова иммунологического ответа у вакцинированного. В изобретении дополнительно предлагаются такие композиции, где эмульсия действует в качестве адъюванта для усиления иммунного ответа, индуцированного иммуногеном, конкретно, для усиления клеточного ответа, гуморального ответа или, предпочтительно, обоих ответов.
В другом воплощении настоящего изобретения предлагается способ получения вакцинной композиции, где иммуноген смешивают с адъювантом согласно настоящему изобретению, особенно, иммуноген в сухой форме, который может быть получен путем лиофилизации или путем стеклования, или иммуноген в водном растворе, особенно, где указанная сухая форма или указанный водный раствор дополнительно включают ионное поверхностно-активное вещество, например, сапонин и необязательно дополнительно включают гидроксид алюминия. Иммуноген может быть выбран из группы, состоящей из инактивированных патогенов, ослабленных патогенов, субъединиц антигенов, очищенных антигенов, неочищенных антигенов или антигенов, полученных рекомбинантно с использованием бактериальных клеток, дрожжевых, растительных, клеток насекомых или животных клеток, экспрессирующих векторы, включающие плазмиды, и т.п. Антигены могут быть очищены с помощью способов, хорошо известных в данной области, включающих в частности ультрафильтрацию, ультрацентрифугирование, эксклюзионную гель-фильтрацию, ион-обменную хроматографию и очистку с ПЭГ. Патоген может иметь бактериальное, вирусное происхождение, может происходить из простейших или может иметь грибное происхождение, или в состав иммуногена может входить антитоксин.
В другом воплощении в настоящем изобретении предлагается способ индукции иммунного ответа у вакцинированного против патогена, причем способ включает введение вакцинируемому вакцинной композиции по настоящему изобретению.
В другом воплощении, в настоящем изобретении предлагаются наборы реагентов, включающие один флакон, содержащий очищенные иммуногены и эмульсию по настоящему изобретению. В одном воплощении, иммуногены, содержащиеся в одном флаконе, включают очищенные антигены вируса ящура.
В другом воплощении, в настоящем изобретении предлагаются наборы реагентов, включающие, по меньшей мере, два флакона, где первый флакон содержит иммуноген, особенно иммуноген в сухой форме или в растворе или в водной среде, особенно где указанная сухая форма или указанный водный раствор дополнительно включают ионное поверхностно-активное вещество, преимущественно сапонин, и необязательно дополнительно включают гидроксид алюминия, а второй флакон содержит адъювант или эмульсию согласно настоящему изобретению. Применение наборов реагентов, которые включают, по меньшей мере, два флакона, особенно эффективно в случаях, где комбинация дискретных компонентов (т.е. смешивание в одном флаконе содержимого, по меньшей мере, двух флаконов) будет приводить в результате к получению состава вакцины с уменьшенной стабильностью.
Следует отметить, что в данном раскрытии и особенно в формуле изобретения термины, такие как «содержит», «содержащий» и т.п. могут иметь значение, которое придается термину в патентном законе США, например, они могут означать «включает», «включенный», «включающий» и т.п.; и что термины, такие как «состоящий преимущественно» и «состоит преимущественно» имеют значение, предписанное им в патентном законе США, например, они позволяют элементам не явным образом упоминаться, но исключать элементы, которые обнаружены в предшествующем уровне техники или которые влияют на основную или новую характеристику изобретения.
Эти и другие воплощения описаны в следующем подробном описании или очевидны из него и охвачены им.
Краткое описание чертежей
Полное и достаточное раскрытие настоящего изобретения, включающее лучший способ его осуществления, более конкретно изложено для специалистов в данной области в оставшейся части описания изобретения, включая ссылку на прилагаемые чертежи, где:
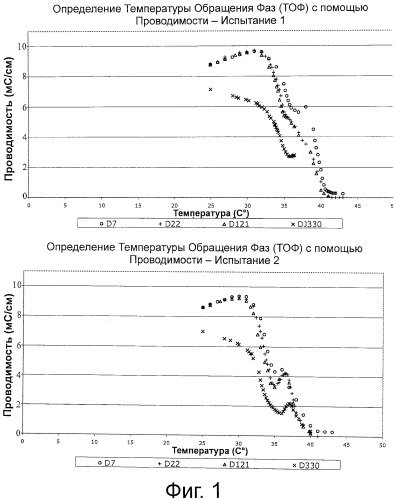
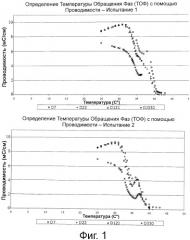
На фиг.1 представлены графики определения температуры обращения фаз, ТОФ (англ. Phase Inversion Temperature, PIT) (измеренной посредством проводимости) для вакцинных составов испытаний 1 и 2 в дни 7, 22, 121, и 330 (одногодичное исследование стабильности). Определение ТОФ является одной мерой стабильности вакцинного состава.
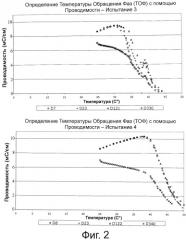
На фиг.2 представлены графики определения ТОФ для вакцинных составов испытаний 3 и 4 в различные дни после получения (одногодичное исследование стабильности).
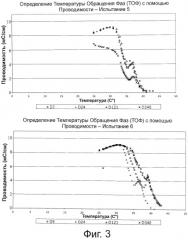
На фиг.3 представлены графики определения ТОФ для вакцинных составов испытаний 5 и 6 в различные дни после получения (одногодичное исследование стабильности).
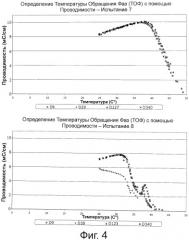
На фиг.4 представлены графики определения ТОФ для вакцинных составов испытаний 7 и 8 в различные дни после получения (одногодичное исследование стабильности).
На фиг.5 представлен график определения ТОФ для вакцинных составов испытания 9 в различные дни после получения (одногодичное исследование стабильности).
На фиг.6 представлены графики определения ТОФ для вакцинных составов (испытаний 1-9), полученных согласно настоящему изобретению, и сохраняемых в течение 36 месяцев.
На фиг.7 представлен график, который выявляет временную зависимость изменений ректальной температуры свиней, подвергнутых обработке согласно материалам и методам, раскрытым в примере 6.
На фиг.8 представлен график, который выявляет максимальное изменение температуры, наблюдаемое для свиней, подвергнутых обработке согласно материалам и методам, раскрытым в примере 6.
На фиг.9 представлен график, который демонстрирует эффективность вакцины (PD50) относительно полезной нагрузки (мкг) для свиней, подвергнутых обработке согласно материалам и методам, которые раскрыты в примере 7.
Подробное описание изобретения
Другие задачи, особенности и аспекты настоящего изобретения будут раскрыты или станут очевидны из следующего подробного описания изобретения. Специалисту в данной области следует понимать, что настоящее обсуждение представляет собой только описание типичных воплощений и не предназначено для ограничения более широких аспектов настоящего изобретения, которые будут воплощены в примерном исполнении. Фактически, специалисту в данной области будет очевидно, что в настоящем изобретении могут быть произведены различные модификации и вариации, не отходя при этом от объема притязаний и сущности изобретения. Например, признаки, проиллюстрированные или описанные как часть одного воплощения, могут использоваться в другом воплощении с получением еще одного воплощения. Подразумевается, что настоящее изобретение охватывает такие модификации и вариации, попадающие в рамки приложенной формулы изобретения и ее эквивалентов. Содержание публикаций, опубликованных патентов и патентов, цитированных в настоящей заявке, настоящим включено с помощью ссылки в полном объеме.
Для удобства здесь собраны определенные термины, применяемые в Описании изобретения, в примерах и в приложенной Формуле изобретения.
При использовании в данном документе, термин «животное» включает всех позвоночных, включающих человека. Он также включает индивидуальное животное во всех стадиях развития, включая стадии эмбриона и плода. Конкретно, термин «позвоночное животное» включает в частности людей, представителей семейства собачьих (например, собаки), кошачьих (например, кошки); лошадиных (например, лошади), жвачных парнокопытных (например, коровы, крупный рогатый скот), свиней (например, свиньи), а также птиц. При использовании в данном документе, термин «корова» или «крупный рогатый скот» используется, как правило, для обозначения животного с происхождением из семейства жвачных парнокопытных любого возраста. Взаимозаменяемые термины включают «бык», «теленок», «вол», «буйвол», «телка», «корова» и тому подобные. Взаимозаменяемые термины включают «поросенок», «свиноматка» и тому подобные. Термин «птичий» при использовании в данном документе относится к любым видам или подвидам таксономической группы птичьих, таких как в частности, курица (племенные птицы, бройлеры и несушки), индейка, утка, гусь, перепел, фазан, попугай, зяблик, ястреб, ворона и бескилевые, включающие страуса, эму и казуара. Термин «свинья» или «поросенок» обозначает животного свиного происхождения, в то время как «свиноматка» обозначает самку с репродуктивными возрастом и способностью.
При использовании в данном документе, термин «вирулентный» обозначает изолят, который сохраняет свою способность инфицировать животное-хозяина.
При использовании в данном документе, термин «инактивированная вакцина» обозначает вакцинную композицию, содержащую инфекционный организм или патоген, который более не способен к репликации или росту. Патоген может иметь бактериальное, вирусное происхождение, может происходить из простейших или может иметь грибное происхождение. Инактивация может осуществляться с помощью разнообразных способов, включающих замораживание-оттаивание, химическую обработку (например, обработку формалином), обработку ультразвуком, облучение, нагревание или другой подходящий способ, достаточный для предотвращения репликации или роста организма, с сохранением при этом его иммуногенности.
При использовании в данном документе, термин «иммуногенность» обозначает способность продуцировать иммунный ответ у животного-хозяина против антигена или антигенов. Иммунный ответ образует основание защитного иммунитета, вызываемого вакциной против специфического инфекционного организма.
При использовании в данном документе, термин «иммунный ответ» обозначает ответ, вызываемый у животного. Иммунный ответ может обозначать клеточный иммунитет (англ. cellular immunity, CMI); гуморальный иммунитет или может включать в себя и то и другое. Настоящее изобретение также предполагает ответ, ограниченный частью иммунной системы. Например, вакцинная композиция по настоящему изобретению может специфично индуцировать усиленный ответ гамма-интерферона.
При использовании в данном документе, термин «антиген» или «иммуноген» обозначает вещество, которое индуцирует специфический иммунный ответ у животного-хозяина. Антиген может включать цельный организм, убитый, ослабленный или живой; субъединицу или часть организма; рекомбинантный вектор, содержащий вставку с иммуногенными свойствами; часть или фрагмент ДНК, способной индуцировать иммунный ответ при презентировании животному-хозяину; белок, полипептид, пептид, эпитоп, гаптен или любую их комбинацию. В ином случае, иммуноген или антиген могут содержать токсин или антитоксин.
При использовании в настоящем документе, термин «мультивалентная» обозначает вакцину, содержащую более одного антигена либо из одного вида (т.е. различные изоляты серотипов вируса ящура), из различных видов (т.е. изоляты как из Pasteurella hemolytica, так и из Pasteurella multocida), или вакцину, содержащую комбинацию антигенов из различных родов (например, вакцина, включающая антигены из Pasteurella multocida, Salmonella, Escherichia coli, Haemophilus somnus и Clostridium).
При использовании в данном документе, термин «адъювант» обозначает вещество, добавляемое к вакцине для усиления иммуногенности вакцины. Механизм того, как функционирует антиген, до конца не ясен. Считается, что некоторые адъюванты усиливают иммунный ответ путем медленного высвобождения антигена, в то время как другие адъюванты сами по себе являются сильно иммуногенными и считается, что они функционируют синергично. Известные вакцинные адъюванты включают в частности масляные и водные эмульсии (например, полный адъювант Фрейнда и неполный адъювант Фрейнда), Corynebacterium parvum, бациллу Кальмета-Герена, гидроксид алюминия, глюкан, декстран сульфат, оксид железа, альгинат натрия, бакто-адъювант, определенные синтетические полимеры, такие как полиаминокислоты и сополимеры аминокислот, сапонин, «REGRESSIN» (Vetrepharm, Athens, Ga.), «AVRIDINE» (N,N-диоктадецил-N',N'-бис(2-гидроксиэтил)-пропандиамин), парафиновое масло, мурамил-дипептид и т.п.
При использовании в данном документе, термин «эмульсия» обозначает комбинацию, по меньшей мере, двух веществ, где первое вещество диспергируется во втором веществе, в котором первое вещество не растворимо. Один пример эмульсии по настоящему изобретению представляет собой масляную фазу, диспергированную в водной фазе.
При использовании в данном документе, термин «неполная эмульсия» обозначает композицию, к которой должен быть добавлен, по меньшей мере, один дополнительный компонент для получения «полной эмульсии». При использовании в данном документе, термин «полная эмульсия» может рассматриваться как эквивалент «готовой к применению» иммунологической композиции по настоящему изобретению. Примером полной эмульсии является иммунологическая композиция в соответствии с настоящим изобретением, которая готова к введению животному в соответствии со способами по настоящему изобретению.
При использовании в настоящем документе, термины «фармацевтически приемлемый носитель» и «фармацевтически приемлемое средство переноса» взаимозаменяемы и обозначают жидкое средство переноса для содержания вакцинных антигенов, которые могут инъецироваться организму-хозяину без побочных эффектов. Подходящие фармацевтически приемлемые носители, известные в данной области, включают в частности стерильную воду, солевой раствор, глюкозу, декстрозу или буферные растворы. Носители могут включать вспомогательные агенты, включающие в частности разбавители, стабилизаторы (т.е., сахара и аминокислоты), консерванты, увлажнители, эмульгаторы, рН-буферные агенты, добавки усиления вязкости, красители и т.д.
При использовании в данном документе, термин «вакцинная композиция» включает, по меньшей мере, один антиген или иммуноген в фармацевтически приемлемом носителе, используемый для индукции иммунного ответа у организма-хозяина. Вакцинные композиции могут быть введены в дозировках и методами, хорошо известными специалистам в области медицины или ветеринарии, принимая во внимание такие факторы, как возраст, пол, масса, вид и состояние животного-реципиента, а также путь введения. Путь введения может быть чрескожным введением через слизистую оболочку (например, пероральное, назальное, ректальное, вагинальное), или может быть ведением через парентеральный путь (внутрикожное, внутримышечное, подкожное, внутривенное или внутрибрюшинное введение). Вакцинные композиции могут вводиться отдельно или могут вводиться совместно или последовательно с другими обработками или терапиями. Формы введения могут включать суспензии, сиропы или эликсиры, и препараты для парентерального, подкожного, внутрикожного, внутримышечного или внутривенного введения (например, введения с помощью инъекций), такие как стерильные суспензии или эмульсии. Вакцинные композиции могут вводиться в виде спрея или могут смешиваться с пищей и/или водой, или могут доставляться в виде предварительной смеси с использованием подходящего носителя, разбавителя или наполнителя, такого как стерильная вода, физиологический солевой раствор, глюкоза и т.д. Композиции могут содержать вспомогательные вещества, такие как увлажнители или эмульгаторы, корректирующие рН буферные агенты, адъюванты, добавки, усиливающие гелеобразование или вязкость, консерванты, ароматизаторы, красители и т.п., в зависимости от требуемых путей введения и приготовления. Стандартные фармацевтические тексты, такие как «Remington's Pharmaceutical Sciences», 1990, могут быть использованы для консультации при приготовлении подходящих препаратов, без проведения излишних экспериментов.
При использовании в данном документе термин «очищенный» не требует абсолютной чистоты; скорее он подразумевается как относительный термин. Таким образом, например, очищенный иммуногенный препарат, такой как белок или инактивированный вирус, является препаратом, в котором иммуноген находится в более обогащенном состоянии, чем иммуноген в его естественной среде. Иммуногенный препарат в данном документе часто обозначается как «очищенный», если иммуноген составляет, по меньшей мере, 60%, по меньшей мере, 70%, по меньшей мере, 80%, по меньшей мере, 90%, по меньшей мере, 95%, или, по меньшей мере, 98% от общего содержания иммуногена в препарате. «Сырой препарат», который соответствует самой низкой степени очистки, может содержать настолько мало, как менее чем 60%, менее чем 20%, менее чем 10%, менее чем 5%, или менее чем 1% иммуногенных компонентов.
Подразумевается, что при использовании в данном документе, термин «высокоочищенный» предполагает «высокую степень чистоты» относительно термина «среднеочищенный». Эта «более высокая степень чистоты» может включать, но никоим образом не ограничивать, уменьшенное процентное содержание примесей в иммунологическом препарате, который является «высокоочищенным» по сравнению с иммунологическим препаратом, который является «среднеочищенным». Как обсуждается в данном документе, «высокоочищенные» иммунологические препараты будут содержать от самого низкого до не детектируемого процентного содержания примесей, которые могут вызывать: снижение целевого иммунного ответа, усиление нецелевого иммунного ответа (например, реакцию гиперчувствительности), или уменьшение стабильности состава. Аналогично, иммунологический препарат, который является «среднеочищенным», содержит относительно сниженное процентное содержание примесей по сравнению с иммунологическим препаратом, который является «минимально очищенным», который также содержит сниженное процентное содержание примесей по сравнению с препаратом, обозначенным как «сырой препарат».
Примеси в иммунологическом препарате могут включать, но никоим образом не ограничиваются этим, вещества, которые вносят отрицательный вклад в иммунологическую композицию по настоящему изобретению. Одним из нескольких примеров примесей, которые вносят отрицательный вклад, является примесь, которая снижает способность иммунологической композиции по настоящему изобретению вызывать иммунный ответ у животных.
С помощью различных методов можно достичь различных уровней чистоты (например, «высокой чистоты», «средней чистоты», и т.п.). Например, комбинация хроматографии и гель-фильтрации может приводить в результате к получению «высокоочищенных» или «среднеочищенных» иммунологических препаратов. Различия источника/типа иммуногенов, а также небольшие вариации в процедурах очистки могут значительно повлиять на конечную степень чистоты иммуногена. Как правило, при использовании в данном документе, иммунологические препараты, содержащие примеси от самого низкого процента до самого высокого, будут описаны как 1) «высокоочищенные», 2) «среднеочищенные», 3) «минимально очищенные», 4) «сырой препарат», соответственно. «Высокоочищенный» препарат будет иметь самый низкий уровень всех типов примесей. «Среднеочищенный» препарат будет, соответственно, иметь относительно низкий уровень большинства типов примесей, но может иметь одну примесь, которая будут более высоко представлена, по сравнению с ее уровнем, который можно наблюдать в «высокоочищенном» препарате. В ином случае, «минимально очищенный препарат» будет иметь относительно низкий уровень некоторых типов примесей, но может иметь более одного типа примесей, которые будут более высоко представлены, по сравнению с их уровнем в «среднеочищенном» препарате. Как и следовало ожидать, «сырой препарат» имеет наиболее высокий уровень всех типов примесей по сравнению с другими типами препаратов, обсуждаемыми в данном документе.
В настоящем изобретении предлагается новая эмульсия масло-в-воде (М/В), включающая:
(1) водный раствор, включающий вакцинный антиген или иммуноген, способный индуцировать иммунный ответ у хозяина;
(2) водный раствор, включающий ионное поверхностно активное вещество;
(3) неионное гидрофильное поверхностно активное вещество;
(4) минеральное масло;
В одном воплощении, новая эмульсия масло-в-воде (М/В) включает:
(1) водный раствор, включающий вакцинный антиген или иммуноген, способный индуцировать иммунный ответ у хозяина;
(2) водный раствор, включающий ионное поверхностно активное вещество, такое как сапонин;
(3) неионное гидрофильное поверхностно активное вещество со значением гидрофильно-липофильного баланса (ГЛБ) более чем 13 и менее чем 40 (ГЛБ≥13, конкретно, с ГЛБ≥13,5, и предпочтительно с ГЛБ≥14);
(4) минеральное масло;
(5) неионное липофильное поверхностно активное вещество;
(6) неионное гидрофильное поверхностно активное вещество с низким значением ГЛБ (значение ГЛБ от 9 до 13).
В другом воплощении, в настоящем изобретении предлагается новая эмульсия масло-в-воде (М/В), включающая:
(1) водный раствор, включающий вакцинный антиген или иммуноген, способный индуцировать иммунный ответ у хозяина;
(2) водный раствор, включающий ионное поверхностно активное вещество, такое как сапонин
(3) необязательный водный раствор, включающий гидроксид алюминия;
(4) неионное гидрофильное поверхностно активное вещество со значением гидрофильно-липофильного баланса (ГЛБ) более чем 13 и менее чем 40 (ГЛБ≥13, конкретно, с ГЛБ≥13,5, и предпочтительно с ГЛБ≥14);
(5) минеральное масло;
(6) неионное липофильное поверхностно активное вещество; и
(7) неионное гидрофильное поверхностно-активное вещество с низким значением ГЛБ (значение ГЛБ от 9 до 13).
Некоторые эмульсии, полученные согласно настоящему изобретению, основаны на комбинации, по меньшей мере, четырех (4) поверхностно-активных веществ, и возможно использование одного или нескольких поверхностно-активных веществ, принадлежащих к каждой группе. Три (3) из этих групп включают неионные поверхностно-активные вещества и одна (1) из этих групп включает ионные поверхностно-активные вещества, например, сапонины.
В одном из некоторых воплощений, концентрация ионного поверхностно-активного вещества (2) в эмульсии (в настоящем описании это означает конечную эмульсию, включающую все ингредиенты, если иное не указано) составляет от около 0,01% до около 10%>.
В одном из воплощений, концентрация неионного поверхностно-активного вещества (7) в эмульсии (в настоящем описании это означает конечную эмульсию, включающую все ингредиенты, если иное не указано) составляет от 1% до 8%, конкретно, от 1,5% до 6%, предпочтительно, от 2% до 5%, более предпочтительно, от 2,5% до 4%, выраженных в виде процентного отношения массы к объему эмульсии (мас./об.).
Эта группа поверхностно-активных веществ включает неионные гидрофильные поверхностно-активные вещества, имеющие низкое значение ГЛБ (значение ГЛБ от 9 до 13). Данная группа включает в частности этоксилированный моноэфир сорбита и жирной кислоты (конкретно, 5 этоксигрупп) (например, этоксилированный сорбитан моноолеат, такой как «TWEEN 81®», диэфиры этоксилированной жирной кислоты и сорбитана, этоксилированные триэфиры сорбита и жирной кислоты (конкретно, 20 этоксигрупп) (например, этоксилированный сорбитан триолеат, такой как «TWEEN 85®»), этоксилированный сорбитан тристеарат, такой как «TWEEN 65®», этоксилированные жирные спирты (конкретно, 5-10 этоксигрупп) (например, «BRIJ 76®», «BRIJ 56®», «BRIJ 96®»), этоксилированные жирные кислоты (конкретно, 5-10 этоксигрупп) (например, «Simulsol 2599®», «MYRJ 45®»), этоксилированное касторовое масло (конкретно, 25-35 этоксигрупп) (например, «ARLATONE 650®», «ARLATONE G®»), и их комбинации.
Предпочтительными являются этоксилированные диэфиры сорбита и жирной кислоты и этоксилированные триэфиры сорбита и жирной кислоты, а также комбинации этих двух видов. Жирную кислоту предпочтительно выбирают из группы, состоящей из олеата, пальмитата, стеарата, изостеарата, лаурината и их комбинации. Предпочтительные этоксилированные триэфиры сорбита и жирной кислоты включают этоксилированный сорбитан триолеат, такой как «TWEEN 85®»), или этоксилированный сорбитан тристеарат, такой как «TWEEN 65®».
В одном из некоторых воплощений концентрация неионного гидрофильного поверхностно-активного вещества (4) как правило составляет от 0,1% до 1,5%, конкретно от 0,2% до 1,4%, предпочтительно, от 0,3% до 1,3%, более предпочтительно, от 0,4% до 1,2%, и выражена в виде процентного отношения массы к объему эмульсии (мас./об.).
Эта вторая группа поверхностно-активных веществ включает неионные гидрофильные поверхностно-активные вещества, имеющие значение гидрофильно-липофильного баланса (ГЛБ) (ГЛБ≥13, конкретно ГЛБ≥13,5, и предпочтительно, ГЛБ≥14). Данная группа включает этоксилированные моноэфиры сорбита и жирной кислоты (конкретно, 20 этоксигрупп) (например, этоксилированный сорбитанмонолауринат, такой как «TWEEN 20®», этоксилированный сорбитанмонопальмитат, такой как «TWEEN 40®», этоксилированный сорбитанмоностеарат, такой как «TWEEN 60®», этоксилированный сорбитанмоноолеат, такой как «TWEEN 80®», этоксилированные жирные спирты (конкретно, 15-30 этоксигрупп) (например, «BRIJ 78®», «BRIJ 98®», «BRIJ 721®»), этоксилированные жирные кислоты (конкретно, 15-30 этоксигрупп) (например, «MYRJ 49®», «MYRJ 51®», «MYRJ 52®», «MYRJ 53®»), неионные блок-сополимеры (например, сополимер полиоксиэтилена/полиоксипроиплена (РОЕ-РОР), такой как «LUTROL F127®», «LUTROL F68®»), и их комбинации.
Для неионных блок-сополимеров процентное содержание может быть ниже и в частности составляет от 0,1% до 0,5%, более конкретно, от 0,2% до 0,4% (отношения массы по объему эмульсии (мас./об.)).
Предпочтительные поверхностно-активные вещества (4) включают этоксилированные моноэфиры сорбита и жирной кислоты, такие как описанные выше.
В одном из некоторых воплощений концентрация неионного липофильного поверхностно-активного вещества (6) составляет от 0,1% до 2,5%, конкретно от 0,2% до 2%, предпочтительно, от 0,2% до 1,5%, более предпочтительно, от 0,2% до 1,2%, и выражена в процентном отношении массы к объему эмульсии (мас./об.).
Данная группа поверхностно-активных веществ включает эфиры сорбита и жирной кислоты (например, сорбитанмонолауринат, типа «SPAN 20®», сорбитанмонопальмитат, такой как «SPAN 40®», сорбитанмоностеарат, такой как «SPAN 60®», сорбитантристеарат, такой как «SPAN 65®», сорбитанмоноолеат, типа «SPAN 80®», сорбитантриолеат, типа «SPAN 85®», сорбитанмоноизостеарат, такой как «ARLACEL 987®», сорбитанизостеарат, такой как «CRILL 6®»), эфиры маннита и жирной кислоты например, «MONTANIDE 80®», маннит моноолеат (такой как «ARLACEL А®»), маннит диолеат, маннит триолеат.маннит тетраолеат), этоксилированные эфиры жирной кислоты и маннита (2, 3 или 4 этоксигруппы) (например, «MONTANIDE 888®», «MONTANIDE 103®», этокслированный маннит моноо