Опосредованная наночастицами доставка сиквенс-специфичных нуклеаз
Иллюстрации
Показать всеИзобретение относится к области биохимии, в частности к способу введения сиквенс-специфичной нуклеазы (ССН) в растительную клетку. При этом способ включает: обеспечение наличия растительной клетки, имеющей клеточную стенку; покрытие наночастицы золота CCH; приведение растительной клетки, имеющей клеточную стенку, и покрытой наночастицы в контакт друг с другом; и инкубацию клетки, имеющей клеточную стенку, совместно с покрытой наночастицей таким образом, чтобы обеспечить поглощение наночастицы и CCH в растительную клетку, содержащую клеточную стенку. Изобретение позволяет эффективно вводить ССН в растительную клетку, имеющую клеточную стенку. 13 з.п. ф-лы, 7 ил., 5 пр.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННУЮ ЗАЯВКУ
Настоящая заявка претендует на приоритет предварительной заявки на патент США № 61/167389, поданной 7 апреля 2009 года.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Уникальные свойства наночастиц могут быть использованы для доставки ДНК в клетки. Среди исследованных наночастиц (например, вольфрама, алюминия, никеля и т.д.), наночастицы золота (НЧЗ), по-видимому, являются наилучшими кандидатами для доставки ДНК. Низкая цитотоксичность и легкость функционализации различными биологически важными лигандами делает наночастицы золота средством первого выбора при трансформации. Размеры наночастиц золота могут варьировать от 1,2 нм до 600 нм. В результате обычно используемого синтеза НЧЗ образуются частицы размером от 20 до 400 нм с отрицательно заряженной (например, покрытой цитратом) поверхностью, в то время как более мелкие НЧЗ размером от 1 до 10 нм заряжены положительно. Плазмидная ДНК, которая является достаточно гибкой, чтобы частично раскручивать свои основания, может быть подвергнута действию наночастиц золота. В случае функционализированных цитратом НЧЗ плазмидная ДНК может частично раскручиваться. Отрицательные заряды на остове ДНК достаточно удалены друг от друга, для того чтобы вызвать притяжение между основаниями за счет сил Ван дер Ваальса, и поэтому в присутствии наночастицы золота плазмидная ДНК прикрепляется к ней и покрывает ее поверхность. Между тем, в случае положительно заряженных НЧЗ электростатические и Ван дер Ваальсовы силы могут вносить свой вклад в покрытие или прикрепление ДНК.
Кроме наночастиц металлов наночастицы полупроводников (например, квантовые точки («КТ»)) с размерами 3-5 нм также могут быть использованы в качестве носителей для доставки молекул в клетки. ДНК и белки могут покрывать или быть присоединенными к поверхности КТ, то есть мультифункционализировать ее лигандом (см., например, Patolsky, F., et al., J. Am. Chem. Soc. 125, 13918 (2003)). Мультифункционализированные карбоновой кислотой или амином КТ могут быть связаны поперечной связью с молекулами, содержащими тиоловую группу (см., например, Dubertret, B. et al., Science 298, 1759 (2002); Akerman, M. E., W. C. W. Chan, P. Laakkonen, S. N. Bhatia, E. Ruoslahti, Proc. Natl. Acad. Sci. U.S.A. 99, 12617 (2002); Mitchell, G. P., C. A. Mirkin, R. L. Letsinger, J. Am. Chem. Soc. 121, 8122 (1999)) или N-гидроксисукцинимидную (NHS) сложноэфирную группу с использованием стандартных протоколов биоконъюгации (см., например, Pinaud, F., D. King, H.-P. Moore, S. Weiss, J. Am. Chem. Soc. 126, 6115 (2004); Bruchez, M., M. Moronne, P. Gin, S. Weiss, A. P. Alivisatos, Science 281, 2013 (1998)). Альтернативным способом мультифункционализации КТ является конъюгация со стрептавидином. Стрептавидин конъюгирует с биотинилированными белками, олигонуклеотидами или антителами (см., например, Dahan M. et al., Science 302, 442 (2003); Pinaud, F., D. King, H.-P. Moore, S. Weiss, J. Am. Chem. Soc. 126, 6115 (2004); Dahan M. et al., Science 302, 442 (2003); Wu. X. Y., et al., Nature Biotechnol. 21, 41 (2003); Jaiswal, J. K., H. Mattoussi, J. M. Mauro, S. M. Simon, Nature Biotechnol. 21, 47 (2003); и Mansson, A., et al., Biochem. Biophys. Res. Commun. 314, 529 (2004)).
Наночастицы были использованы для доставки плазмидной ДНК в различные животные клетки. Было обнаружено, что когда покрытые ДНК наночастицы инкубируют с клетками, не имеющими клеточной стенки, эти клетки поглощают наночастицы и начинают экспрессировать любые гены, кодируемые этой ДНК. В тех случаях, когда желательна доставка наночастиц в клетки, обычно имеющие клеточную стенку, эту клеточную стенку удаляют перед добавлением частиц к протопластам (см. Torney, F. et al., Nature Nanotechnol. 2, (2007)). В растительных клетках клеточная стенка действует как барьер для доставки экзогенно применяемых молекул. Множество инвазивных методов, таких как генная пушка (баллистическая трансфекция), микроинъекция, электропорация и трансфекция с помощью Agrobacterium, применялись для обеспечения доставки генов и малых молекул в растительные клетки, имеющие клеточную стенку. Доставка малых молекул и белков через клеточную стенку в растительную клетку была бы перспективна для развития передовых технологий in vitro и in vivo манипуляции клетками, тканями и органами интактных растений.
Хотя для бактерий, дрожжей, животных клеток и мхов добавление гена - введение чужеродной ДНК в заранее определенный участок генома - хорошо отработано, в случае высших растений это остается серьезной проблемой. Сайт-специфичное встраивание трансгена в растительные клетки происходит с очень низкой частотой по сравнению со случайным встраиванием даже тогда, когда вводимая ДНК содержит большие участки последовательности, гомологичные ДНК хозяина (Halfter et al. 1992; Lee et al. 1990; Mia and Lam (1995)). Например, высокоэффективная система агробактериальной трансфекции и гербицидная селекция у риса приводили к направленному встраиванию гена с частотой 5×10-4. Попытки повысить эффективность направленного встраивания гена у растений включали в себя использование маркеров для отрицательной селекции и использование генно-инженерных растений, обнаруживших более высокую частоту направленного встраивания. Несмотря на эти усилия случайное встраивание ДНК в результате негомологичных процессов продолжает оставаться главным препятствием для направленного встраивания генов у растений. Принимая во внимание общую пользу, ожидаемую от направленного встраивания генов при модификации сельскохозяйственных культур для сельского хозяйства и промышленной биотехнологии, решение этой проблемы является крайне необходимым.
В этом отношении существенное увеличение частоты направленного встраивания генов наблюдали у широкого круга растительных и животных модельных систем после индукции двухцепочечного разрыва ДНК (ДЦР) в конкретном участке генома клетки-хозяина, которая стимулирует естественный клеточный процесс гомологично направленной репарации ДЦР. Существующие в природе сайт-специфичные эндонуклеазы, сайты узнавания которых редко встречаются в растительном геноме, были использованы для этой цели, чтобы таким образом управлять встраиванием трансгена в последовательность-мишень, предварительно перенесенную в геном растения путем случайного встраивания. Эти исследования показывают перспективность использования направленной индукции ДЦР для повышения эффективности направленного встраивания генов в растительные клетки, хотя внесение ДЦР в нативный локус остается проблематичным.
Решение проблемы направленного изменения генома или манипуляции с ним в животных клетках было достигнуто за счет использования различных белков, специфично связывающихся с нуклеотидной последовательностью, таких как лейциновые застежки-молнии, белки с цинковыми пальцами и т.д. Эти белки участвуют в регуляции генов в качестве факторов транскрипции и/или могут быть использованы для индуцирования ДЦР в участках нативного генома. ДЦР может быть внесен несколькими различными классами сиквес-специфичных нуклеаз, такими как мегануклеазы, лейциновые застежки-молнии, белки с цинковыми пальцами и т.д., и в последнее время создаются новые гибридные варианты этих белков. Одними из наиболее описанных белков, специфично связывающихся с нуклеотидной последовательностью, являются белки с цинковыми пальцами (ZFP). Цинковый палец C2H2 был впервые обнаружен в факторе транскрипции амфибии TFIIIA, и с тех пор было установлено, что он является наиболее распространенным мотивом распознавания ДНК у всех видов многоклеточных. Рентгеноструктурный анализ C2H2 ZFP Zif268 выявил удивительный силлабический тип распознавания белок-ДНК, при котором каждый цинковый палец специфичен в отношении конкретного субсайта из 3 или 4 п.н. в случае их последовательного расположения, и было сделано предположение о возможности использования этого пептидного мотива в качестве каркаса для ДНК-связывающих доменов с новой специфичностью. С тех пор большое количество ZFP, сконструированных для того, чтобы связываться с новыми последовательностями, было с успехом использовано во множестве различных лабораторий в области искусственных факторов транскрипции и других функциональных гибридных белков. Домен C2H2 белка с цинковым пальцем был использован в качестве каркаса для сиквенс-специфичного связывания ДНК (Pavelitch and Pabo 1991), и нуклеазы с доменом цинкового пальца (ZFN) были получены путем слияния доменов белков с цинковыми пальцами с неспецифичным в отношении последовательности доменом нуклеазы, полученным из эндонуклеазы рестрикции FokI типа IIS (Kim et al. 1996). Рекомбинантные ZFN были использованы для обеспечения высокоэффективного нацеливания на эндогенный геномный локус в трансформированных (Moehle et al. 2007) и исходных клетках человека (Lombardo et al. 2007).
Первые попытки использования ZFN в растениях оказались многообещающими (Lloyd et al. 2005; Wright et al. 2005; Maeder et al. 2008). Конструкция, несущая ген ZFN под контролем индуцибельного промотора вместе с соответствующей распознаваемой ею последовательностью, была стабильно встроена в Arabidopsis, и было показано введение целевых мутаций в результате негомологичного соединения концов в сайте узнавания со средней частотой 7,9% среди индуцированных проростков потомства (Lloyd et al. 2005). Аналогично, из 66 растений табака, регенерированных из протопластов, трансформированных ZFN, предназначенной для расщепления локуса SuRA, у трех были обнаружены делеции одной пары оснований в сайте-мишени, появившиеся в результате негомологичного соединения концов при репарации (Maeder et al. 2008). Клетки табака, содержащие предварительно встроенный нефункциональный репортерный ген, у которого отсутствовал участок из 600 п.н., непосредственно фланкирующий последовательность распознавания цинкового пальца, при котрансформации их конструкциями, содержащими соответствующий ген ZFN и донорную ДНК, гомологичную предварительно встроенной последовательности, у которой отсутствовал участок из 600 п.н., обнаружили признаки гомологичной репарации репортерного гена (Wright et al. 2005). Совсем недавно основанный на дрожжевой системе тест был использован для выявления ZFN, способных расщеплять ген эндохитиназы растений (Cai et al., 2009). Агробактериальная доставка Ti плазмиды, несущей как ZFN, так и донорную ДНК конструкцию, содержащую кассету гена устойчивости к гербицидам pat, фланкированную короткими участками гомологии с локусом эндохитаназы, обеспечила до 10% направленного гомологичного встраивания трансгена точно в сайт расщепления ZFN. Важно отметить, что другие конструкции цинковых пальцев на основе домена C3H1 были использованы в растениях (Shukla et al., 2009, Cai et al. 2009).
Настоящее изобретение относится к способам использования наночастиц для неинвазивной доставки сиквенс-специфичных нуклеаз в растительные клетки, имеющие клеточную стенку.
КРАТКАЯ СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Следующие варианты осуществления изобретения описывают системы, средства и способы, которые предназначены быть примером и иллюстрацией данного изобретения и не ограничивают его объем.
В соответствии с настоящим изобретением предложены способы введения сиквенс-специфичной нуклеазы в растительную клетку, этот способ включает в себя: обеспечение наличия растительной клетки, имеющей клеточную стенку; покрытие наночастицы, по меньшей мере, сиквенс-специфичной нуклеазой; приведение растительной клетки, имеющей клеточную стенку, и наночастицы, покрытой сиквенс-специфичной нуклеазой, в контакт друг с другом; и обеспечение поглощения покрытой сиквенс-специфичной нуклеазой наночастицы растительной клеткой, имеющей клеточную стенку.
Кроме приведенных в качестве примера аспектов и вышеописанных вариантов осуществления изобретения дополнительные аспекты и варианты осуществления изобретения станут очевидны из следующего описания.
КРАТКОЕ ОПИСАНИЕ ФИГУР
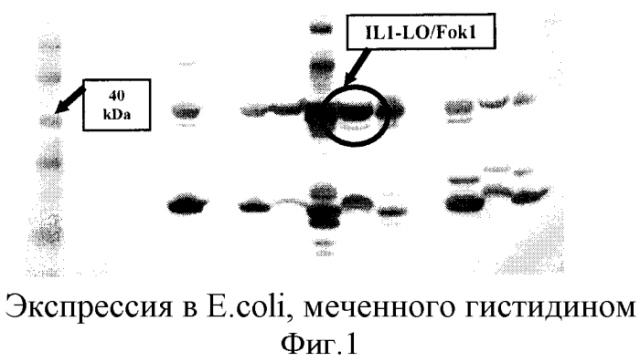
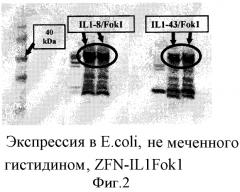
На фиг.1 и 2 показана экспрессия в E.coli, меченного гистидином (1) и не меченного гистидином (2), ZFN-IL1 FokI, соответственно.
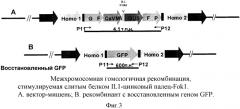
На фиг.3 показана межхромосомная гомологичная рекомбинация, стимулируемая слитым белком IL1-цинковый палец-FokI, где A представляет вектор-мишень и B представляет рекомбинант с восстановленным геном GFP.
На фиг.4 показано схематическое изображение плазмиды pDAB1585.
На фиг.5 показаны клональные клеточные линии BY2-E, обнаружившие опосредованную НЧЗ интернализацию YFP после двух часов инкубации клеток; фотография A (флуоресцеин изотиоцианат (ФИТЦ)), B (родамин), C (дифференциальное интерференционное контрастирование), D (A+B), E (A+B+C), F (отраженное инвертированное изображение): интернализация YFP, наблюдаемая с помощью флуоресцентной микроскопии.
На фиг.6 показана межхромосомная гомологичная рекомбинация, стимулируемая белком мегануклеазы I-SceI, где A представляет вектор-мишень и B представляет рекомбинант с восстановленным геном GFP.
На фиг.7 показано схематическое изображение плазмиды pDAB100375.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В последующем описании употребляется много терминов. Для обеспечения ясного и единообразного понимания описания и формулы изобретения, включая объем этих терминов, приводятся следующие определения:
Возвратное скрещивание. Возвратным скрещиванием может быть процесс, при котором селекционер повторно скрещивает гибридное потомство с одним из родителей, например гибрид первого поколения F1 с одним из родительских генотипов гибрида F1.
Зародыш. Зародышем может быть маленькое растение, содержащееся в зрелом семени.
Наночастица. Микроскопическая частица, имеющая, по меньшей мере, одно наноразмерное измерение, обычно менее 100 нм. Наночастицы, пригодные для использования в настоящем изобретении, могут иметь размер от 1 нм до 0,4 мкм. Квантовая точка может иметь срединный диаметр от 1 нм до 10 нм, предпочтительно 2-4 нм. Наночастицы, используемые в настоящей заявке, включают в себя без ограничений наночастицы золота, наночастицы вольфрама, покрытые золотом наночастицы, пористые наночастицы, мезопористые наночастицы, наночастицы диоксида кремния, наночастицы полимера, наночастицы желатина, нанооболочки, наноядра, наносферы, наностержни, магнитные наночастицы, наночастицы полупроводников, квантовые точки, наноматрицы, дендримерные наноматрицы и их комбинации.
Квантовая точка. Квантовая точка является полупроводниковой наночастицей, которая ограничивает перемещение электронов зоны проводимости, дырок валентной зоны или экситонов (связанных пар электронов зоны проводимости и дырок валентной зоны) во всех трех пространственных направлениях. Ограничение может быть обусловлено электростатическими потенциалами (создаваемыми внешними электродами, легированием, механическим напряжением, примесями), наличием зоны соприкосновения между различными полупроводниковыми материалами (например, в нанокристаллических системах ядро-оболочка), наличием полупроводниковой поверхности (например, в полупроводниковом нанокристалле) или их комбинацией. Квантовая точка может иметь дискретный квантованный энергетический спектр. Соответствующие волновые функции пространственно локализованы внутри квантовой точки, но распространяются на многие периоды кристаллической решетки. Квантовая точка содержит небольшое определенное число (порядка 1-100) электронов зоны проводимости, дырок валентной зоны или экситонов (т.е. определенное число элементарных электрических зарядов).
Наноматрицы включают в себя без ограничений дендримеры. Дендримеры представляют собой сфероидальные или шарообразные наночастицы, созданные для того, чтобы переносить молекулы, инкапсулированные в их внутренние пустоты или прикрепленные к поверхности. Эти молекулы являются многократно разветвленными молекулами; ветвление позволяет возникать поливалентным взаимодействиям между поверхностью и внутренним веществом. Примером дендримера являются каскадные полимеры сферического катионного полиамидоамина (ПАМАМ). Эти полимеры состоят из первичных аминов на поверхности и третичных аминов внутри. Этот тип дендримера частично разлагается при термической обработке в присутствии растворителей, что приводит к меньшей жесткости пространственной структуры и большей гибкости. Большой положительный заряд дендримеров способствует возникновению электростатических взаимодействий с ДНК, а гибкая структура позволяет дендримеру сжиматься, когда он связан с ДНК, и расправляться при освобождении от ДНК. Эффективность трансфекции или трансформации повышается в результате положительного заряда и гибких структурных свойств дендримера. Дендримеры можно получить от компании Qiagen (Qiagen, Germantown, MD), дендримеры для потребителей поставляются на рынок под названием SuperfectTM Transfection Reagent (Cat # 301305).
Мультифункционализированные. Если не указано иное, то термин «мультифункционализированные» используется для описания или моно- или мультифункционализированных наночастиц. Термин «монофункционализированные частицы» относится к функционализированным наночастицам или агломератам наночастиц, с которыми химически связаны функциональные группы одного типа. Термин «мультифункционализированные частицы» относится к наночастицам или агломератам наночастиц, с которыми химически связаны функциональные группы, по меньшей мере, двух, а возможно трех и более различных типов.
Устойчивость к гербициду. Устойчивость к дозе гербицида относится к способности растения выживать (т.е. растение может не погибнуть) при такой дозе действующего вещества, которая подавляла бы рост и/или приводила бы неустойчивое растение к гибели. В некоторых случаях устойчивые растения могут временно пожелтеть или иначе проявить некоторые вызванные гербицидом повреждения, но потом восстанавливаются.
Стабилизированный. Термин «стабилизированный» относится к признакам растения, которые воспроизводимо передаются от одного поколения к следующему поколению инбредных растений того же сорта.
Поглощение. Термин «поглощение» относится к перемещению частиц или матриц, таких как наночастицы, например, золота, дендримеры или квантовые точки, через клеточную стенку или клеточную мембрану, где это перемещение не происходит только за счет импульса, сообщаемого частице чем-либо иным, кроме клетки, которой эта частица поглощается. Неограничивающими примерами устройств или способов, которые вызывают перемещение частицы через клеточную стенку или клеточную мембрану только за счет сообщаемого частице импульса, являются биолистика, генная пушка, микроинъекция и/или импалефекция.
Нуклеиновая кислота. Термины «нуклеиновая кислота», «полинуклеотид» и «олигонуклеотид» являются взаимозаменяемыми и относятся к дезоксирибонуклеотидному, рибонуклеотидному полимеру или иному нуклеотидному или нуклеозидному полимеру в линейной или кольцевой конформации, находящемуся или в одно-, или в двухцепочечной форме. Применительно к настоящему раскрытию эти термины не следует рассматривать как ограничивающие по отношению к длине полимера. Эти термины могут охватывать известные аналоги естественных нуклеотидов, а также нуклеотиды с модифицированным основанием, сахаром и/или фосфатными группами (например, фосфотиоатные остовы). Обычно аналог конкретного нуклеотида имеет такую же специфичность спаривания оснований; т.е. аналог A будет спариваться с T.
Хромосома. Хромосома представляет собой хроматиновый комплекс, включающий в себя весь или часть генома клетки. Геном клетки часто характеризуется ее кариотипом, который является совокупностью всех хромосом, составляющих геном клетки. Геном клетки может включать в себя одну или несколько хромосом. «Эписома» является реплицирующейся нуклеиновой кислотой, нуклеопротеиновым комплексом или другой структурой, содержащей нуклеиновую кислоту, которая не является частью хромосомного кариотипа клетки. Примеры эписом включают в себя плазмиды и некоторые вирусные геномы. «Доступный участок» представляет собой участок клеточного хроматина, в котором сайт-мишень, присутствующий в нуклеиновой кислоте, может быть связан экзогенной молекулой, которая распознает этот сайт-мишень. Не желая быть связанными какой-либо конкретной теорией, считается, что доступный участок - это участок, который не упакован в нуклеосомную структуру. Точную структуру доступного участка часто можно определить по его чувствительности к химическим или ферментным зондам, например нуклеазам. «Сайт-мишень» или «последовательность-мишень» представляет собой нуклеотидную последовательность, которая образует часть нуклеиновой кислоты, с которой связывается связывающая молекула при наличии достаточных для связывания условий. Например, последовательность 5'-GAATTC-3' является сайтом-мишенью для эндонуклеазы рестрикции EcoRI.
Ген. Применительно к настоящему раскрытию термин «ген» включает в себя участок ДНК, кодирующий продукт гена, а также все участки ДНК, которые регулируют синтез продукта гена независимо от того, соседствуют ли такие регуляторные последовательности с кодирующими и/или транскрибируемыми последовательностями или нет. Исходя из этого ген включает в себя, но не обязательно ограничивается этим, промоторные последовательности, терминаторы, последовательности, регулирующие трансляцию, такие как сайты связывания рибосом и сайты внутренней посадки рибосом, энхансеры, сайленсеры, инсуляторы, пограничные элементы, точки начала репликации, сайты присоединения к матриксу и участки контроля локусов.
Экспрессия. Термины «экспрессия» или «генная экспрессия» являются взаимозаменяемыми и относятся к преобразованию информации, содержащейся в гене, в продукт гена. Продуктом гена может быть непосредственный транскрипционный продукт гена (например, мРНК, тРНК, рРНК, антисмысловая РНК, рибозим, структурная РНК или любой другой тип РНК) или белок, получаемый в результате трансляции мРНК. Продукт гена также включает в себя РНК, которые были модифицированы в результате таких процессов как кэппирование, полиаденилирование, метилирование и редактирование, и белки, модифицированные, например, метилированием, ацетилированием, фосфорилированием, убиквитинированием, АДФ-рибозилированием, миристилированием и гликозилированием. Термин «модуляция» генной экспрессии относится к изменению активности гена. Модуляция экспрессии может включать в себя без ограничений активацию гена или репрессию гена.
Белок. Термины «полипептид», «пептид» и «белок» являются взаимозаменяемыми и относятся к полимеру аминокислотных остатков. Эти термины также применяются к аминокислотным полимерам, у которых одна или несколько аминокислот являются химическими аналогами или модифицированными производными соответствующих аминокислот, встречающихся в природе.
Последовательность. Термин «последовательность» относится к нуклеотидной последовательности любой длины, которая может быть ДНК или РНК, может быть линейной, кольцевой или разветвленной и может быть или одноцепочечной, или двухцепочечной. Термин «донорная последовательность» относится к нуклеотидной последовательности, которая встраивается в геном. Донорная последовательность может быть любой длины, например от 2 до 25000 нуклеотидов в длину (или любое целое число между ними или больше их), предпочтительно от примерно 100 до 5000 нуклеотидов в длину (или любое целое число между ними), более предпочтительно от примерно 200 до 2500 нуклеотидов в длину.
Гомологичная последовательность. Термин «гомологичная последовательность» относится к первой последовательности, которая обладает определенной степенью идентичности по последовательности со второй последовательностью и чья последовательность может быть идентичной последовательности второй последовательности. Термин «гомологичная неидентичная последовательность» относится к первой последовательности, которая обладает определенной степенью идентичности по последовательности со второй последовательностью, но чья последовательность не является идентичной последовательности второй последовательности. Например, полинуклеотид, включающий в себя последовательность дикого типа мутантного гена, является гомологичным и неидентичным последовательности мутантного гена. В некоторых вариантах осуществления изобретения степень гомологии между двумя последовательностями является достаточной для осуществления гомологичной рекомбинации между ними с использованием нормальных клеточных механизмов. Две гомологичных неидентичных последовательности могут быть любой длины, и степень их негомологичности может составлять один нуклеотид (например, для исправления геномной точечной мутации при помощи направленной гомологичной рекомбинации) или достигать 10 или более тысяч пар нуклеотидов (например, при встраивании гена в заранее определенный сайт на хромосоме). Два полинуклеотида, включающих в себя гомологичные неидентичные последовательности, не обязательно должны быть одинаковой длины. Например, экзогенный полинуклеотид (т.е. донорный полинуклеотид) длиной от 20 до 10000 нуклеотидов или нуклеотидных пар может быть использован.
Рекомбинация. Термин «рекомбинация» относится к процессу обмена генетической информацией между двумя полинуклеотидами. Применительно к настоящему раскрытию термин «гомологичная рекомбинация (ГР)» относится к специализированной форме такого обмена, который имеет место, например репарации двухцепочечных разрывов в клетке. Этот процесс требует гомологии нуклеотидных последовательностей, использует «донорную» молекулу для матричной репарации молекулы-«мишени» (т.е. молекулы, которая имеет двухцепочечный разрыв) и известен под разными наименованиями, таким как «некроссинговерная конверсия генов» или «конверсия коротких участков гена», потому что он приводит к передаче генетической информации от донора к мишени. Не желая быть связанными какой-либо конкретной теорией, такая передача может включать в себя исправление ошибочно спаренных оснований гетеродуплексной ДНК, которая образуется между разорванной мишенью и донором, и/или «синтез-зависимое спаривание цепей», при котором донор используется для ресинтеза генетической информации, которая станет частью мишени, и/или связанные с этим процессы. Такая специализированная ГР часто приводит к изменению последовательности молекулы-мишени таким образом, что часть или вся последовательность донорного полинуклеотида встраивается в полинуклеотид-мишень.
Расщепление. Термины «расщепление», «индуцирование двухцепочечного разрыва» и «разрыв» являются взаимозаменяемыми и относятся к разрыву ковалентного остова молекулы ДНК. Расщепление может быть инициировано различными способами, включая без ограничений ферментативный или химический гидролиз фосфодиэфирной связи. Возможно как одноцепочечное расщепление, так и двухцепочечное расщепление, и двухцепочечное расщепление может происходить в результате двух отдельных событий одноцепочечного расщепления. Расщепление ДНК может приводить к образованию или тупых концов или липких концов. В некоторых вариантах осуществления изобретения слитые полипептиды используются для направленного двухцепочечного расщепления ДНК. «Домен расщепления» включает в себя одну или несколько полипептидных последовательностей, обладающих каталитической активностью для расщепления ДНК. Домен расщепления может содержаться в одной полипептидной цепи, или расщепляющая активность может возникать в результате объединения двух (или более) полипептидов. «Неполный домен расщепления» представляет собой полипептидную последовательность, которая в сочетании со вторым полипептидом (или таким же, или другим) образует комплекс, обладающий расщепляющей активностью (как правило, двухцепочечной расщепляющей активностью). Термины «двухцепочечный разрыв» и «двухцепочечное расщепление» используются как синонимы.
Хроматин. Хроматин представляет собой нуклеопротеиновую структуру, вмещающую в себя геном клетки. Клеточный хроматин включает в себя нуклеиновую кислоту, преимущественно ДНК, и белок, включая гистоны и негистоновые хромосомные белки. Основная часть эукариотического клеточного хроматина существует в форме нуклеосом, где нуклеосомное ядро включает в себя приблизительно 150 пар оснований ДНК, связанных с октамером, включающим в себя по два каждого гистона H2A, H2B, H3 и H4; и ДНК-линкер (переменной длины в зависимости от организма) находится между нуклеосомными ядрами. Молекула гистона HZ обычно связана с ДНК-линкером. Применительно к настоящему раскрытию предполагается, что термин «хроматин» охватывает все типы клеточных нуклеопротеинов, как прокариотических, так и эукариотических. Клеточный хроматин включает в себя как хроматин хромосом, так и хроматин эписом.
Связывание. Термин «связывание» относится к сиквенс-специфичному, нековалентному взаимодействию между макромолекулами (например, между белком и нуклеиновой кислотой). При взаимодействии во время связывания не все компоненты обязательно являются сиквенс-специфичными (например, контакты в фосфатных остатках в остове ДНК) при условии, что взаимодействие в целом является сиквенс-специфичным. Такие взаимодействия, как правило, характеризуются константой диссоциации (Kd) 10-6 M-1 или ниже. Термин «сродство» относится к силе связывание: увеличенное сродство при связывании коррелирует с более низкой Kd.
Оперативная связь. Термины «оперативная связь» и «оперативно связанный» (или «операбельно связанный») являются взаимозаменяемыми и относятся к расположению в непосредственной близости двух или более компонентов (таких как элементы последовательности), при котором компоненты расположены так, что оба компонента функционируют нормально, и допускается возможность того, что, по меньшей мере, один из компонентов может обладать функцией, на которую оказывает действие, по меньшей мере, один из других компонентов. В качестве иллюстрации, регулирующая транскрипцию последовательность, такая как промотор, является оперативно связанной с кодирующей последовательностью, если эта регулирующая транскрипцию последовательность регулирует уровень транскрипции кодирующей последовательности в ответ на наличие или отсутствие одного или нескольких факторов регуляции транскрипции. Регулирующая транскрипцию последовательность, как правило, оперативно связана с кодирующей последовательностью, но не обязательно непосредственно примыкает к ней. Например, энхансер является последовательностью, регулирующей транскрипцию, которая оперативно связана с кодирующей последовательностью, даже если они не являются смежными. В случае слитых полипептидов термин «оперативно связанный» может относиться к тому факту, что каждый из компонентов, будучи связанным с другим компонентом, выполняет ту же функцию, какую он выполнял бы, если бы не был связан. Например, в случае слитого полипептида, в котором ДНК связывающий домен ZFP слит с доменом расщепления, ДНК связывающий домен ZFP и домен расщепления находятся в оперативной связи, если в этом слитом полипептиде область ДНК связывающего домена ZFP способна связываться с его сайтом-мишенью и/или его сайтом связывания, в то время как домен расщепления способен расщеплять ДНК вблизи от сайта-мишени.
Термин «сиквенс-специфичная нуклеаза (ССН)» относится к нескольким классам бифункциональных белков, способных распознавать специфичные и уникальные нуклеотидные последовательности (нативные или искусственно созданные сайты узнавания), таким как, без ограничений, мегануклеазы, лейциновые застежки-молнии и белки с цинковыми пальцами. Мегануклеазы представляют собой семейство ферментов, которые способны с высокой специфичностью расщеплять двухцепочечную ДНК в присутствии ионов двухвалентных металлов (Ca, Mn, Mg). Однако они отличаются от эндонуклеаз рестрикции по своим распознавательным свойствам и структуре (Belfort, M. Roberts RJ. Homing endonucleases: keeping the house in order; Nucleic Acid Research 1997, 25: 3379-3388). В частности, если эндонуклеазы рестрикции распознают короткие последовательности нуклеиновых кислот (3-8 п.н.), то мегануклеазы распознают более длинные последовательности (12-40 п.н.), что обеспечивает улучшенную специфичность при внесении ДЦР (Mueller, JE, Bryk, M. Loizos, N. Belfort M. Homing endonucleases. In Nucleases 2nd Edition. Linn, SM, Lloyd, RS, Roberts, RJ (Eds) Cold Spring Harbor Laboratory Press: 1993 111-143). Лейциновые застежки-молнии представляют собой класс белков, которые вовлечены в белок-белковые взаимодействия многих эукариотических регуляторных белков, являющихся важными факторами транскрипции, связанными с генной экспрессией. Термин «лейциновая застежка-молния» относится к структурному мотиву, общему для этих факторов транскрипции у представителей нескольких царств, включая животных, растения, дрожжи и т.д. Лейциновая застежка-молния образована двумя полипептидами (гомодимер или гетеродимер), которые связываются со специфичной последовательностью ДНК таким образом, что лейциновые остатки равномерно распределены по α-спирали, так что лейциновые остатки двух полипептидов оказываются на одной стороне спирали.
Связывающие ДНК белки с цинковыми пальцами. Связывающий ДНК белок с цинковым пальцем ZFP (или связывающий домен) представляет собой белок или домен большего белка, который связывает ДНК сиквенс-специфичным образом при помощи одного или нескольких цинковых пальцев, которые представляют собой участки аминокислотной последовательности связывающего домена, чья структура стабилизирована за счет координационных связей с ионом цинка. Термин «связывающий ДНК белок с цинковым пальцем» часто сокращают как белок с цинковым пальцем или ZFP. Связывающие домены цинкового пальца могут быть «сконструированы» так, чтобы связываться с заранее определенной нуклеотидной последовательностью. Неограничивающими примерами способов конструирования белков с цинковыми пальцами являются синтез и отбор. Синтезированным белком с цинковым пальцем является белок, не встречающийся в природе, чье строение/состав определены, в основном, исходя из рациональных критериев. Рациональные критерии для конструирования включают в себя применение правил замещения и компьютеризированных алгоритмов обработки информации в базе данных, хранящей информацию о существующих ZFP-конструкциях и данные о связывании. См., например, патенты США №№ 6140081; 6453242; 6534261 и 6785613; см., также международные заявки WO 98153058; WO 98153059; WO 98153060; WO 021016536 и WO 031016496; и патенты США №№ 6746838; 6866997 и 7030215.
Геномная последовательность. Геномные последовательности включают в себя последовательности, присутствующие в хромосомах, эписомах, геномах органелл (например, митохондрий, хлоропластов), искусственных хромосомах и в любом другом типе нуклеиновой кислоты, присутствующем в клетке, таком как, например, амплифицированные последовательности двойных микрохромосом и геномы эндогенных или инфицирующих бактерий и вирусов. Геномные последовательности могут быть нормальными (т.е. дикого типа) или мутантными; мутантные последовательности могут включать в себя, например, инсерции, делеции, транслокации, 25 перестройки и/или точечные мутации. Геномная последовательность может также включать в себя один из целого ряда различных аллелей.
Растительные клетки. Растительные клетки включают в себя без ограничений клетки односемянодольных (однодольных) или двусемянодольных (двудольных) растений, или водорослей, или мхов. Неограничивающие примеры однодольных включают в себя злаковые растения, такие как кукуруза, рис, ячмень, овес, пшеница, сорго, рожь, сахарный тростник, ананас, лук, банан и кокосовый орех. Неограничивающие примеры двудольных включают в себя табак, томат, подсолнечник, хлопчатник, сахарную свеклу, картофель, латук, дыню, сою, майолу (рапс) и люцерну. Растительные клетки могут быть получены из любой части растения и/или на любой стадии развития растения.
Целевая область. Целевая область представляет собой любой участок полимера нуклеиновой кислоты, такой как, например, ген или некодирующая последовательность внутри или рядом с геном, в котором желательно связывание экзогенной молекулы. Связывание может осуществляться с целью направленного расщепления ДНК и/или направленной рекомбинации. Целевая область может находиться, например, в хромосоме, эписоме, геноме органеллы (например, митохондриальном, хлоропластном), плазмиде, геноме инфицирующего вируса или в любой другой нуклеотидной последовательности. Целевая область может находиться в кодирующей области гена, в транскрибируемых не кодирующих областях, таких как, например, лидерные последовательности, концевые последовательност