Способ обеспечения улучшенного уплотнения с помощью фибрина
Иллюстрации
Показать всеИзобретение относится к медицине. Описана фибриновая матрица, описан способ ее получения и способ обработки или предотвращения дефекта на влажной ткани нуждающегося в обработке объекта. Описано использование для герметичного уплотнения дефекта в слизистой оболочке или другой влажной ткани. Фибриновая матрица является эффективной для уплотнения подтеканий ткани. 6 н. и 29 з.п. ф-лы, 3 ил., 1 табл., 3 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к фибриновой матрице с улучшенными уплотняющими свойствами, ее получению и использованию.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Фибриновый уплотнитель, как правило, представляет собой продукт крови, получаемый как из промышленных источников, так и из некоторых региональных центров переливания крови. К числу компонентов, обычно используемых для получения фибриновых уплотнителей, относятся, главным образом, фибриноген, дополненный различным количеством фактора VIII, фактора XIII, фибронектина, витронектина и фактора фон Виллебранда (vWF). Фибриногенный компонент, как правило, активируется последней протеазой коагулирующего каскада - тромбином.
Фибриновый уплотнитель образуется в результате ферментативной реакции, включающей среди прочего фибриноген, тромбин и фактор XIII. Тромбин преобразует фибриноген в фибрин путем ферментативного действия при скорости, обусловленной концентрацией тромбина. Фактор XIII, как правило, присутствует в фибриногенном компоненте уплотнителя и представляет собой фермент системы коагуляции крови, поперечно связывающий и стабилизирующий фибриновый сгусток. Этот процесс минует большинство этапов нормальной коагуляции и имитирует ее последнюю фазу. Некоторые производители добавляют антипротеолитические вещества в состав фибринового уплотнителя (см. патент WO 93/05822) или специально удаляют плазминоген с целью остановить или отсрочить фибринолиз (см. патенты США №№ 5792835 и 7125569).
В патенте США № 4427650 раскрывается тканевый адгезив, который можно наносить в виде сухой порошкообразной смеси сразу и непосредственно на рану или на операционное поле. Адгезив состоит из твердых порошкообразных биологически активных компонентов и содержит от 60 до 96% вес. фибриногена, выделенного преимущественно из крионерастворимого глобулина, от 0,05 до 5% вес. ингибитора фибринолиза и от 0,1 до 15% вес. тромбина и (или) протромбина.
В патенте США № 5962405 раскрывается лиофилизированный фибриногенный препарат для получения фибриногенного раствора, используемого в качестве тканевого адгезива. Фибриногенный препарат содержит вещество, улучшающее растворимость.
Некоторое время назад стало известно, что фибриновый уплотнитель можно накладывать на раны, такие как открытые раны человека, с целью их закрытия, остановки кровотечения и предотвращения попадания в рану других веществ, таких как инфекционные вещества.
Сообщалось о результатах применения фибринового уплотнителя для уплотнения дефектов в тканях, находящихся в постоянном движении, например тканях желудочно-кишечного тракта и легких. Однако в этих сообщениях присутствуют расхождения.
Один описанный подход к сокращению послеоперационных дефектов, таких как подтекания по линии скобочного или ниточного (скобочного/ниточного) шва после желудочно-кишечной резекции, подразумевает усиление скобочного/ниточного шва. В продаже имеются различные продукты для усиления скобочного/ниточного шва. Например, врачи применяют неабсорбируемые или полуабсорбируемые продукты для усиления скобочного шва, такие как Seamguard®, Peristrips Dry® и Surgisis®. Однако в ранних экспериментальных и клинических исследованиях абсорбируемый материал для усиления скобочного шва продемонстрировал существенные преимущества по сравнению с неабсорбируемым или полуабсорбируемым материалом для усиления скобочного шва (Yo et al. «Buttressing of the staple line in gastrointestinal anastomoses: overview of new technology designed to reduce perioperative complications». Dig Surg. 2006; 23:283-291). Недавние сообщения об использовании фибрина в качестве абсорбируемого усилителя скобочного шва для предотвращения послеоперационных подтеканий в области желудочно-кишечного тракта (Fullum et al. «Decreasing anastomotic and staple line leaks after laparoscopic Roux-en-Y gastric bypass». Surg Endosc. 2009; 23:1403-1408; Efthimiou et al. «Fibrin sealant associated with increased body temperature and leukocytosis after laparoscopic gastric bypass». Surg Obes Relat Dis. 17 марта 2009 г.) позволяют предположить, что существующие композиции фибриновых уплотнителей непригодны для усиления скобочных/ниточных швов.
В патенте США № 5690675 раскрывается способ закрытия ран в легочной ткани посредством двухэтапного способа, по существу состоящего из наложения скрепляющих элементов (например, скоб, клипс, штифтов, крючков) на околораневую область, где скрепляющие элементы могут образовывать проникающие отверстия. Скрепляющие элементы покрыты предварительно сформированным слоем коллагена, фибрина, фибриногена, эластина, альбумина или их комбинацией, и под воздействием на данную область энергии материал вплавляется в ткань и герметично уплотняет проникающие отверстия в ткани.
В патенте США № 5883078 раскрывается стабильный тканевый адгезив, содержащий фибриноген и активатор или проактиватор протромбина. Адгезив может быть представлен в жидкой или сухой форме. В одном варианте осуществления твердый 2-сторонний тканевый адгезив получают путем наложения сухого адгезива в твердой форме на раневую поверхность и последующей обработки второй раневой поверхности (второй части ткани) и кратковременного сжимания двух частей вместе. Препарат быстро растворяется при помощи присутствующей крови и (или) раневого секрета и затем отвердевает с началом коагуляции, при этом достигается плотное соединение и гемостатический эффект. Твердый 2-сторонний тканевый адгезив особенно подходит для соединения частей мягких тканей, таких как печень или селезенка.
Lillemoe et al. [(2004) J Gastrointest Surg., том 8, № 7, стр. 766-774 в статье под названием «Does Fibrin Glue Sealant Decrease the Rate of Pancreatic Fistula After Pancreaticoduodenectomy? Results of a Prospective Randomized Trial»] показали, что местное нанесение фибринового клея-уплотнителя на поверхность панкреатического анастомоза не способствовало снижению частоты возникновения свища поджелудочной железы или общих осложнений у пациентов после панкреатикодуоденэктомии, и пришли к заключению, что применение этого вещества в данном случае не приносит пользы.
Другое исследование («The sealing effect of fibrin glue against alveolar air leakage evaluated up to 48h; comparison between different methods of application» Kawamura et al. (2005 г.) Eur J of Cardiothorac Surg. 28(1):39-42) раскрывает уплотняющее действие фибринового клея против утечки альвеолярного воздуха на примере животной модели и оценивает различные способы применения. Использовали раствор A, состоящий из протеинового концентрата, содержащего фибриноген, и раствор B, содержащий тромбин. В рамках способа нанесения растиранием и распылением раствор A наносили по каплям и осторожно растирали на поверхности области утечки воздуха. Затем оба раствора одновременно распыляли в виде смешанного аэрозоля. В рамках другого способа получали двойной слой путем нанесения по каплям раствора A на поверхность области утечки воздуха, после чего по каплям наносили раствор B. В рамках другого способа на животных моделях (собаки) использовали коллагеновую матрицу, с одной стороны покрытую сухим фибриногеном и тромбином (TachoComb), и проверяли результаты по истечении 24 часов. По словам авторов, уплотняющий эффект фибринового клея остается относительно нестабильным в течение периода до 12 часов после нанесения. Кроме того, авторы пришли к выводу, что способ нанесения растиранием и распылением может способствовать повышению скорости достижения фибриновым уплотнителем своей полной силы по сравнению с другими двумя способами.
Другое исследование, проведенное Yo et al. (2006 г.) (Dig Surg 23: 283-291), раскрывает попытки уменьшить осложнения анастомоза, такие как кровотечение или подтекание по линии скобочного шва, при выполнении желудочно-кишечных резекций. Yo отмечает, что у животной модели крысы при толстокишечном анастомозе применение фибринового клея для уплотнения и предотвращения подтекания не представляется целесообразным. В работе раскрывается, что при резекции желудка применение фибринового клея для поддержки и уплотнения скобочного шва представляется более успешным.
В патенте США № 7196054 раскрывается способ обработки поврежденной ткани у пациента, включающий нанесение на поврежденную ткань композиции в форме сухого порошка, содержащего фибриноген в количестве, достаточном для формирования фибриновой матрицы в присутствии тромбина, фактора XIII, Ca2+ и водного раствора; введение в композицию тромбина, фактора XIII, Ca2+ и водного раствора в количествах, достаточных для формирования фибриновой матрицы в присутствии фибриногена.
Fullum et al. (2009 г.) раскрывает, что несостоятельность анастомоза и подтекания по линии скобочного шва (ASL) появляются после лапароскопического шунтирования желудка с гастроеюноанастомозом по Ру (LRYGB) у пациентов, страдающих ожирением. Фибриновый уплотнитель наносили вдоль линии скобочного шва на желудке. Авторы пришли к выводу, что оперативная техника, включая подходящий размер скоб, усиление скобочного шва, сшивание разреза вручную, фиксирующий шов, испытание на протекание, проводимое во время операции, и фибриновые уплотнители, стала инструментом для снижения частоты возникновения ASL после LRYGB. Авторам не удалось установить, какой из компонентов сыграл основную роль в предотвращении ASL.
В отличие от этого Efthimiou et al. (2009 г.) раскрывает, что использование фибринового уплотнителя не повлияло на степень несостоятельности анастомоза и подтеканий по линии скобочного шва при LRYGB.
Существует неудовлетворенная потребность в усовершенствованном составе фибринового уплотнителя для уплотнения дефектов в тканях, находящихся в постоянном движении, например тканях желудочно-кишечного тракта и легких.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящее время фибриновые уплотнители применяют в основном для гемостаза; это действие может быть усилено аутогенными факторами свертывания крови, например фибриногеном, присутствующим в крови, покрывающей раневую область.
Фибриновый уплотнитель применяется также для уплотнения ткани при подтекании, например при утечке воздуха и (или) текучей среды, например мочи, пищеварительной жидкости, серозной жидкости. Обычно при наличии в тканях таких подтеканий аутогенные факторы свертывания крови отсутствуют. Большинство уплотнителей, включая синтетические уплотнители, не эффективны для уплотнения подтеканий в тканях. Без привязки к механизму воздух/жидкость может выступать в качестве барьера между уплотнителем и тканью и, таким образом, препятствует непосредственному контакту между уплотнителем и тканью.
Как правило, хирурги часто максимально высушивают раневую подтекающую поврежденную ткань перед нанесением уплотнителя. Обычно высушивание выполняется вручную при помощи губки/марли и газового спрея (Hidas et al. «Sutureless nephron-sparing surgery: use of albumin glutaraldehyde tissue adhesive (BioGlue)». Urology, 2006; 67:697-700). Эти процедуры по высушиванию повышают риск слипания ткани (Kamel RM. «Prevention of postoperative peritoneal adhesions». Eur J Obstet Gynecol Reprod Biol. 2010; 150(2):111-118).
Кроме того, эти процедуры по высушиванию также проблематично выполнить на недоступных для хирурга участках, например при выполнении лапароскопических операций.
Настоящее изобретение предлагает фибриновую матрицу, эффективную для уплотнения подтеканий ткани.
В одном аспекте настоящее изобретение относится к способу нанесения фибриновой матрицы на влажную ткань, включающему: нанесение эффективного количества твердой фибриновой уплотнительной смеси на влажную ткань; и нанесение эффективного количества жидкой фибриновой уплотнительной композиции поверх по меньшей мере части нанесенной твердой фибриновой уплотнительной смеси, причем эффективные количества твердой фибриновой уплотнительной смеси и жидкой фибриновой уплотнительной композиции достаточны для формирования фибриновой матрицы на влажной ткани, обладающей более высокой уплотняющей способностью, связанной с нанесением эффективного количества либо жидкой фибриновой уплотнительной композиции, либо твердой фибриновой уплотнительной смеси.
В одном варианте осуществления настоящего изобретения уплотняющая способность возрастает по меньшей мере в 1,2 раза по отношению к нанесению жидкой фибриновой уплотнительной композиции.
В другом варианте осуществления настоящего изобретения уплотняющая способность возрастает приблизительно в 1,7 раза по отношению к нанесению жидкой фибриновой уплотнительной композиции.
В другом дополнительном варианте осуществления настоящего изобретения нанесение осуществляется на ткань, которая является необогащенной, имеет небольшое количество, недостаточное количество или не имеет кровеносных сосудов, и (или) на ткани, медленно выделяющие текучую среду или некровоточащие.
В одном варианте осуществления настоящего изобретения твердая фибриновая уплотнительная смесь содержит твердый компонент, содержащий фибриноген, и твердый компонент, содержащий протеолитический ферментный компонент, способный образовывать фибрин при взаимодействии с фибриногеном.
В другом дополнительном варианте осуществления настоящего изобретения компонент твердой фибриновой уплотнительной смеси, содержащий фибриноген, готовят на стадии высушивания фибриноген-содержащего раствора с концентрацией фибриногена менее 25 мг/мл.
В одном варианте осуществления настоящего изобретения концентрация фибриногена составляет приблизительно 20 мг/мл.
Еще в одном варианте осуществления настоящего изобретения протеолитический фермент представляет собой тромбин.
В другом дополнительном варианте осуществления настоящего изобретения нанесение осуществляется на тканевый дефект.
Еще в одном варианте осуществления настоящего изобретения нанесение осуществляется по меньшей мере на часть скобочного или ниточного шва на ткани.
Другой аспект настоящего изобретения относится к способу получения фибриновой матрицы на влажной поверхности, включающему следующие стадии: предоставление твердого компонента, содержащего фибриноген; предоставление твердого компонента, содержащего протеолитический фермент, способный к образованию фибрина при взаимодействии с фибриногеном; предоставление жидкой фибриновой уплотнительной композиции; нанесение эффективного количества твердых компонентов по меньшей мере на часть влажной поверхности; и нанесение эффективного количества жидкой фибриновой уплотнительной композиции поверх по меньшей мере части нанесенных твердых компонентов.
В одном варианте осуществления настоящего изобретения влажная поверхность не содержит фибриногена.
В другом варианте осуществления настоящего изобретения жидкую фибриновую уплотнительную композицию предоставляют в твердой форме и восстанавливают перед нанесением.
В другом дополнительном варианте осуществления настоящего изобретения жидкую фибриновую уплотнительную композицию предоставляют в замороженном виде и размораживают перед нанесением.
В другом варианте осуществления настоящего изобретения твердый компонент предоставляют в жидкой форме и высушивают перед нанесением.
Еще в одном варианте осуществления настоящего изобретения твердый компонент предоставляют в замороженном виде и высушивают перед нанесением.
В другом дополнительном варианте осуществления настоящего изобретения твердые компоненты наносят одновременно или один за другим.
В другом варианте осуществления настоящего изобретения жидкие компоненты наносят одновременно или один за другим.
В другом дополнительном варианте осуществления настоящего изобретения твердые компоненты представлены в виде смеси.
В одном варианте осуществления настоящего изобретения поверхность представляет собой ткань.
В одном варианте осуществления настоящего изобретения ткань является необогащенной, имеет небольшое количество, недостаточное количество или не имеет кровеносных сосудов и (или) медленно выделяет текучую среду или не кровоточит.
В другом аспекте настоящее изобретение относится к фибриновой матрице, получаемой в соответствии с настоящим изобретением.
Еще в одном аспекте настоящее изобретение предлагает способ обработки или предотвращения дефекта на влажной ткани нуждающегося в обработке объекта, включающий следующие стадии:
a) предоставление компонента, содержащего твердый фибриноген, предоставление компонента, содержащего твердый протеолитический фермент, способный к образованию фибрина при взаимодействии с фибриногеном; и предоставление жидкой фибриновой уплотнительной композиции;
b) нанесение эффективного количества твердых компонентов из п. a) по меньшей мере на часть влажной поверхности; и
c) нанесение эффективного количества жидкой фибриновой уплотнительной композиции из п. a) поверх по меньшей мере части нанесенных твердых компонентов.
В одном варианте осуществления настоящего изобретения влажная ткань является необогащенной, имеет небольшое количество, недостаточное количество или не имеет кровеносных сосудов и (или) медленно выделяет текучую среду или не кровоточит.
В другом варианте осуществления настоящего изобретения дефект представляет собой подтекание в ткани.
В другом дополнительном варианте осуществления настоящего изобретения просачивающееся вещество является необогащенным, имеет небольшое количество, недостаточное количество или не имеет плазмы или компонентов крови.
В одном варианте осуществления настоящего изобретения жидкую фибриновую уплотнительную композицию предоставляют в твердой форме и восстанавливают перед нанесением.
В другом дополнительном варианте осуществления настоящего изобретения жидкую фибриновую уплотнительную композицию предоставляют в замороженном виде и размораживают перед нанесением.
В одном варианте осуществления настоящего изобретения твердый компонент предоставляют в жидкой форме и высушивают перед нанесением.
Еще в одном варианте осуществления настоящего изобретения твердый компонент предоставляют в замороженном виде и высушивают перед нанесением.
В другом дополнительном варианте осуществления настоящего изобретения твердые компоненты наносят одновременно или один за другим.
В одном варианте осуществления настоящего изобретения жидкие компоненты наносят одновременно или один за другим.
В другом варианте осуществления настоящего изобретения твердые компоненты из п. a) представлены в виде смеси.
В другом дополнительном варианте осуществления настоящего изобретения дефект представляет собой скобу или нить.
В одном аспекте настоящее изобретение предлагает набор, содержащий: (i) контейнер(ы), содержащий(ие) твердые компоненты, содержащие (a) фибриногенный компонент и (b) протеолитический ферментный компонент, способный к образованию фибрина при взаимодействии с фибриногеном, причем компоненты (a) и (b) находятся в отдельных контейнерах или в одном и том же контейнере в виде смеси; и (ii) по меньшей мере два отдельных контейнера, причем по меньшей мере один отдельный контейнер содержит жидкий, замороженный или твердый фибриногенный компонент, и по меньшей мере второй отдельный контейнер содержит жидкий, замороженный или твердый протеолитический ферментный компонент, способный к образованию фибрина при взаимодействии с фибриногеном, при этом если по меньшей мере два отдельных контейнера (ii) содержат твердые компоненты, то компоненты (a) и (b) находятся в одном и том же контейнере в виде смеси.
В одном варианте осуществления настоящего изобретения протеолитический фермент представляет собой тромбин.
В другом варианте осуществления настоящего изобретения набор используют применительно к влажной поверхности.
В другом дополнительном варианте осуществления настоящего изобретения набор применяют для уплотнения подтеканий в тканях, которые являются необогащенными, имеют небольшое количество, недостаточное количество или не имеют кровеносных сосудов, и (или) тканях, медленно выделяющих текучую среду или некровоточащих.
Фибриновую матрицу или набор в соответствии с настоящим изобретением можно использовать для обработки или предотвращения дефекта на влажной ткани.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
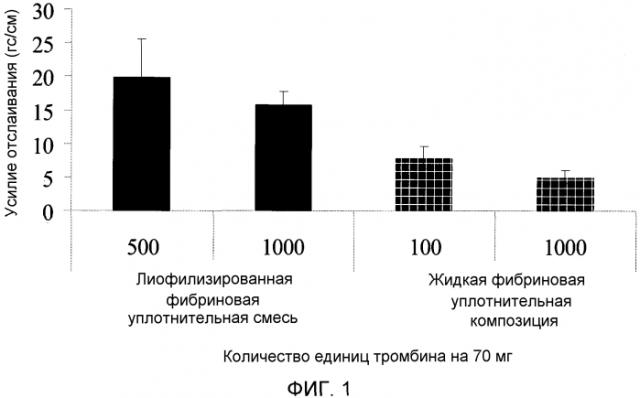
На фигуре 1 представлено усилие, необходимое для отделения двух слоев ткани подвздошной кишки (усилие отслаивания), связанных вместе при помощи двух различных фибриновых уплотнительных композиций: смеси лиофилизированного фибриногена и тромбина в сравнении с двухкомпонентной жидкой фибриновой уплотнительной композицией.
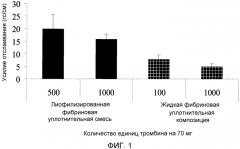
На фигуре 2 представлена уплотняющая способность (измеренная путем разрушающего испытания) смеси лиофилизированного фибриногена и тромбина, двухкомпонентной жидкой фибриновой уплотнительной композиции и фибриновой матрицы, полученной путем последовательного нанесения лиофилизированного фибриногена и тромбина и двухкомпонентного жидкого фибринового уплотнителя.
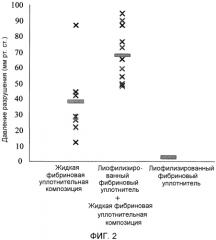
На фигуре 3 представлена уплотняющая способность (измеренная путем разрушающего испытания) фибрина, полученного путем нанесения лиофилизированного тромбина с последующим распылением жидкого фибринового уплотнителя; фибрина, полученного путем нанесения лиофилизированного фибриногена с последующим распылением жидкого фибринового уплотнителя; фибрина, полученного путем нанесения смеси лиофилизированного фибриногена и тромбина с последующим распылением жидкого фибринового уплотнителя; и фибриновой композиции, полученной путем нанесения сухого альбумина с последующим распылением жидкого фибринового уплотнителя.
ПОДРОБНОЕ ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способу нанесения фибриновой матрицы на слизистую оболочку или другую влажную ткань, причем способ включает в себя последовательное нанесение твердой фибриновой уплотнительной смеси на поверхность ткани с последующим нанесением жидкой фибриновой уплотнительной композиции поверх по меньшей мере части поверхности. Настоящее изобретение также относится к эффективному уплотнению дефекта на слизистой оболочке или другой влажной ткани путем последовательного нанесения сначала твердой фибриновой уплотнительной смеси, а затем жидкой фибриновой уплотнительной композиции.
В основе настоящего изобретения лежат следующие данные исследования.
Силу адгезии (или усилие отслаивания) различных испытываемых фибриновых композиций изучали путем проведения исследования на отслаивание. Испытание позволяет измерить прочность соединения фибринового клея между слоями подслизистой оболочки тонкой кишки свиньи. В одном варианте осуществления испытываемую адгезивную композицию наносили на серозное поле подвздошной кишки свиньи. После нанесения испытываемой фибриновой уплотнительной композиции ткань подвздошной кишки сворачивали (сероза к серозе) и оставляли фибриновую уплотнительную композицию для полимеризации. Усилие, необходимое для отделения двух слипшихся слоев ткани подвздошной кишки друг от друга (усилие отслаивания), измеряли при помощи универсальных разрывных испытательных машин LFPLUS производства Lloyd Instruments. Обычно чем выше измеренное усилие отслаивания, тем больше сила адгезии испытываемой композиции. В соответствии с настоящим изобретением было установлено, что сила адгезии существенно повысилась благодаря использованию лиофилизированной фибриновой уплотнительной композиции вместо жидкой фибриновой уплотнительной композиции. Было установлено, что сила адгезии лиофилизированной фибриновой уплотнительной композиции была приблизительно в 2,7 раза выше по сравнению с силой адгезии жидкой фибриновой уплотнительной композиции.
Уплотняющие свойства различных фибриновых композиций измеряли путем проведения разрушающего испытания. Разрушающее испытание позволяет определить и оценить способность уплотнителя предотвращать подтекание. Коротко говоря, алюминиевую трубку, соединенную с источником воды и имеющую отверстия, вводят в трубчатый сегмент подвздошной кишки свиньи, который уплотняют и зажимают на обоих концах трубки. После этого в алюминиевую трубку подают воду, вода поступает через отверстия в пространство между подвздошной кишкой и алюминиевой трубкой, при этом обратный ток воды в алюминиевую трубку исключается. Перед подачей воды выполняют 10-миллиметровый разрез перпендикулярно длине кишки, разрез сначала сшивают нитью по средней линии, а затем на область разреза наносят испытываемую фибриновую уплотнительную композицию через трафарет из парафильма площадью 6 см2, который размещают вокруг области разреза. После нанесения испытываемой композиции фибрин оставляют для отверждения (или полимеризации) в течение 10 минут и заполняют кишечник водой для изучения его способности выдерживать давление. При поступлении воды в пространство между подвздошной кишкой и трубкой давление воды возрастает до тех пор, пока уплотнение разреза не откроется и не произойдет резкое понижение давления. Уровень давления измеряют при помощи манометра (D-logmate 590 MRC (Израиль)), соединенного с линией подачи жидкости. Давление, измеренное до понижения, регистрируют и принимают за давление разрушения. Обычно более высокое зарегистрированное давление разрушения указывает на более высокие уплотняющие свойства испытываемой композиции.
В соответствии с настоящим изобретением также было установлено, что лиофилизированный фибриновый уплотнитель, показавший более высокую силу адгезии по сравнению с жидким фибриновым уплотнителем, оказался неэффективным для уплотнения. В отличие от этого жидкая фибриновая уплотнительная композиция обладает лучшим уплотняющим действием, чем лиофилизированный фибриновый уплотнитель.
Кроме того, неожиданно установлено, что последовательное нанесение лиофилизированного фибринового уплотнителя и жидкой фибриновой уплотнительной композиции обеспечивает взаимоусиливающее повышение уплотняющего свойства. Отмечено повышение уплотняющей способности приблизительно в 1,7 раза по сравнению с уплотняющей способностью жидкой фибриновой уплотнительной композиции. Однако взаимоусиливающее повышение уплотняющих свойств не было выявлено при последовательном нанесении лиофилизированного фибриногена или лиофилизированного тромбина с последующим введением жидкой фибриновой уплотнительной композиции.
Также было установлено, что высушивание слизистой оболочки перед нанесением жидкой фибриновой уплотнительной композиции (например, путем нанесения сухого белка, такого как сухой альбумин, на слизистый слой) не приводит к повышению уплотняющих характеристик жидкой фибриновой уплотнительной композиции.
Эти данные способствовали разработке усовершенствованного способа создания фибриновой матрицы с более высокой уплотняющей способностью на слизистой оболочке или другой влажной ткани. Фибриновую матрицу, полученную в соответствии с принципами настоящего изобретения, можно использовать для уплотнения дефектов в слизистой оболочке или другой влажной ткани, например на тканях, находящихся в постоянном движении, таких как ткани желудочно-кишечного тракта и легких.
Термин «ткань» относится к ассоциации клеток и (или) клеточных компонентов, объединенных для выполнения конкретной функции. Клетки в ткани могут принадлежать к одному типу или более чем к одному типу. Ткань может быть искусственной, где клетки выращены для обеспечения функционирования подобно ткани в живом организме. Ткань может быть тканью организма человека или животного.
Термин «фибриновая матрица» относится к фибрину, полученному путем последовательного нанесения твердой фибриновой уплотнительной смеси и жидкой фибриновой уплотнительной композиции.
Термин «эффективное количество твердой фибриновой уплотнительной смеси» относится к количеству твердого компонента, содержащего фибриноген, и количеству твердого компонента, содержащего протеолитический фермент, способный к образованию фибрина при взаимодействии с фибриногеном, которые после гидратации на влажной ткани образуют фибриновый сгусток.
Термин «эффективное количество жидкой фибриновой уплотнительной композиции» относится к количеству жидкого компонента, содержащего фибриноген, и количеству жидкого компонента, содержащего протеолитический фермент (способный к образованию фибрина при взаимодействии с фибриногеном), которые обеспечивают образование фибринового сгустка после смешивания жидких компонентов.
Без привязки к механизму получается, что после нанесения твердой уплотнительной смеси на влажную ткань происходит ее гидратация. Гидратированная твердая уплотнительная смесь заполняет ткань, отверждая жидкость, присутствующую во влажной ткани и образуя фибриновый слой в непосредственной близости к ткани. Затем наносят жидкую фибриновую уплотнительную композицию на эту заполненную ткань, что приводит к повышению уплотняющей способности и прочности.
Преимущество состоит в том, что отверждение влаги на поверхности без необходимости использовать губку или марлю способно снизить риск образования спаек в послеоперационном периоде.
Термин «спайка» относится к неправильному соединению между тканями и (или) органами. Обычно спайки образуются после хирургических операций, например вследствие неравномерной обработки тканей; вследствие высушивания поверхности ткани и (или) из-за присутствия реакционно-способных инородных тел (например, шовных материалов, тальковой пудры или остатков волокна) на операционном поле.
Термин «слизистая оболочка» или «слизистая ткань» относится к влажной ткани, покрывающей некоторые органы и полости организма. Обычно слизистая ткань секретирует слизистый материал. Примеры слизистой ткани включают, помимо прочего, слизистую оболочку полости рта, например буккальную и сублингвальную; слизистую оболочку носа; слизистую оболочку глаза; слизистую оболочку половых органов; ректальную слизистую оболочку; слизистую оболочку уха; слизистую оболочку легких; слизистую оболочку бронхов; слизистую оболочку желудка; слизистую оболочку кишечника; слизистую оболочку органов обоняния; слизистую оболочку матки; и слизистую оболочку пищевода. Термин «слизистый» используется для определения сырого (влажного) и вязкого материала, такого как вещество, богатое муцином, альбумином гликопротеина и (или) другим компонентом, обуславливающим вязкость.
Термин «другая влажная ткань» относится к смачиваемой ткани. Ткань может смачиваться физиологическими жидкостями организма, такими как сыворотка, инфильтрат сыворотки, кровь и воспалительные жидкости, и (или) другими жидкостями (текучими средами), такими как фосфатный буферный раствор (ФБР). В одном варианте осуществления настоящего изобретения текучая среда не содержит факторов свертывания крови (т.е. не содержит фибриногена).
В рамках настоящего документа термин «дефект» относится к надрыву, расхождению, каналу, фиссуре, проколу, ране, свищу, отверстию, порезу, щели, перфорации, трещине, проколу или разрыву, подтеканию, например в ткани. Например, дефект может возникнуть в результате наложения анастомоза. Дефект может быть врожденным, например грыжа; вызван патологией в организме, например серома, грыжа, инфекция, воспаление; возникнуть после хирургического вмешательства, наложения ниточного и (или) скобочного шва; или обусловлен внешними факторами, например такими как несчастный случай, травмы.
Термин «подтекание» относится к просачиванию или вытеканию вещества, например текучей среды, вязкого материала и (или) воздуха, например через надрыв, расхождение, канал, фиссуру, прокол, рану, свищ, отверстие, порез, щель, перфорацию, трещину, прокол или разрыв в ткани.
Термин «анастомоз» обычно используется для обозначения хирургической процедуры, применяемой для повторного соединения двух или более участков органа или ткани. Процедуру можно выполнять после рассечения мочевыводящих путей (уретры), горла (пищевода) или при проведении хирургических операций на кишечнике. Процедуру также можно выполнять после удаления пораженной ткани (такой как воспаленная, раковая ткань или ткань с иной патологией, например при язвенной болезни).
Настоящее изобретение также относится к набору, содержащему: (i) контейнер(ы), содержащий(ие) твердые компоненты, содержащие (a) фибриногенный компонент и (b) протеолитический ферментный компонент, способный к образованию фибрина при взаимодействии с фибриногеном; и (ii) по меньшей мере два отдельных контейнера, причем по меньшей мере один отдельный контейнер содержит жидкий, замороженный или твердый фибриногенный компонент, и по меньшей мере второй отдельный контейнер содержит жидкий, замороженный или твердый протеолитический ферментный компонент, способный к образованию фибрина при взаимодействии с фибриногеном.
Компоненты (a) и (b) элемента (i) могут находиться в отдельных контейнерах или в одном и том же контейнере в виде смеси. В одном варианте осуществления, если по меньшей мере два отдельных контейнера (ii) содержат твердые компоненты, то компоненты (a) и (b) находятся в одном и том же контейнере в виде смеси. В другом варианте осуществления, если по меньшей мере два отдельных контейнера (ii) содержат твердые компоненты, то по меньшей мере один контейнер содержит водный раствор для их гидратации.
В отличие от имеющихся в продаже фибриновых наборов, предназначенных специально для гемостаза, набор, составляющий предмет настоящего изобретения, также допустим для уплотнения подтеканий в тканях, которые не являются обогащенными, имеют небольшое количество, недостаточное количество или не имеют кровеносных сосудов.
Неограничивающими примерами тканей, не являющихся обогащенными, имеющих небольшое количество, недостаточное количество или не имеющих кровеносных сосудов, являются: твердая мозговая оболочка, мочевой пузырь, глаза, легкие и желчный пузырь.
В одном варианте осуществления настоящего изобретения набор предназначен для уплотнения подтеканий в тканях, не являющихся обогащенными, имеющих небольшое количество, недостаточное количество или не имеющих кровеносных сосудов.
Термин «гемостаз» относится к способности агента останавливать кровотечение из поврежденного кровеносного сосуда и (или) способствовать удержанию крови внутри кровеносного сосуда.
Кроме того, в отличие от имеющихся в продаже фибриновых наборов, предназначенных специально для остановки кровотечения из поврежденного кровеносного сосуда и (или) для удержания крови внутри кровеносного сосуда, набор, составляющий предмет настоящего изобретения, также допустим для уплотнения подтеканий веществ, не содержащих крови и плазмы, например таких как цереброспинальная жидкость (ЦСЖ), воздух, содержимое кишечника, желчь, лимфатическая жидкость и жидкая часть стекловидного тела.
В одном варианте осуществления фибриновая матрица или набор, составляющий предмет настоящего изобретения, предназначен для уплотнения подтеканий в тканях, медленно выделяющих текучую среду или некровоточащих. Термин «медленное выделение текучей среды» обозначает, например, незначительное кровотечение. Термин «медленное выделение текучей среды» охватывает случаи кровотечения, где имеет место относительно низкая кровопотеря при относительно низкой скорости.
Набор также может содержать инструкцию по применению. Набор также может содержать средства для рассечения и (или) сшивания ткани или органа скобами или нитью, такие как механические или ручные режущие и сшивающие устройства. В качестве контейнера можно использовать ампулу, предварительно наполненный шприц, бутылек, трубку или любой другой допустимый контейнер, содержащий твердые или жидкие компоненты. Контейнеры могут быть разного размера и содержать различный объем (массу) композиций, например каждый жидкий компонент может иметь объем не более приблизительно 10 мл, а каждый твердый компонент может иметь массу сухого вещества не более приблизительно 3 г. В набор также может быть необязательно включен аппликатор для введения твердых и жидких компонентов.
Фибриновую матрицу или набор в соответствии с настоящим изобретением можно использовать для любых терапевтических целей. Термин «любые терапевтические цели» относится к любым видам лечения и профилактики у объекта. Примеры терапевтических целей включают, помимо прочего, уплотнение высве