4'-азидонуклеозиды, активные в отношении hcv
Иллюстрации
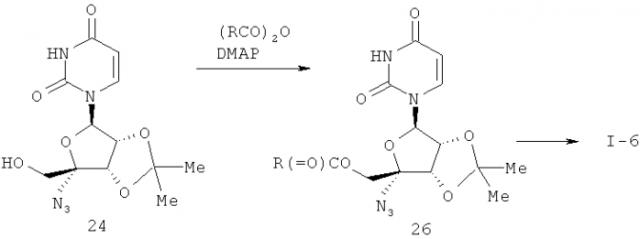
Показать всеНастоящее изобретение относится к соединениям для лечения вирусного гепатита формулы:
где R1, R2 и R3 независимо выбраны из водорода и С1-6алкилкарбонила; при условии, что по меньшей мере один из R1, R2 и R3 отличается от водорода, и при условии, что соединение согласно формуле I не является сложным (2R,3R,4S,5R)-4-ацетокси-5-ацетоксиметил-5-азидо-2-(2,4-диоксо-3,4-дигидро-2Н-пиримидин-1-ил)-тетрагидро-фуран-3-иловым эфиром уксусной кислоты, а также их фармацевтически приемлемым солям и фармацевтическим композициям на их основе. Предложены новые эффективные средства для лечения инфекции вируса гепатита С. 5 н. и 7 з.п. ф-лы, 9 пр., 8 ил.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Согласно настоящему изобретению предложены ацилированные нуклеозиды, которые представляют собой пролекарства ингибитора РНК-зависимой вирусной РНК-полимеразы вируса гепатита С (HCV). При пероральном введении данные соединения легко поглощаются из ЖК (желудочно-кишечный) тракта и эффективно превращаются обратно в родительский нуклеозид в крови. Эти пролекарства представляют собой ингибиторы РНК-зависимой репликации вирусной РНК и являются полезными в качестве ингибиторов полимеразы NS5B HCV, в качестве ингибиторов репликации HCV и для лечения инфекции гепатитом С у млекопитающих. В частности, изобретение касается применения ацилированных пиримидиновых нуклеозидных соединений, которые обеспечивают улучшенное поглощение лекарственного средства при пероральном введении нуклеозида.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Вирус гепатита С является ведущей причиной хронического заболевания печени во всем мире. (Boyer, N. et al., J. Hepatol. 2000 32:98-112). Пациенты, инфицированные HCV, подвергаются риску развития цирроза печени и последующей гепатоклеточной карциномы, и, следовательно, HCV является главным показанием для трансплантации печени.
HCV классифицировали как члена вирусного семейства Flaviviridae, которое включает роды флавивирусов, пестивирусов и хапацеивирусов, который включает вирусы гепатита С (Rice, С.М., Flaviviridae: The viruses and their replication. In: Fields Virology, Editors: B.N.Fields, D.М.Knipe and P.М.Howley, Lippincott-Raven Publishers, Philadelphia, Pa., Chapter 30, 931-959, 1996). HCV представляет собой оболочечный вирус, содержащий геном в виде одноцепочечной РНК положительной полярности, имеющей размер приблизительно 9,4 т.п.н. Вирусный геном состоит из высококонсервативной нетранслируемой 5'-области (UTR), длинной открытой рамки считывания, кодирующей полибелковый предшественник из приблизительно 3011 аминокислот, и короткой 3' UTR.
Генетический анализ HCV идентифицировал шесть главных генотипов, которые дивергируют по последовательности ДНК более чем на 30%. Различали более чем 30 подтипов. В США приблизительно 70% инфицированных индивидуумов имеют инфекцию Типа 1а и 1b. Тип 1b является самым превалирующим подтипом в Азии. (X. Forns and J. Bukh, Clinics in Liver Disease 1999 3:693-716; J. Bukh et al., Semin. Liv. Dis. 1995 15:41-63). К сожалению, инфекции типа 1 являются более устойчивыми к терапии, чем генотипы типа 2 или 3 (N.N. Zein, Clin. Microbiol. Rev.. 2000 13:223-235).
Вирусные структурные белки включают коровый белок нуклеокапсида (С) и два гликопротеина оболочки, Е1 и Е2. HCV также кодирует две протеазы, цинк-зависимую металлопротеиназу, кодируемую областью NS2-NS3, и сериновую протеазу, кодируемую областью NS3. Данные протеазы требуются для расщепления конкретных областей полибелка-предшественника на зрелые пептиды. Карбоксильная половина неструктурного белка 5, NS5B, содержит РНК-зависимую РНК-полимеразу. Функция остальных неструктурных белков, NS4A и NS4B, и функция NS5A (аминоконцевой половины неструктурного белка 5) остается неизвестной. Считается, что большинство неструктурных белков, кодируемых РНК-геномом HCV, участвует в репликации РНК.
В настоящее время для лечения инфекции HCV доступно ограниченное число одобренных терапий. Были сделаны обзоры новых и существующих терапевтических подходов для лечения инфекции HCV и ингибирования активности полимеразы NS5B HCV: R.G. Gish, Sem. Liver. Dis., 1999 19:5; Di Besceglie, A.M. and Bacon, B.R., Scientific American, October: 1999 80-85; G. Lake-Bakaar, Current and Future Therapy for Chronic Hepatitis С Virus Liver Disease, Curr. Drug Targ. Infect Dis. 2003 3(3):247-253; P. Hoffmann et al., Recent patent on experimental therapy for hepatitis С virus infection (1999-2002), Exp. Opin. Ther. Patents 2003 13(11): 1707-1723; M.P. Walker et al., Promising Candidates for the treatment of chronic hepatitis C, Exp. Opin. Investing. Drugs 2003 12(8): 1269-1280; S.-L. Tan et al., Hepatitis С Therapeutics: Current Status and Emerging Strategies, Nature Rev. Drug Discov. 2002 1:867-881; J.Z. Wu and Z. Hong, Targeting NS5B RNA-Dependent RNA Polymerase for Anti-HCV Chemotherapy, Curr. Drug Targ. - Infect. Dis. 2003 3(3):207-219.
В настоящее время имеется ограниченное число одобренных терапий, доступных в настоящее время, для лечения инфекции HVC. Были сделаны обзоры новых и существующих терапевтических подходов для лечения HCV и ингибирования полимеразы NS5B HCV: R.G. Gish, Sem. Liver. Dis., 1999 19:5; Di Besceglie, A.M. and Bacon, B.R., Scientific American, October: 1999 80-85; G. Lake-Bakaar, Current and Future Therapy for Chronic Hepatitis С Virus Liver Disease, Curr. Drug Targ. Infect Dis. 2003 3(3):247-253; P. Hoffmann et al., Recent patents on experimental therapy for hepatitis С virus infection (1999-2002), Exp. Opin. Ther. Patents 2003 13(11): 1707-1723; F.F. Poordad et al. Developments in Hepatitis С therapy during 2000-2002, Exp. Opin. Emerging Drugs 2003 8(1):9-25; M.P. Walker et al., Promising Candidates for the treatment of chronic hepatitis C, Exp. Opin. Investig. Drugs 2003 12(8); 1269-1280; S.-L Tan et al., Hepatitis С Therapeutics: Current Status and Emerging Strategies, Nature Rev. Drug Discov. 2002 1:867-881; R. De Francesco ef al. Approaching a new era for hepatitis С virus therapy: inhibitors of the NS3-4A serine protease and the NS5B RNA-dependent RNA polymerase, Antiviral Res. 2003 58:1-16; Q.M. Wang ef al. Hepatitis С virus encoded proteins: targets for antiviral therapy, Drugs of the Future 2000 25(9):933-8-944; J.A. Wu and Z. Hong, Targeting NS5B-Dependent RNA Polymerase forAnti-HCV Chemotherapy Cur. Drug Targ. - lnf. Dis.2003 3:207-219. В обзорах процитированы соединения, в настоящее время находящиеся на разных стадиях процесса разработки. Комбинированная терапия двумя или тремя агентами, направленными на одинаковые или разные мишени, стала стандартной терапией для предотвращения или замедления развития устойчивых штаммов вируса, и соединения, раскрытые в приведенных выше обзорах, могли бы использоваться в комбинированной терапии с соединениями по настоящему изобретению, и данные обзоры тем самым являются включенными посредством ссылки во всей их полноте.
Рибавирин (1а; амид 1-((2R,3R,4S,5R)-3,4-дигидрокси-5-гидроксиметил-тетрагидро-фуран-2-ил)-1 Н-[1,2,4]триазол-3-карбоновой кислоты; VIRAZOLE®) представляет собой синтетический, не индуцирующий интерферон, противовирусный нуклеозидный аналог широкого спектра. Рибавирин имеет активность in vitro против нескольких ДНК- и РНК-вирусов, включая Flaviviridae (Gary L. Davis, Gastroenterology 2000 118:S104-S114). В монотерапии рибавирин снижает уровни сывороточной аминотрансферазы до нормальных у 40% пациентов, но он не снижает сывороточные уровни РНК HCV. Рибавирин также демонстрирует значительную токсичность, и известно, что он индуцирует анемию. Рибавирин является ингибитором инозинмонофосфатдегидрогеназы. Рибовирин не одобрен в монотерапии против HCV, но данное соединение одобрено в комбинированной терапии с интерфероном α-2а и интерфероном α-2b. Вирамидин 1b представляет собой пролекарство, превращающееся в 1а в гепатоцитах.
Интерфероны (IFN) были доступны для лечения хронического гепатита в течение почти десятилетия. IFN представляют собой гликопротеины, продуцируемые иммунными клетками в ответ на вирусную инфекцию. Распознают два отличных типа интерферона: тип 1 включает несколько интерферонов альфа и один интерферон β, тип 2 включает интерферон γ. Интерферон типа 1 продуцируется, главным образом, инфицированными клетками и защищает соседние клетки от инфекции de novo. IFN ингибируют вирусную репликацию многих вирусов, включая HCV, и, при использовании в качестве единственного лечения инфекции гепатитом С, IFN подавляет сывороточную РНК HCV до недетектируемых уровней. Дополнительно IFN нормализует уровни сывороточной аминотрансферазы. К сожалению, эффекты IFN являются временными. Прекращение терапии приводит к 70%-ной частоте рецидивов, и только 10-15% демонстрируют стойкий вирусологический ответ с нормальными уровнями сывороточной аланинтрансферазы. (L.-B. Davis, выше).
Одним ограничением ранней терапии IFN был быстрый клиренс белка из крови. Химическая дериватизация IFN полиэтиленгликолем (ПЭГ) приводила к (получению) белков со значительно улучшенными фармакокинетическими свойствами. PEGASYS® представляет собой конъюгат интерферона α-2а и 40 кДа разветвленного монометокси ПЭГ, и PEG-INTRON® представляет собой конъюгат интерферона α-2b и 12 кДа монометокси ПЭГ. (В.A. Luxon et al., Clin. Therap.2002 24(9): 1363-1383; A. Kozlowski and J.M. Harris, J. Control. Release, 2001 72:217-224).
Интерферон α-2а и интерферон α-2b в настоящее время одобрены в качестве монотерапии для лечения HCV. ROFERON-A® (Roche) представляет собой рекомбинантную форму интерферона α-2а. PEGASYS® (Roche) представляет собой ПЭГилированную (т.е. модифицированную полиэтиленгликолем) форму интерферона α-2а. INTRON-A® (Schering Corporation) представляет собой рекомбинантную форму интерферона α-2b, и PEG-INTRON® (Schering Corporation) представляет собой ПЭГилированную форму интерферона α-2b.
Другие формы интерферона α, а также интерферона β, γ, τ и ω в настоящее время находятся в клинической разработке для лечения HCV. Например, в разработке находятся INFERGEN® (интерферон альфакон-1) от InterMune, OMNIFERON® (природный интерферон) от Viragen, ALBUFERON® от Human Genome Sciences, REBIF® (интерферон β-1а) от Ares-Serono, Omega Interferon от BioMedicine, Oral Interferon Alpha от Amarillo Biosciences, и интерферон γ, интерферон τ и интерферон γ-1b от InterMune.
Комбинированная терапия HCV рибавирином и интерфероном-α в настоящее время представляет собой оптимальную терапию. Объединение рибавирина и ПЭГ-IFN (ниже) приводит к стойкому вирусному ответу у 54-56% пациентов. SVR (стойкий вирусный ответ) достигает 80% для HCV типа 2 и 3 (Walker, выше). К сожалению, комбинация также продуцирует побочные эффекты, которые ставят клинические проблемы. Депрессия, гриппоподобные симптомы и кожные реакции ассоциированы с подкожным INF-α, и гемолитическая анемия ассоциирована с длительным лечением рибавирином.
Другие макромолекулярные соединения для лечения инфекции вирусом гепатита С, в настоящее время находящиеся в доклинической или клинической разработке, включают: lnterleukin-10 от Schering-Plough, 1P-S01 от Intemeuron, Merimebodib (VX-497) от Vertex, HEPTAZYME® от RPI, IDN-6556 от Idun Pharma, XTL-002 от XTL, HCV/MFS9 от Chiron, CIVACIR® (иммуноглобулин против гепатита С) от NABI, ZADAXIN® (тимозин α-1) от SciClone, тимозин плюс ПЭГилированный интерферон от SciClone, CEPLENE®; терапевтическую вакцину, направленную на Е2 от Innogenetics, терапевтическую вакцину от Intercell, терапевтическую вакцину от Epimmune/Genencor, терапевтическую вакцину от Merix, терапевтическую вакцину Chron-VacC от Tripep.
Другие макромолекулярные подходы включают рибозимы, направленные на РНК HCV. Рибозимы представляют собой короткие встречающиеся в природе молекулы с эндонуклеазной активностью, которые катализируют специфичное в отношении последовательности расщепление РНК. Альтернативным подходом является применение антисмысловых олигонуклеотидов, которые связываются с РНК и стимулируют расщепление, опосредованное РНКазойН.
Теперь был идентифицирован целый ряд потенциальных молекулярных мишеней для разработки лекарственных средств - терапевтических агентов против HCV, включающий, но не ограничивающийся автопротеазой NS2-NS3, протеазой N3, хеликазой N3 и полимеразой NS5B. РНК-зависимая РНК-полимераза абсолютно необходима для репликации одноцепочечного, смыслового РНК-генома, и данный фермент вызывал значительный интерес среди медицинских химиков.
Нуклеозидные ингибиторы могут действовать либо в качестве терминатора цепи, либо в качестве конкурентного ингибитора, который препятствует связыванию нуклеотида с полимеразой. Для функционирования в качестве терминатора цепи, нуклеозидный аналог должен поглощаться клеткой и превращаться in vivo в его трифосфатную форму для конкуренции в качестве субстрата в сайте связывания нуклеотида полимеразы. Это превращение до трифосфата обычно опосредуется клеточными киназами, которые накладывают дополнительные структурные ограничения на любой нуклеозид. Нуклеозидполимеразы также являются существенным компонентом при нормальном делении клетки и для ограничения потенциальных токсичных побочных эффектов, нуклеозидные ингибиторы должны селективно ингибировать вирусные полимеразы без нарушения существенного клеточного роста и репарации посредством ингибирования полимераз хозяина. Таким образом, требование фосфорилирования эндогенными киназами и селективности по отношению к эндогенным полимеразам накладывает строгие требования на структуру потенциальных нуклеозидных терапевтических средств.
НУКЛЕОЗИДНЫЕ ПРОЛЕКАРСТВА
В то время как нуклеозиды часто являются мощными противовирусными и химиотерапевтическими агентами, их практическая польза часто ограничивается двумя факторами. Во-первых, плохие фармакокинетические свойства часто ограничивают поглощение нуклеозида из кишечника; и, во-вторых, субоптимальные физические свойства ограничивают возможности приготовления в виде препарата, которые могли бы применяться для улучшения доставки активного ингредиента.
Альберт (Albert) ввел термин «пролекарство» для описания соединения, которое не имеет подлинной биологической активности, но которое способно к метаболическому превращению до активного лекарственного вещества (A. Albert, Selective Toxicity, Chapman and Hall, London, 1951). Недавно были сделаны обзоры пролекарств (Р.Ettmayer etal., J. Med Chem. 2004 47(10):2393-2404; К. Beaumont et al., Curr. Drug Metab. 2003 4:461-485; H. Bundgaard, Design of Prodrugs: Bioreversible derivatives for various functional groups and chemical entities in Design of Prodrugs, H. Bundgaard (ed) Elsevier Science Publishers, Amersterdam 1985; G. M. Pauletti et al. Adv. Drug Deliv. Rev.1997 27:235-256; R.J. Jones and N. Bischofberger, Antiviral Res. 1995 27; 1-15 and С.R. Wagner et al., Med. Res. Rev. 2000 20:417-45). В то время как метаболическое превращение может катализироваться специфичными ферментами, часто гидролазами, активное соединение также может регенерировать посредством неспецифичных химических процессов.
Термин «фармацевтически приемлемые пролекарства» относится к соединению, которое метаболизируется, например гидролизуется или окисляется, у хозяина с образованием соединения по настоящему изобретению. При биопревращении должно предотвращаться образование фрагментов с токсикологическими склонностями. Типичные примеры пролекарств включают соединения, которые имеют биологически лабильные защитные группы, связанные с функциональной группировкой активного соединения. При конструировании пронуклеотидов использовали алкилирование, ацилирование или другие липофильные модификации гидроксильной группы(групп) на группировке сахара. Данные пронуклеотиды могут гидролизоваться или деалкилироваться in vivo с генерацией активного соединения.
Факторами, ограничивающими пероральную биодоступность, часто являются поглощение из желудочно-кишечного тракта и экскреция первого прохода стенки кишки и печени. Оптимизация трансклеточного поглощения через ЖК тракт требует D(7,4) большего, чем ноль. Оптимизация коэффициента распределения, однако, не гарантирует успех. Пролекарство возможно должно избегать активных выводящих транспортеров в энтероците. Внутриклеточный метаболизм в энтероците может приводить к пассивному транспорту или активному транспорту метаболита выводящими насосами обратно в просвет кишки. Пролекарство также должно сопротивляться нежелательным биопревращениям в крови до достижения клеток-мишеней или рецепторов.
Часто требуются высокие уровни противовирусных лекарственных средств в системе кровообращения для поддержания достаточно высоких уровней API (активный фармацевтический ингредиент) в крови для того, чтобы минимизировать риск генерации устойчивых популяций. Например, в недавних испытаниях использовали дозы сложного (2R,3R,4R,5R)-5-(4-амино-2-оксо-2Н-пиримидин-1-ил)-4-фтор-2-изобутирилоксиметил-4-метил-тетрагидро-фуран-3-илового эфира изомасляной кислоты (II: R7128) вплоть до 1500 мг BID (два раза в сутки) и QID (четыре раза в сутки). (S. Le Pogam ef al., "No Evidence of R7128 Drug Resistance After Up To 4 Weeks Treatment of GT1,2 and 3 Hepatitis С Virus Infected Individuals", 44th Annual Meeting of the European Association for the Study of the Liver (EASL), Copenhagen, Denmark, Apr 22-Apr 26, 2009). Это часто приводит к высоким суточным дозам, для которых требуется большой размер пилюли или капсулы, или более частое введение лекарственной формы. Когда требуются высокие дозы активного фармацевтического ингредиента, возможность добавления разбавителей или эксципиентов для улучшения биодоступности часто ограничивается. Таким образом, разработка новых ингибиторов полимеразы HCV требует идентификации соединений, которые являются биодоступными, превращаются в соответствующий трифосфат и являются мощными ингибиторами полимеразы HCV.
Обязательное требование для фосфорилирования in vivo недавно привело к интересу к нуклеозидмонофосфатным пролекарствам, содержащим маскированную фосфатную группировку, которая является чувствительной к внутриклеточной ферментативной активации, приводящей к (образованию) нуклеозидмонофосфата. Поскольку при образовании нуклеозидтрифосфатов стадией, лимитирующей скорость, является первая стадия, приводящая к монофосфату, последующее добавление второго и третьего фосфатов легко идет на основе монофосфата (смотрите, например, Р. Perrone et al., J. Med. Chem., 2007, 50(8):1840; S.J. Heckerand M.D. Erion, J. Med Chem. 2008 51(8):2328).
Химическая модификация активного соединения с образованием потенциального пролекарства дает совершенно новую молекулярную субстанцию, которая может демонстрировать нежелательные физические, химические и биологические свойства, отсутствующие у родительского соединения. Нормативные требования для идентификации метаболитов могут создавать проблемы, если многочисленные пути приводят к множеству метаболитов. Таким образом, идентификация пролекарств остается неопределенной и бросающей вызов задачей. Кроме того, оценка фармакокинетических свойств потенциальных пролекарств является бросающим вызов и затратным предприятием. Фармакокинетические результаты от животных моделей может быть сложно экстраполировать на людей.
Целью настоящего изобретения является предложение новых соединений, способов и композиций для лечения хозяина, инфицированного вирусом гепатита С.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В настоящее время отсутствует предупредительное лечение или обычно эффективная терапия для лечения инфекций вирусом гепатита С (HCV). Одобренные в настоящее время терапии, которые только существуют против HCV, имеют ограниченную эффективность и связаны с серьезными побочными эффектами. Следовательно, важной является разработка и развитие новых более эффективных терапий с меньшей токсичностью.
Настоящее изобретение относится к соединениям формулы I, где:
R1 и R2 (1) в каждом случае независимо выбраны из группы, состоящей из водорода, C1-6алкилкарбонила, С1-6алкоксикарбонила и С1-6аминоалкилкарбонила или
(2) взятые в совокупности и R1, и R2 группировки вместе представляют собой С(=O);
R3 представляет собой водород, С1-6алкилкарбонил, С1-6алкоксикарбонил или C1-6аминоалкилкарбонил;
и их фармацевтически приемлемой соли при условии, что по меньшей мере один из R1, R2 и R3 отличается от водорода.
Согласно настоящему изобретению также предложен способ лечения заболевания - вирусной инфекции вирусом гепатита С (HCV) путем введения терапевтически эффективного количества соединения согласно формуле I пациенту, нуждающемуся в этом. Соединение можно вводить одно или вводить совместно с другими противовирусными соединениями или иммуномодуляторами.
Согласно настоящему изобретению также предложен способ ингибирования репликации HCV в клетке путем введения соединения согласно формуле I в эффективном количестве для ингибирования HCV.
Согласно настоящему изобретению также предложена фармацевтическая композиция, содержащая соединение согласно формуле I и по меньшей мере один фармацевтически приемлемый носитель, разбавитель или эксципиент.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
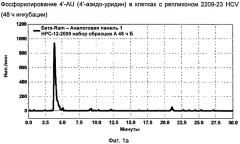
Фиг.1а иллюстрирует профиль фосфорилирования 4'-AU (4'-азидо-урацил) в клетках с репликоном HCV.
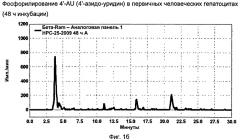
Фиг.16 иллюстрирует профиль фосфорилирования 4'-AU в человеческих гепатоцитах.
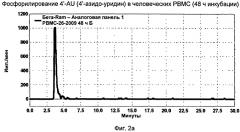
Фиг.2а иллюстрирует профиль фосфорилирования 4'-AU в РВМС (одноядерные клетки периферической крови). Фиг.26 и Фиг.2в иллюстрируют профиль фосфорилирования 4'-азидо-цитидина (4'-АС) в РВМС после 1 ч инкубации и 120 ч инкубации соответственно.
Фиг.3а и 3б обеспечивают сравнение профиля фосфорилирования 4'-AU в первичных человеческих гепатоцитах, клетках костного мозга и РВМС. Сходные профили были получены у 3 доноров.
Фиг.4 иллюстрирует эффективность 4'-AU по сравнению с 4'-АС в человеческих гепатоцитах.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Триацильные производные 4'-азидо-цитидина (4'-АС) исследовали в качестве ингибиторов полимеразы NS5B HCV (К. Klumpp et al; J. б/о. Chem., 2008 283(4):2167-2176). К сожалению, несмотря на то, что 4'-АС представляет собой мощный ингибитор вирусной репликации, клинические исследования были остановлены развитием неприемлемых побочных эффектов. Родственный пиримидиновый нуклеозид, 4'-азидо-уридин (4'-AU) не был активным в анализе репликона, который широко используется для оценки потенциальных ингибиторов полимеразы (V. Lohmann et al., J. Virol. 2003 77:3007-3019, K.J. Blight et al., Science 2000 290(5498): 1870-1871). При химическом получении трифосфата и оценке в анализе полимеразы HCV он ингибировал фермент с Ki 0,038±8 мкМ по сравнению с Ki 0,040±25 мкМ для 4'-азидо-цитидинтрифосфата (D. Smith et al., Bioorg. Med. Chem. Lett. 2007 17:2570). Следовательно, предполагалось, что отсутствие активности в анализе репликона указывает на то, что 4'-AU не фосфорилировался in vivo. Это объяснение было поддержано демонстрацией того, что, в то время как 4'-АС фосфорилировался РВМС (одноядерные клетки периферической крови), 4'-AU не превращался в соответствующий фосфорилированный нуклеозид (ФИГ.1).
Теперь неожиданно обнаружили, что фосфорилирование 4'-AU действительно эффективно осуществляется в первичных человеческих гепатоцитах (ФИГ.2). Поскольку специфичное в отношении клетки фосфорилирование происходит в ткани-мишени для репликации HCV, имеется потенциал для терапии селективно фосфорилированным нуклеозидом, который дополнительно свидетельствует о том, что ограниченное фосфорилирование в других клетках возможно будет приводить к меньшим возможностям для неблагоприятной токсичности.
Элемент в единственном числе здесь используется в отношении одного или более чем одного такого элемента, например «соединение» относится к одному или более чем одному соединению или по меньшей мере к одному соединению. Термины в единственном числе или предваряемые фразами «один или более чем один» и «по меньшей мере один», как таковые, могут здесь использоваться взаимозаменяемо.
Фраза «как определено здесь выше» относится к самому широкому определению для каждой группы, как приведено в кратком изложении сущности изобретения или в самом широком пункте формулы изобретения. Во всех других воплощениях, приведенных ниже, заместители, которые могут присутствовать в каждом воплощении и которые прямо не определены, сохраняют самое широкое определение, приведенное в кратком изложении сущности изобретения.
Термины «включают(ет)» и «включающий» в том виде, как они используются в данном описании изобретения, либо в переходной фразе, либо в основной части пункта формулы изобретения, следует интерпретировать как имеющие значение, допускающее поправки. То есть, данные термины следует интерпретировать синонимично фразам "имеющий по меньшей мере" или "включающий по меньшей мере". При использовании в контексте способа термин «включающий» означает то, что способ включает по меньшей мере перечисленные стадии, но может включать дополнительные стадии. При использовании в контексте соединения или композиции термин «включающий» означает то, что соединение или композиция включает по меньшей мере перечисленные характеристики или компоненты, но также может включать дополнительные характеристики или компоненты.
Термин «независимо» используется здесь для указания того, что переменная применяется в любом случае безотносительно к присутствию или отсутствию переменной, имеющей такое же или другое определение, в пределах того же самого соединения. Таким образом, в соединении, в котором R" появляется дважды и определяется как «независимо углерод или азот», оба R" могут представлять собой углерод, оба R" могут представлять собой азот, или один R" может представлять собой углерод, а другой - азот.
Когда любая переменная (например, R1, R4a, Аr, X1 или Het) встречается больше, чем один раз в любой группировке или формуле, отображающей и описывающей соединения, применяемые или заявленные в настоящем изобретении, ее определение при каждом появлении является независимым от ее определения при каждом другом появлении. Также комбинации заместителей и/или переменных являются разрешенными, только если такие соединения приводят к стабильным соединениям.
Каждый из символов «*» в конце связи или «----», нарисованный через связь, относится к точке присоединения функциональной группы или другой химической группировки к остальной молекуле, частью которой она является. Таким образом, например:
MeC(=O)OR4 где или .
Связь, нарисованная в системе кольца (в отличие от связи, соединенной с определенной вершиной), указывает на то, что связь может быть присоединена к любому подходящему атому кольца.
Термин «возможный» или «возможно» в том виде, как он здесь используется, означает то, что событие или обстоятельство, описанное далее, может, но не обязательно происходит, и что описание включает случаи, когда событие или обстоятельство происходит, и случаи, в которых оно не происходит. Например, «возможно замещенный» означает то, что возможно замещенная группировка может включать водород или заместитель.
Термин «примерно» используется здесь для обозначения приблизительно, в районе, грубо или около. При использовании термина «примерно» в сочетании с числовым интервалом он модифицирует данный интервал, расширяя границы выше и ниже изложенных числовых значений. В общем, термин «примерно» используется здесь для модификации числового значения выше и ниже заявленного значения на отклонение 20%.
Перечисление числового интервала для переменной в том виде, как оно здесь используется, предназначено для выражения того, что изобретение можно воплощать на практике с переменной, равной любому из значений в пределах данного интервала. Таким образом, для переменной, которая является дискретной по своей природе, переменная может быть равной любому целочисленному значению из числового интервала, включая конечные точки интервала. Аналогично, для переменной, которая является непрерывной по своей природе, переменная может быть равна любому реальному значению из числового интервала, включая конечные точки интервала. В качестве примера, переменная, которая описана, как имеющая значения от 0 и 2, может составлять 0, 1 или 2 для переменных, которые являются дискретными по своей природе, и может составлять 0,0; 0,1; 0,01; 0,001 или любое другое реальное значение для переменных, которые являются непрерывными по своей природе.
Соединения формулы I демонстрируют таутомерию. Таутомерные соединения могут существовать в виде двух или более чем двух соединений, способных к взаимному превращению. Прототропные таутомеры образуются в результате миграции ковалентно связанного атома водорода между двумя атомами. Таутомеры обычно существуют в равновесии, и попытки выделить индивидуальные таутомеры обычно дают смесь, химические и физические свойства которой согласуются со смесью соединений. Положение равновесия зависит от химических свойств в пределах молекулы. Например, у многих алифатических альдегидов и кетонов, таких как ацетальдегид, преобладает кето форма, тогда как у фенолов преобладает енольная форма. Обычные прототропные таутомеры включают кето/енольные , амид/имидная кислота и амидиновые таутомеры. Последние два являются особенно обычными в гетероарильных и гетероциклических кольцах, и настоящее изобретение охватывает все таутомерные формы соединений.
В первом воплощении настоящего изобретения предложено соединение согласно формуле I, где R1, R2 и R3 являются такими, как описано здесь выше.
Во втором воплощении настоящего изобретения предложено соединение согласно формуле I, где R1, R2 и R3 представляют собой С1-6алкилкарбонил.
В третьем воплощении настоящего изобретения предложено соединение согласно формуле I, где R1 и R2 представляют собой С1-6алкилкарбонил, и R3 представляет собой водород.
В четвертом воплощении настоящего изобретения предложено соединение согласно формуле I, где R1 и R2 представляют собой водород, и R3 представляет собой C1-6алкилкарбонил или С1-6аминоалкилкарбонил.
В пятом воплощении настоящего изобретения предложено соединение, выбранное из соединений 1-1 -1-6 ТАБЛИЦЫ I.
В шестом воплощении настоящего изобретения предложен способ лечения инфекции HCV, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения согласно формуле I, где R1, R2 и R3 являются такими, как определено здесь выше. Во всех других воплощениях, приведенных ниже, заместители, которые могут присутствовать в каждом воплощении, и которые явно не определены, сохраняют самое широкое определение, приведенное в кратком изложении сущности изобретения.
В седьмом воплощении настоящего изобретения предложен способ лечения инфекции HCV, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения согласно формуле I, где R1, R2 и R3 представляют собой С1-6алкилкарбонил.
В восьмом воплощении настоящего изобретения предложен способ лечения инфекции HCV, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения согласно формуле I, где R1 и R2 представляют собой С1-6алкилкарбонил, и R3 представляет собой водород.
В девятом воплощении настоящего изобретения предложен способ лечения инфекции HCV, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения согласно формуле I, где R1 и R2 представляют собой водород, и R3 представляет собой C1-6алкилкарбонил или C1-6аминоалкилкарбонил.
В десятом воплощении настоящего изобретения предложен способ лечения инфекции HCV, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения согласно формуле I, где R1, R2 и R3 являются такими, как описано здесь выше, и совместное введение по меньшей мере одного модулятора иммунной системы и/или по меньшей мере одного противовирусного агента, который ингибирует репликацию HCV.
В одиннадцатом воплощении настоящего изобретения предложен способ лечения инфекции HCV, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения согласно формуле I, где R1, R2 и R3 являются такими, как описано здесь выше, и совместное введение по меньшей мере одного модулятора иммунной системы, выбранного из группы, состоящей из интерферона, интерлейкина, фактора некроза опухолей и колониестимулирующего фактора.
В двенадцатом воплощении настоящего изобретения предложен способ лечения инфекции HCV, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения согласно формуле I, где R1, R2 и R3 являются такими, как описано здесь выше, и совместное введение по меньшей мере одного модулятора иммунной системы, где модулятор иммунной системы представляет собой интерферон или химически дериватизированный интерферон.
В тринадцатом воплощении настоящего изобретения предложен способ лечения инфекции HCV, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения согласно формуле I, где R1, R2 и R3 являются такими, как описано здесь выше, и совместное введение по меньшей мере одного противовирусного агента, который ингибирует репликацию HCV.
В четырнадцатом воплощении настоящего изобретения предложен способ лечения инфекции HCV, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения согласно формуле I, где R1, R2 и R3 являются такими, как описано здесь выше, и совместное введение по меньшей мере одного противовирусного агента, выбранного из группы, состоящей из ингибитора протеазы HCV, другого нуклеозидного ингибитора полимеразы HCV, ненуклеозидного ингибитора полимеразы HCV, ингибитора хеликазы HCV, ингибитора праймазы HCV и ингибитора слияния HCV.
В другом воплощении настоящего изобретения предложено применение соединения согласно формуле I, где R1, R2 и R3 являются такими, как определено здесь выше, для лечения инфекции HCV.
В другом воплощении настоящего изобретения предложено применение соединения формулы I, где R1, R2 и R3 являются такими, как определено здесь выше, для изготовления лекарственного средства для лечения инфекции HCV.
В другом воплощении настоящего изобретения предложено применение соединения согласно формуле I, где R1, R2 и R3 представляют собой C1-6алкилкарбонил, для лечения инфекции HCV.
В другом воплощении настоящего изобретения предложено применение соединения формулы I, где R1, R2 и R3 представляют собой C1-6алкилкарбонил, для изготовления лекарственного средства для лечения инфекции HCV.
В другом воплощении настоящего изобретения предложено применение соединения согласно формуле I, где R1 и R2 представляют собой C1-6алкилкарбонил, и R3 представляет собой водород, для лечения инфекции HCV.
В другом воплощении настоящего изобретения предложено применение соединения формулы I, где R1 и R2 представляют собой С1-6алкилкарбонил, и R3 представляет собой водород, для изготовления лекарственного средства для лечения инфекции HCV.
В другом воплощении настоящего изобретения предложено применение соединения согласно формуле I, где R1 и R2 представляют собой водород, и R3 представляет собой C1-6алкилкарбонил или С1-6аминоалкилкарбонил, для лечения инфекции HCV.
В другом воплощении настоящего изобретения предложено применение соединения формулы I, где R1 и R2 представляют собой водород, и R3 представляет собой С1-6алкилкарбонил или С1-6аминоалкилкарбонил, для изготовления лекарственного средства для лечения инфекции HCV.
В другом воплощении настоящего изобретения предложено применение соединения согласно формуле I, где R1, R2 и R3 являются такими, как описано здесь выше, в комбинации с по меньшем мере одним модулятором иммунной системы и/или по меньшей мере одним противовирусным агентом, который ингибирует репликацию HCV, для лечения инфекции HCV.
В другом воплощении настоящего изобретения предложено применение соединения согласно формуле I, где R1, R2 и R3 являются такими, как описано здесь выше, для лечения инфекции HCV в комбинации с по меньшем мере одним модулятором иммунной системы, выбранным из группы, состоящей из интерферона, интерлейкина, фактора некроза опухоли и колониестимулирующего фактора.
В другом воплощении настоящего изобретения предложено применение соединения согласно формуле I, где R1, R2 и R3 являются такими, как описано здесь выше, для лечения инфекции HCV в комбинации с по меньшем мере одним модулятором иммунной системы, где модулятор иммунной системы представляет собой интерферон или химически дериватизированный интерферон.
В другом воплощении настоящего изобретения предложено применение соединения согласно формуле I, где R1, R2 и R3 являются такими, как описано здесь выше, для лечения инфекции HCV в комбинации с по меньшем мере одним антивирусным агентом, который ингибирует репликацию HCV.
В другом воплощении настоящего изобретения предложено применение соединения согласно формуле I, где R1, R2 и R3 являются такими, как описано здесь выше, для лечения инфекции HCV в комбинации с по меньшем мере одним антивирусным агентом, выбранным из группы, состоящей из ингибитора протеазы HCV, другого нуклеозидного ингибитора полимеразы HCV, ненуклеозидного ингибитора полимеразы HCV, ингибитора хеликазы HCV, ингибитора праймазы HCV и ингибитора слияния HCV.
В другом воплощении настоящего изобретения предложена фармацевтическая композиция, содержащая терапевтически эффективное количество соединения согласно формуле I, где R1, R2 и R3 являются такими, как описано здесь выше, смешанног