Производные (тио)морфолина в качестве модуляторов sip
Иллюстрации
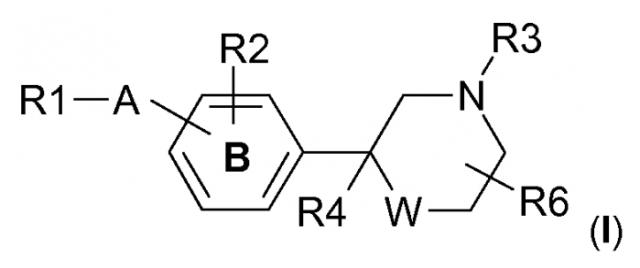
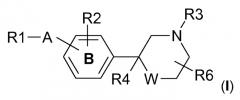
Показать всеИзобретение относится к производным (тио)морфолина формулы (I), обладающим свойством модулятора сфингозин-1-фосфата (S1P), фармацевтической композиции на их основе и их применению. В общей формуле (I) R1 выбран из циано, (2-4С)алкинила, (1-4С)алкила, (3-6С)циклоалкила, (4-6С)циклоалкенила, (6-8С)бициклоалкила, (8-10С)бициклической группы, каждый из которых может быть замещен (1-4С)алкилом, фенила, бифенила, нафтила, каждый из которых может быть замещен одним-тремя заместителями, независимо выбранными из галогена, (1-4С)алкила, в случае необходимости замещенного одним или более атомами фтора, (2-4С)алкинила, (1-4С)алкокси, в случае необходимости замещенного одним или более атомами фтора, амино, ди(1-4С)алкиламино и (3-6С)циклоалкила, фенила, замещенного фенокси, бензилом, бензилокси, фенилэтилом или моноциклическим гетероциклом, каждый из которых может быть замещен (1-4С)алкилом, 5-6-членного моноциклического гетероцикла, содержащего 1-3 гетероатома, выбранных из N, О и S, в случае необходимости замещенного галогеном, (1-4С)алкилом или фенилом, в случае необходимости замещенным (1-4С)алкилом, и 9-10-членного бициклического гетероцикла, содержащего 1-2 гетероатома, выбранных из N и О, в случае необходимости замещенного (1-4С)алкилом; А выбран из -СО-O-, -NH-CO-, -CO-NH, -С=С-, -ССН3-O- и связующей группы -Y-(СН2)n-Х-, в которой Y присоединен к R1 и выбран из связи, -О-, -SO2-, -СН2-O-, -СО-, -СО-O-, -CO-NH-, -NH-CO-, -С=С- и -С≡С-; n означает целое число от 1 до 7; и X присоединен к фениленовой группе и выбран из связи, -О-, -S-, и -NH; кольцевая структура В представляет собой фенилен; R2 обозначает Н, (1-4С)алкил, в случае необходимости замещенный одним или более атомами фтора, (1-4С)алкокси или галоген; и R3 обозначает (1-4С)алкилен-R5, в котором алкиленовая группа может быть замещена одним или двумя атомами галогена, или R3 обозначает (3-6С)циклоалкилен-R5 или -CO-CH2-R5, в которой R5 обозначает -ОН, -PO3H2, -OPO3H2, -СООН или тетразол-5-ил; R4 обозначает Н или (1-4С)алкил; R6 обозначает один или более заместителей, независимо выбранных из Н, (1-4С)алкила или оксо; W обозначает -О- или -S-. 4 н. и 14 з.п. ф-лы, 1 ил., 237 пр.
Реферат
Область изобретения
Это изобретение относится к новым производным (тио)морфолина, имеющими сродство с рецепторами S1P, к фармацевтической композиции, содержащей указанные соединения, а также к применению указанных соединений для получения лекарственного средства для лечения, облегчения или профилактики заболеваний и состояний, в которых участвует любой рецептор S1P или в котором участвует модуляция эндогенной системы трансдукции сигналов S1P через любой рецептор S1P.
Уровень техники
Сфингозин-1-фосфат (S1P) представляет собой биоактивный сфинголипид, который опосредует широкий спектр клеточных ответов, таких как пролиферация, организация цитоскелета и миграция, адгезивная и жесткая сборка и морфогенез. S1P может связываться членами семейства генов дифференцировки эндотелиальных клеток (рецепторы ED Г) локализованных в плазматической мембране, связанных с G-белком рецепторов. До настоящего времени пять членов этого семейства были идентифицированы как рецепторы S1P в различных типах клеток, S1P1 (EDG-1), S1P2 (EDG-5), S1P3 (EDG-3), S1P4 (EDG-6) и S1P5 (EDG-8). S1P может приводить к перегруппировкам цитоскелета во многих типах клеток, регулируя трафик иммунных клеток, сосудистый гомеостаз и коммуникацию клеток в центральной нервной системе (ЦНС) и в периферических органных системах.
Известно, что S1P секретируется сосудистым эндотелием, и присутствует в крови в концентрациях 200-900 наномоль, и связывается альбумином и другими белками плазмы. Это обеспечивает как стабильный резервуар во внеклеточных жидкостях, так и эффективную доставку на рецепторы поверхности клеток с высоким сродством. S1P связывается с низким наномолярным сродством с этими пятью рецепторами S1P1-5. Кроме того, тромбоциты также содержат S1P и могут быть локально высвобождены, вызывая, например, вазоконстрикцию. Подтипы рецепторов S1P1, S1P2 и S1P3 широко экспрессируются и представляют собой доминирующие рецепторы в сердечно-сосудистой системе. Далее, S1P1 также является рецептором на лимфоцитах. Рецепторы S1P4 почти исключительно встречаются в гематопоэтической и лимфоидной системах. S1P5 прежде всего (хотя не исключительно) экспрессируется в центральной нервной системе. Экспрессия S1P5 у мышей, по-видимому, ограничена олигодендроцитами, миелинизирующими клетками мозга, в то время как у крыс и людей была обнаружена экспрессия на уровне астроцитов и эндотелиальных клеток, но не олигодендроцитов.
Модуляторы рецептора S1P представляют собой соединения, которые сигнализируют как (ант)агонисты на одном или более рецепторов S1P. Настоящее изобретение относится к модуляторам рецептора S1P5, в частности агонистам, и предпочтительно к агонистам с селективностью по рецепторам S1P1 и/или S1P3 ввиду нежелательных сердечно-сосудистых и/или иммуномодулирующих эффектов. В настоящее время обнаружено, что агонисты S1P5 могут использоваться в лечении когнитивных нарушений, в частности возрастного снижения когнитивной функции.
Хотя продолжаются исследования с целью разработки терапии, которая может использоваться для лечения возрастного снижения когнитивной функции и деменции, они еще не привели к многим успешным результатам. Поэтому существует потребность в новой терапии с желательными свойствами.
Описание изобретения
В настоящее время обнаружено, что производные (тио)морфолина формулы (I)
в которой
R1 выбран из
циано,
(2-4C)алкинила,
(1-4C)алкила,
(3-6C)циклоалкила,
(4-6C)циклоалкенила,
(6-8C)бициклоалкила, (8-10C)бициклической группы, каждый из которых может быть замещен (1-4C)алкилом,
фенила, бифенила, нафтила, каждый из которых может быть замещен одним или более заместителями, независимо выбранными из галогена, (1-4C)алкила, в случае необходимости замещенного одним или более атомами фтора, (2-4C)алкинила, (1-4C)алкокси, в случае необходимости замещенного одним или более атомами фтора, амино, ди(1-4C)алкиламино, -SO2-(1-4C)алкила, -CO-(1-4C)алкила, -CO-O-(1-4C)алкила, -NH-CO-(1-4C)алкила и (3-6C)циклоалкила,
фенила, замещенного фенокси, бензилом, бензилокси, фенилэтилом или моноциклическим гетероциклом, каждый из которых может быть замещен (1-4C)алкилом,
моноциклического гетероцикла, в случае необходимости замещенного галогеном, (1-4C)алкилом или фенилом, в случае необходимости замещенным (1-4C)алкилом,
и
бициклического гетероцикла, в случае необходимости замещенного (1-4C)алкилом;
A выбран из -CO-O-, -O-CO-, -NH-CO-, -CO-NH, -C=C-, -CCH3-O- и связующей группы -Y-(CH2)n-X-, в которой
Y присоединен к R1 и выбран из связи, -O-, -S-, -SO-, -SO2-, -CH2-O-, -CO-, -O-CO-, -CO-O-, -CO-NH-, -NH-CO-, -C=C- и -C≡C-;
n означает целое число от 1 до 10; и
X присоединен к фениленовой/пиридильной группе и выбран из связи, -O-, -S-, -SO-, -SO2-, -NH, -CO-, -C=C- и -C≡C-;
кольцевая структура B может содержать один атом азота;
R2 обозначает Н, (1-4C)алкил, в случае необходимости замещенный одним или более атомами фтора, (1-4C)алкокси, в случае необходимости замещенный одним или более атомами фтора, или галоген; и
R3 обозначает (1-4C)алкилен-R5, в котором алкиленовая группа может быть замещена (CH2)2, образуя циклопропильную группу, или одним или двумя атомами галогена, или R3 обозначает (3-6C)циклоалкилен-R5 или -CO-CH2-R5, в которой R5 обозначает -OH, -PO3H2, -OPO3H2, -COOH, -COO(1-4C)алкил или тетразол-5-ил;
R4 обозначает Н или (1-4C)алкил;
R6 обозначает один или более заместителей, независимо выбранных из Н, (1-4C)алкила или оксо;
W обозначает -O-, -S-, -SO- или -SO2-;
или их фармацевтически приемлемая соль, сольват или гидрат; при условии, что производное формулы (I) не является 2-(4-этилфенил)-4-морфолиноэтанолом или 4-[4-(2-гидроксиэтил)-2-морфолинил]бензолацетонитрилом,
демонстрируют сродство к рецепторам S1P.
В частности, соединения по изобретению демонстрируют селективное сродство к рецептору S1P5 по сравнению с рецептором(ами) S1P1 и/или S1P3.
Применение соединения 2-(4-этилфенил)-4-морфолиноэтанол как реагента в получении 2-(2-арилморфолино)этиловых эфиров напроксена описано в Database CA [Online] Chemical Abstracts Service, Columbus, OHIO, US; 2008, Hu, Ai-Xi et al., XP002558960, восстановленном из базы данных STN Номер доступа 2008:1527686; и Huaxue Xuebao, 66 (22), 2553-2557 Coden: HHHPA4; ISSN: 0567-7351, 2008. Не сообщалось о какой бы то ни было фармакологической активности этого соединения.
Точно так же в Farmatsiya (Sofia), Vol.45, no.1, 1998, стр. 3-11, XP009126794 Yordanova, K. et al. описывают применение 4-[4-(2-гидроксиэтил)-2-морфолинил]-бензолацетонитрила как реагента в получении антидепрессантных производных фенилморфолина. Не сообщалось о какой бы то ни было фармакологической активности этого соединения.
Кроме того, только синтез и охарактеризовывание 3-метил-2-[4-(фенилметокси)фенил]-4-морфолиноэтанол гидрохлорида указаны в Database CA [Online] Chemical Abstracts Service, Columbus, OHIO, US; 2005, Hu, Ai-Xi et al.: “Synthesis and characterization of 2-arylmorpholine hydrochloride” Hunan Daxue Xuebao, Ziran Kexueban, vol.32, no. 4, 2005, стр. 72-76. Не сообщалось о какой бы то ни было фармакологической активности этого соединения.
Соединения по изобретению являются модуляторами рецептора S1P, в частности рецептора S1P5. Более конкретно, соединения по изобретению являются агонистами рецептора S1P5. Соединения по изобретению могут быть использованы для лечения, облегчения и профилактики заболеваний и состояний, в которых участвуют (любые) рецептор(ы) S1P - в особенности S1P5 - или в котором участвует модуляция эндогенной системы передачи сигналов S1P через любой рецептор S1P. В частности, соединения согласно настоящему изобретению могут использоваться для лечения, облегчения или профилактики нарушений ЦНС (центральная нервная система), таких как нейродегенеративные нарушения, в особенности - но не ограничиваясь ими - когнитивные расстройства (в частности, возрастное снижение когнитивной функции) и родственные состояния, болезнь Альцгеймера, (сосудистая) деменция, болезнь Нимана-Пика и когнитивные дефициты при шизофрении, обсессивно-компульсивном поведении, большой депрессии, аутизме, рассеянном склерозе, боли и т.д. Предпочтительно, соединения согласно настоящему изобретению могут использоваться для лечения, облегчения или профилактики когнитивного расстройства (в частности, возрастного снижения когнитивной функции) и родственных состояний.
В вариантах осуществления изобретения кольцевая структура B представляет собой фенилен.
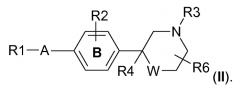
В варианте осуществления изобретения соединения имеют структуру (II)
В другом варианте осуществления изобретения соединения имеют формулу (I), в которой, R3 выбран из -(CH2)2-OH, -CH2-COOH, -(CH2)2-COOH, -(CH2)3-COOH, -CH2-CHCH3-COOH, -CH2-C(CH3)2-COOH, -CHCH3-CH2-COOH, -CH2-CF2-COOH, -CO-CH2-COOH, 1,3-циклобутилен-COOH, -(CH2)2-PO3H2, -(CH2)3-PO3H2, -(CH2)2-OPO3H2, -(CH2)3-OPO3H2, -CH2-тетразол-5-ила, -(CH2)2-тетразол-5-ила и -(CH2)3-тетразол-5-ила. Предпочтенные группы R3 выбраны из -CH2-COOH, -(CH2)2-COOH, -(CH2)3-COOH, -CH2-CHCH3-COOH, -CH2-C(CH3)2-COOH, -CHCH3-CH2-COOH, -(CH2)2-PO3H2, -(CH2)3-PO3H2 и -(CH2)2-OPO3H2 и, в частности, -(CH2)2-COOH и -(CH2)2-PO3H2. Наиболее предпочтительной является -(CH2)2-COOH.
В другом варианте осуществления W обозначает -O- или -S-. В предпочтительных вариантах осуществления W обозначает -O-.
В другом варианте осуществления изобретения R4 обозначает Н или метил и, в частности, R4 обозначает Н.
В другом варианте осуществления соединения имеют формулу (I), в которой R2 обозначает Н, метил, метокси, трифторметил, дифторметил, трифторметокси, дифторметокси, Cl или F. В других предпочтительных вариантах осуществления R2 обозначает Н или трифторметил.
Далее, в варианте осуществления изобретения A выбран из -CO-O-, -NH-CO-, -CO-NH, -C=C-, -CCH3-O- и связующей группы -Y-(CH2)n-X-, в которой
Y присоединен к R1 и выбран из связи, -O-, -SO2-, -CH2-O-, -CO-, -CO-O-, -NH-CO-, -C=C- и -C≡C-; n означает целое число от 1 до 7; и X присоединен к фениленовой/пиридильной группе и выбран из связи, -O-, -S- и -NH. Предпочтительно А выбран из -CO-NH, -C=C-, -CCH3-O- и связующих групп -(CH2)n-X- и -O-(CH2)n-X-. В предпочтительных вариантах осуществления A обозначает CH2-O-.
В других вариантах осуществления изобретения R1 выбран из циано, этинила, (1-4C)алкила, циклопентила, циклогексила, циклогексенила, 6,6-диметил-бицикло[3.1.1]гепт-2-ила, инданила, в случае необходимости замещенного метилом, бифенила, нафтила, фенила, в случае необходимости замещенного одним, двумя или тремя заместителями, независимо выбранными из хлора, фтора, брома, (1-4C)алкила, (2-4C)алкинила, (1-4C)алкокси, диметиламино, трифторметила, трифторметокси и (3-6C)циклоалкила, и R1 далее выбран из фенила, монозамещенного фенокси, бензилом, бензилокси, фенилэтилом, пиразолилом или триазолилом, и R1 далее выбран из пиразолила, тиазолила, оксадиазолила, тиенила, тетрагидрофуранила, пиридинила, тетрагидропиранил, каждый из которых может быть замещен хлором, (1-4C)алкилом или фенилом, замещенным (1-4C)алкилом, и R1 далее выбран из индолила, имидазопиридинила, дигидробензофуранила и бенздиоксанила, каждый из которых может быть замещен (1-4C)алкилом. В предпочтительных вариантах осуществления, R1 выбран из этинила, (1-4C)алкила, циклопентила, циклогексила, циклогексенила, бифенила, нафтила, фенила, в случае необходимости замещенного одним, двумя или тремя заместителями, независимо выбранными из хлора, фтора, брома, (1-4C)алкила, (1-4C)алкокси, диметиламино, трифторметила и трифторметокси, и далее выбран из фенила, монозамещенного фенокси, бензилом, бензилокси, фенилэтилом, пиразолилом или триазолилом, и далее выбран из тиазолила, тиенила, тетрагидрофуранила, пиридинила, тетрагидропиранила, каждый из которых может быть замещен хлором или (1-4C)алкилом, и бенздиоксанила. В частности, R1 выбран из (1-4C)алкила, циклопентила, циклогексила, пиридинила и фенила, причем последние две группы могут быть замещены одним или двумя заместителями, независимо выбранными из хлора, фтора, брома, (1-4C)алкила, (1-4C)алкокси и трифторметила. В предпочтительных вариантах осуществления R1 обозначает (1-4C)алкил или дихлорфенил.
В чрезвычайно предпочтительном варианте осуществления изобретения R1 обозначает 2,6-дихлорфенил; A обозначает связующую группу -Y-(CH2)n-X-, в которой Y присоединен к R1 и обозначает связь, n=1, и X присоединен к фениленовой группе и обозначает -O-; R2 обозначает Н; R3 обозначает -(CH2)2-COOH; и R4 обозначает Н.
В других предпочтительных вариантах осуществления изобретения R1 обозначает (1-4C)алкил; A обозначает связующую группу -Y-(CH2)n-X-, в которой Y присоединен к R1 и обозначает связь, n означает целое число, выбранное из чисел от 1 до 6, и X присоединен к фениленовой/пиридильной группе и обозначает -O- или связь; R2 обозначает Н; R3 выбран из -(CH2)2-COOH, -(CH2)3-COOH, -CH2-CHCH3-COOH, -CH2-C(CH3)2-COOH, -CHCH3-CH2-COOH, -(CH2)2-PO3H2, -(CH2)3-PO3H2 и -(CH2)2-OPO3H2; и R4 обозначает Н. Предпочтительно R1 и -(CH2)n- вместе обозначают линейную октильную группу. Далее предпочтительно R3 обозначает -(CH2)2-PO3H2. В другом предпочтительном варианте осуществления X обозначает -O-.
Термин галоген относится к фтору, хлору, брому или йоду. Предпочтительными галогенами являются фтор и хлор, и в частности хлор.
Термин (1-4C)алкил означает разветвленную или неразветвленную алкильную группу, имеющую 1-4 атома углерода, например метил, этил, пропил, изопропил и бутил. Предпочтительной алкильной группой является метил.
Термин (1-4C)алкокси означает алкоксигруппу, имеющую 1-4 атома углерода, в которой алкильная группа является такой, как определено выше. Предпочтительной алкоксигруппой является метокси.
Термин (1-4C)алкилен означает разветвленную или неразветвленную алкиленовую группу, имеющую 1-4 атома углерода, например, метилен, -CCH3CH2- и т.п. В определении R3, который обозначает (1-4C)алкилен-R5, один или более атомов углерода в алкиленовой группе могут (среди прочего) независимо быть замещенными (CH2)2 с образовыванием циклопропильной группы, то есть образуя группу R3, такую как
Термин (2-4C)алкинил означает разветвленную или неразветвленную алкинильную группу, имеющую 2-4 атома углерода, в которой тройная связь может присутствовать в группе в различных положениях, например, этинил, пропаргил, 1-бутинил, 2-бутинил и т.д.
Термин (3-6C)циклоалкил означает циклическую алкильную группу, имеющую 3-6 атомов углерода, такую как циклопропил, циклобутил, циклопентил или циклогексил. Предпочтительными являются циклопентил и циклогексил.
Термин (4-6C)циклоалкенил означает циклическую алкенильную группу, имеющую 4-6 атомов углерода и включающую одну или две двойных связи, например циклогексенил.
Термин (3-6C)циклоалкилен означает циклическую алкильную группу, имеющую две точки присоединения. Предпочтительным является 1,3-циклобутилен, имеющий структуру
Термин (6-8C)бициклоалкил означает конденсированную кольцевую систему из двух циклоалкильных групп, имеющих вместе 6-8 атомов углерода, например бицикло[3.1.1]гепт-2-ил.
Термин (8-10C)бициклическая группа означает конденсированную кольцевую систему из ароматической и неароматической кольцевой структуры, имеющих вместе 8-10 атомов углерода, например индан.
Термин моноциклический гетероцикл охватывает моноциклические гетероарильные группы и неароматические гетеромоноциклические группы, например, фуранил, тиенил, пирролил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, триазолил, оксадиазолил, пиридил, пиридазинил, пиримидинил, пиразинил, триазинил, тетрагидрофуранил, тетрагидропиранил, диоксанил, морфолинил и т.п.
Термин бициклический гетероцикл охватывает бициклические гетероарильные группы и неароматические гетеробициклические группы, например, индолил, индазолил, изоиндолил, индолизинил, бензимидазолил, имидазотиазолил, имидазопиридинил, бензфуранил, дигидробензофуранил, бенздиоксанил, хинолинил, изохинолинил, хинолизинил, тетрагидроизохинолинил и т.п.
В отношении заместителей, термин "независимо" означает, что заместители могут быть одними и теми же или отличными друг от друга в одной и той же молекуле.
Соединения по изобретению могут соответственно быть получены способами, доступными в данной области техники, и как проиллюстрировано в экспериментальном разделе этого описания.
Соединения согласно настоящему изобретению могут содержать один или более центров асимметрии и могут, таким образом, представлять собой рацематы и рацемические смеси, отдельные энантиомеры, диастереомерные смеси и индивидуальные диастереомеры. Дополнительные центры асимметрии могут присутствовать в зависимости от природы различных заместителей на молекуле. Каждый такой центр асимметрии независимо производет два оптических изомера, и все возможные оптические изомеры и диастереомеры в смесях как чистые или частично очищенные соединения включены в рамки этого изобретения. Настоящее изобретение включает все такие изомерные формы этих соединений. Независимые синтезы этих диастереомеров или их хроматографические разделения могут быть осуществлены, как это известно в данной области техники, методологией подходящей модификацией, раскрытой здесь. Их абсолютная стереохимия может быть определена рентгеновской кристаллографией кристаллических продуктов или кристаллических промежуточных соединений, которые дериватизуют, в случае необходимости, реагентом, содержащим центр асимметрии известной абсолютной конфигурации. Если желательно, рацемические смеси соединений могут быть разделены так, чтобы были выделены индивидуальные энантиомеры. Разделение может быть осуществлено способами, известными в данной области техники, такими как реакция сочетания рацемической смеси соединений с энантиомерно чистым соединением с образованием диастереомерной смеси с последующим разделением индивидуальных диастереомеров обычными методами, такими как фракционная кристаллизация или хроматография.
Соединения могут существовать как полиморфы, которые также включены в настоящее изобретение. Кроме того, соединения могут образовывать сольваты с водой (то есть гидраты) или обычными органическими растворителями, и такие сольваты также находятся в рамках этого изобретения.
Изотопно меченное соединение формулы (I) или его фармацевтически приемлемые соли, включая соединения формулы (I), изотопно меченные так, чтобы быть обнаруживаемым PET или SPECT, также находится в рамках изобретения. То же самое относится к соединениям формулы (I), меченным [13C]-, [14C]-, [3H]-, [18F]-, [125I]- или другими изотопно обогащенными атомами, подходящим для связывания с рецептором или исследований метаболизма.
Термин "фармацевтически приемлемая соль" относится к таким солям, которые, в рамках нормального медицинского суждения, являются подходящими для использования в контакте с тканями человека и животных без нежелательной токсичности, раздражения, аллергической реакции и т.п. и соразмерны с приемлемым отношением выгоды/риска. Фармацевтически приемлемые соли известны в данной области техники. Они могут быть получены in situ выделением и очисткой соединений по изобретению или отдельно, путем введения их в реакцию с фармацевтически приемлемыми нетоксичными основаниями или кислотами, включая неорганические или органические основания и неорганические или органические кислоты.
Соединения по изобретению могут вводиться энтерально или парентерально. Точная доза и режим введения этих соединений и их композиций зависят от биологической активности соединения per se, возраста, массы тела и пола пациента, потребности индивидуального пациента, которому вводят лекарственное средство, степень расстройства или потребности и суждения врача. В общем, парентеральное введение требует более низких дозировок, чем другие способы введения, которые больше зависят от адсорбции. Однако дозировки для человека предпочтительно составляют от 0,001 до 10 мг на кг массы тела. В общем, энтеральные и парэнтеральные дозировки составляют от 0,1 до 1000 мг в сутки полных активных ингредиентов.
Смешанные с фармацевтически подходящими вспомогательными средствами, например, как описано в стандартной ссылке “Remington, The Science and Practice of Pharmacy” (21st edition, Lippincott Williams & Wilkins, 2005, см. особенно Часть 5: Pharmaceutical Manufacturing), соединения могут быть прессованы в твердые лекарственные формы, такие как пилюли или таблетки, или обработаны в капсулы или суппозитории. Посредством фармацевтически подходящих жидкостей соединения могут также быть нанесены в форме раствора, суспензии или эмульсии.
Для того чтобы получить лекарственные формы, например таблетки, возможно использование обычных добавок, таких как наполнители, красители, полимерные связующие и т.п. В общем, может использоваться любая фармацевтически подходящая добавка, которая не противодействует функции активных соединений.
Подходящие носители, с которыми могут вводиться соединения по изобретению, включают, например, лактозу, крахмал, производные целлюлозы и т.п. или их смеси, используемые в подходящих количествах. Композиции для внутривенного введения могут, например, быть растворами соединений по изобретению в стерильном изотоническом водном буфере. Если необходимо, внутривенные композиции могут включать, например, солюбилизирующие агенты, стабилизаторы и/или местный анестетик для ослабления боли в месте инъекции.
Фармацевтические композиции по изобретению могут быть составлены для любого пути введения и могут включать по меньшей мере одно соединение согласно настоящему изобретению и его фармацевтически приемлемые соли с любым фармацевтически подходящим ингредиентом, эксципиентом, носителем, адъювантом или носителем.
"Фармацевтически подходящий" означает, что носитель, разбавитель или эксципиент должен быть совместим с другими ингредиентами состава и не быть вредными для реципиента.
В варианте осуществления изобретение относится к фармацевтической упаковке или набору, включающим одну или более емкостей, наполненных одной или более фармацевтическими композициями по изобретению. К такой емкости(ям) могут быть приложены различные письменные материалы, такие как инструкции для использования или уведомления в форме, предписанной государственным органом, регулирующим производство, использование или продажу органом, регулирующим производство, использование или продажу, для медицинского или ветеринарного введения.
Если не указано иное, все технические и научные термины, используемые здесь, имеют то же самое значение, как обычно понимается специалистом в области техники, к которой относится это изобретение. Хотя способы и материалы, подобные или эквивалентные описанным здесь, могут использоваться в практике или испытании настоящего изобретения, подходящие способы и материалы описаны в этом документе.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигура 1. Процент альтернации у молодых и старых самцов мышей C57BL/6J в T-лабиринте, получавших либо носитель (контрольные группы), либо соединение 34b (10 мг/кг; перорально).
Следующие примеры предназначены для дальнейшей более подробной иллюстрации изобретения.
ПРИМЕРЫ
§1. МАТЕРИАЛЫ И МЕТОДЫ
Спектры ядерного магнитного резонанса (1H ЯМР) определяли в обозначенном растворителе, используя Bruker Avance-I 400 с 9,4T магнитом (1H: 400 МГц, 13C: 100 МГц), оборудованный широкополосной инверсионной головкой BBI с Z-градиентом и АТМ, или Bruker Avance-DRX 600 с 14,1T магнитом, оборудованный обратной тройной резонансной криоголовкой TXI с Z-градиентом и АТМ, при 300 K, если не указано иное. Спектры определяли в дейтеризованном хлороформе (CDCl3) с 99,8% атома D; или в диметилсульфоксиде-d6 (ДМСО-d6), содержащем 0,03 об./об. % тетраметилсилана; оба получены от Aldrich Chemical; сдвиги (δ) даны в ppm слабопольного сдвига от тетраметилсилана. Константы связывания J даны в Гц. Формы пиков в спектрах ЯМР обозначены символами 'кв.' (квартет), 'дкв.' (дублет квартетов), 'т' (триплет), 'дт' (дублет триплетов), 'д' (дублет), 'дд' (дублет дублетов), 'с' (синглет), 'уш.с' (уширенный синглет) и 'м' (мультиплет). NH и ОН сигналы идентифицировали после смешивания образца с каплей D2O.
Температуру плавления регистрировали на приборе для измерения температуры плавления Büchi B-545.
Все реакции, включающие чувствительные к влажности соединения или условия, осуществляли в безводной атмосфере азота.
Реакции были проверены при использовании тонкослойной хроматографии (TLC) на покрытых пластмассовых планшетах с силикагелем (предварительно покрытые силикагелем Merck 60 F254) с обозначенным элюентом. Пятна визуализировали УФ-светом (254 нм) или I2.
Жидкостная хроматография - Масс-спектрометрия (LC-MS)
Система A: Колонка: Acquity UPLC BEH C18 1,7 мкм, 50 Ч 2,1 мм с 1,7 мкм частицами. Колонку термостатировали в сушильном шкафу для колонок при 45°C.
Детекция: Диодная матрица от 210 до 260 нм
| стадия | общее время (мин) | поток (мкл/мин) | А(%) | B(%) |
| 0 | 0 | 800 | 95 | 5 |
| 1 | 0,1 | 800 | 95 | 5 |
| 2 | 4,5 | 800 | 10 | 90 |
| 3 | 5 | 800 | 10 | 90 |
| 4 | 5,01 | 800 | 95 | 5 |
A=99,9% воды с 0,1% CH3COOH
B=99,9% CH3CN с 0,1% CH3COOH
Система B: Колонка: Waters Sunfire C18, 30 Ч 4,6 мм с 2,5 мкм частицами. Колонку термостатировали в сушильном шкафу для колонок при 23°C.
Детекция: UV/VIS-метр с длиной волны 254 нм + испарительный детектор рассеяния света, функционирующий при 70° Цельсия и давлении N2 1,7 бар.
| стадия | общее время (мин) | поток (мкл/мин) | А(%) | B(%) |
| 0 | 0 | 1800 | 95 | 5 |
| 1 | 1,8 | 1800 | 0 | 100 |
| 2 | 2,6 | 1800 | 0 | 100 |
| 3 | 2,8 | 1800 | 95 | 5 |
| 4 | 3,0 | 1800 | 95 | 5 |
A=99,9% воды с 0,1% HCOOH
B=99,9% CH3CN с 0,1% HCOOH
Обозначенное время удерживания (Rt) для Системы B дано для пика в хроматограмме полного ионного тока (TIC), которая показала массу для [M+H]+ в пределах 0,5 amu точности расчетного точного MW и имела ассоциированный пик на хроматограмме испарительного светорассеивания (ELS) с % относительной области (чистота) >85%.
§2. ОБЩИЕ АСПЕКТЫ СИНТЕЗОВ
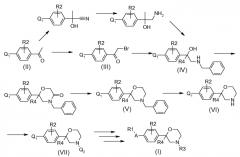
Подходящие синтезы заявленных соединений и промежуточных соединений, содержащих 2-арилморфолиногруппы, соответствуют путям, как описано ниже; см. Схему 1.
Схема 1
Q1 обозначает группу, эквивалентную R1-A, или группу, которая может быть превращена в R1-A. Q2 обозначает группу, эквивалентную R3, или группу, которая может быть превращена в R3. В отношении деталей, см. полные детали, данные ниже.
Синтез начинается с соответствующим образом замещенного метилфенилкетона (II). Соответствующим образом замещенные метилфенилкетоны коммерчески доступны или могут быть получены из других коммерчески доступных метилфенилкетонов, например O-алкилированием (не)замещенных 4-гидроксиацетофенонов. Это O-алкилирование может быть осуществлено с подходящим алкилирующим агентом, таким как 1-бромоктан или бензил бромид, в растворителях, таких как диметилсульфоксид (ДМСО), ацетон или ацетонитрил, в присутствии основания, такого как гидроксид калия или карбонат калия, при температурах от 0°C до 60°C. Как другой пример, 1-(4-бензилокси-3-трифторметил-фенил)-этанон был получен из 4'-фтор-3'-(трифторметил)метилфенилкетона реакцией с бензиловым спиртом в присутствии сильного основания, такого как трет-бутоксид калия, в растворителе, таком как тетрагидрофуран, при температуре приблизительно 70°C.
Соответствующим образом замещенный метилфенилкетон (II) бромируют, получая 2'-бромацетофеноны (III). Бромирование может быть осуществлено с бромидом меди (II) в подходящем растворителе, таком как этилацетат, с нагреванием с обратным холодильником; через реакцию соответствующего силиленольного эфира, полученного с DIPEA и TMSOTf, при 0°C, с NBS в растворителе, таком как дихлорметан, при температуре окружающей среды; или с тетра-N-бутиламмоний трибромидом, в растворителе, таком как метанол, при температуре окружающей среды.
Реакция 2'-бромацетофенонов (III) с бензил амином, в растворителе, таком как этанол и хлороформ, при температурах от 0°C до температуры окружающей среды дает аминокетоны (R4=H), которые непосредственно восстанавливали восстановителем, таким как боргидрид натрия, в растворителе, таком как этанол и хлороформ, при температурах от 0°C до температуры окружающей среды, получая аминоспирты (IV, R4=H). Альтернативно, 2'-бромацетофеноны (III) могут быть восстановлены подходящим восстановителем, таким как NaBH4, в растворителе, таком как 1,4-диоксан, при температуре окружающей среды, с последующей обработкой основанием, таким как KOH, в смеси воды и подходящего растворителя, такого как Et2O, получая 2-арилоксираны, которые, при обработке бензиламином при температуре 80°C, дают аминоспирты (IV, R4=H). Другой способ для синтеза аминоспиртов (IV, R4=Me) осуществляют реакцией соответствующим образом замещенного метилфенилкетона с триметилсилил цианидом в присутствии кислоты Льюиса, такой как йодид цинка, при температуре окружающей среды, в чистом виде, с последующим восстановлением промежуточного соединения цианогидрина восстановителем, таким как литий-алюминийгидрид, в растворителе, таком как тетрагидрофуран, и последующим формирование имина с бензальдегидом в присутствии кислого катализатора, такого как п-толуолсульфоновая кислота, в растворителе, таком как толуол, и наконец восстановлением промежуточного имина боргидридом натрия, в растворителе, таком как метанол, при температурах от -15°C до температуры окружающей среды.
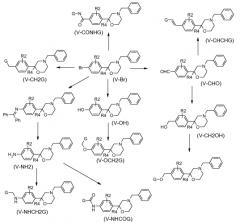
Аминоспирты (IV) могут быть введены в реакцию с активированной монохлоруксусной кислотой или бромуксусной кислотой в растворителе, таком как дихлорметан, с основанием, таким как триэтиламин, и затем циклизованы в растворителе, таком как 2-пропанол, с основанием, таким как гидроксид калия, с получением морфолин-3-онов. Эти морфолин-3-оны могут затем быть восстановлены восстановителем, таким как гидрид бора, в растворителе, таком как тетрагидрофуран, при температурах от 0°C до температуры окружающей среды, с получением N-бензил морфолинов (V). Некоторые из N-бензил морфолинов (V) могут быть превращены в другие N-бензил морфолины (V), см. Схему 2. Например, N-бензил-2-(4-бромфенил)-морфолин (V-Br) использовался как исходный материал в следующих последовательностях:
Таким образом, обработка V-Br н-бутил литием при -75°C в растворителе, таком как тетрагидрофуран или простой диэтиловый эфир, с последующим гашением формамидом, таким как N,N-диметилформамид или N-формилморфолин, приводит к формированию V-CHO. Если промежуточные соединения лития гасят подходящим изоцианатом, тогда образуются соответствующие амиды V-CONHG.
Восстановление V-CHO восстановителем, таким как боргидрид натрия, в растворителе, таком как метанол, при температурах от 0°C до температуры окружающей среды, давало бензиловые спирты V-CH2OH.
Соединения типа V-CH2OH могут быть подвергнуты реакции сочетания в условиях реакции Mitsunobu с фенолами в растворителе, таком как тетрагидрофуран или дихлорметан, при температуре окружающей среды.
Соединения типа V-CHO могут также быть подвергнуты реакции сочетания с подходящим фосфонийилидом, в растворителе, таком как тетрагидрофуран, при температуре около 70°C, давая соединения типа V-CHCHG. Этот илид может быть получен из подходящей соли фосфония с сильным основанием, таким как гидрид натрия, в растворителе, таком как тетрагидрофуран, при температурах около 0°C.
V-Br может также быть превращен в V-OH с подходящим катализатором палладия в растворителе, таком как 1,4-диоксан (Anderson K.W.; Ikawa T., Tundel R.E., Buchwald S.L. J. Am. Chem. Soc. 2006 128(33), 10694-10695). Соединения V-OH могут алкилироваться, например, в условиях переноса фаз в растворителе, таком как вода и 1,4-диоксан, с основанием, таким как гидроксид калия, и катализатором переноса фаз, таким как тетрабутиламмоний бромид, при температурах вокруг температуры кипения растворителя.
Схема 2
G обозначает группу, которая является частью R1-A в конечных соединениях I.
В условиях катализа палладием IV-Br может также быть превращен в V-CH2G с подходящим металлорганическим реагентом, таким как реагент бора (Suzuki-реакция) или цинковый реагент (Negishi-реакция), в растворителе, таком как толуол или тетрагидрофуран, при температурах около температуры кипения растворителя. Также V-Br может быть подвергнут реакции сочетания с подходящим донором амина, таким как бензофенон имин, в условиях катализа палладием в присутствии основания, такого как трет-бутоксид натрия, в растворителе, таком как толуол, при температурах около 100°C. Последующая обработка водным раствором кислоты, такой как соляная кислота, при температуре окружающей среды приводит к промежуточным соединениям V-NH2. V-NH2 могут быть введены в реакцию с подходящим алкилирующим агентом и основанием, таким как N-этилдиизопропиламин, в растворителе, таком как метанол, при температуре окружающей среды, с получением вторичных аминов V-NHCH2G. V-NH2 могут также быть введены в реакцию с подходящим реагентом ацилирования, таким как ацил хлорид, с подходящим основанием, таким как N-этилдиизопропиламин, в растворителе, таком как ацетонитрил, при температурах от 0°C до температуры окружающей среды, с получением амидов V-NHCOG.
Удаление N-бензильной группы в N-бензил морфолинах (V) может быть осуществлено гидрированием в растворителе, таком как этанол, и с катализатором, таким как гидроксид палладия, или альтернативно реакцией с ACE-Cl в растворителе, таком как 1,2-дихлорэтан, с последующей реакцией промежуточного карбамата с метанолом. Полученные морфолины (VI) могут быть превращены в другие морфолины (VI) последовательностью стадий. См. схему 3. Например, (VI-OH) может быть защищен по азоту подходящей защитной группой (P.G.M. Wuts, T.W. Greene Protective groups in organic synthesis, 4th ed., John Wiley & Sons, 2006), такой как трет-бутилоксикарбонил (ВОС), реакцией с ди-трет-бутил бикарбонатом в растворителе, таком как ацетонитрил, при температуре окружающей среды. Затем фенольная группа может быть введена в реакцию с подходящим алкилирующим реагентом в растворителе, таком как ацетонитрил, в присутствии основания, такого как карбонат калия, при температуре окружающей среды. После этого трет-бутилоксикарбонильная (ВОС) группа может быть удалена обработкой кислотой, такой как хлорид водорода, в растворителе, таком как этанол, при температурах от температуры окружающей среды до 60°C, давая модифицированный морфолин (VI-OG).
Схема 3
Морфолины (VI) могут быть введены в реакцию с эфиром (мет)акриловой кислоты, в так называемой реакции Майкла, в растворителе, таком как ацетонитрил, метанол или N,N-диметилформамид, при температурах от температуры окружающей среды до 85°C, и в конечном счете с добавлением некоторого количества основания, такого как триэтиламин или 1,8-диазабицикло[5.4.0]ундец-7-ена, с получением эфиров морфолин-4-ил-пропионовой кислоты (VIIa, Q2=CH2CH2COOR'). В случае если эти эфиры морфолин-4-ил-пропионовой кислоты (VIIa, Q2=CH2CH2COOR') содержат фенольную группу (VIIA-ОН), эти соединения могут быть модифицированы следующим образом: реакцией с подходящим алкилирующим реагентом, таким как алкил бромид или алкил хлорид, в присутствии основания, такого как карбонат калия или карбонат цезия, в растворителе, таком как ацетонитрил и/или тетрагидрофуран, при температуре окружающей среды, с получением соединения типа VIIa-OG. Альтернативно, VIIA-ОН может быть превращен в VIIa-OG реакцией с подходящим спиртом в присутствии трифенилфосфина и подходящего азо-реагента, такого как диизопропил азодикарбоксилат, в растворителе, таком как тетрагидрофуран или дихлорметан. Кроме того, VII-ОН может бы