Штамм bifidobacterium longum, пригодный для применения в иммуномодуляции, индукции продукции цитокинов, лечении аутоиммунного заболевания, контроле отношения il - 10:il - 12, и его использование
Иллюстрации
Показать всеГруппа изобретений относится к штамму Bifidobacterium longum NCIMB 41675, составу, его содержащему, и продукту питанию, содержащему указанные штамм или состав. Предложенный штамм обладает способностью к индукции продукции цитокинов и контролю отношения IL-10:IL-12 и пригоден для применения в иммуномодуляции, лечении аутоиммунного заболевания. Предложенные штамм, состав и продукт питания обладают пробиотическими свойствами. 3 н. и 22 з.п. ф-лы, 16 ил., 4 табл., 8 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к штамму бифидобактерий {Bifidobacterium) и его использованию в качестве пробиотических бактерий, в частности, в качестве иммуномодулирующего биотерапевтического вещества.
Уровень техники
Механизмы защиты желудочно-кишечного тракта человека от его колонизации кишечными бактериями исключительно сложны и включают иммунные и неиммунные взаимодействия (1). Врожденные защитные механизмы включают низкий pH желудка, желчные соли, перистальтику, муциновые слои и антимикробные вещества и составы, такие, как лизоцим (2). Иммунные механизмы включают специализированные лимфоидные образования, подстилающие М-клетки (называемые также комплексами Пейера), распределенные по всей тонкой и прямой кишке (3). Люминальные антигены, присутствующие в данных местах, стимулируют развитие субпопуляций Т- и В-клеток с образованием цитокиновых сетей и секрецию антител в желудочно-кишечный тракт (4). Кроме того, антигены могут попадать через эпителиальные клетки к интраэпителиальным лимфоцитам и к иммуноцитам находящейся под ними собственной пластины слизистой оболочки (5). Таким образом, человек тратит значительные силы на иммунную защиту желудочно-кишечного тракта. Поскольку слизистая оболочка кишечника является самой большой поверхностью, посредством которой человек контактирует с окружающей средой, ему необходимы специальные механизмы, посредством которых регулируется иммунный ответ на 100 тонн пищи, которая проходит через желудочно-кишечный тракт в течение среднего времени жизни человека. Кроме того, кишечник населяют более 500 видов бактерий, концентрация которых в прямой кишке составляет 1011-1012/г. В связи с этим регулирующие механизмы должны быть способны различать не патогенные бактерии, нормально живущие в кишечнике, от нашествий патогенов, которые могут вызвать серьезные проблемы у хозяина. Кишечная флора активно участвует в защите хозяина, борясь с попадающими через пищеварительную систему потенциально патогенными микроорганизмами.
Считается, что некоторые виды пробиотических бактерий более эффективны, когда они получены из видов, для лечения которых предназначены, или из близко родственных видов. Поэтому существует потребность в пробиотических штаммах, полученных из животных-компаньонов, и отличных от штаммов, полученных от людей, которые можно было бы использовать для лечения животных-компаньонов.
В публикации WO 01/90311 описаны пробиотические микроорганизмы, выделенные из образцов фекалий кошек и обладающие пробиотическим действием. Однако данные бактерии были получены из фекальных образцов, и поэтому они могут не представлять собой часть естественной флоры, присутствующей в верхних отделах желудочно-кишечного тракта.
Соответственно, существует потребность в штаммах бактерий, получаемых путем выделения из естественной флоры, присутствующей в верхних отделах желудочно-кишечного тракта, особенно подходящих для кошек и обладающих пробиотическими свойствами и способностью выживать в процессе их обработке. Существует также потребность в составах, содержащих такие штаммы и удобных в использовании.
Сущность изобретения
В настоящем изобретении предлагается выделенный штамм бифидобактерий №41675 по NCIMB.
Штамм бифидобактерий может быть в форме живых клеток. Штамм бифидобактерий может быть в форме не живых клеток.
Бифидобактерии могут быть выделены из образцов ткани толстой кишки здоровых кошек, взятых путем биопсии.
Штамм бифидобактерий может обладать значительным иммуномодулирущим действием при его оральном потреблении.
В настоящем изобретении предлагается также состав, содержащий упомянутый штамм бифидобактерий.
Состав может дополнительно содержать пробиотический материал. Состав может дополнительно содержать пребиотический материал. Состав может дополнительно содержать носитель для орального приема. Носитель для орального приема может быть одним из фармацевтически приемлемых носителей, таким, как, например, капсула, таблетка, порошок. Носителем для орального приема может быть также пищевой продукт, такой, как, например, масляная суспензия, суспензия на основе молока, сыр, состав на основе какао-масла, соус и/или состав на основе йогурта.
В настоящем изобретении предлагается также продукт питания, содержащий штамм бифидобактерий или состав в соответствии с настоящим изобретением.
Продукт питания может быть может быть сухим продуктом питания. Продукт питания может быть влажным продуктом питания. Продукт питания может быть кормом для животных-компаньонов.
В настоящем изобретении предлагаются также штамм бифидобактерий, или состав, или продукт питания в соответствии с настоящим изобретением, которые могут использоваться в качестве лекарственного средства.
В настоящем изобретении предлагаются также штамм бифидобактерий, или состав, или продукт питания в соответствии с настоящим изобретением, которые могут использоваться для профилактики и/или лечения нежелательных воспалительных процессов.
В настоящем изобретении предлагаются также штамм бифидобактерий, или состав, или продукт питания в соответствии с настоящим изобретением, которые могут использоваться для профилактики и/или лечения нежелательных воспалительных процессов в желудочно-кишечном тракте.
В настоящем изобретении предлагаются также штамм бифидобактерий, или состав, или продукт питания в соответствии с настоящим изобретением, которые могут использоваться для профилактики и/или лечения аутоиммунных нарушений, вызванных нежелательными воспалительными процессами.
В настоящем изобретении предлагаются также штамм бифидобактерий, или состав, или продукт питания в соответствии с настоящим изобретением, которые могут использоваться для профилактики и/или лечения диарейных состояний, вызванных нежелательными воспалительными процессами.
В настоящем изобретении предлагаются также штамм бифидобактерий, или состав, или продукт питания в соответствии с настоящим изобретением, для коррекции или улучшения работы иммунной системы животных-компаньонов.
В настоящем изобретении предлагаются также штамм бифидобактерий, или состав, или продукт питания в соответствии с настоящим изобретением, которые могут использоваться для профилактики и/или лечения аутоиммунных заболеваний у животных-компаньонов.
В настоящем изобретении предлагаются также штамм бифидобактерий, или состав, или продукт питания в соответствии с настоящим изобретением, которые могут использоваться для профилактики и/или лечения воспалений у животных-компаньонов.
В настоящем изобретении предлагается штамм бифидобактерий AH121A (номер по NCIMB 41675), а также его мутанты и варианты.
Мутант может быть генетически модифицированным мутантом. Вариант может быть естественно встречающимся вариантом бифидобактерий.
Штамм может получен путем выделения из разрезанного и промытого кошачьего желудочно-кишечного тракта.
Штамм может быть пробиотиком. Штамм может быть в форме биологически чистой культуры.
В настоящем изобретении предлагается также выделенный штамм бифидобактерий, номер по NCIMB 41675.
Штаммы бифидобактерий могут быть в форме живых клеток. В качестве альтернативы, штаммы бифидобактерий могут быть в форме не живых клеток.
Как правило, пробиотические бактерии используются в форме живых клеток. Однако возможно их использование и в форме не живых клеток, например, в виде умерщвленных культуры или составов, содержащих полезные факторы, экспрессируемые пробиотическими бактериями. Умерщвленные культуры могут включать микроорганизмы, убитые под воздействием высокой температуры, экстремальных значений pH или давления. При использовании не живых клеток изготовление конечного продукта из них упрощается, они могут быть включены в широкое разнообразие фармацевтических форм, и условия хранения препаратов из них значительно менее жесткие, чем для препаратов, содержащих живые клетки. Так, например, в патенте США 4347240 описано успешное использование убитых высокой температурой клеток штамма Lactobacillus casei YIT 9018 для лечения и/или профилактики роста опухолей.
В настоящем изобретении предлагается также использование бактерий, получаемых выделением из разрезанного и промытого кошачьего желудочно-кишечного тракта, для сохранения и улучшения здоровья животного-компаньона, а также использование составов, содержащих молочнокислые бактерии.
В настоящем изобретении предлагается также состав, содержащий предлагаемый штамм бифидобактерий. Состав может включать еще один пробиотический материал. Состав может включать пребиотический материал.
Бифидобактерии являются симбиотическими микроорганизмами. Они были выделены из микрофлоры желудочно-кишечного тракта человека. Иммунная система желудочно-кишечного тракта не дает выраженной реакции на представителей данной микрофлоры, так как иначе возникшая воспалительная реакция разрушила бы также клетки-хозяева и нарушила бы функционирование тканей. Поэтому существуют определенные механизмы, благодаря которым иммунная система может распознавать не патогенных членов семейства желудочно-кишечной микрофлоры и отличать их от патогенных организмов. Это обеспечивает сохранность клеток-хозяев с одной стороны, и поддержание требуемого защитного барьера от патогенной флоры, с другой стороны.
В контексте настоящего описания термины «мутант», «вариант» и «генетически модифицированный мутант» включают штамм бифидобактерий, генетические и фенотипические свойства которого отличаются от соответствующих свойств родительского штамма. Термин «встречающийся в природе вариант штамма Bifidobacterium longum» подразумевает организмы, отобранные в результате селекции из организмов, в которых произошли спонтанные изменения целевых свойств. Намеренные изменения свойств родительского штамма осуществляются обычными генно-инженерными методами (in vitro), такими, как разрыв генов, коньюгационный перенос и прочие. Термин «генетическое модифицирование» включает введение экзогенных и/или эндогенных последовательностей ДНК в геном штамма бифидобактерий, например, путем их вставки в геном бактериального штамма посредством векторов на основе плазмидной ДНК или бактериофагов.
Термины «естественные мутации» и «индуцированные мутации» включают изменения по меньшей мере одного основания путем делеции, вставки, обращения или иных изменений ДНК, которые могут приводить к изменению аминокислотной последовательности, кодируемой последовательностью ДНК.
Термины «мутант», «вариант» и «генетически модифицированный мутант» включают также штамм бифидобактерий, который был подвергнут генетическим изменениям, которые накапливаются в геноме в степени, в сущности и по своей природе одинаковой для всех микроорганизмов, и/или генетическим изменениям, которые происходят в результате спонтанных мутаций, приобретений и/или потерь, которые не могут быть получены путем намеренных (in vitro) преобразований генома, но которые могут быть получены путем естественного отбора вариантов и/или мутантов, и которые обеспечивают требуемые преимущества, повышающие жизнеспособность бактерий при воздействии на них агрессивных факторов среды, таких, как, например, антибиотики. Мутант может быть создан путем намеренной (in vitro) вставки тех или иных генов в геном, которые принципиально не меняют биохимической функциональности организма, но продукты экспрессии которых могут быть использованы для идентификации или селекции бактерий, например, которые придают устойчивость к антибиотикам.
Сведущим в данной области техники будет понятно, что мутантные или вариантные штаммы бифидобактерий могут быть идентифицированы посредством анализа последовательности их ДНК на гомологию с родительским штаммом. Штаммы бифидобактерий, имеющие высокую степень идентичности последовательности ДНК с родительским штаммом, могут считаться мутантными или вариантными штаммами. Штамм бифидобактерий, имеющий степень идентичности (гомологии) последовательности ДНК соответствующей последовательности родительского штамма, составляющую 96% или более, 97% или более, 98% или более, или 99% или более, может считаться мутантным или вариантным штаммом. Гомологичность последовательностей может быть определена с помощью программы BLAST, общедоступной на сайте http://www.ncbi.nlm.nih,gov/BLAST/.
Мутанты родительского штамма включают также производные штаммы бифидобактерий, имеющие гомологию межгенной спейсерной полинуклеотидной последовательности 16s-23s, составляющую по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% по отношению к соответствующей последовательности родительского штамма. Такие мутанты могут дополнительно содержать мутации ДНК в других последовательностях ДНК бактериального генома.
Краткое описание чертежей
Настоящее изобретение будет более понятным из нижеследующего подробного описания его воплощений, приводимых только в качестве примеров, сопровождаемого прилагаемыми чертежами.
Фиг.1. Фотография В. longum AH121A, выращенных на агаре с красителем конго красный.
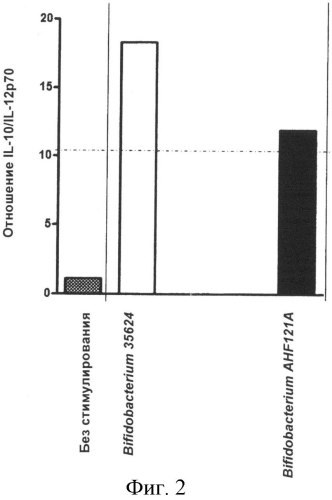
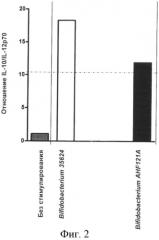
Фиг.2. Столбчатая диаграмма, отображающая отношение экспрессии IL-10:IL-12р70 в мононуклеарах периферической крови, не стимулируемых и стимулируемых штаммом Bifidobacterium longum AH121A;
Фиг.3. Столбчатая диаграмма, отображающая выживаемость бактерий штамма AH121A в условиях низких значений pH (бактерии находились в среде с pH 2,5 в течение 6 часов; выживание определяли способом чашечного подсчета).
Фиг.4-6. Столбчатые диаграммы, отображающие выработку цитокинов в культурах in vitro мононуклеаров периферической крови.
Фиг.7А-7Е. Графики индукции IL-10 (в пг/мл) в мононуклеарах периферической крови после стимуляции in vitro в зависимости от количества бактерий в лунке, для штаммов AH121A и Bifidobacterium 35624;
Фиг.8A-8D. Графики индукции IL-1β (в пг/мл) в мононуклеарах периферической крови после стимуляции in vitro в зависимости от количества бактерий в лунке, для штаммов AH121A и Bifidobacterium 35624;
Фиг.9A-9D. Графики индукции IL-6 (в пг/мл) в мононуклеарах периферической крови после стимуляции in vitro в зависимости от количества бактерий в лунке, для штаммов AH121A и Bifidobacterium 35624;
Фиг.10A-10D. Графики индукции IL-8 (в пг/мл) в мононуклеарах периферической крови после стимуляции in vitro в зависимости от количества бактерий в лунке, для штаммов AH121A и Bifidobacterium 35624;
Фиг.11A-11D. Графики индукции IL-12p70 (в пг/мл) в мононуклеарах периферической крови после стимуляции in vitro в зависимости от количества бактерий в лунке, для штаммов AH121A и Bifidobacterium 35624;
Фиг.12А-12Е. Графики индукции TNF-α (в пг/мл) в мононуклеарах периферической крови после стимуляции in vitro в зависимости от количества бактерий в лунке, для штаммов AH121A и Bifidobacterium 35624;
Фиг.13А-13С. Графики индукции IFN-γ (в пг/мл) в мононуклеарах периферической крови после стимуляции in vitro в зависимости от количества бактерий в лунке, для штаммов AH121A и Bifidobacterium 35624;
Фиг.14A-14D. Графики индукции G-CSF (в пг/мл) в мононуклеарах периферической крови после стимуляции in vitro в зависимости от количества бактерий в лунке, для штаммов AH121A и Bifidobacterium 35624;
Фиг.15. Столбчатые диаграммы, отображающие влияние AH121A на выработку IL-10 и IL-12p70 в человеческих дендритных клетках миелоидного типа.
Фиг.16. Столбчатые диаграммы, отображающие влияние AH121A на человеческие Т-клетки, не подвергавшиеся воздействию CD4.
Подробное описание изобретения
Штамм Bifidobacterium longum AH121A был внесен в Национальную коллекцию промышленных и морских бактерий (NCIMB - Абердин, Великобритания) 5 ноября 2009 года с присвоением ему номера NCIMB 41675.
Штамм Bifidobacterium longum UCC35624 был внесен в Национальную коллекцию промышленных и морских бактерий (NCIMB - Абердин, Великобритания) 13 января 1999 года с присвоением ему номера NCIMB 41003.
Штамм Bifidobacterium longum может быть генетически модифицированным мутантом или встречающимся в природе вариантом.
Штамм Bifidobacterium longum предпочтительно имеет форму живых клеток.
В качестве альтернативы, штамм Bifidobacterium longum может быть в форме неживых клеток.
В контексте настоящего описания термин «животное-компаньон» означает домашнее животное. Предпочтительно термин «животное-компаньон» означает домашнее животное из семейства кошачьих (кошку), семейства псовых (собаку), кролика, хорька, лошадь, корову и им подобных животных. Наиболее предпочтительно «животное-компаньон» означает домашнее животное из семейства кошачьих.
Штаммы молочнокислых бифидобактерий
В первом типе воплощений настоящего изобретения, допускающем множество вариаций без отхода от идеи и масштабов настоящего изобретения, предлагается штамм молочнокислых бактерий рода Bifidobacteria, который может быть получен путем выделения из разрезанного и промытого кошачьего желудочно-кишечного тракта, и который обладает пробиотическим действием по отношению к животным. Пробиотиками называются микроорганизмы, живые или мертвые, их компоненты, такие, как белки, углеводороды или очищенные фракции бактериальных ферментов, которые благоприятно воздействуют на животное-хозяина. Кроме того, данный термин может быть также распространен на неживые клетки, например, на умерщвленные культуры или составы, или составы, содержащие благоприятные факторы, вырабатываемые пробиотическими бактериями. Они могут включать микроорганизмы, убитые под воздействием высокой температуры, экстремальных значений pH или давления. Для целей настоящего описания подразумевается, что термин «пробиотики» дополнительно включает метаболиты, вырабатываемые микроорганизмами в соответствии с настоящим изобретением во время брожения, если отдельно не указано иное. Такие метаболиты могут выделяться ими в сбраживаемую среду, или храниться в самих микроорганизмах. В контексте настоящего описания термин «пробиотик» включает также бактерии, гомогенизированные бактерии, экстракты из бактерий, супернатанты бактериальных ферментов и их смеси, которые оказывают благоприятное воздействие на животное-хозяина при их скармливании животному в терапевтических дозах.
Было определено, что молочнокислые бактерии рода Bifidobacteria, выделенные непосредственно из рассеченного и промытого желудочно-кишечного тракта млекопитающих, имеют сродство к желудочно-кишечному тракту при скармливании их соответствующим млекопитающим в виде живых бактериальных клеток, и также они оказывают значительное иммуномодулирующее действие на данное млекопитающее при скармливании в виде живых клеток, не живых клеток или в фракционированом виде. И хотя теоретически это не обязательно, считается, что пробиотические бифидобактерии в соответствии с настоящим изобретением вызывают благоприятные реакции в организме хозяина, в чем и заключается их пробиотическое действие. Было определено, что пробиотические бифидобактерии, выделенные из рассеченного и промытого желудочно-кишечного тракта, могут модулировать иммунную систему хозяина за счет непосредственного взаимодействия со слизистой оболочкой эпителия и клетками иммунной системы хозяина. Такое иммуномодулирующее действие, в сочетании с прочими видами воздействий, традиционно ассоциируемыми с пробиотическими бактериями, в частности, предотвращением сродства к кишечнику патогенов за счет прямого на них воздействия или за счет конкуренции за питательные вещества, обеспечивает исключительно высокую эффективность бифидобактерии в соответствии с настоящим изобретением в качестве пробиотического организма.
Бифидобактерии в соответствии с настоящим изобретением, получаемые выделением из рассеченного и промытого кошачьего желудочно-кишечного тракта, обладают антимикробным действием in vitro против ряда патогенных штаммов/видов бактерий. И хотя теоретически это не обязательно, такое антимикробное действие in vitro указывает на потенциально возможную их пробиотическую активность в животных in vivo, предпочтительно по отношению к животным-компаньонам, таким, как животные семейства кошачьих. Молочнокислые бактерии в соответствии с настоящим изобретением предпочтительно облают антимикробным действием против Salmonella typhimurium, Listeria monocytogenes, Listeria innocua или Eschericia coli, предпочтительно против смеси данных штаммов, и еще более предпочтительно против всех данных штаммов.
И хотя теоретически это не обязательно, считается, что антимикробное действие молочнокислых бактерий в соответствии с настоящим изобретением может быть результатом различных взаимодействий, в которых участвуют молочнокислые бактерии в соответствии с настоящим изобретением. Сведущими в данной области техники ранее высказывалось предположение, что некоторые штаммы бифидобактерий, выделенные из образцов фекалий, обладают пробиотическим действием в желудочно-кишечном тракте после их орального потребления за счет того, что они образуют барьерный слой на слизистой оболочке кишечника и тем самым препятствуют креплению к слизистой оболочке патогенных организмов. Это требует потребления «живых», а точнее, жизнеспособных клеток бактерий, так, чтобы в кишечнике прижилась колония таких бактерий. Мы, однако, считаем, что бифидобактерий в соответствии с настоящим изобретением, полученные выделением из рассеченного и промытого кошачьего желудочно-кишечного тракта, могут обладать значительным пробиотическим действием как при их потреблении в жизнеспособной форме, так и в не жизнеспособной форме, благодаря выработке, при брожении in vitro, вещества или веществ, которые ингибируют рост патогенных микроорганизм, или убивают патогенные микроорганизмы, и/или усиливают иммунные способности животного-хозяина. Такая форма пробиотического действия очень желательна, так как при ней бактерии в соответствии с настоящим изобретением могут быть даны животному в виде живых культур, неживых культур или очищенных продуктов брожения, и тем не менее оказывать на животное-хозяина благоприятный лечебный эффект.
Предпочтительно, чтобы молочнокислые бактерии в соответствии с настоящим изобретением могли сохранять жизнеспособность после прохождения через желудок. Это желательно для того, чтобы живые культуры бактерий можно было принимать орально, и после прохождения ими через пищевод и желудок они могли колонизовать желудочно-кишечный тракт. Колонизация желудочно-кишечного тракта молочнокислыми бактериями в соответствии с настоящим изобретением желательна для того, чтобы они могли оказывать на животное-хозяина долговременное благоприятное пробиотическое воздействие. Оральный прием не жизнеспособных клеток или выделенных из них компонентов также дает временные преимущества, но так как бактерии в данном случае являются не жизнеспособными, они не могут расти и постоянно оказывать пробиотическое действие in situ. В результате этого может потребоваться постоянный прием доз бифидобактерий хозяином, чтобы поддерживать обеспечиваемые ими преимущества для здоровья хозяина. В противоположность этому, жизнеспособные клетки, которые способны пройти через желудочно-кишечный тракт и остаться жизнеспособными, колонизуют слизистые оболочки кишечника за счет прилипания к ним и последующего разрастания, тем самым обеспечивают постоянный пробиотический эффект in situ. Поэтому предпочтительно, чтобы молочнокислые бактерии в соответствии с настоящим изобретением сохраняли жизнеспособность после нахождения в среде-суспензии, имеющей pH 2.5, в течение 1 часа. В контексте настоящего описания термин «сохранять жизнеспособность» означает, что по меньшей мере 25% бактерий, изначально помещенных в суспендированную питательную среду, остаются жизнеспособными по результатам метода чашечного подсчета, известного сведущим в данной области техники. Термин сохранять жизнеспособность» предпочтительно означает, что по меньшей мере 50% бактерий, изначально помещенных в суспендированную питательную среду, остаются жизнеспособными. При этом предпочтительно также, чтобы молочнокислые бактерии в соответствии с настоящим изобретением сохраняли жизнеспособность при воздействии на них среды с низкими значениями pH, так как это отражает воздействие на них желудочного сока в желудке и верхнем отделе кишечника in vivo при оральном их потреблении животными.
Штамм молочнокислых бактерий вида Bifidobacteria, получаемых выделением из рассеченного и промытого кошачьего желудочно-кишечного тракта, может использоваться для обеспечения пробиотического воздействия при его оральном потреблении животными, предпочтительно животными-компаньонами, или человеком. Не ограничивающие примеры благоприятного воздействия орального потребления предлагаемых бифидобактерий на составляющие здоровья и физиологии животного включают терапевтическое снятие симптомов или профилактику болезненных состояний, таких, как воспалительные расстройства, иммунодефицит, болезнь воспаленного кишечника, синдром раздраженного кишечника, рак (в особенности новообразования желудочно-кишечного тракта и иммунной системы), диарейные состояния, диарея, связанная с приемом антибиотиков, аппендицит, аутоиммунные расстройства, рассеяный склероз, болезнь Альцгеймера, амилоидоз, ревматоидный артрит, артрит, патологическая подвижность суставов, сахарный диабет, резистентность к инсулину, бактериальные инфекции, вирусные инфекции, грибковые инфекции, пародонтоз, болезни мочеполовой системы, травмы, вызванные хирургическими вмешательствами, метастатическая болезнь, вызванная хирургическим вмешательством, сепсис, потеря веса, избыточный вес, чрезмерное накопление жировой ткани, анорексия, приступы лихорадки, кахексия, заживление ран, язвы, инфекции желудочно-кишечного тракта, аллергия, астма, респираторные заболевания, нарушения системы кровообращения, ишемическая болезнь сердца, анемия, расстройства аппарата свертываемости крови, болезни почек, болезни центральной нервной системы, болезни печени, нарушения питания, остеопороз, эндокринные заболевания, болезни кожных покровов. Наиболее предпочтительным является применение предлагаемого штамма для лечения болезней желудочно-кишечного тракта, включая лечение и профилактику диареи, коррекцию иммунной системы, предпочтительно лечение или профилактику аутоиммунных заболеваний и воспалений; сохранение или улучшение состояния здоровью кожных покровов и шерсти, предпочтительно лечение или профилактику атопических заболеваний кожи, устранение или уменьшение эффектов старения, включая уровень сознания и умственной активности; предотвращение расстройств, связанных с осью гипоталамус-гипофиз-надпочечник, улучшения состояния суставов, в том числе их подвижности.
Результаты лечения перечисленных выше заболеваний могут быть оценены с помощью способов, известных сведущим в данной области техники. Так, например, воспалительные расстройства, включая аутоиммунные болезни, могут быть обнаружены и наблюдаться с использованием таких тестов на работу иммунной системы in vivo, как бластогенез лимфоцитов, активность естественных клеток-киллеров, выработка антител в ответ на вакцины, задержанная гиперчувствительность и их сочетания. Ниже приводится краткое описание данных методов, хотя они хорошо знакомы сведущим в данной области техники.
1. Бластогенез лимфоцитов. В ходе данного теста измеряется пролиферативная реакция in vitro лимфоцитов, выделенных из свежей цельной крови испытуемых и контрольных животных на различные митогены, и представляет собой общую оценку функционирования Т- и В-клеток. Для проведения данного теста из цельной крови выделяли мононуклеары периферической крови с помощью методов центрифугирования и разделения по плотности по Ficoll-Hypaque. Выделенные мононуклеары периферической крови дважды промывали в среде RPMI 1640 с добавлением HEPES, L-глютамин и пенициллина/стрептомицина. Промытые клетки ресуспендировали в среде RPMI 1640, определяли их количество и доводили до требуемого значения концентрацию клеток. 2×105 клеток подвергали воздействию диапазона концентраций (от 0,1 мкг/мл до 100 мкг/мл) различных митогенов, некоторые примеры которых включали митоген фитолакки (производства Gibco), фитогемагглютинин (Gibco) и конконавалин А (производства Sigma), троекратно в течение 72 часов при температуре 37°C и в атмосфере, содержавшей 5% CO2, с добавлением 10% эмбриональной бычьей сыворотки (производства Sigma). Спустя 54 часа клетки облучали Н-тимидином активностью 10 мкКи, после чего клетки собирали и проводили подсчет сцинтилляций с помощью прибора TopCount NXT в 72 часу.
2. Активность естественных клеток-киллеров. Как описано в патенте США 6310 090, данный тест позволяет измерить активность in vitro естественных клеток-киллеров, выделенных из свежей крови подопытных и контрольных животных. Естественные клетки-киллеры являются компонентами врожденных иммунных функций млекопитающего. Для оценки цитотоксической активности NK-клеток использовались клетки аденокарциномы щитовидной железы кошек. Предварительно было показано, что используемая клеточная линия была чувствительна, то есть убивалась NK-клетками кошек. Клетки-мишени выращивали в колбе Т75, содержавшей 20 мл минимальной среды (MEM производства Sigma Chem. Co., Сент-Луис, штат Миссури, США) с добавлением 10% эмбриональной бычьей сыворотки, 100 ед./мл пенициллина и 100 мкг/мл стрептомицина. После достижения конфлюэнтности клетки-мишени обрабатывали трипсином, троекратно промывали и ресуспендировали в полной среде (RPMI-1640+10% эмбриональной бычьей сыворотки +100 ед./мл пенициллина +100 мкг/мл стрептомицина) до концентрации 5×105 клеток/мл. По три аликвоты клеток-мишеней объемом 100 мкл наносили пипеткой на планшет с 96 лунками с U-образным дном (производства Costar, Кэмбридж, штат Массачусетс) и инкубировали в течение 8 часов в качестве подготовки клеток для лучшей адгезии друг к другу. После этого к клеткам-мишеням добавляли лимфоциты (клетки-эффекторы, 100 мкл), выделенные центрифугированием по Ficoll-Hypaque (как описано выше), так что отношение количества клеток-эффекторов к количеству клеток-мишеней (отношение Е:Т) составляло 10:1. После 10 часов инкубации при температуре 37°C добавляли 20 мкл субстрата, содержащего 5 мкг 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразол-бромида (МТТ). Смесь инкубировали в течение 4 часов при 37°C, после чего не метаболизированный МТТ отсасывали. Кристаллы формазана растворяли путем добавления 200 мкл 95%-ного этанола. Оптическую плотность измеряли на длине волны 570 нм с помощью считывающего устройства для микропланшетов. Процент специфичного лизиса NK-клеток рассчитывали следующим образом:
Специфичная цитотоксичность (%)=
100×{1-[(ODклеток-мишеней и клеток-эффекторов-ODклеток-эффекторов)/(ODклеток-мишеней)]}
3. Выработка антител при реакции на вакцины. Подопытным субъектам давали набор (до 5 вакцин) спустя по меньшей мере 12 недель после кормления пробиотиком или контрольного кормления. Вакцины могут быть смесью вакцин для первичной и повторной вакцинации. Не ограничивающие примеры наборов вакцин, которые могут использоваться для данного теста, могут включать смеси вакцин производства Fort Dodge Animal Health. He ограничивающие примеры вакцин, которые могут использоваться для данного теста, могут включать вакцины от кошачьей чумы, аденовирусной инфекции, корона-вирусной инфекции, парагриппа и парвовируса. Конкретный тип используемых вакцин определяет также история вакцинации подопытного субъекта. Уровень антител, специфичных к введенной вакцине, в крови измеряли в течение 3 недель, и таким образом определяли длительность и силу иммунного ответа у контрольной группы и группы, получавшей пробиотический корм.
4. Гиперчувствительность замедленного типа. Данный тест представляет собой метод неинвазивной оценки состояния иммунной системы in vivo. В ходе теста производится подкожная инъекция поликлонального митогена «фитогеммаглютинин» (РНА) в сочетании с овечьими эритроцитами, в качестве мультивалентной вакцины, гистамина (100 мкл гистамин-фосфата 0,0275 г/л производства Greer, Ленуар, штат Северная Каролина, США) или солевого раствора с фосфатным буфером (PBS 8,5 г/л производства Sigma). Иммунный ответ измеряли и записывали в виде толщины кожной складки с помощью штангенциркуля через 0, 24, 48 и 72 часа после инъекции. Увеличенная толщина кожной складки свидетельствует о большей гиперчувствительности иммунного ответа, которая может быть уменьшена за счет лечения бактериями в соответствии с настоящим изобретением.
Дополнительные методы для оценки эффекта от употребления бифидобактерий в соответствии с настоящим изобретением описаны в патентах США 6133323 и 6310090.
Кроме того, эффективность устранения эффектов старения может быть определена методами двойной рентгеновской абсорбциометрии или сканирующей компьютерной томографии, позволяющих определить массу жира в организме и содержание минералов в костях. Подобным образом, данный метод может также использоваться для определения анатомических изменений, таких, как потеря веса или изменение плотности костных тканей в подопытных субъектах после перенесенной инфекции.
Бифидобактерии в соответствии с настоящим изобретением могут также использоваться для снижения уровня стресса у животных-компаньонов. Для определения уровня стресса, а также при его последующей коррекции и снижении могут быть измерены уровни гормонов стресса в крови, таких, как эпинефрин, норэпинефрин, допамин, кортизол, С-реактивный белок и прочие белки острой фазы. Данные гормоны узнаются биомаркерами стресса, и их содержание может быть легко измерено способами, хорошо известными сведущим в данной области техники. Кроме того, с помощью компьютерной томографии может быть непосредственно измерен размерен размер надпочечника, как показатель активности оси гипоталамус-гипофиз-надпочечник in vivo.
Кроме того, путем оценки состояния кожно-шерстяного покрова животного-компаньона, проводимого опытным специалистом, могут быть выявлены проблемы с кожным и шерстяным покровом, и наблюдаться прогресс в улучшении состоянии кожно-шерстяного покрова. Примеры критерий оценки кожно-шерстяного покрова могут включать: а) показатель линьки - определяется по стандартной процедуре, при которой расчесывают шерсть, собирают и взвешивают вычесанные волосы, и по их весу сравнивают испытываемое животное с контрольным; b) субъективную оценку кожи и шерсти - проводится опытным специалистом по таким факторам, как линька, перхоть, блеск, однородность, мягкость и плотность шерсти; с) функциональную оценку барьерной функции кожи - проводится путем протирки участка кожи марлей, смоченной в ацетоне. При данном методе с кожи удаляется одноклеточный слой, в результате чего на данном участке кожи нарушается ее барьерная функция, обеспечиваемая липидными фракциями рогового слоя. Нарушение барьерной функции характеризуется количественно путем измерения увеличения трансэпидермальной потери воды (TEWL) и степени покраснения поврежденного участка кожи способами, хорошо известными сведущим в данной области техники. Покраснение измеряется в баллах с помощью специальной камеры и системы освещения. Показатели потери воды (TEWL) и покраснения в баллах измеряются до обработки кожи, сразу после обработки, в конце 5-го и 24-го часа после обработки, и на основании этих данных оценивается состояние защитных и ранозаживляющих функций кожи.
Кроме того, лечение инфекций желудочно-кишечного тракта у животных-компаньонов может включать улучшение состояния их бактериальной микрофлоры. Улучшение состояния микрофлоры у животных-компаньонов предпочтительно включает уменьшение содержания количества патогенных бактерий в фекалиях животных-компаньонов. Содержание патогенных бактерий в фекалиях животных-компаньонов может быть определено количественно стандартным методом чашечного подсчета, известным сведущим в данной области техники. К патогенным бактериям предпочтительно относятся бактерии, выбираемые из группы, состоящей из бактерий видов Clostridia, Escherichia, Salmonella, им подобных и их смесей. Не ограничивающие примеры подходящих штаммов патогенных бактерий включают С.perfringens, С.difficile, Eschericia coli, Salmonella typhimurium и их смеси.
Способ использо