Никелевый комплекс 5,10,15,20-тетракис[3',5'-ди(2"-метилбутилокси)фенил]-порфина, проявляющий свойство стационарной фазы для газовой хроматографии
Иллюстрации
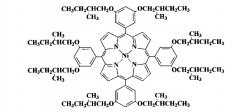
Показать всеИзобретение относится к никелевому комплексу 5,10,15,20-тетракис [3′,5′-ди-(2″-метилбутилокси)фенил]-порфина формулы:
Изобретение позволяет получить никелевый комплекс, проявляющий свойство стационарной фазы для газовой хроматографии. 1 табл.
Реферат
Изобретение относится к химической промышленности, а именно к получению металлокомплексов порфирина, в частности к никелевому комплексу 5,10,15,20-тетракис[3′,5′-ди-(2′′-метилбутилокси)фенил]-порфина, который может быть использован как дихроичный краситель для жидкокристаллических материалов, термостабилизатор полимерных композиций, модификатор полимерных мембран, а также в качестве стационарной фазы для газовой хроматографии.
Уровень техники
Среди современных физико-химических методов анализа газовая хроматография является наиболее доступной, производительной и позволяющей разделять близкокипящие структурные изомеры производных бензола, полициклических ароматических углеводородов, стероидов, гербицидов и т.д.
Успехи газовой хроматографии по разделению структурных изомеров связаны, в основном, с использованием в качестве стационарных фаз термотропных жидких кристаллов, которые проявляют значительную селективность в аналитическом разделении различных веществ, более высокую по сравнению с обычными стационарными фазами [Вигдергауз М.С., Вигалок Р.В., Дмитриева Г.В. Хроматография в системе газ - жидкий кристалл // Успехи химии, 1981. Т. 50. С. 943-972]. Для эффективного разделения структурных изомеров с высокими температурами кипения, в частности изомеров диметилпиридина (лутидина), в качестве стационарных фаз применяют высокотемпературные жидкие кристаллы. Использование обычных неподвижных фаз, подобных кабельному маслу, полиэтиленгликолю и др. не позволяет осуществить полное разделение вышеупомянутых соединений [Sakagami S., Nakamiro M. // Bull. Chem. Soc. Jap., 1984. Vol 57. №7. P. l157-1158].
Использование в газовой хроматографии комплексов никеля, меди, палладия и платины основано на высоком селективном удерживании тех анализируемых веществ, которые могут быть координационно связаны в качестве лигандов. Комплексы металлов обладают высокой химической избирательностью, что обуславливает перспективность их использования в хроматографическом разделении [Wenzel T.J., Yarmaloff L.W., Cyr L.Y.S. Metal chelate polymers as selective sorbents for gas cromatography // J. Chromatogr., 1987. V. 396. Р. 51-64]. Сведения о проявлении селективных свойств по отношению к позиционным изомерам органических веществ, в том числе и с высокими температурами кипения, сорбентами, в которых в качестве стационарной фазы использовались бы производные порфирина и их металлокомплексы, в литературе отсутствуют. Это может быть связано со сложностью их синтеза, низким выходом целевых продуктов и ограниченной растворимостью в органических растворителях, что не позволяет нанести указанные стационарные фазы на твердый носитель.
Известна жидкокристаллическая стационарная фаза - 4-метокси-4′-этоксиазоксибензол [Егорова К.В., Беляев Н.В., Вигдергауз М.С. П,n′-метоксиэтоксиазоксибензол как предпочтительная жидкокристаллическая неподвижная фаза хроматографического фрагмента универсальной системы химического анализа // Изв. вузов. Химия и хим. технол., 1985. Т. 28. №6. С. 3]. Эта жидкокристаллическая стационарная фаза проявляет достаточную селективность по отношению к низкокипящим химическим веществам, в частности к п- и м-ксилолам (коэффициент селективности α для ксилолов 1, 13), но не может быть использована для разделения химических веществ с более высокими температурами кипения, в частности 3,4- и 3,5-лутидинов.
Известна жидкокристаллическая стационарная фаза - 4-бутилокси-4′-формилазобензол [XVI Международная конференция по химической термодинамике в России; X Международная конференция по проблемам сольватации и комлексообразования в растворах. Суздаль, 1-6 июля, 2007 г., т II, 4S-500. Кувшинова С.А., Бурмистров В.Α., Блохина C.B., Шарапова А.В., Фокин Д.С, Койфман О.И. Влияние ассоциативного состояния полярных мезогенов на их мезоморфизм и структурную селективность]. Однако эта жидкокристаллическая стационарная фаза проявляет низкую структурную селективность по отношению к высококипящим изомерам, в частности к 3,4- и 3,5-лутидинам (α = 1,27).
Известна жидкокристаллическая стационарная фаза - 4-цианофениловый эфир 4[4′-(2-гидроксиэтилокси)фенилазо]коричной кислоты [Патент РФ №2323208, опубл. 27.04.2008]. Однако эта жидкокристаллическая стационарная фаза проявляет низкую структурную селективность по отношению к высококипящим изомерам, в частности к 3,4- и 3,5-лутидинам (α = 1,30).
Известна жидкокристаллическая стационарная фаза - 4-(4-цианофенил)-4′-(4-гидроксигексилокси)-бензилиденанилин [Патент РФ №2339616, опубл. 27.11.2008]. Однако эта жидкокристаллическая стационарная фаза проявляет низкую структурную селективность по отношению к высококипящим изомерам, в частности к 3,4- и 3,5-лутидинам (α = 1,40).
Известна жидкокристаллическая стационарная фаза - бис(4-децилоксифенилоксикарбонил)салицилаль-N-додецилимин]атомедь [Крестов А.Г., Блохина C.B., Галяметдинов Ю.Г., Ольхович М.В., Лоханов В.В. Сорбент на основе мезоморфного комплекса меди в газовой хроматографии органических соединений // Ж. физ. химии, 1993. Т. 67. №1. С.151-154]. Однако эта жидкокристаллическая стационарная фаза проявляет низкую структурную селективность по отношению к высококипящим изомерам, в частности к 3,4- и 3,5-лутидинам (α = 1,30).
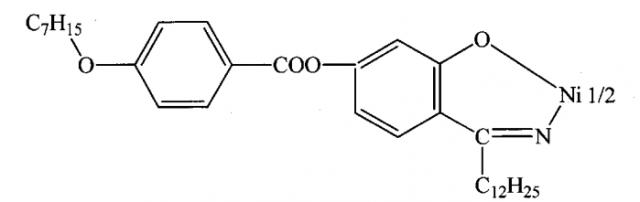
Наиболее близким структурным аналогом заявленного соединения является бис(4-гептилоксифенилоксикабонил)салицилаль-N-додецилимин]атоникель [Ольхович М.В. Автореферат дисс. ... к.х.н., Иваново, 2000 г.] следующей формулы:
Это вещество проявляет жидкокристаллические свойства в интервале от 130,2 до 138,5°C, обладает способностью к разделению высококипящих позиционных изомеров, в частности 3,5- и 3,4-лутидинов, и может быть использовано в качестве жидкокристаллической стационарной фазы в газовой хроматографии для анализа смесей органических соединений.
Основными недостатками этого соединения являются:
- низкая структурная селективность (α) по отношению к высококипящим изомерам органических соединений, например, для 3,5- и 3,4-лутидинов она составляет 1,30;
- чрезвычайно узкий рабочий интервал, который определяется температурным интервалом существования мезофазы - 8,3°С;
- чрезвычайно низкая селективность разделения других изомеров лутидина - не выше 1,05.
Сущность изобретения
Изобретательской задачей является поиск нового никелевого комплекса, который проявлял бы более высокую структурную селективность по отношению ко всем изомерам лутидина и работал бы в широком интервале температур.
Поставленная задача решена никелевым комплексом 5,10,15,20-тетракис[3′,5′-ди-(2′′-метилбутилокси)фенил]-порфина формулы:
Структура заявленного соединения доказана методами электронной спектроскопии и ЯМР 1H.
В электронном спектре никелевого комплекса 5,10,15,20-тетракис[3′,5′-ди-(2′′-метилбутилокси)фенил]-порфина в хлороформе наблюдаются следующие характерные полосы поглощения (приведены максимумы поглощения в нм, (коэффициенты экстинкции ε·10-3/lgε)): 529 (22,5/4,35); 418 (300,7/5,48).
В спектре ЯМР 1H никелевого комплекса 5,10,15,20-тетракис[3′,5′-ди-(2′′-метилбутилокси)фенил]-порфина в хлороформе-Д наблюдаются резонансные сигналы следующих протонов (приведены химические сдвиги в м.д. относительно ТМС): 8,88s (8Н, β-H); 7,22d (8Н, 2′,6′-Н); 6,94t (4Н, 4′-Н); 3,95dd (8Н, ОСН); 3,86dd (8Н, ОСН′); 1,94sc (8Н, С*Н); 1,62sp (8Н, СН2); 1,30sp (8Н, СН2′); 1,05d (24Н, СН3); 1,00t (24H, Et-CH3).
Заявленное соединение позволяет получить следующие преимущества.
- более высокая структурная селективность (α) по отношению к 3,5- и 3,4-лутидинам - 1,43;
- значительно более широкий рабочий интервал температур - от 20°С до 350°С;
- значительно более высокая селективность разделения всех других изомеров лутидина.
К тому же изобретение обладает следующими дополнительными преимуществами:
- выход в процессе синтеза составляет 91%, что позволяет получать заявленное соединение в количествах, достаточных для проведения газохроматографического эксперимента;
- хорошая растворимость в органических растворителях, что позволяет качественно наносить его на твердый носитель.
Сведения, подтверждающие возможность воспроизведения изобретения
Для синтеза никелевого комплекса 5,10,15,20-тетракис [3′,5′-ди-(2′′-метилбутилокси)фенил]-порфина используют следующие вещества:
1. Хлористый метилен ТУ 2631-019-44493179-98 с изм. 1, 2, 3
2. Бензол ГОСТ 5955-75 с изм. 1, 2
3. n-Ксилол ТУ 2631-103-44493179-06
4. Метанол ГОСТ 2222-95
5. Диметилформамид ТУ 6-09-3720-79
6. Трифторуксусная кислота ТУ 6-09-3877-80
7. Диэтаноламин ТУ 6-09-2652-91
8. Эфират трифторида бора ТУ 60-09-804-71
9. Трибромид бора ТУ 6-09-5304-86
10. n-Хлоранил ТУ 6-09-15-70
11. Пиррол ТУ 6-09-3255-78
12. 3,5-Диметоксибензальдегид SIGMA-ALDRICH
13. 1-Бром-2-метилбутан SIGMA-ALDRICH
14. Ацетилацетонат никеля SIGMA-ALDRICH
15. Силикагель для хроматографии MACHEREY-NAGEL, Germany
16. Алюминия оксид для хроматографии ТУ 6-09-3916-75
17. Гидроксид калия ГОСТ 24363-80
18. Уксусная кислота ГОСТ 19814-74
19. Поташ ГОСТ 4221-87
Заявленное соединение получают следующим образом:
Стадия 1. К кипящему раствору 5,0 мл трифторуксусной к-ты в 300 мл n-ксилола постепенно прибавляют раствор 5,0 мл (0,072 моль) пиррола и 12,0 г (0,072 моль) 3,5-диметоксибензальдегида в 50 мл n-ксилола (30 мин), затем кипятят 1 ч и отгоняют ксилол с водяным паром, а остаток отфильтровывают, промывают водой и высушивают. Остаток растворяют в бензоле и хроматографируют на оксиде алюминия II степени активности по Брокману хлористым метиленом, собирают порфириновую фракцию, которую упаривают, растворяют в бензоле и хроматографируют повторно на силикагеле, элюируют бензолом, затем перекристаллизовывают из смеси с метанолом. Выход - 2,78 г (18,1%)
К раствору 1,7 г (10,0 ммоль) 3,5-диметоксибензальдегида и 0,7 мл (10,0 ммоль) пиррола в 1000 мл хлористого метилена (содержащего ~0,4% этанола) прибавляют 0,4 мл (3,2 ммоль) эфирата трифторида бора в атмосфере аргона. Смесь перемешивают 2,0 ч, прибавляют 1,8 г (7,32 ммоль) n-хлоранила и перемешивают дополнительно 2,5 ч, добавляют 1,0 мл (10,4 ммоль) диэтаноламина и отгоняют хлористый метилен, остаток промывают раствором гидроксида калия, отфильтровывают, помывают водой и высушивают на воздухе при 70°С. Выход 0,6 г (28,1%). Получили тетракис(3,5-диметоксифенил)порфин.
Стадия 2. 1,0 г (1,17 ммоль) тетракис(3,5-диметоксифенил)порфина растворяют в 30 мл осушенного хлористого метилена, затем при перемешивании и охлаждении до 0°С добавляют раствор 1,5 мл (15,9 ммоль) трибромида бора в 15 мл хлористого метилена. Затем смесь перемешивают 12 ч при комнатной температуре и при охлаждении добавляют 5 мл метанола и перемешивают 1,0 ч, затем добавляют смесь 5 мл конц. раствора аммиака и 50 мл воды и перемешивают еще 0,5 ч, добавляют уксусную кислоту до слабокислой реакции и отгоняют органические растворители на ротационном испарителе. Осадок отфильтровывают, промывают водой и высушивают на воздухе при 70°С. Выход 0,85 г (98%). Получили 5,10,15,20-тетракис(3′, 5′-диоксифенил)порфин.
Стадия 3. К раствору 0,4 г (0,54 ммоль) 5,10,15,20-тетракис(3′,5′-диоксифенил)порфина и 1,0 мл (8,3 ммоль) 1-бром-2-метилбутана в 20 мл осушенного ДМФА прибавляют 2,0 г измельченного поташа и смесь перемешивают при комнатной температуре 48 ч (контроль за прохождением реакции по ТСХ), затем смесь выливают в 100 мл воды, кипят 3 ч, охлаждают, отфильтровывают осадок, промывают водой, высушивают на воздухе, растворяют в хлористом метилене и хроматографируют на оксиде алюминия II степени активности по Брокману, элюируют хлористым метиленом и собирают первую зону порфирина. Элюат упаривают и продукт осаждают метанолом. Выход 0,58 г (83,0%). Получили 5,10,15,20-тетракис[3′,5′-ди-(2′′-метилбутилокси)фенил]порфин.
Стадия 4. Кипятят 3,0 ч раствор 0,5 г (0,38 ммоль) 5,10,15,20-тетракис[3′,5′-ди-(2′′-метилбутилокси)фенил]порфина и 1,0 г (3,90 ммоль) ацетилацетоната никеля в 30 мл ДМФА, затем массу выливают в воду, отфильтровывают осадок, промывают водой и высушивают при 70°С на воздухе, растворяют в хлористом метилене, хроматографируют на оксиде алюминия II степени активности по Брокману, порфириновую зону упаривают и осаждают метанолом. Получают целевой продукт - никелевый комплекс 5,10,15,20-тетракис[3′,5′-ди-(2′′-метилбутилокси)фенил]-порфина. Выход 0,47 г (91,0%), Тпл = 73-80°С.
Использование заявленного соединения в качестве стационарной фазы в газовой хроматографии для разделения позиционных изомеров лутидина иллюстрируется следующим примером.
Навеску никелевого комплекса 5,10,15,20-тетракис[3′,5′-ди-(2′′-метилбутилокси)фенил]-порфина в количестве 0,408 г растворяют в 30 мл хлороформа марки ХЧ. Полученный раствор добавляют к 4,08 г твердого носителя марки Хроматон N-AW (0,125-0,16 мм) и нагревают на водяной бане при перемешивании до полного испарения растворителя. Для удаления следов хлороформа проводят сушку в течение 12 часов в вакууме при 100°С и остаточном давлении 2 мм рт. ст. Далее насадку, представляющую собой твердый носитель с нанесенной на него стационарной фазой, помещают в колонку из нержавеющей стали (1000×3 мм) и кондиционируют 6 ч в потоке гелия при 100°С. Количество неподвижной фазы составляет 10% от массы насадки.
Времена удерживания сорбатов измеряют на газовом хроматографе Shimadzu GC-2014 (Япония) с пламенно-ионизационным детектором при чувствительности, обеспечивающей регистрацию ионизационного тока 3.2·10-10 А. Измерения проводят в изотермическом режиме в интервале температур 20-350°С. Точность термостатирования 0.1°С. Температуры испарителя и детектора устанавливают на 20°С выше температуры колонки. В качестве газа-носителя используют гелий с содержанием основного вещества 99.99%. Расход гелия поддерживают в пределах 30-60 мл/мин, измеряя его пенным расходомером. Замеры расхода выполняют при каждой температуре опыта по окончании определения времени удерживания сорбата. Для того, чтобы условия эксперимента соответствовали предельному разбавлению, а концентрация сорбата - линейному участку изотермы растворения, в колонку вводят малые - не более 0.1 мкл - объемы сорбатов. Применяют шприц объемом 10 мкл (Shimadzu, Австралия). «Мертвое» время удерживания определяют по пропану. Времена удерживания регистрируют автоматически с погрешностью не более 0.01 с. Это позволяет измерять времена удерживания соединений в пяти параллельных опытах с отклонением от среднестатистического значения не более 0.5%.
Коэффициент селективности по Херингтону определяют как частное от деления времен удерживания различных изомеров лутидина с учетом мертвого времени удерживания. Рассчитывают средний коэффициент селективности из пяти измерений.
Испытание жидкокристаллической стационарной фазы на основе соединения-прототипа - бис(4-гептилоксифенилоксикабонил)салицилальN-додецилимин]атоникель проводили аналогично испытанию заявленного соединения.
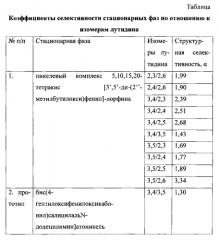
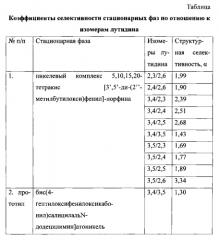
В таблице приведены коэффициенты селективности стационарных фаз на основе никелевого комплекса 5,10,15,20-тетракис[3′,5′-ди-(2′′-метилбутилокси)фенил]-порфина и бис(4-гептилоксифенилоксикабонил)салицилальN-додецилимин]атоникеля по отношению к изомерам лутидина.
Данные таблицы с очевидностью подтверждают, что заявленное соединение проявляет более высокую структурную селективность по отношению к 3,5- и 3,4-лутидинам и позволяет эффективно разделять другие позиционные изомеры лутидина, что делает возможным его использование в качестве стационарной фазы для газовой хроматографии в процессах количественного анализа смесей органических соединений.
Никелевый комплекс 5,10,15,20-тетракис [3′,5′-ди-(2″-метилбутилокси)фенил]-порфина формулы: проявляющий свойство стационарной фазы для газовой хроматографии.