Способ восстановления дефектов гиалинового хряща суставных поверхностей суставов конечностей
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к травматологии и ортопедии, и может быть использовано при лечении полнослойных локальных остеохондральных дефектов суставов. Для этого проводят артроскопию крупного сустава, определяют локализацию и размер остеохондрального или хондрального дефекта, удаляют свободный фрагмент и выполняют абразивную хондропластику и микрофрактуринг. Для восстановления дефектов гиалинового хряща в зону дефекта хрящевой ткани вводят смесь клеток стромальной сосудистой фракции (ССФ) одновременно с фибриновым клеем с использованием системы дуплоджект. После проведения артротомии пораженный сустав выдерживают 5 минут, после чего выполняют 8-10 циклов пассивных сгибательно-разгибательных движений. В менее крупные суставы - голеностопный или локтевой - вводят клетки ССФ под контролем электронно-оптического преобразователя без вскрытия сустава под анестезией. Изобретение позволяет проводить восстановление дефектов гиалинового хряща суставных поверхностей смесью клеток стромальной сосудистой фракции в сжатые сроки и без нанесения дополнительной травмы. 1 з.п. ф-лы, 7 ил., 1 пр.
Реферат
Изобретение относится к медицине, а именно к травматологии и ортопедии, и может быть использовано при лечении полнослойных локальных остеохондральных дефектов суставов.
Известен ряд способов лечения полнослойных локальных остеохондральных дефектов суставов. Наиболее распространенным способом лечения пациентов с данной патологией является хирургическое вмешательство, которое проводится после эндоскопического обследования сустава - артроскопии, при которой определяется размер дефекта хряща и возможность фиксации его фрагмента. Так фиксация фрагмента хряща возможна лишь при свежих травмах до 3 недель и наличии остеохондрального фрагмента. В остальных случаях производится удаление хрящевого фрагмента, выполняется абразивная хондропластика с формированием стабильных краев хрящевого дефекта с помощью кюретки и, по возможности, микрофрактуринг зоны дефекта, рассчитанные на индукцию образования фиброзного хряща [1].
Известно, что хрящевая ткань обладает крайне низким репаративным потенциалом, поэтому, чаще всего, разрушенный хрящ если и восстанавливается, то с образованием фиброзной, волокнистой хрящевой ткани, существенно отличающейся по структуре, биохимическому составу матрикса и по механическим свойствам. В дальнейшем это ведет к развитию деформирующего остеоартроза с болевым синдромом и контрактурой. Поиск биотехнологических способов восстановления полнослойных дефектов гиалинового хряща направлен на выбор оптимального источника клеток-предшественников и способа их доставки в область повреждения, выбор адекватного носителя и способа фиксации.
Известны способы лечения дефектов суставного хряща инъекцией эмбриональной ткани [2]. Недостатками данных способов являются риски, связанные с применением аллогеной ткани - возможным отторжением, инфекцией, существуют и проблемы с наличием донорского материала.
Известен способ имплантации аутологичных хондроцитов (ACI), культивированных in vitro, затем пересаженных в зону дефекта и закрепленных с помощью надкостницы, или искусственной мембраны. К недостаткам данного способа относятся: длительные сроки получения культуры клеток (порядка 3 недель), расширение хирургической агрессии при заборе надкостницы, кроме того, искусственная мембрана является чужеродным материалом, высока и стоимость такого лечения [3].
В настоящее время не вызывает сомнения тот факт, что источником эмбрионального развития хрящевых тканей является мезенхима, в составе которой ведущую роль играют полипотентные мезенхимные стволовые клетки. Мезенхимным стволовым клеткам посвящен ряд исследований, из которых следует, что потомками этой клеточной популяции во взрослом организме человека являются мультипотентные мезенхимальные стромальные клетки костного мозга. Они отличаются от стволовых кроветворных клеток, так как не экспрессируют антигены гемопоэтических клеток - CD34, CD14, CD45. Часть мультипотентных мезенхимальных стромальных клеток, при определенных условиях (соответствующее микроокружение, цитокиновое влияние, действие факторов роста и пр.), способна дифференцироваться по хондробластическому пути в хондрогенные клетки - прехондробласты, хондробласты, хондроциты [4, 5].
Рядом исследователей показано, что клетки стромально-васкулярного фенотипа, полученные из жировой ткани, могут являться источником клеток-предшественников хрящевой ткани. Стромальные клетки жировой ткани представляют собой популяцию клеток, обладающих высокой степенью пластичности и высокой интенсивностью пролиферации [6, 7].
Наиболее близким заявляемому способу, по своему техническому решению, является предложенный Стадниковым А.А. и др. способ восстановления дефектов гиалинового хряща коленного суставова, включающий введение меземхимальных стволовых клеток, полученных липосакцией подкожно-жировой клетчатки из различных тканей с последующей ферментной обработкой, после проведения абразивной хондроплатики и микрофрактуринга методом артроскопии [8]. В данном способе речь идет только о восстановлении коленного сустава.
Сущность изобретения состоит в совокупности существенных признаков, достаточной для достижения искомого технического результата, который заключается в создании способа восстановления дефектов гиалинового хряща суставных поверхностей суставов конечностей смесью клеток стромальной сосудистой фракции (ССФ), полученных в достаточных количествах в сжатые сроки, за счет точной доставки ее к зоне дефекта и надежного крепления.
Сущность изобретения состоит в том, что способ восстановления дефектов гиалинового хряща суставных поверхностей суставов конечностей включает введение в сустав стромальных клеток без нанесения дополнительной травмы. Введение клеток ССФ производят после эндоскопического обследования - артроскопии сустава, определения локализации и размера остеохондрального или хондрального дефекта, удаления свободного фрагмента и выполнения абразивной хондропластики, микрофрактуринга. Под местной анестезией или наркозом производят липосакцию жировой клетчатки из области передней брюшной стенки, и/или ягодичной области, и/или наружной поверхности бедер, осуществляют забор аутологичной жировой ткани, из которой получают клетки ССФ. Для крупных суставов проводят артротомию пораженного сустава, полученные клетки ССФ вводят точно в область дефекта хрящевой ткани одновременно с фибриновым клеем, используя систему дуплоджект, выдерживают 5 минут, после чего выполняют 8-10 циклов пассивных сгибательно-разгибательных движений. Рану послойно ушивают.
В менее крупные суставы - голеностопный, локтевой, возможно инъекционное введение клеток ССФ без вскрытия сустава под контролем электронно-оптического преобразователя под местной или общей анестезией.
Артроскопия сустава позволяет визуально выявить остеохондральный или хондральный дефект, определить его локализацию, размер и глубину поражения.
Удаление свободного фрагмента и выполнение абразивной хондропластики и микрофрактуринга необходимо для подготовки поверхности сустава к имшантации клеток ССФ.
Жировая ткань пациента является богатым источником аутологичного материала, что предотвращает риск имуннологического отторжения и позволяет получить в сжатые сроки большое количество клеток. Клетки ССФ, полученные из аутологичной жировой ткани, подвергнутой ферментной обработке, содержат мезенхимные стволовые клетки, эндотелиальные предшественники, М2 поляризированные макрофаги и Т-лимфоциты, которые служат источником регенерации и закрытия дефекта хряща.
Использование неэмбриональных клеток стромально-васкулярного фенотипа исключает риск развития необластических процессов.
Проведение артротомии пораженного сустава для крупных суставов обеспечивает доступ к поврежденному участку хряща.
Введение клеток ССФ точно в область дефекта хрящевой ткани обеспечивает условия для полноценной ее регенерации, одновременное введение клеток ССФ с фибриновым клеем позволяет создать благоприятные условия для прикрепления, выживания и дифференцировки трансплантируемых клеток, а также предотвращает их неконтролируемую миграцию, применение системы дуплоджект обеспечивает одновременное введение клеток ССФ и фибринового клея.
Выдержка сустава в течение 5 минут после нанесения клеток и фибринового клея обеспечивает фиксацию клеток ССФ в области дефекта хрящевой ткани, что соответствует инструкции по применению клея.
Выполнение 8-10 циклов пассивных сгабательно-разгибательньк движений в суставе необходимо для контроля крепления клеток ССФ.
Применение инъекционного введения клеток ССФ без вскрытая сустава под контролем электронно-оптического преобразователя для менее крупных суставов - голеностопного, локтевого, возможно в связи с малыми размерами суставной полости.
Предложенный способ не требует длительного выращивания клеток in vitro, что сокращает сроки лечения.
Способ поясняют приведенные иллюстрации, где:
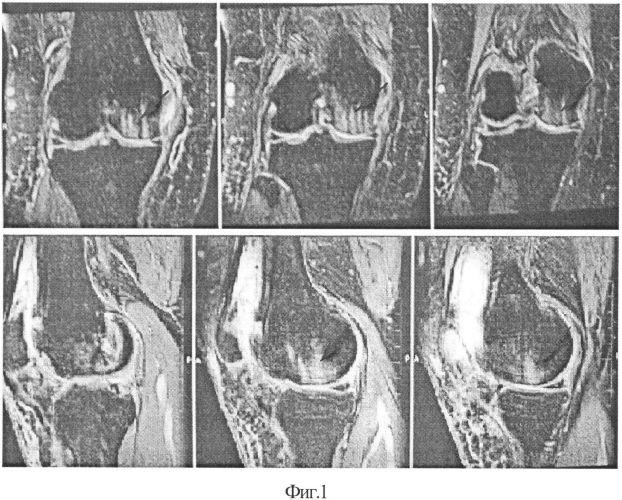
На фиг.1 приведена МРТ правого коленного сустава пациентки М. при поступлении;
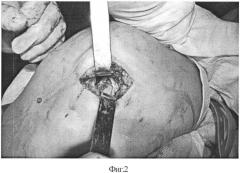
На фиг.2 - снимок в момент проведения артротомии;
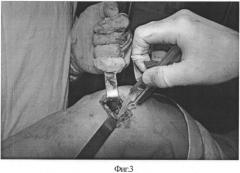
На фиг.3 - проведение имплантации клеток ССФ с фиксацией клеем тиссукол-кит на этапе операции;
На фиг.4, фиг.5 - вид конечности в ранний послеоперационный период;
На фиг.6 - МРТ пациентки М. на сроке 5 месяцев после операции;
На фиг.7 - конечность пациентки М. во время осмотра на сроке 2 года после операции.
Способ осуществляют следующим образом.
Выполняют эндоскопическое обследование (артроскопию) сустава пациента с целью определения локализации и размера остеохондрального или хондрального дефекта, удаляют свободный фрагмент и выполняют абразивную хондропластику и, по возможности, микрофрактуринг. Под местной анестезией или наркозом производят липосакцию жировой клетчатки из области передней брюшной стенки, и/или ягодичной области, и/или наружной поверхности бедер. Осуществляют забор аутологичной жировой ткани, проводят ее ферментную обработку для получения клеток ССФ.
Процедуру введения клеток проводят в условиях операционной под анестезией. Производят артротомию пораженного сустава, для чего иглу системы дуплоджект подводят точно в область дефекта хрящевой ткани, и осуществляют одновременное введение клеток ССФ и фибринового клея. Выдерживают время полимеризации фибринового клея 5 минут, после чего выполняют 8-10 циклов пассивных сгабательно-разгибательньк движений. Рану послойно ушивают.
Процедура введения для менее крупных суставов - голеностопного, локтевого, может предусматривать применение инъекционного введения клеток ССФ без вскрытая сустава под контролем электронно-оптического преобразователя под местной или общей анестезией. Клетки вводят точно в область дефекта хрящевой ткани одновременно с фибриновым клеем, для чего под контролем электронно-оптического преобразователя, используя систему дуплоджект, в условиях операционной под местной или общей анестезией путем инъекции в область дефекта хрящевой ткани, производят одновременное введение клеток ССФ и фибринового клея. Выдерживают время полимеризации фибринового клея 5 минут, после чего выполняют 8-10 циклов пассивных сгибательно-разгибательных движений.
В последующем пациенту рекомендуют 1 месяц ходьбы с костылями, без нагрузки на оперированную ногу, затем - дозированная, постепенная нагрузка. Проводят стандартное восстановительное лечение (физиолечение, ЛФК, массаж). На сроке 4-6 месяцев результат лечения оценивают по данным физикального обследования, рентгенографии, МРТ.
Клинический пример
Пациентка М, 50 лет, поступила в отделение ортопедии ГАУЗ «РКБ МЗ РТ» 08.06.11 с диагнозом «Правосторонний гонартроз 2 ст. с болевым синдромом с поражением медиального отдела». Больна около 3 лет. Лечилась консервативно. С марта 2011 г. выраженное ухудшение в виде усиления болевого синдрома. Консервативное лечение малоэффективно. По данным МРТ: дегенеративные изменения обоих менисков, субхондральный отек медиального мыщелка бедренной кости, синовит (фиг.1). 09.06.11 выполнена операция: артроскопия правого коленного сустава. Выявлена локальная хондромаляция медиального мыщелка бедренной кости 4 ст. диаметром 2,0×2,0 см. Произведена абразивная хондропластика, остеоперфорация. Больной предложена хондропластика аутологичными клетками ССФ. Получено согласие. 09.06.11 из передней стенки живота методом липосакции произведен забор жировой ткани объемом 300 мл. В лабораторных условиях выделено 5 млн клеток стромальной васкулярной фракции. 10.06.11 (на следующий день) произведена артротомия (фиг. 2), имгшантация 5 млн клеток ССФ с фиксацией клеем тиссукол-кит (фиг. 3), с использованием системы дуплоджект, с выдержкой после нанесения 5 минут, выполнены 8-10 циклов пассивных сгибательно-разгибательных движений. Рана послойно ушита.
Ранний послеоперационный период без особенностей (фиг.4, 5). Рекомендована ходьба с костылями без нагрузки на оперированную конечность и сгибание до 90 градусов - 4 недели, с 5 по 8 неделю - нагрузка до 50% веса, объем движений до 120 градусов. На сроке 5 месяцев после операции произведена повторная МРТ: отмечено, практически, полное спадение субхондрального отека, незначительный синовит (фиг. 6). Болевой синдром купирован. Сгибание в коленном суставе 130 градусов. Пациентка осмотрена на сроке 1 и 2 года после операции (фиг. 7): болевой синдром возникает лишь при значительной нагрузке и носит временный характер. Трудоспособность восстановлена.
Источники информации
1. Штробель М. Руководство по артроскопической хирургии: в 2 томах / М. Штробель // - М. - 2011. - Т. 2. - 344 с.
2. Печенюк В.И.; Рунович А.А.; Сухих Г.Т.; Житницкий Р.Е.; Курильская Т.Е.; Никифоров С.Б. патент RU (11) 2195940 (13) С2.
Дата публикации: 2003.01.10, регистрационный номер заявки: 2000116568/14, дата подачи заявки: 2000.06.28, дата начала отсчета срока действия патента: 2000.0628, дата публикации заявки: 2002.06.27, опубликовано: 2003.01.10) + (патент ФРГ 341063).
3. Brittberg, М. Treatment of deep cartilage defects in the knee with autologous chondrocyte transplantation / M. Brittberg, A. Lindahl, A Nilsson et al. / / N. Engl. J. Med. - 1994. - Vol. 331, №14. - P. 889-895.
4. Мазуров B.M. Болезни суставов, 2008, 397 c. Спецлит.
5. Caplan A.I. Mesenchymal stem cells: building blocks for molecular medicine in the 21st century / A1 Caplan, S.P. Bruder / / TRENDS in Mol. Med - 2001. - Vol. 7, №6, P. 259-264.
6. Трактуев Д.О. Стромальные клетки жировой ткани - пластический тип клеток, обладающий высоким терапевтическим потенциалом / Д.О. Трактуев, Е.Б. Парфенова, В.А. Ткачук, К.Л. Марч // Цитология. - 2006. - Т. 48, №2 - с. 83-93.
7. Lin Y. Molecular and cellular characterization during chondrogenic Differentiation of adipose tissue-derived stromal cells in vitro and cartilage formation in vitro / Y. Lin, E. Luo, X Chen at all //J. Cell Mol. Med. - 2005. - Vol .9, №4 - P. 929-939.
8. Стадников A.A. и др. Новые методы лечения дефектов гиалинового хряща коленного сустава у больных гонантрозом, Научно-практическая ревматология, 2009, №3, с. 1-5.
1. Способ восстановления дефектов гиалинового хряща суставных поверхностей суставов конечностей, включающий артроскопию сустава, определение локализации и размера остеохондрального или хондрального дефекта, удаление свободного фрагмента и выполнение абразивной хондропластики, микрофрактуринга, восстановление дефектов гиалинового хряща с применением мезенхимных стволовых клеток введением клеточного материала в область дефекта хрящевой ткани одновременно с фибриновым клеем с использованием системы дуплоджект в крупные суставы, после проведения артротомии пораженного сустава выдерживание 5 минут, выполнение 8-10 циклов пассивных сгибательно-разгибательных движений в суставе, отличающийся тем, что в зону дефекта хряща вводят смесь клеток стромальной сосудистой фракции (ССФ).
2. Способ по п. 1, отличающийся тем, что в менее крупные суставы - голеностопный, локтевой, применяют инъекционное введение смеси клеток ССФ без вскрытия сустава под контролем электронно-оптического преобразователя под местной или общей анестезией.