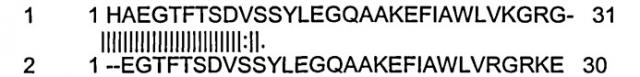Дважды ацилированные производные glp-1
Иллюстрации
Показать всеИзобретение относится к области биотехнологии, конкретно к производным аналога GLP-1, и может быть использовано в медицине. Синтезируют соединение, обладающее активностью GLP-1 и являющееся производным аналога GLP-1, где аналог имеет первый остаток K37 в позиции, соответствующей позиции 37 GLP-1 (7-37) (SEQ ID №1), второй остаток K26 в позиции, соответствующей позиции 26 GLP-1 (7-37), а также не более четырех аминокислотных модификаций по сравнению с GLP-1 (7-37), включая K37 и Q или R в позиции, соответствующей позиции 34 в GLP-1 (7-37). При этом производное имеет пролонгирующую группировку, присоединенную через линкер к каждой из эпсилон-аминогрупп K26 и K37, соответственно, где пролонгирующая группировка имеет формулу Соединения 2а, и линкер содержит Соединение 6 и/или Соединение 5. Изобретение позволяет получить лекарственное средство для перорального введения, эффективное в лечении или профилактике сахарного диабета и заболеваний, связанных с сахарным диабетом, а также способное улучшить параметры липидного обмена и функционирование бета-клеток и отсрочить или предотвратить прогрессирование диабетического заболевания. 3 н. и 9 з.п. ф-лы, 58 пр.
Реферат
Область изобретения
Изобретение относится к производным глюкагон-подобного пептида 1 (GLP-1) и к его применению в фармацевтических целях, а именно к дважды ацилированным производным GLP-1, ацилированным в позициях 26 и 37, а также к их применению в фармацевтических целях.
Включение списка последовательностей посредством ссылки
Список последовательностей, озаглавленный как «Список последовательностей», является 584-байтным, созданным 17 ноября 2010 и включенным в данный документе посредством ссылки.
Уровень техники
Journal of Medicinal Chemistry (2000), vol. 43, no. 9, p.1664-669 раскрывает производные GLP-1(7-37), которые дважды ацилированы на K26,34 - см. Таблицу 1.
WO 98/08871 раскрывает ряд производных GLP-1, включая некоторые дважды ацилированные на K26,34, см. примеры 3, 7, 17, 24, 32, 33 и 36. Лираглутид, моноацилированное производное GLP-1 для введения один раз в день, которое выпущено на рынок в 2009 году Novo Nordisk A/S, также описано в WO 98/08871 (Пример 37).
WO 99/43706 раскрывает ряд моноацилированных и дважды ацилированных производных GLP-1, в том числе некоторые производные K26,37 (см. с.148-178).
WO 2005/027978 раскрывает ряд производных GLP-1, включая некоторые дважды ацилированные на одном и том же остатке, K37, см. Примеры 8 и 9.
WO 2009/030738 раскрывает ряд производных GLP-1, в том числе один дважды ацилированный на K31, Dap34, см. Пример 37.
Journal of Controlled Release (2010), vol. 144, p.10-16 предусматривает ацилированные аналоги эксендина-4 и раскрывает, в частности, дважды ацилированный эксендин-4 (K12,27-diLUA-Exendin-4) (LUA представляет собой лауриновую кислоту, С12).
WO 06/097537 раскрывает ряд производных GLP-1, включая семаглутид (Пример 4), моноацилированное производное GLP-1 для введения раз в неделю, который находится в стадии разработки в Novo Nordisk A/S.
Angewandte Chemie International Edition 2008, vol. 47, p.3196-3201 докладывает об открытии и описании класса производных 4-(p-йодофенил)масляной кислоты, которые предположительно демонстрируют стабильное нековалентное связывающее взаимодействие и с мышиным сывороточным альбумином (MSA), и с человеческим сывороточным альбумином (HSA).
Сущность изобретения
Изобретение относится к производным пептидов GLP-1.
Производные ацилированы на нативном лизине в позиции 26, а также на лизине, заменяющем нативный глицин в позиции 37. Боковые цепи являются альбумин-связывающими группировками. Они включают пролонгирующую группировку, предпочтительно выбранную среди двухосновных жирных кислот и жирных кислот с дистальной фенильной, фенокси- или тиофеновой группой, все могут быть замещенными. Карбоксильная группа жирной кислоты или двухосновной жирной кислоты ацилирована, возможно через линкер, на остатке лизина пептида GLP-1, предпочтительно на его эпсилон-аминогруппе. Пептид GLP-1 может быть аналогом GLP-1(7-37) (SEQ ID №1) с общим количеством до десяти различий аминокислот в сравнении с GLP-1(7-37), например, с одним или более чем одним добавлением, одним или более чем одним удалением, и/или одной или более чем одной заменой.
Более конкретно, изобретение относится к производному аналога GLP-1, который содержит первый остаток K в позиции, соответствующей позиции 37 GLP-1(7-37) (SEQ ID №1), второй остаток K в позиции, соответствующей позиции 26 GLP-1(7-37), и максимум десять аминокислотных модификаций по сравнению с GLP-1(7-37), где первый остаток K обоназначен как K37, а второй остаток K обозначен как K26; где производное содержит две альбумин-связывающие группировки, присоединенные к K26 и K37, соответственно, где каждая альбумин-связывающая группировка включает пролонгирующую группировку, выбранную среди Соединения (далее Соед.) 1, Соед. 2, Соед. 3 и Соед. 4:
Соед. 1: НООС-(СН2)x-СО-*
Соед. 2: НООС-С6Н4-O-(СН2)y-СО-*
Соед. 3: R1-C6H4-(CH2)z-CO-*
Соед. 4: HOOC-C4SH2-(CH2)w-CO-*,
где x является целым числом в диапазоне 6-18, y является целым числом в диапазоне 3-17, z является целым числом в диапазоне 1-5, R1 представляет собой группу с молекулярной массой не более 150 Да, a w является целым числом в диапазоне 6-18; при условии, что когда пролонгирующая группировка представляет собой Соед. 1, альбумин-связывающая группировка дополнительно содержит линкер формулы Соед. 5:
Соед. 5:
где k является целым числом в диапазоне 1-5, и n является целым числом в диапазоне 1-5; или к его фармацевтически приемлемой соли, амиду или сложному эфиру.
Изобретение относится также к такому производному для применения в качестве лекарственного средства, в частности, для применения в лечении и/или профилактике всех форм сахарного диабета и связанных с ним заболеваний, таких как пищевые расстройства, сердечно-сосудистые заболевания, желудочно-кишечные заболевания, диабетические осложнения, критические заболевания и/или синдром поликистоза яичников; и/или для улучшения параметров липидного обмена, улучшения функционирования β-клеток и/или для отсрочки или предотвращения прогрессирования диабетического заболевания.
Изобретение относится также к промежуточным продуктам в форме пептидов GLP-1 и боковых цепей, которые являются релевантными для изготовления некоторых пептидов GLP-1 и производных изобретения.
Производные изобретения являются биологически активными. Помимо этого, либо в качестве альтернативы, они обладают пролонгирующим фармакокинетическим профилем. Помимо этого, либо в качестве альтернативы, они устойчивы к расщеплению желудочно-кишечными ферментами. Помимо этого, либо в качестве альтернативы, они обладают высокой биодоступностью. Эти свойства имеют важное значение в разработке следующего поколения соединений GLP-1 для подкожного, внутривенного и/или, в частности, перорального приема.
Подробное описание изобретения
Изобретение относится к производным пептидов GLP-1. Производные ацилированы на нативном лизине в позиции 26, а также на лизине, заменяющем нативный глицин в позиции 37. Боковые цепи являются альбумин-связывающими группировками. Они включают пролонгирующую группировку, предпочтительно выбранную среди двухосновных жирных кислот и жирных кислот с дистальной, или концевой, фенильной, тиофеновой или фенокси-группой, каждая из которых может быть замещенной. Карбоксильная группа жирной кислоты или двухосновной жирной кислоты ацилирована, возможно через линкер, на остатке лизина пептида GLP-1, предпочтительно на его эпсилон-аминогруппе. Пептид GLP-1 может быть аналогом GLP-1(7-37) (SEQ ID №1) с общим количеством до десяти различий аминокислот в сравнении с GLP-1(7-37), например, с одним или более чем одним добавлением, одним или более чем одним удалением, и/или одной или более чем одной заменой.
Более конкретно, в первом аспекте изобретение относится к производному аналога GLP-1, который содержит первый остаток K в позиции, соответствующей позиции 37 GLP-1(7-37) (SEQ ID №1), второй остаток K в позиции, соответствующей позиции 26 GLP-1(7-37), и максимум десять аминокислотных замен по сравнению с GLP-1(7-37), где первый остаток K обозначен как K37, а второй остаток K обозначен как K26, где производное содержит две альбумин-связывающие группировки, присоединенные к K26 и K37, соответственно, где каждая альбумин-связывающая группировка включает пролонгирующую группировку, выбранную среди Соед. 1, Соед. 2, Соед. 3 и Соед. 4:
Соед. 1: НООС-(СН2)x-СО-*
Соед. 2: НООС-С6Н4-O-(СН2)y-СО-*
Соед. 3: R1-C6H4-(CH2)z-CO-*
Соед. 4: HOOC-C4SH2-(CH2)w-CO-*,
где x является целым числом в диапазоне 6-18, y является целым числом в диапазоне 3-17, z является целым числом в диапазоне 1-5, R1 представляет собой группу с молекулярной массой не более 150 Да, a w является целым числом в диапазоне 6-18; при условии, что когда пролонгирующая группировка представляет собой Соед. 1, альбумин-связывающая группировка дополнительно содержит линкер формулы Соед. 5:
Соед. 5:
где k является целым числом в диапазоне 1-5, и n является целым числом в диапазоне 1-5; или к его фармацевтически приемлемой соли, амиду или сложному эфиру.
Таким образом, в первом аспекте изобретение относится к производному аналога GLP-1, который содержит первый остаток K в позиции, соответствующей позиции 37 GLP-1(7-37) (SEQ ID №1), второй остаток K в позиции, соответствующей позиции 26 GLP-1(7-37), и максимум десять аминокислотных замен по сравнению с GLP-1(7-37), где первый остаток K обозначен как K37, а второй остаток K обозначен как K26, где производное содержит две альбумин-связывающие группировки, присоединенные к K26 и K37, соответственно, где каждая альбумин-связывающая группировка включает пролонгирующую группировку, выбранную среди Соед. 1, Соед. 2, Соед. 3 и Соед. 4:
Соед. 2: НООС-С6Н4-O-(СН2)y-СО-*
Соед. 3: R1-C6H4-(CH2)z-CO-*
Соед. 4: HOOC-C4SH2-(CH2)w-CO-*,
где y является целым числом в диапазоне 3-17, z является целым числом в диапазоне 1-5, R1 представляет собой группу с молекулярной массой не более 150 Да, a w является целым числом в диапазоне 6-18; или к его фармацевтически приемлемой соли, амиду или сложному эфиру.
Во втором аспекте изобретение относится к производному аналога GLP-1, который содержит первый остаток K в позиции, соответствующей позиции 37 GLP-1(7-37) (SEQ ID №1), второй остаток K в позиции, соответствующей позиции 26 GLP-1(7-37), и максимум десять аминокислотных замен по сравнению с GLP-1(7-37), где первый остаток K обозначен как K37, а второй остаток K обозначен как K26, где производное содержит две альбумин-связывающие группировки, присоединенные к K26 и K37, соответственно, где альбумин-связывающая группировка включает i) пролонгирующую группировку формулы Соед. 1:
Соед. 1: НООС-(СН2)x-СО-*,
где x является целым числом в диапазоне 6-18; и ii) линкер формулы Соед. 5:
Соед. 5:
где k является целым числом в диапазоне 1-5, и n является целым числом в диапазоне 1-5;
или к его фармацевтически приемлемой соли, амиду или сложному эфиру.
В третьем аспекте изобретение относится к производному аналога GLP-1, который содержит первый остаток K в позиции, соответствующей позиции 37 GLP-1(7-37) (SEQ ID №1), второй остаток K в позиции, соответствующей позиции 26 GLP-1(7-37), и максимум десять аминокислотных замен по сравнению с GLP-1(7-37), где первый остаток K обозначен как K37, а второй остаток K обозначен как K26;
при этом производное содержит две пролонгирующие группировки, присоединенные к K26 и K37, соответственно, через линкер, где удлиняющая группировка выбрана среди Соед. 1, Соед. 2, Соед. 3 и Соед. 4:
Соед. 1: НООС-(СН2)x-СО-*
Соед. 2: НООС-С6Н4-O-(СН2)y-СО-*
Соед. 3: R1-C6H4-(CH2)z-CO-*
Соед. 4: HOOC-C4SH2-(CH2)w-CO-*,
где x является целым числом в диапазоне 6-18, y является целым числом в диапазоне 3-17, z является целым числом в диапазоне 1-5, R1 представляет собой группу с молекулярной массой не более 150 Да, a w является целым числом в диапазоне 6-18; и линкер содержит Соед. 5:
Соед. 5:
где k является целым числом в диапазоне 1-5, и n является целым числом в диапазоне 1-5; или к его фармацевтически приемлемой соли, амиду или сложному эфиру.
Изобретение также относится к промежуточному продукту в форме аналога GLP-1, который включает следующие изменения по сравнению с GLP-1(7-37) (SEQ ID №1): (i) (8Aib, 31H, 34Q, 37K), (ii) (des7-8, 34R, 37K, 38E), (iii) (des7-8, 34R, 37K), (iv) (8Aib, 9G, 34R, 37K), (v) (8Aib, 23R, 34R, 37K), (vi) (31H, 34Q, 37K), (vii) (9Q, 34R, 37K); (viii) (30Е, 34R, 37K), (ix) (34R, 37K, 38G), (х) (34R, 36G, 37K), или (xi) (34R, 37K, 38E), или к фармацевтически приемлемой соли, амиду или эфиру любого из его аналогов.
Изобретение также относится к промежуточному продукту, включающему пролонгирующую группировку, выбранную среди Соед. 2c, Соед. 3b и Соед. 4b:
Соед. 2c: НООС-С6Н4-O-(СН2)y-СО-PG
Соед. 3b: R1-C6H4-(CH2)z-CO-PG
Соед. 4b: HOOC-C4SH2-(CH2)w-CO-PG,
где y является целым числом в диапазоне 3-17, z является целым числом в диапазоне 1-5, R1 представляет собой группу с молекулярной массой не более 150 Да, а w является целым числом в диапазоне 6-18, и *-CO-PG является активированным эфиром; где, возможно, дистальная *-СООН-группа пролонгирующей группировки, если она присутствует, функционирует как нереактивный эфир; или к его фармацевтически приемлемой соли, амиду или сложному эфиру.
И, наконец, изобретение также относится к фармацевтическому применению аналогов и производных изобретения, в частности, к применению в лечении и/или профилактике всех форм сахарного диабета и связанных с ним заболеваний, таких как пищевые расстройства, сердечно-сосудистые заболевания, желудочно-кишечные заболевания, диабетические осложнения, критические заболевания и/или синдром поликистоза яичников; и/или для улучшения параметров липидного обмена, улучшения функционирования β-клеток и/или для отсрочки или предотвращения прогрессирования диабетического заболевания.
В дальнейшем, греческие буквы могут быть представлены их символами или соответствующим письменным именем, например: α = альфа, β = бета; ε = эпсилон, γ = гамма; ω = омега и т.д. Кроме того, греческая буква µ может быть обозначена "u", например, µl=ul, или µМ=uМ.
Звездочка (*) в химической формуле обозначает i) точку присоединения, ii) радикал и/или iii) неподеленный электрон.
Аналоги GLP-1
Термин «GLP-1-аналог» или «аналог GLP-1», используемый в данном документе, относится к пептиду, или соединению, представляющему собой вариант человеческого глюкагон-подобного пептида-1 (GLP-1(7-37)), последовательность которого включена в список последовательностей как SEQ ID №1. Пептид с последовательностью SEQ ID №1 также может быть обозначен как «нативный GLP-1».
В списке последовательностей первому аминокислотному остатку SEQ ID №1 (гистидину) присваивается №1. Тем не менее, в дальнейшем - в соответствии с установившейся практикой в данной области - это остаток гистидина называют №7, и последующие аминокислотные остатки пронумерованы соответственно, заканчивая глицином №37. Поэтому, как правило, в данном документе любая ссылка на номер аминокислотного остатка или номер позиции в последовательности GLP-1(7-37) является ссылкой на последовательность, начинающуюся с His в позиции 7 и заканчивающуюся Gly в позиции 37.
GLP-1-аналоги производных изобретения могут быть описаны посредством ссылки на i) номер аминокислотного остатка в нативном GLP-1(7-37), который соответствует аминокислотному остатку, который был модифицирован (например, соответствующей позиции в нативном GLP-1), и на ii) фактическую модификацию. Ниже приведены неограничивающие примеры подходящей номенклатуры аналогов.
Неограничивающий пример GLP-1-аналога производного изобретения является аналогом, который только изменен таким образом, что содержит первый остаток лизина в позиции, соответствующей позиции 37 GLP-1(7-37). Аминокислотная последовательность этого аналога в остальном идентична нативному GLP-1, и этот аналог может быть обозначен как K37-GLP-1(7-37). Это обозначение представляет аминокислотную последовательность нативного GLP-1, где глицин в позиции 37 был заменен на лизин.
Этот GLP-1-аналог производного изобретения, кроме того, включает второй остаток лизина в позиции, соответствующей позиции 26 в GLP-1(7-37). Так как аминокислотная последовательность этого аналога в остальном идентична нативному GLP-1, то такой аналог по-прежнему обозначается как K37- GLP-1(7-37), а K26 подразумевается ссылкой на нативный GLP-1(7-37), SEQ ID №1.
Соответственно, K37- GLP-1(7-37) обозначает аналог GLP-1(7-37), в котором природный глицин в позиции 37 был заменен на лизин.
Термин «аналог K37-GLP-1(7-37)» относится к аналогу GLP-1(7-37), который включает модификацию K37 и по меньшей мере одну дополнительную модификацию по сравнению с GLP-1(7-37).
GLP-1-аналог, являющийся частью производного изобретения, включает первый остаток K в позиции, соответствующей позиции 37 GLP-1(7-37) (SEQ ID №1), второй остаток K в позиции, соответствующей позиции 26 GLP-1(7-37), а также не более десяти аминокислотных модификаций по сравнению с GLP-1(7-37), где первый остаток K обозначается как K37, а второй остаток K обозначается как K26. Другими словами, это модифицированный пептид GLP-1(7-37), в котором количество аминокислотных остатков изменено по сравнению с нативным GLP-1(7-37) (SEQ ID №1). Эти изменения, или модификации, могут представлять собой, независимо, одну или более чем одну аминокислотную замену, добавление и/или удаление.
Другим неограничивающим примером аналога производного изобретения является [Aib8,Arg34,Lys37]GLP-1(7-37), который обозначает аналог GLP-1(7-37), в котором аланин в позиции 8 был заменен на α-аминоизомасляную кислоту (Aib), лизин в позиции 34 был заменен на аргинин, и глицин в позиции 37 был заменен на лизин. Этот аналог может быть обозначен как (8Aib, R34, K37) GLP-1(7-37).
Дополнительным неограничивающим примером аналога производного изобретения является аналог, «который включает 34Е, 34Q или 34R», что относится к аналогу GLP-1, который содержит глутаминовую кислоту (Е), глутамин (Q) или аргинин (R) в позиции, соответствующей позиции 34 нативного GLP-1(SEQ ID №1), и который может включать другие модификации по сравнению с SEQ ID №1.
Еще одним неограничивающим примером аналога производного изобретения является аналог GLP-1(7-37) (SEQ ID №1), который просто обозначается как «(8Aib, 31Н, 34Q, 37K)». Это обозначение относится к аналогу, который идентичен SEQ ID №1, за исключением этих четырех замен, т.е. к аналогу, в котором аланин в позиции 8 был заменен α-аминоизомасляной кислотой (Aib), триптофан в позиции 31 был заменен гистидином, лизин в позиции 34 был заменен глутамином, и глицин в позиции 37 был заменен лизином. Этот аналог не содержит других модификаций по сравнению с SEQ ID №1.
Еще одним неограничивающим примером аналога производного изобретения является аналог, содержащий des7 (или Des7), который относится к аналогу GLP-1(7-37), в котором N-концевая аминокислота, гистидин, была удалена. Это аналог может быть обозначен как GLP-1(8-37).
Подобным образом, (des7+des8); (des7, des8); (des7-8); или (Des7, Des8), в связи с аналогом GLP-1(7-37), где может подразумеваться ссылка на GLP-1(7-37), относится к аналогу, в котором аминокислоты, соответствующие двум N-концевых аминокислотам нативного GLP-1, гистидину и аланину, были удалены. Этот аналог может быть обозначен как GLP-1(9-37).
Еще одним неограничивающим примером аналога производного изобретения является аналог, содержащий Imp7, и/или (Aib8 или S8), который относится к аналогу GLP-1(7-37), который, по сравнению с нативным GLP-1, включает замену гистидина в позиции 7 на имидазолпропионовую кислоту (Imp); и/или замену аланина в позиции 8 на α-аминоизомасляную кислотоу (Aib), или на серин.
Аналоги, «содержащие» определенные указанные модификации, могут включать дополнительные модификации по сравнению с SEQ ID №1. Два неограничивающих примера аналогов, которые включают Imp7, и/или (Aib8 или S8), и являются частью производных изобретения, представляют собой пептидные части Соед. 47 и Соед. 58.
Неограничивающими примерами аналога GLP-1(7-37), содержащего (des7+des8), Arg34, Lys37 и Glu38, являются следующие: [Des7,Des8,Arg34,Lys37]GLP-1(7-37)-Glu38-пептид и N9-{2-[2-(1Н-имидазол-4-ил)этилкарбамоил]-2-метилпропионил}[Arg34,Lys37]GLP-1(9-37) Glu38-пептид. В последнем соединении дипептидный миметик N-конца нативного GLP-1(His-Ala) присоединен к новому N-концу, Glu 9, через амидную связь.
Подходящие His- или His-Ala-миметики, которые могут быть использованы в качестве своего рода заместителя удаленных N-концевых аминокислот, если таковые есть, содержат гетероциклические азотсодержащие ароматические кольцевые структуры, например, пиридин или имидазол. Предпочтительными His-или His-Ala-миметиками являются производные имидазола или пиридина, отличные от His и His-Ala, в одном воплощении с заместителем со свободной карбокси-группой, которая может образовывать амидную связь с аминогруппой N-концевой аминокислоты пептида. Термин «имидазол» относится к имидазолам как к классу гетероциклов с аналогичной кольцевой структурой, но различными заместителями, и, наоборот, для пиридина.
Как видно из приведенных выше примеров, аминокислотные остатки могут быть идентифицированы по их полному имени, их однобуквенному коду и/или их трехбуквенному коду. Эти три способа полностью эквивалентны.
Выражения «позиция эквивалентна» или «соответствующая позиция» могут быть использованы для описания места введения модификации в последовательность модифицированного GLP-1(7-37) со ссылкой на нативный GLP-1(7-37) (SEQ ID №1). Эквивалентные или соответствующие позиции, а также ряд модификаций можно легко вывести, например, путем простой рукописной записи и визуального контроля; и/или можно использовать стандартную программу для выравнивания белков или пептидов, такую как «align», которая является выравниванием по Нидлману-Вуншу. Алгоритм описан в Needleman, S.B. and Wunsch, C.D., (1970), Journal of Molecular Biology, 48:443-453, и программу для выравнивания Myers and W. Miller "Optimal Alignments in Linear Space" CABIOS (computer applications in the biosciences) (1988) 4:11-17. Для выравнивания могут по умолчанию быть использованы матрица весов выравнивания BLOSUM50 и идентичная матрица, и штраф на первый остаток в делеции может быть установлен на -12, или предпочтительно на -10, а штраф на дополнительные остатки в делеции на -2, или предпочтительно на -0,5.
Пример такого выравнивания приведен ниже, где последовательность №1 представляет собой SEQ ID №1, а последовательность №2 представляет собой ее аналог (des7-8, 34R, 37K, 38Е).
#1: GLP-1(7-37)
# 2: GLP-1(7-37)_Analogue
# Matrix: EBLOSUM62
# Gap_penalty: 10.0
# Extend_penalty: 0.5
# Length: 32
# Identity: 27/32 (84.4%)
# Similarity: 28/32 (87.5%)
# Gaps: 3/32 (9.4%)
# Score: 138.0
В случае неприродных аминокислот, таких как Imp и/или Aib, включенных в последовательность, или в случае His-Ala-миметиков, они с целью выравнивания могут быть заменены на X. При необходимости Х в дальнейшем может быть исправлен вручную.
Термин «пептид», например, используемый в контексте GLP-1-аналогов производных изобретения, относится к соединению, которое содержит ряд аминокислот, взаимосвязанных с помощью амидных (или пептидных) связей.
В частном воплощении пептид в значительной степени или в основном состоит из аминокислот, соединенных посредством амидных связей (например, по меньшей мере 50%, 60%, 70%, 80% или по меньшей мере 90% по молярной массе). В другом частном воплощении пептид состоит из аминокислот, соединенных пептидными связями.
Пептиды изобретения содержат по меньшей мере пять конститутивных аминокислот, соединенных пептидными связями. В частных воплощениях пептид включает по меньшей мере 10, предпочтительно по меньшей мере 15, более предпочтительно по меньшей мере 20, более предпочтительно по меньшей мере 25, или наиболее предпочтительно по меньшей мере 28 аминокислот.
В частном воплощении пептид состоит по меньшей мере из пяти конститутивных аминокислот, предпочтительно состоит по меньшей мере из 10, по меньшей мере из 15, по меньшей мере из 20, по меньшей мере 25, или наиболее предпочтительно состоит по меньшей мере из 28 аминокислот.
В дополнительном частном воплощении пептид а) состоит из или б) содержит i) 29, ii) 30, iii) 31 или iv) 32 аминокислоты.
В еще одном частном воплощении пептид состоит из аминокислот, соединенных пептидными связями.
Аминокислоты представляют собой молекулы, содержащие аминогруппу и карбоксильную группу, и, возможно, одну или более чем одну дополнительную группу, которые часто называют боковыми цепями.
Термин «аминокислота» включает протеогенные аминокислоты (кодируемые генетическим кодом, в том числе природные аминокислоты и стандартные аминокислоты), а также непротеогенные (не найденные в белках и/или не закодированные стандартным генетическим кодом) и синтетические аминокислоты. Таким образом, аминокислоты могут быть выбраны из группы протеиногенных аминокислот, непротеиногенных аминокислот и/или синтетических аминокислот.
Неограничивающими примерами аминокислот, которые не кодируются генетическим кодом, являются гамма-карбоксиглутаминовая кислота, орнитин и фосфосерин. Неограничивающими примерами синтетических аминокислот являются D-изомеры аминокислот, такие как D-аланин (в дальнейшем иногда сокращенный как «а», например, в «а8», который, соответственно, относится к D-Ala8) и D-лейцин, Aib (α-аминоизомасляная кислота), β-аланин и дезаминогистидин (desH, альтернативное название имидазолпропионовой кислоты, сокращенно Imp).
В дальнейшем все аминокислоты, для которых не указан оптический изомер, будут пониматься как L-изомеры (если не указано иное).
GLP-1-производные и аналоги изобретения обладают GLP-1-активностью. Этот термин относится к способности связываться с GLP-1-рецептором и инициировать путь передачи сигнала, приводящий к инсулинотропному действию или другим физиологическим эффектам, известным в данной области. Например, аналоги и производные изобретения могут быть проверены на GLP-1-активность путем анализа, описанного в примере 50 данного документа.
GLP-1-производные
Термин «производное», используемый в данном документе в связи с GLP-1-пептидом или аналогом, означает химически модифицированный GLP-1-пептид или аналог, в котором один или более чем один заместитель был ковалентно присоединен к пептиду. Заместители могут быть отнесены к боковой цепи.
В частном воплощении боковая цепь способна образовывать нековалентные агрегаты с альбумином, что способствует циркуляции производных с током крови, а также обеспечивает эффект увеличения времени действия производного в связи с тем фактом, что агрегат GLP-1-производного и альбумина только медленно распадается, высвобождая активный фармацевтический ингредиент. Таким образом, заместитель, или боковая цепь, в целом предпочтительно относится к альбумин-связывающей группировке.
В частном воплощении боковая цепь имеет по меньшей мере 10 атомов углерода, или по меньшей мере 15, 20, 25, 30, 35, или по меньшей мере 40 атомов углерода. В другом частном воплощении боковая цепь может также включать по меньшей мере 5 гетероатомов, в частности, кислород и азот, например, по меньшей мере 7, 9, 10, 12, 15, 17, или по меньшей мере 20 гетероатомов, например, по меньшей мере 1, 2 или 3 N-атома и/или по меньшей мере 3, 6, 9, 12, или 15 O-атомов.
В другом частном воплощении альбумин-связывающая группировка содержит часть, которая особенно подходит для связывания альбумина и, следовательно, замедления, и, соответственно, может быть названа пролонгирующей группировкой. Пролонгирующая группировка может находиться на противоположном конце альбумин-связывающей группировки по отношению к точке его прикрепления к пептиду или вблизи этого конца.
В еще одном частном воплощении альбумин-связывающая группировка включает часть между пролонгирующей группировкой и точкой прикрепления к пептиду, которая может быть названа линкером, линкерной группировкой, спейсером и т.д. Линкер может быть необязательным, и, следовательно, в этом случае альбумин-связывающая группировка может быть идентична пролонгирующей группировке.
В частных воплощениях альбумин-связывающая группировка и/или пролонгирующая группировка является липофильной и/или отрицательно заряженной при физиологическом значении рН (7,4).
Альбумин-связывающая группировка, пролонгирующая группировка или линкер могут быть ковалентно присоединены к остатку лизина пептида GLP-1 путем ацилирования. Дополнительная или альтернативная химия конъюгирования включает алкилирование, образование эфира или образование амида или связывание с остатком цистеина, например, с помощью малеимид- или галоацетамид-(например, бром-/фтор-/йод-) связывания.
В предпочтительном воплощении активный эфир альбумин-связывающей группировки, предпочтительно включающий пролонгирующую группировку и линкер, ковалентно связан с аминогруппой остатка лизина, предпочтительно его эпсилон-аминогруппой, с образованием амидной связи (это процесс именуется ацилированием).
Если не указано иное, то когда дается ссылка на ацилирование остатка лизина, следует понимать, что оно происходит на эпсилон-аминогруппе.
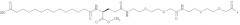
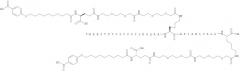
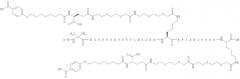
Производное, содержащее две пролонгирующие группировки, присоединенные к K26 и K37, возможно через линкер, может быть названо производным, ацилированным дважды, или производным с двойным ацилированием на эпсилон-аминогруппах остатков лизина в позициях, соответствующих позициям 26 и 37 GLP-1(7-37), соответственно.
Для наших целей термины «альбумин-связывающая группировка», «пролонгирующая группировка» и «линкер» могут включать непрореагировавшие, а также прореагировавшие формы этих молекул. Либо ни одна из этих форм или другая форма имеется в виду, что становится ясно из контекста, в котором этот термин используется.
В одном аспекте каждая пролонгирующая группировка включает или состоит из пролонгирующей группировки, независимо выбранной среди Соед. 1, Соед. 2, Соед. 3 и Соед. 4:
Соед. 1: НООС-(СН2)x-СО-*
Соед. 2: НООС-С6Н4-O-(СН2)y-СО-*
Соед. 3: R1-C6H4-(CH2)z-CO-*
Соед. 4: HOOC-C4SH2-(CH2)w-CO-*,
где x является целым числом в диапазоне 6-18, y является целым числом в диапазоне 3-17, z является целым числом в диапазоне 1-5, R1 представляет собой группу с молекулярной массой не более 150 Да, a w является целым числом в диапазоне 6-18.
В одном воплощении *-(СН2)x-* относится к прямому или разветвленному, предпочтительно прямому, алкилену, где x является целым числом в диапазоне 6-18.
В другом воплощении *-(СН2)y-* относится к прямому или разветвленному, предпочтительно прямому, алкилену, где y является целым числом в диапазоне 3-17.
В третьем воплощении *-(CH2)z-* относится к прямому или разветвленному, предпочтительно прямому, алкилену, где z является целым числом в диапазоне 1-5.
В еще одном воплощении *-(CH2)w-* относится к прямому или разветвленному, предпочтительно прямому, алкилену, где w является целым числом в диапазоне 6-18.
В другом аспекте альбумин-связывающая группировка включает либо состоит из пролонгирующей группировки, выбранной среди двухосновных жирных кислот и жирных кислот с дистальной (концевой) фенильной или фенокси-группой, при этом обе могут быть замещенными. Дополнительные заместители фенильной и/или или фенокси-группы имеют молярную массу не более 150 Да, предпочтительно не более 125 Да, более предпочтительно не более 100 Да, еще более предпочтительно не более 75 Да, или наиболее предпочтительно не более 50 Да. Примеры заместителей включают, но не ограничиваясь ими, карбоксил, гидроксил, низший линейный или разветвленный С1-С5-алкил, такой как метил и третбутил, и галоген, такой как йод.
Для прикрепления к пептиду GLP-1 кислотная группа жирной кислоты или одна из кислотных групп двухосновной жирной кислоты формирует амидную связь с эпсилон-аминогруппой остатка лизина в пептиде GLP-1, предпочтительно с помощью линкера.
Термин «жирная кислота» относится к алифатическим одноосновным кислотам, имеющим от 4 до 28 атомов углерода, предпочтительно неразветвленным, и/или имеющим четное число атомов, которые могут быть насыщенными или ненасыщенными.
Термин «двухосновная жирная кислота» относится к жирным кислотам, описанным выше, но с дополнительной карбоксильной группой в позиции омега. Таким образом, двухосновные жирные кислоты являются дикарбоновыми кислотами.
В предпочтительном воплощении пролонгирующая группировка выбрана среди НООС-(СН2)n-СО-*, НООС-С6Н4-O-(СН2)m-СО-* и R1-C6H4-(CH2)p-СО-*, где n является целым числом в диапазоне 8-16, m является целым числом в диапазоне 7-17, p является целым числом в диапазоне 1-5, a R1 представляет собой группу с молекулярной массой не более 150 Да.
Номенклатура является такой, которая обычно используется в данной области, например, в приведенных выше формулах *-СООН, а также НООС-* относится к карбокси; *-С6Н4-* к фенилену; *-СО-*, а также *-ОС-* к карбонилу (O=С<**); С6Н5-О-* к фенокси; C4H4S или C4SH4 к тиофену; и *-C4SH2-* к двойным радикалам любого из них (любому тиофенилену). В частных воплощениях ароматические структуры, такие как фенокси-, и фенилен-радикалы, могут находиться, независимо друг от друга, в орто-, мета- или пара-положении. В другом воплощении тиофениленовый двойной радикал может быть 2,3-, 2,4-, либо 2,5-.
Молярная масса (M) химического вещества (такого как группа R1) представляет собой массу одного моля вещества. Молярная масса приводится в дальтонах, символ Да, с определением 1 Да = 1 г/моль.
Молярная масса может быть рассчитана из стандартных атомных масс и часто приведена в химических каталогах. Молярная масса соединения определяется суммой стандартных атомных масс атомов, которые образуют соединение, умноженной на константу молярной массы, Mu, равную 1 г/моль. Например, молекулярная масса третбутила (С4Н9) составляет М (C4H9)=([4×12,01]+[9×1,008])×1 г/моль=57 Да.
Стандартные атомные массы опубликованы Международным союзом чистой и прикладной химии (IUPAC), а также перепечатаны в самых разнообразных учебниках, коммерческих каталогах, плакатах и т.д.
Как указывалось выше, GLP-1-производные данного изобретения являются дважды ацилированными, т.е. две альбумин-связывающие группировки ковалентно прикреплены к GLP-1-пептиду. Точками прикрепления являются нативный остаток лизина в позиции, соответствующей позиции 26 GLP-1(7-37), и остаток лизина, которым был заменен нативный глицин в позиции, соответствующей позиции 37 GLP-1(7-37).
В частном воплощении две альбумин-связывающие группировки (т.е. целые боковые цепи) являются подобными, предпочтительно в значительной степени идентичными, или, наиболее предпочтительно, идентичными.
В другом частном воплощении две пролонгирующие группировки являются подобными, предпочтительно в значительной степени идентичными, или, наиболее предпочтительно, идентичными.
В еще одном частном воплощении два линкера являются подобными, предпочтительно в значительной степени идентичными, или, наиболее предпочтительно, идентичными.
Термин «в значительной степени идентичны» включает отличия в идентичности, которые связаны с формированием одной или более чем одной соли, сложного эфира и/или амида; предпочтительно с формированием одной или более чем одной соли, метилового эфира и простого амида; более предпочтительно с формированием не более двух солей, метиловых эфиров и/или простых амидов; еще более предпочтительно с формированием не более одной соли, метилового эфира и/или простого амида; или наиболее предпочтительно с формированием не более чем одной соли.
В контексте химических соединений, таких как альбумин-связывающие группировки, пролонгирующие группировки и линкеры, сходство и/или идентичность можно определить с помощью любой подходящей компьютерной программы и/или алгоритма, известного в данной области.
Например, сходство двух пролонгирующих группировок, двух линкеров и/или двух целых боковых цепей может соответственно быть определено с помощью методики «молекулярных отпечатков пальцев». Методика молекулярных отпечатков представляет собой математический способ представления химической структуры (см., например Chemoinformatics: A textbook, Johann Gasteiger and Thomas Engel (Eds), Wiley-VCH Verlag, 2003).
Примеры подходящих отпечатков включают, но не ограничиваясь ими, отпечатки UNITY, отпечатки MDL и/или отпечатки ECFP, такие как отпечатки пальцев ECFP_6 (ECFP означает методику отпечатков пальцев с расширенной способностью к взаимодействию).
В частном воплощении две пролонгирующие группировки, два линкера и/или две целые боковые цепи представлены в виде а) отпечатков пальцев ECFP_6, б) отпечатков пальцев UNITY; и/или в) отпечатков пальцев MDL.
Для вычисления сходства двух пальцев предпочтительно используют коэффициент Танимото и для а), и для б), и для в).
В частном воплощении, используется ли а), б) или в), две пролонгирующие группировки, два линкера и/или две целые боковые цепи, соответственно, имеют сходство по меньшей мере 0,5 (50%); предпочтительно по меньшей мере 0,6 (60%); более предпочтительно по меньшей мере 0,7 (70%) или по меньшей мере 0,8 (80%); еще более предпоч