Визуализация хирургических траекторий
Иллюстрации
Показать всеГруппа изобретений относится к медицине и к визуализации хирургической траектории. Имеют место этапы приема информации в виде трехмерного изображения области, подлежащей хирургическому вмешательству, и комбинирования принятой информации в виде трехмерного изображения с данными из преобразованного в цифровую форму атласа. В результате получается комбинированная карта области, подлежащей хирургическому вмешательству. Комбинированная карта включает ожидаемые положения анатомических структур в области, подлежащей хирургическому вмешательству. Кроме того, имеются этапы приема хирургической траектории для хирургического вмешательства, определения положений пересечений хирургической траектории с анатомическими структурами и предоставления положений пересечений в системе координат, совмещенной с хирургической траекторией. Группа изобретений позволяет более четко предоставить хирургу необходимую в ходе операции информацию. 3 н. и 12 з.п. ф-лы, 10 ил.
Реферат
Область техники, к которой относится изобретение
Данное изобретение относится к способу визуализации хирургической траектории. Способ комбинирует информацию в виде трехмерного изображения с преобразованной в цифровую форму анатомической моделью для сегментирования анатомических структур в информации в виде трехмерного изображения. Планируемая хирургическая траектория проецируется на комбинированные изображения для визуализации хирургической траектории.
Данное изобретение, кроме того, относится к системе и компьютерному программному продукту для выполнения указанного способа.
Уровень техники
Такой способ, например, известен из публикации Guo и др., Development and Application of Functional Databases for Planning Deep-Brain Neurosurgical Procedures (Разработка и применение функциональных баз данных для планирования нейрохирургических процедур на глубоких структурах головного мозга). Из публикации Guo и др. известно слияние предоперационных MRI (магнитно-резонансных изображений), полученных у отдельных пациентов, с преобразованными в цифровую форму анатомическими атласами. Только по магнитно-резонансным изображениям очень трудно или даже невозможно визуально дифференцировать мелкие различные неврологические структуры, такие как субталамическое ядро (STN), которое часто является мишенью во время процедур стимуляции глубоких мозговых структур. При использовании дополнительной информации из анатомических атласов и/или вероятностных функциональных атласов возможно увеличение точности и воспроизводимости определения локализации хирургических мишеней по данному предоперационному хирургическому планированию. В публикации Guo и др. вероятностные функциональные атласы на основе дополнительной стандартизированной (EP) электрофизиологической информации, доступной перед операцией, используются для содействия определению хирургической мишени и для обеспечения анатомического мечения для данных трехмерного изображения. Слитые изображения и стандартизированная электрофизиологическая информация вместе служат для обеспечения возможности представления на дисплее положения иглы зонда вдоль действительной или моделированной хирургической траектории. Положение иглы зонда представлено в объеме трехмерного изображения и на двухмерных срезах тела пациента.
Однако совмещение атласа с предоперационными магнитно-резонансными изображениями имеет ограниченную воспроизводимость вследствие погрешностей совмещения, присущих любому способу совмещения. Обработка изображения, такая как сегментация, может использоваться для дальнейшего усовершенствования анатомического мечения. Однако данная методика также имеет присущую ей ограниченную точность. Кроме того, во время операции, имплантированный зонд может непреднамеренно отклоняться от планируемой траектории (например, вследствие такого недостатка как небольшое сгибание зонда) или анатомическая структура может немного сдвигаться вследствие самой хирургической процедуры (например, имплантация зонда в ткань генерирует небольшое силовое поле, которое отталкивает ткань в сторону; потеря спинномозговой жидкости во время операции может привести к изменениям давления в ткани, приводя к более крупным деформациями, именуемыми «мозговым сдвигом»). Поэтому прецизионная имплантация зонда в маленькую область-мишень обычно требует интраоперационных измерений (например, электрофизиологических измерений) для точного определения точки мишени и для коррекции ошибок вследствие неточностей при предоперационном планировании или вследствие анатомических сдвигов во время операции или вследствие (непреднамеренных) отклонений зонда от планируемой траектории. Правильная интерпретация таких интраоперационных измерений имеет решающее значение для точного определения локализации мишени, но может представлять собой очень трудный для выполнения анализ, ввиду сложности данных и количества информации, необходимой для обработки специалистами при выполнении данного анализа.
Проблемой, связанной со способом, описанным в публикации Guo и др., является то, что полученные данные не обеспечивают получение хирургом достаточно четкой и однозначной информации, которая, как можно было ожидать, могла бы помочь врачу в распознавании типа неврологических структур и определении локализации хирургической мишени вдоль планируемой и проложенной хирургических траекторий.
Цель изобретения
Целью изобретения является предоставление более четкого способа представления хирургу достаточно ясной информации для установления типа ожидаемых неврологических структур вдоль планируемой и проложенной хирургических траекторий.
Сущность изобретения
В соответствии с первым аспектом изобретения, данная цель достигается предоставлением способа визуализации хирургической траектории, причем способ включает прием информации в виде трехмерного изображения подлежащей хирургическому вмешательству области, комбинирование принятой информации в виде трехмерного изображения с данными из базы данных анатомических моделей, например, из преобразованного в цифровую форму анатомического атласа, для получения комбинированной карты подлежащей хирургическому вмешательству области, причем комбинированная карта включает ожидаемые положения анатомических структур в области, подлежащей хирургическому вмешательству, прием хирургической траектории для операции, определение положений пересечений хирургической траектории с анатомическими структурами и предоставление положений пересечений в системе координат, совмещенной с хирургической траекторией.
В результате использования данного способа пользователь получает четкий обзор того, какие анатомические структуры следует ожидать и в каком положении вдоль хирургической траектории. Действительно, способ в соответствии с изобретением представляет в виде карты трехмерную анатомическую информацию на хирургическую траекторию. С помощью способа в соответствии с изобретением пользователь узнает, какие структуры следует ожидать и в каком положении вдоль планируемой или проложенной хирургической траектории. Поэтому легче избегать критических структур, определить локализацию хирургической мишени или, например, высвободить определенное лекарственное средство у конкретной анатомической структуры.
Способ в соответствии с изобретением комбинирует (i) информацию в виде трехмерного медицинского изображения с (ii) базой данной анатомической модели для сегментирования анатомических структур в информации в виде трехмерного медицинского изображения и (iii) локальные измерения хирургическим зондом, характерные для анатомической структуры или типа ткани, полученные во время хирургического вмешательства. База данных моделей комбинируется с информацией в виде трехмерного изображения для получения трехмерного анатомического мечения визуализирующей информации (например, совмещением цифрового анатомического атласа с магнитно-резонансной визуализацией). По меньшей мере, одна планируемая хирургическая траектория по направлению, по меньшей мере, к одной хирургической мишени комбинируется с анатомически мечеными трехмерными изображениями, и поперечное сечение траектории с анатомически меченой информацией в виде трехмерного изображения проецируется в виде анатомического мечения на хирургическую траекторию.
Возможно интраоперационное обновление данных медицинского изображения и соответствующего анатомического мечения путем периоперационной визуализации, например, с использованием плоскопанельной трехмерной рентгеновской системы, интраоперационной магнитно-резонансной визуализации или трехмерного ультразвукового исследования. Локальные измерения с использованием, по меньшей мере, одного хирургического зонда могут выполняться вдоль планируемой хирургической траектории для интраоперационного подтверждения идентификации типа анатомической структуры в участке (участках) измерения зондом. Данные, извлеченные из локальных измерений, совместно визуализируются с помеченой хирургической траекторией для содействия их интерпретации и для подтверждения интраоперационной точной локализации хирургической мишени. Данные, извлеченные из локальных измерений, дополнительно могут комбинироваться с меченой хирургической траекторией для компьютерной обработки (например, с использованием алгоритмов анализа создания кластеров) для извлечения характерных признаков, показательных для определенной анатомической структуры, которые могут быть представлены пользователям для подтверждения локализации мишени.
В предпочтительном варианте осуществления, комбинированная карта включает статистическую карту области, подлежащую хирургическому вмешательству, причем статистическая карта включает вероятности присутствия анатомических структур в положениях в данной области. На такой статистической карте, переходы от одной анатомической структуры к другой являются не резкими, но происходят постепенно. Таким образом, пересечения не представляют одиночные точки, где одна структура лежит, прилегая к другой структуре. Вместо этого, пересечения представляют собой срезы хирургической траектории, где вероятность первой структуры постепенно уменьшается, тогда как вероятность, по меньшей мере, одной другой структуры постепенно увеличивается. Например, в определенном положении вдоль хирургической траектории может иметься 30% вероятность нахождения в первой структуре и 70% вероятность нахождения во второй структуре. В некоторых положениях даже более чем две различные анатомические структуры могут иметь значимую вероятность. Следует отметить, что в способе использования резких пересечений используются только вероятности 0% и 100%.
Для ясного указания того, какие структуры следует ожидать и в каком положении в хирургической траектории, положения пересечений могут быть представлены в виде расстояния между пересечениями и мишенью хирургической траектории. Это обеспечивает пользователю возможность видеть то, как близко к области-мишени можно ожидать нахождение определенной анатомической структуры. Хирургическая траектория может представлять собой планируемую или проложенную траекторию. При планировании траектории данный способ содействует обнаружению относительно безопасного и легкодоступного пути к мишени. При прокладывании траектории с использованием хирургического инструмента способ в соответствии с изобретением может помочь пользователю видеть, у какого типа анатомической структуры он работает в настоящее время, и, возможно, какие типы структур можно ожидать при следовании дальше по ходу по направлению к структуре-мишени.
В практическом варианте осуществления способа в соответствии с изобретением, хирургический инструмент представляет собой электрофизиологический зонд, и способ дополнительно включает этап приема электрофизиологических сигналов от зонда, этап извлечения признаков из принятых электрофизиологических сигналов, этап установления взаимосвязи между извлеченными признаками и положениями в системе координат и этап визуализации извлеченных признаков в комбинации с взаимосвязанными положениями в системе координат.
В одном варианте осуществления, используются данные CT (компьютерно-томографического) или подобного компьютерно-томографическому трехмерному изображению области вокруг позвоночника. С использованием сегментации и анатомического моделирования трехмерное изображение анатомически метится и планируется хирургическая траектория. Хирургический зонд со встроенным волокном для измерения оптической отражательной способности используется для локального анатомического картирования возле наконечника зонда («фотонной иглы»). Информация в виде трехмерного изображения и связанное с ним анатомическое мечение обновляется периоперационной трехмерной рентгеновской визуализацией с использованием плоскопанельной ротационной рентгеновской установки. Оптические спектры получают в различных положениях зонда. Оптические спектры визуализируются вместе с картой, которая визуализирует близость и направленность определенного анатомического мечения относительно наконечника хирургического зонда на основании проложенной траектории наконечника хирургического зонда на трехмерном (анатомически меченом) изображении.
Данные и другие аспекты изобретения очевидны и будут выяснены со ссылкой на описанные ниже варианты осуществления.
Краткое описание чертежей
На чертежах:
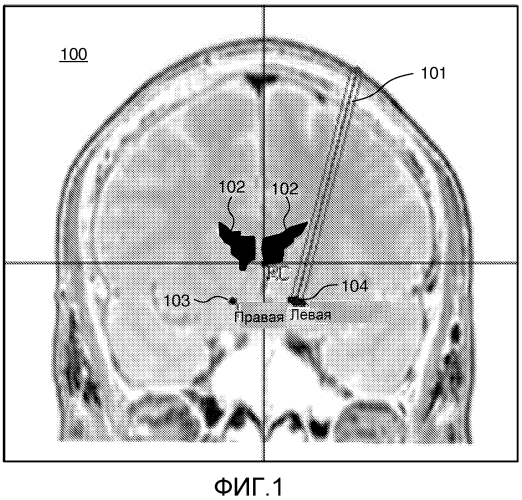
на фиг. 1 показано изображение, включающее данные магнитно-резонансной визуализации, атлас и хирургическую траекторию,
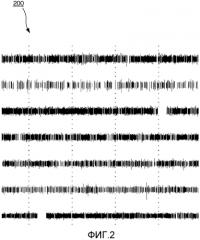
на фиг. 2 показан пример выходных сигналов электрофизиологической регистрации,
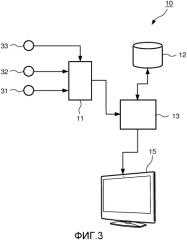
на фиг. 3 показана блок-схема системы в соответствии с изобретением,
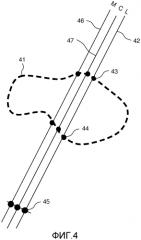
фиг. 4 иллюстрирует расчет положения пересечения анатомического среза и хирургической траектории,
на фиг. 5, 6 и 7 показаны иллюстративные визуализации хирургической траектории, обеспечиваемые системой в соответствии с изобретением,
на фиг. 8a и 8b показаны другие примеры визуализации нейроэлектрофизиологических величин в комбинации с анатомической информацией о хирургической траектории,
На фиг. 9 показана зависимость уровня помех от частоты разрядов импульсов, и
На фиг.10 показана схема последовательности операций способа в соответствии с изобретением.
Подробное описание изобретения
Далее, изобретение будет описано иллюстративным вариантом осуществления, связанным с нейрохирургическим вмешательством с использованием нейрохирургических зондов. Однако изобретение не ограничивается использованием с нейроэлектрофизиологической (EP) системой. При других хирургических вмешательствах, где знание об анатомических структурах вдоль хирургической траектории (планируемой и/или прокладываемой) полезно в клинических и/или диагностических целях, настоящее изобретение также может оказывать благоприятное воздействие. Изобретение может, например, подходить для вмешательств под контролем оптической иглы.
На фиг. 1 показано изображение 100, включающее данные магнитно-резонансной визуализации, атласа и трех хирургических траекторий 101. Известно использование такого изображения 100 для предоперационного планирования хирургической траектории. На данном изображении информация из атласа используется для указания определенных структур 102, 103, 104 в области мозга, которая показана на магнитно-резонансном изображении. На изображении 100 показано магнитно-резонансное изображение среза мозга человека. Хирургическая траектория 101 проходит через ткань мозга по направлению к мишени 104 планируемого хирургического вмешательства. В данном примере, мишень 104 хирургического вмешательства представляет собой определенную часть субталамического ядра (STN) 104. В данном примере, траектория 101 выбрана так, чтобы другая структура 102 не затрагивалась или не повреждалась хирургическим инструментом, используемым для хирургического вмешательства. Например, очень важно избежать повреждения основных кровеносных сосудов или желудочков.
Изображение 100, показанное на фиг. 1, помогает планировать хирургическую операцию. Известно использование регистрации электрофизиологических (EP) параметров при выполнении хирургических операций. На фиг. 2 показан пример выводимых данных 200 регистрации EP параметров. Такая регистрация нейроэлектрофизиологических параметров обычно выполняется с использованием так называемых микроэлектродных иголок; он представляют собой иголки, несущие миниатюрные электроды (диаметром приблизительно 10 мкм) на кончике и которые могут использоваться для улавливания электрических сигналов («спайков») от отдельных клеток мозга (нейронов) около наконечника электрода. При типичной процедуре, нейрофизиолог исследует записи во множественных положениях (до 100 положений, причем каждая регистрация представляет собой обычно данные, полученные за 10-20 секунд). Обычно такие регистрации выполняются в ступенчато углубляющихся положениях, при типичных размерах шагов 0,5 мм, т.е. гораздо ниже разрешения, доступного в клинических системах магнитно-резонансной визуализации. На основании сравнения статистических характеристик различных регистраций (например, характеристики привязки по времени спайков, такие как пакетирование и средняя частота разрядов, амплитуда шума и т.д.), нейрофизиолог должен преобразовать измеренные данные в функциональные свойства исследованных участков, т.е. сопоставлять функциональную анатомию с регистрируемыми положениями. Как ясно из фиг. 2, анализ EP записей является сложным и требует большого опыта, особенно когда необходимо его выполнение в условиях дефицита времени. Поэтому, в соответствии с изобретением, предоставляется система для визуализации хирургической траектории.
На фиг. 3 показана блок-схема системы 10 в соответствии с изобретением. Система 10 включает блок 11 ввода данных для приема информации 31 в виде трехмерного изображения подлежащей хирургическому вмешательству области. Информация 31 в виде трехмерного изображения может поступать, например, из магнитно-резонансного или компьютерно-томографического сканнера. Блок 11 ввода данных также предоставлен для приема информации 32 о траектории, определяющей планируемую или прокладываемую хирургическую траекторию. Например, если система 10 используется для визуализации получаемой в реальном масштабе времени информации во время хирургической операции возможно также, чтобы блок 11 ввода данных был обеспечен для приема EP данных 33 из системы регистрации EP данных. Процессор 13 предоставлен для обработки вводимых данных 31, 32, 33. Обработка данных включает несколько этапов, некоторые из которых обязательны, а некоторые возможны. Во-первых, принятая информация 31 в виде трехмерного изображения комбинируется с преобразованными в цифровую форму данными анатомического атласа для получения комбинированной карты подлежащей хирургическому вмешательству области. Данные анатомического атласа могут поступать из базы данных, хранящихся в запоминающем устройстве 12, которое является частью системы 10. Альтернативно, система 10 соединена с такой базой данных через закрытую сеть или широкую зональную сеть, такую как интернет, для приема из нее данных атласа. В данном варианте осуществления, так называемый анатомический атлас используется для получения анатомических данных о релевантных областях. Однако эти анатомические данные могут быть также предоставлены другим путем, например подходящим средством визуализации. Примером является сегментация величины интенсивности CT изображений, связанных с различными типами ткани (костной тканью, кровью и т.д.), для получения анатомических данных. В целом, анатомические данные могут быть получены из анатомической модели, хранящейся подходящим образом.
Комбинированная карта включает ожидаемые положения анатомических структур в области, подлежащей хирургическому вмешательству. Комбинированная карта создается с использованием методик распознавания изображений для обнаружения переходов между структурами на информации в виде трехмерного изображения и путем сравнения информации в виде трехмерных изображений с информацией из анатомического атласа. Комбинированная карта может, например, представлять собой изображение или перечень точек данных, описывающих ожидаемые положения важных анатомических структур. Карта может выглядеть в виде изображения 100, показанного на фиг. 1. Когда доступна комбинированная карта, процессор 13 использует принятые данные 32 хирургической траектории для определения положений пересечений хирургической траектории с анатомическими структурами. Когда положения этих пересечений известны, известно также, какая анатомическая структура лежит на хирургической траектории. Это обеспечивает возможность планирования и следования траектории, которая не наносит вреда критическим структурам, таким как кровеносные сосуды.
Положения этих пересечений предоставлены в системе координат совмещенными с хирургической траекторией. Такая система координат помогает обеспечению наглядного обзора анатомических структур, которые следует ожидать вдоль траектории. Например, положения пересечений могут быть предоставлены в виде расстояния от начала или точки-мишени траектории. Расстояние предпочтительно измеряется вдоль траектории. Когда положения пересечений известны, то информация может визуализироваться, например, представлением траектории или графическим представлением траектории на дисплее 15. С использованием, например, текстовых маркировок, цветового кодирования или высвечивания на дисплее представляется положение важных структур относительно хирургической траектории.
Фиг. 4 иллюстрирует расчет положения пересечения 43, 44 анатомического среза 41 хирургической траектории 42. В нейрохирургии часто более чем одна игла используется для хирургической операции. Обычно используются пять регистрирующих микроигл, которые называются «центральной», «латеральной», «медиальной», «передней» и «задней». Каждая игла имеет свою собственную траекторию 42, 46, 47 и свои собственные пересечения 43, 44 с анатомическими структурами 41. Кроме того, каждая хирургическая траектория обычно заканчивается в несколько отличающейся точке-мишени 45. Таким образом, положения пересечений 43, 44 должны рассчитываться для каждой иглы отдельно, и для каждой иглы указанные положения 43, 44 предоставляются в системе координат, совмещенной с соответствующими хирургическими траекториями 42, 46, 47.
На фиг. 5, 6 и 7 показаны иллюстративные визуализации хирургических траекторий, полученных системой 10, в соответствии с изобретением. На фиг. 5 визуализируются анатомические структуры, расположенные вдоль планируемых хирургических траекторий пяти EP-игл. Хирургическая процедура нацелена на субталамическое ядро (STN) в качестве мишени. На расстоянии 0 мм от точек-мишеней все пять иголок находятся в субталамическом ядре. Для центральной 51, латеральной 52, медиальной 53 илы определено, что перед субталамическим ядром пересекаются вставочная зона (ZI) и таламус (Th). Ожидается, что задняя 54 и передняя 55 иглы также пересекут таламус (Th). Когда иглы вводятся в мозг пациента за пределы точек-мишеней, то они могут проникнуть в плотную часть черного вещества (SN). Как видно на фиг. 5, не все иглы достигнут одинаковых структур на одинаковом расстоянии от мишени. Система и способ в соответствии с изобретением обеспечивают возможность визуализации каждой иглы, когда ожидается достижение ею анатомической структуры и какой именно анатомической структуры.
Заштрихованные отрезки гистограммы на фиг. 5 представляют ожидаемые анатомические структуры на планируемом хирургическом канале. При выполнении хирургического вмешательства данная картина может использоваться для демонстрации хирургу, чего следует ожидать, и где расположены иглы в настоящее время. На данной глубине линия 56 начерчена для показа, где иглы находятся в настоящее время. На фиг. 5 все иглы находятся в таламусе (Th). В данном варианте осуществления, все иглы перемещаются вместе и имеют одинаковое расстояние до их соответствующих точек-мишеней. Альтернативно, манипулирование иглами может осуществляться отдельно, и каждая игла имеет свой собственный соответствующий текущий уровень глубины.
На фиг. 6 визуализируется траектория только одной иглы 61. В данном варианте осуществления, пересечения хирургической траектории с анатомическими структурами не показаны в виде резкого перехода от одной структуры к другой. Процедура комбинирования трехмерных изображений области, подлежащей хирургическому вмешательству, с данными из анатомического атласа приводит к ожидаемым положениям для различных структур с некоторыми допусками на ошибки. В частности, в положениях, близких к переходу от одного типа ткани к другому, в ряде случаев нельзя быть полностью уверенным в типе анатомической структуры. Поэтому, в данном варианте осуществления используется статистическая карта области, подлежащей хирургическому вмешательству. Статистическая карта включает вероятности присутствия анатомической структуры в определенном положении. При использовании такой статистической карты для визуализации хирургического хода иглы 61 результаты могут быть подобны гистограмме, показанной на фиг. 6. Например, на «текущей глубине», игла, вероятно, находится в таламусе (Th). Когда игла пройдет немного дальше по ходу, она достигнет положения, в котором неизвестно, находится ли она уже во вставочной зоне (ZI) или еще в таламусе (Th).
На фиг. 7 показана визуализация анатомических структур при пяти хирургических траекториях 62, 63, 64, 65, 66 вместе с величинами параметров 82, 83, 84, 85, 86, извлеченных из интраоперационно полученных нейроэлектрофизиологических данных в тех же участках. Данное представление содействует процессу принятия решения, поскольку и анатомические, и электрофизиологические данные доступны при простом общем осмотре. Нейроэлектрофизиологические данные могут быть получены от одного или более зондов, используемых, например, для определения локализации функциональной мишени при терапии стимуляцией глубоких структур мозга (DBS). Известны способы автоматизированного анализа нейроэлектрофизиологических данных для извлечения определенных сигнальных признаков из необработанных данных. Путем установления связи указанных извлеченных признаков с положениями в системе координат, использованной для визуализации анатомических структур вдоль (планируемой или проложенной) траектории, легче оценить релевантность извлеченных величин. Ложно отрицательные и/или ложно положительные результаты, которые часто возникают при извлечении признаков из нейроэлектрофизиологических данных, легче распознаются при представлении извлеченных признаков вместе с ожидаемыми анатомическими положениями, соответствующими этим извлеченным признакам. Вместо извлечения признаков из нейроэлектрофизиологических данных 33 возможна визуализация самих нейроэлектрофизиологических данных в соответствующем положении, где они были зарегистрированы.
В одном варианте осуществления, используются данные комьютерно-томографического или подобного комьютерно-томографическому трехмерного изображения области вокруг позвоночника. С использованием сегментации и анатомического моделирования трехмерное изображение анатомически метится, и планируется хирургическая траектория. Хирургический зонд со встроенным волокном для измерения оптической отражательной способности используется для локального анатомического картирования у кончика зонда («фотонной иглы»). Информация в виде трехмерного изображения и связанное анатомическое мечение обновляется периоперационной трехмерной рентгеновской визуализацией с использованием плоскопанельной ротационной рентгеновской установки. Оптические спектры получают в различных положениях зонда. Оптические спектры визуализируются вместе с картой, которая визуализирует близость и направленность определенного анатомического мечения относительно наконечника хирургического зонда на основании проложенной траектории наконечника хирургического зонда на трехмерном (анатомически меченом) изображении.
На фиг. 8a и 8b показаны другие примеры визуализации величин нейроэлектрофизиологических параметров в комбинации с анатомической информацией о хирургическом ходе. На фиг. 8a показан уровень помех (ось y) в зависимости от глубины вдоль хирургической траектории (ось x). Мишенью данной траектории является субталамическое ядро (STN), которое, как определено, находится на глубине 0 мм. Как видно на чертеже, уровень помех близко к области мишени высок. Резкое увеличение наблюдается после вхождения в STN (указанное треугольниками 91). Внутри STN уровень помех остается постоянно высоким (указанных кружками 92), а после выхода из STN уровень помех резко падает. Однако уровень помех остается выше исходного уровня 94, наблюдавшегося перед вхождением в STN, и далее увеличивается после вхождения в черную субстанцию (SN, указанная квадратами 93). Из Фиг. 8a ясно, что один уровень помех недостаточен при дифференцировке STN от SN. Высокие уровни помех наблюдаются в обеих анатомических структурах. При комбинировании анатомических известных данных и трехмерных изображений с нейроэлектрофизиологическими сигналами таким образом, как это осуществляется в соответствии с изобретением, можно легче и надежнее дифференцировать различные анатомические структуры.
На фиг. 8b показана зависимость частоты разрядов импульсов (ось y) от глубины вдоль хирургической траектории (ось x). Вхождение в STN отмечено очень высокими частотами разрядов импульсов (указанное треугольниками 91). Частота разрядов импульсов уменьшается внутри STN (указано кружками 92) и после вхождения в SN (указанного треугольниками 93) снова увеличивается. Поэтому, одна частота разрядов импульсов недостаточна при дифференцировке STN от SN. Также такие показатели, как частота разрядов импульсов, проявляют высокую вариабельность вследствие чувствительности измерения к близости нейронных единиц. На некоторых глубинах вдоль хирургической траектории и внутри STN частота разрядов импульсов падает ниже исходного уровня 94. Эти положения указаны кружками 92a. Исходя только из одной частоте разрядов импульсов, хирург может принимать неправильные решения. При комбинировании анатомических данных и трехмерных изображений с нейроэлектрофизиологическими сигналами таким образом, как это осуществляется в соответствии с изобретением, можно легче и надежнее дифференцировать различные анатомические структуры.
На фиг. 9 уровень помех (ось y) наносится на график зависимости от частоты разрядов импульсов (ось x): в отсутствие информации о глубинекомбинация уровня помех и частоты разрядов импульсов отчетливо дифференцирует STN и SN от других областей. Все величины, измеренные внутри STN (треугольники 91 и кружки 92) и SN (квадраты 93), находятся значительно выше исходного уровня 94. Все другие измеренные величины находятся ниже исходного уровня 94. Однако данные показатели недостаточны для дифференцировки STN (кружки 92) и SN (треугольники 91). При использовании способа и системы в соответствии с изобретением для дифференцировки STN от SN используется информация о глубине, и она указывается на графике, например, с использованием различных форм или цветов для точек данных на различных глубинах.
На фиг. 10 показана последовательность операций способа в соответствии с изобретением. Способ начинается с этапа 71 приема изображения для приема информации в виде трехмерного изображения, например, полученного от магнитно-резонансного или компьютерно-томографического сканнера. В комбинации с этапом 72 принятая информации в виде трехмерного изображения комбинируется с данными из преобразованного в цифровую форму анатомического атласа для получения комбинированной карты области, подлежащей хирургическому вмешательству. Комбинированная карта включает ожидаемые положения анатомических структур в области, подлежащей хирургическому вмешательству. На этапе 73 ввода информации о траектории, по меньшей мере, принимается, по меньшей мере, одна хирургическая траектория для хирургического вмешательства. Траектория может приниматься в виде планируемого маршрута через область, подлежащую хирургическому вмешательству. Принимаемая информация о траектории может также включать текущее положение хирургического инструмента. Последовательность действительных положений хирургического инструмента формирует проложенную траекторию. Принятая траектория на этапе 73 ввода информации о траектории может представлять собой или планируемую, или уже проложенную траекторию. Альтернативно, принятая траектория представляет собой комбинацию планируемой и действительно проложенной траектории. Интерполяция и экстраполяция могут использоваться для формирования или коррекции хирургической траектории.
На этапе 74 расчета пересечений рассчитываются положения пересечений, по меньшей мере, одной хирургической траектории с поверхностями анатомических структур. Данные положения предоставляются в виде выводимой информации на этапе 75 вывода информации. Для облегчения понимания данных о положении положения пересечений предоставляются в системе координат, совмещенной с хирургической траекторией, с тем, чтобы было легко понять, какие анатомические структуры следует ожидать в различных положениях вдоль хирургической траектории. Затем предоставленные положения могут использоваться для визуализации хирургической траектории, например, как показано на одной из фиг. 5, 6 и 7.
Следует понимать, что изобретение также распространяется на компьютерные программы, в частности компьютерные программы на носителе информации или в носителе информации, адаптированном для внедрения изобретения в практику. Программа может быть в форме кода источника, кода объекта, кода промежуточного источника и кода объекта, такого как частично составленная форма, или в любой другой форме, подходящей для использования при осуществлении способа в соответствии с изобретением. Следует также понимать, что такая программа может иметь много различных структурных конструкций. Например, программный код, осуществляющий функционирование способа или системы в соответствии с изобретением, может быть подразделен на одну или более подпрограмм. Для специалиста в данной области будут очевидны многие различные пути распределения функционирования среди данных подпрограмм. Подпрограммы могут храниться вместе в одном исполнимом файле для формирования самодостаточной программы. Такой исполнимый файл может включать исполнимые инструкции, например инструкции процессора и/или инструкции интерпретирующей программы (например, инструкции интерпретирующей программы Java). Альтернативно, одна или более или все подпрограммы могут храниться, по меньшей мере, в одном внешнем библиотечном файле и быть связанными с основной программой или статически, или динамически, например, во время исполнения. Основная программа включает, по меньшей мере, один вызов, по меньшей мере, одной из подпрограмм. Также подпрограммы могут включать функциональные вызовы друг друга. Вариант осуществления, относящийся к продукту в виде компьютерной программы, включает исполняемые компьютером инструкции, соответствующие каждому из этапов обработки, по меньшей мере, одного из изложенных способов. Данные инструкции могут быть подразделены на подпрограммы и/или храниться в одном или более файлов, которые могут быть связаны статистически или динамически. Другой вариант осуществления, относящийся к продукту в виде компьютерной программы, включает исполняемые компьютером инструкции, соответствующие каждому из средств, по меньшей мере, одного из описанных систем и/или продуктов. Эти инструкции могут быть подразделены на подпрограммы и/или храниться в одном или более файлов, которые могут быть связаны статистически или динамически.
Носитель компьютерной программы может представлять собой любую структуру или устройство, способное осуществить программу. Например, носитель может включать среду хранения информации, такую как ROM (постоянное запоминающее устройство), например CD-ROM (постоянное запоминающее устройство на компакт-диске) или полупроводниковое ROM, или магнитная записывающая среда, например гибкий диск или жесткий диск. Кроме того, носитель может представлять собой передающий носитель, такой как электрический или оптический сигнал, который может передаваться по электрическому или оптическому кабелю или по радио или другому средству. Когда программа осуществляется таким сигналом, носитель может быть составлен таким кабелем или другим устройством или средством. Альтернативно, носитель может представлять собой интегрированную схему, в который встроена программа, причем интегрированная схема приспособлена для выполнения или для использования при выполнении релевантного способа.
Следует отметить, что указанные выше варианты осуществления скорее иллю