Терапевтическое средство или профилактическое средство для лечения фибромиалгии
Иллюстрации
Показать всеНастоящее изобретение предлагает терапевтическое средство или профилактическое средство для лечения фибромиалгии, причем указанное средство содержит, предпочтительно, в качестве эффективного ингредиента циклогексановое производное, представленное приведенной ниже формулой, или его фармацевтически приемлемую соль. Технический результат состоит в разработке терапевтического средства или профилактического средства, которое является эффективным при лечении фибромиалгии и обладает обезболивающим действием как на ноцицептивную боль, так и невропатическую боль. 8 з.п. ф-лы, 1 ил., 13 табл.
Реферат
Область техники
Настоящее изобретение относится к терапевтическому средству или профилактическому средству для лечения фибромиалгии.
Уровень техники
Фибромиалгия представляет собой заболевание с основными жалобами на системную диффузную боль и усталость и с объективными симптомами характерных болезненных точек. Показано, что похожие на психосоматические нарушения симптомы, такие как нарушение сна, страх, депрессия и раздражительность, и/или сопутствующие нарушения, такие как учащенное мочеиспускание, синдром раздраженного кишечника, дисменорея и синдром сухого глаза, часто наблюдаются при фибромиалгии. Известно, что по мере развития симптомов фибромиалгии больные могут чувствовать сильную боль, даже когда они получают небольшое раздражающее воздействие, и что в результате повседневная жизнь становится трудной, и качество жизни будет заметно снижаться.
Современную диагностику фибромиалгии в нашей стране проводят на основе классификационного критерия American College of Pheumatology, который опубликован в 1990 г (непатентный документ 1). Хотя патогенный механизм фибромиалгии еще не выяснен, полагают, что ее патогенный механизм будет отличаться от патогенного механизма ноцицептивной боли, которая вызвана повреждением живого организма, или от патогенного механизма невропатической боли, вызванной или спровоцированной временным повреждением или дисфункцией нервной системы, так как она не сопровождается ни воспалением, ни поражением нерва.
В качестве терапевтических средств для лечения фибромиалгии прегабалин, который представляет собой блокатор кальциевых каналов, и дулоксетин и милнаципран, которые представляют собой антидепрессанты, проявляющие ингибирующее действие на повторное поглощение серотонина и норадреналина (SNRI), ободрены US Food and Drug Administration (Управление по контролю за продуктами питания и лекарственными средствами США); и использовались некоторые нестероидные противовоспалительные средства, так как они, как считают, являются эффективными при лечении фибромиалгии (непатентный документ 2).
Однако в настоящее время обезболивающий эффект прегабалина и дулоксетина, которые были одобрены в качестве терапевтического средства для лечения фибромиалгии, у некоторых больных может быть плохим, и среди больных имеют место большие индивидуальные различия в эффективности лекарственных средств. Для ибупрофена и напроксена, которые представляют собой нестероидные противовоспалительные средства, было сообщено, что какой-либо статистически значимый обезболивающий эффект не наблюдается при лечении фибромиалгии (непатентный документ 3). Следовательно, весьма необходима разработка нового лекарства, которое обладает сильным обезболивающим действием на боли, вызванные различными механизмами, и является эффективным у широкого ряда больных фибромиалгией.
С другой стороны, что касается производного пиразола (патентный документ 1) и производного циклогексана приведенной ниже формулы, которое имеет сульфонильную группу на ароматическом кольце, связанном с пиразольным кольцом (патентный документ 2), то раскрыто их терапевтическое действие на ноцицептивную боль и/или невропатическую боль; но их применение в качестве фармацевтического средства для какого-либо конкретного заболевания, такого как фибромиалгия, не раскрыто и даже не предполагается.
Документы предшествующего уровня техники
Патентные документы
Патентный документ 1: WO 08/105383.
Патентный документ 2: WO 00/066562.
Непатентные документы
Непатентный документ 1: Wolfe et al., Arthitis Pheum., 1990, vol. 33, p. 160.
Непатентный документ 2: Nickerson B., US Pharma., 2009, vol. 34, p. 49.
Непатентный документ 3: Abeles et al., Am. J. Med., 2008, vol. 121, p. 555.
Описание изобретения
Проблемы, решаемые с помощью изобретения
Таким образом, цель настоящего изобретения состоит в разработке терапевтического средства или профилактического средства, которое обладает обезболивающим действием как на ноцицептивную боль, так и на невропатическую боль, и является эффективным при лечении фибромиалгии.
Средства для решения проблем
Для решения описанной выше проблемы заявители настоящего изобретения провели интенсивные исследования, чтобы установить, что новые циклогексановые производные, обладающие прекрасным обезболивающим действием как на ноцицептивную боль, так и на невропатическую боль, также оказывают прекрасное терапевтическое и профилактическое действие на фибромиалгию.
То есть, настоящее изобретение предлагает терапевтическое средство или профилактическое средство для лечения фибромиалгии, причем указанное средство содержит в качестве эффективного ингредиента циклогексановое производное, представленное формулой (I):
или его фармацевтически приемлемую соль или его пролекарство;
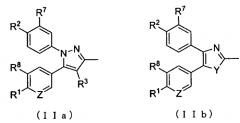
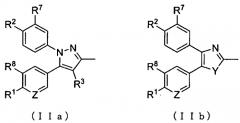
где А представляет собой заместитель, представленный формулой (IIa) или (IIb):
;
R1 и R2 каждый независимо друг от друга представляет собой атом водорода, атом хлора, C1-C3-галогеналкильную группу, C1-C4-алкильную группу или C1-C4-алкокси-группу; R3 представляет собой атом водорода или атом хлора; R4 представляет собой атом фтора, гидроксиметильную группу или гидроксильную группу; R5 и R6 каждый независимо друг от друга представляет собой атом водорода, атом фтора, C1-C3-галогеналкильную группу, карбоксильную группу, метоксикарбонильную группу, этоксикарбонильную группу, C1-C4-алкокси-группу, гидроксильную группу или C2-C5-алкилкарбонилокси-группу, или необязательно вместе образуют оксо-группу; R7 и R8 каждый независимо друг от друга представляет собой атом водорода или атом фтора; Y представляет собой атом кислорода или атом серы; Z представляет собой атом азота или метиновую группу.
В описанном выше циклогексановом производном предпочтительно, чтобы каждый заместитель R1 и R2 независимо друг от друга представлял собой трифторметильную группу, метильную группу или метокси-группу, и более предпочтительно, чтобы R3 представлял собой атом водорода; R4 представлял собой гидроксиметильную группу или гидроксильную группу; каждый заместитель R5 и R6 независимо друг от друга представлял собой атом водорода, атом фтора, трифторметильную группу, карбоксильную группу, метокси-группу, гидроксильную группу или ацетилокси-группу (или необязательно вместе могут образовывать оксо-группу).
Эффекты изобретения
Циклогексановое производное или его фармацевтически приемлемая соль или пролекарство в соответствии с настоящим изобретением проявляют заметное обезболивающее действие на фибромиалгию.
Краткое описание чертежей
ФИГ. 1 показывает действие циклогексанового производного в соответствии с настоящим изобретением на экспериментальной модели фибромиалгии на крысах (пероральное введение).
Способ осуществления изобретения
Терапевтическое средство или профилактическое средство для лечения фибромиалгии настоящего изобретения отличается содержанием в качестве эффективного ингредиента циклогексанового производного формулы (I):
,
где А представляет собой заместитель, представленный приведенными ниже формулами (IIa) или (IIb):
;
R1 и R2 каждый независимо друг от друга представляет собой атом водорода, атом хлора, C1-C3-галогеналкильную группу, C1-C4-алкильную группу или C1-C4-алкокси-группу; R3 представляет собой атом водорода или атом хлора; R4 представляет собой атом фтора, гидроксиметильную группу или гидроксильную группу; R5 и R6 каждый независимо друг от друга представляет собой атом водорода, атом фтора, C1-C3-галогеналкильную группу, карбоксильную группу, метоксикарбонильную группу, этоксикарбонильную группу, C1-C4-алкокси-группу, гидроксильную группу или C2-C5-алкилкарбонилокси-группу; или R5 и R6 необязательно вместе могут образовывать оксо-группу; R7 и R8 каждый независимо друг от друга представляет собой атом водорода или атом фтора; Y представляет собой атом кислорода или атом серы; и Z представляет собой атом азота или метиновую группу,
или его фармацевтически приемлемой соли или пролекарства.
Определение «С1-С4-алкильная группа» означает линейную, разветвленную или циклическую алкильную группу, содержащую от 1 до 4 атомов углерода, и ее примеры включают метильную группу, этильную группу, н-пропильную группу, изопропильную группу, циклопропильную группу, циклопропилметильную группу, н-бутильную группу, втор-бутильную группу и трет-бутильную группу.
Определение «С1-С4-алкокси-группа» означает линейную, разветвленную или циклическую алкилокси-группу, содержащую от 1 до 4 атомов углерода, и ее примеры включают метокси-группу, этокси-группу, н-пропилокси-группу, изопропилокси-группу, циклопропилокси-группу, н-бутокси-группу, втор-бутокси-группу и трет-бутокси-группу.
Определение «С1-С3-галогеналкильная группа» означает линейную алкильную группу, содержащую от 1 до 3 атомов углерода, где часть или все атомы водорода группы заменены атомом(ами) галогена (атом галогена означает атом фтора, атом хлора, атом брома или атом йода), и ее примеры включают монохлорметильную группу, монофторметильную группу, дифтор-метильную группу, трифторметильную группу, трихлорметильную группу и пентафторэтильную группу.
Примеры «С2-С5-алкилкарбонилокси-группы» включают ацетилокси-группу, этаноилокси-группу, пропаноилокси-группу, изопропаноилокси-группу, бутаноилокси-группу, изобутаноилокси-группу и пивалоилокси-группу.
В формуле (I) А предпочтительно представляет собой формулу (IIa); Y предпочтительно представляет собой атом кислорода; и Z предпочтительно представляет собой метиновую группу.
Заместитель R1 предпочтительно представляет собой атом водорода, атом хлора, трифторметильную группу, метильную группу, этильную группу, н-пропильную группу, изопропильную группу, метокси-группу, этокси-группу, н-пропилокси-группу или изопропилокси-группу, более предпочтительно трифтометильную группу, метильную группу или метокси-группу, и еще более предпочтительно метильную группу.
Заместитель R2 предпочтительно представляет собой атом водорода, атом хлора, трифторметильную группу, метильную группу, этильную группу, н-пропильную группу, изопропильную группу, метокси-группу, этокси-группу, н-пропилокси-группу или изопропилокси-группу, и более предпочтительно метокси-группу.
Заместитель R3 предпочтительно представляет собой атом водорода; и R4 предпочтительно представляет собой гидроксиметильную группу или гидроксильную группу, и более предпочтительно гидроксильную группу.
Заместитель R5 предпочтительно представляет собой атом водорода, атом фтора, трифторметильную группу, карбоксильную группу, метокси-группу, этокси-группу, н-пропилокси-группу, изопропилокси-группу, гидроксильную группу, ацетилокси-группу, пропаноилокси-группу, бутаноилокси-группу или изобутаноилокси-группу, более предпочтительно атом водорода, гидроксильную группу или карбоксильную группу, и еще более предпочтительно гидроксильную группу.
Заместитель R6 предпочтительно представляет собой атом водорода, атом фтора, трифторметильную группу, карбоксильную группу, метокси-группу, этокси-группу, н-пропилокси-группу, изопропилокси-группу, гидроксильную группу, ацетилокси-группу, пропаноилокси-группу, бутаноилокси-группу или изобутаноилокси-группу, более предпочтительно атом водорода или гидроксильную группу, и еще более предпочтительно атом водорода. Заместители R5 и R6 необязательно вместе могут образовывать оксо-группу.
Заместители R7 и R8 каждый предпочтительно представляет собой атом водорода.
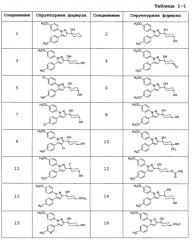
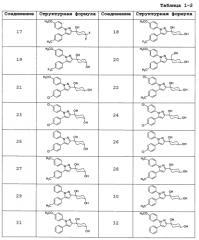
Среди соединений, представленных формулой (I), или их фармацевтически приемлемых солей (далее называемых «соединение (I)»), предпочтительные конкретные примеры представлены в таблице 1, но настоящее изобретение не ограничено ими.
В случаях, где соединение (I) имеет асимметричный(е) атом(ы) углерода, все его энантиомеры и смеси находятся в пределах объема настоящего изобретения.
В случаях, где соединение (I) имеет стереоизомер(ы), все его стереоизомеры и смеси также находятся в пределах объема настоящего изобретения.
Примеры «фармацевтически приемлемой соли» включают соли неорганических кислот, такие как солянокислая соль, сернокислая соль, фосфорнокислая соль и соль бромисто-водородной кислоты; соли органических кислот, такие как щавелевокислая соль, малоновокислая соль, лимоннокислая соль, фумаровокислая соль, молочнокислая соль, яблочнокислая соль, янтарнокислая соль, виннокислая соль, уксуснокислая соль, трифторуксуснокислая соль, малеиновокислая соль, глюконовокислая соль, бензойнокислая соль, аскорбиновокислая соль, соль метансульфоновой кислоты, соль п-толуолсульфоновой кислоты и соль коричной кислоты; соли неорганических оснований, такие как натриевая соль, калиевая соль, кальциевая соль, магниевая соль и аммонийная соль; и соли органических оснований, такие как метиламинная соль, диэтиламинная соль, триметиламинная соль, триэтиламинная соль, пиридиниевая соль, триэтаноламинная соль, этилендиаминная соль и гуанидиновая соль. Кроме того, соединение (I) может образовывать гидрат или сольват, и также в соединение (I) входят кристаллические полиморфы.
Соединение (I) может быть синтезировано, например, в соответствии со способами получения, описанными ниже. Символы в каждой реакционной формуле имеют такие же значения, что и определенные выше, если не указано другое значение.
В случаях, где исходное соединение имеет карбоксильную группу или гидроксильную группу, защитная группа, как это обычно используется, может быть введена в соединение, и защитная группа может быть снята, как это необходимо, после проведения реакции. Примеры защитной группы для гидроксильной группы включают С1-С4-алкильную группу, фенильную группу, тритильную группу, С1-С4-аралкильную группу (например, бензильную группу), ацильную группу (например, формильную группу, ацетильную группу или бензоильную группу), С7-С10-аралкилкарбонильную группу (например, бензилкарбонильную группу) и замещенную силильную группу (например, триметил-силильную группу, триэтилсилильную группу или трет-бутил-диметилсилильную группу). Примеры защитной группы для карбоксильной группы включают С1-С4-алкильную группу.
Способы снятия защитной группы меняются в зависимости от типа защитной группы, и снятие может быть проведено в соответствии со способом, который описан в документе предшествующего уровня техники (Protective groups in organic synthesis, Wiley-Interscience), или способом, аналогичным такому способу.
В описанных ниже способах получения в качестве исходного соединения может быть использована соль. Примеры солей включают те же соли, что и фармацевтически приемлемые соли, описанные выше.
Соединение (I), полученное способами получения, описанными ниже, может быть выделено и очищено в соответствии с известными средствами, и примеры известных средств включают экстракцию растворителем, перекристаллизацию и хроматографию.
В случаях, где соединение (I) имеет оптические изомеры, стереоизомеры, региоизомеры и/или ротамеры, каждый из них может быть получен в виде единственного соединения известным способом синтеза и известным методом разделения.
Способ получения 1: Способ получения соединения (Ic), соединения (Id), соединения (Ie) и соединения (If)
[где заместители R5a и R6a каждый независимо друг от друга представляет собой атом водорода, С1-С3-галогеналкильную группу, карбоксильную группу или подобную группу; заместители R7 и R8 каждый независимо друг от друга представляет собой С1-С4-алкильную группу или подобную группу; а другие символы имеют те же значения, что и определенные выше].
Соединение (Ic) может быть получено алкилированием соединения (Ia) и соединение (Id) может быть получено алкилированием соединения (Ib). Соединение (Ie) может быть получено ацилированием соединения (Ia) и соединение (If) может быть получено ацилированием соединения (Ib).
Стадия 1 и стадия 2
Реакцию алкилирования соединения (Ia) или соединения (Ib) обычно проводят путем введения в реакцию соединения (Ia) или соединения (Ib) с алкилгалогенидом в растворителе в присутствии основания. В качестве растворителя соответствующим образом выбирают растворитель, который не ингибирует реакцию. Примеры растворителя, который не ингибирует реакцию, включают простые эфиры, такие как тетрагидрофуран, 1,4-диоксан и диметиловый эфир этиленгликоля; ацетон, ацетонитрил и N,N-диметилформамид. В качестве растворителя также может быть использован их смешанный растворитель.
Примеры основания включают гидрокарбонаты щелочного металла, такие как гидрокарбонат натрия и гидрокарбонат калия; карбонаты щелочного металла, такие как карбонат калия и карбонат цезия; амины, такие как триэтиламин, диизопропил-этиламин и пиридин; трет-бутоксид калия; и гидрид натрия.
Количество используемого основания предпочтительно составляет от 0,5 до 6 молей, более предпочтительно от 0,8 до 3 молей из расчета на 1 моль соединения (Ia) или соединения (Ib).
Количество используемого алкилгалогенида предпочтительно составляет от 0,5 до 5 молей, более предпочтительно от 0,8 до 2 молей из расчета на 1 моль соединения (Ia) или соединения (Ib).
Реакционная температура процесса алкилирования предпочтительно составляет от -78 до 200°С, более предпочтительно от -20 до 100°С.
Реакционное время процесса алкилирования меняется в зависимости от реакционных условий и предпочтительно составляет от 5 минут до 78 часов, более предпочтительно от 30 минут до 48 часов.
Стадия 3 и стадия 4
Реакцию ацилирования соединения (Ia) или соединения (Ib) обычно проводят путем введения в реакцию соединения (Ia) или соединения (Ib) с ацилирующим агентом, таким как галогенангидрид или ангидрид кислоты, в растворителе в присутствии основания. В качестве растворителя соответствующим образом выбирают растворитель, который не ингибирует реакцию. Примеры растворителя, который не ингибирует реакцию, включают галогенированные углеводороды, такие как дихлорметан, хлороформ, тетрахлорид углерода и 1,2-дихлорэтан; и простые эфиры, такие как тетрагидрофуран, 1,2-диметоксиэтан и 1,4-диоксан. В качестве растворителя также может быть использован их смешанный растворитель.
Примеры основания включают пиридин, триэтиламин, диизопропилэтиламин, N,N-диметиламинопиридин и подобные соединения.
Количество используемого галогенангидрида или ангидрида кислоты предпочтительно составляет от 0,5 до 3 молей, более предпочтительно от 0,8 до 1,5 молей из расчета на 1 моль соединения (Ia) или соединения (Ib).
Количество используемого основания предпочтительно составляет от 0,1 до 6 молей, более предпочтительно от 0,8 до 3 молей из расчета на 1 моль соединения (Ia) или соединения (Ib).
Реакционная температура процесса ацилирования предпочтительно составляет от -20 до 150°С, более предпочтительно от 0 до 100°С.
Реакционное время процесса ацилирования меняется в зависимости от реакционных условий и предпочтительно составляет от 5 минут до 72 часов, более предпочтительно от 30 минут до 48 часов.
Способ получения 2: Способ получения соединения (Ih)
где заместители R5a и R6a каждый независимо друг от друга представляет собой атом водорода, атом фтора, С1-С3-галоген-алкильную группу, С1-С4-алкокси-группу, С2-С5-алкилкарбонилокси-группу или подобную группу; а другие символы имеют те же значения, что и определенные выше.
Соединение (Ih) может быть получено фторированием соединения (Ig).
Стадия 5
Реакцию фторирования соединения (Ig) обычно проводят путем введения в реакцию соединения (Ig) с фторирующим агентом в растворителе. В качестве растворителя соответствующим образом выбирают растворитель, который не ингибирует реакцию. Примеры растворителя, который не ингибирует реакцию, включают углеводороды, такие как октан, гексан, бензол и толуол; галогенированные углеводороды, такие как дихлорметан, хлороформ, тетрахлорид углерода и 1,2-дихлорэтан; простые эфиры, такие как тетрагидрофуран, 1,2-диметоксиэтан и 1,4-диоксан; и алкилнитрилы, такие как ацетонитрил. В качестве растворителя также может быть использован их смешанный растворитель.
Примеры фторирующего агента включают алкиламиносера-трифториды, такие как (диметиламино)сератрифторид (DAST) и бис(2-метоксиэтил)аминосератрифторид.
Количество используемого фторирующего агента предпочтительно составляет от 0,25 до 20 молей, более предпочтительно от 0,5 до 4 молей из расчета на 1 моль соединения (Ig).
Реакционная температура процесса фторирования предпочтительно составляет от -20 до 150°С, более предпочтительно от 0 до 100°С.
Реакционное время процесса фторирования меняется в зависимости от реакционных условий и предпочтительно составляет от 5 минут до 72 часов, более предпочтительно от 30 минут до 48 часов.
Способ получения 3: Способ получения соединения (Ij)
где символы имеют те же значения, что и определенные выше.
Соединение (Ij) может быть получено фторированием соединения (Ii).
Стадия 6
Реакцию фторирования соединения (Ii) обычно проводят путем введения в реакцию соединения (Ii) с фторирующим агентом в растворителе. В качестве растворителя соответствующим образом выбирают растворитель, который не ингибирует реакцию. Примеры растворителя, который не ингибирует реакцию, включают углеводороды, такие как октан, гексан, бензол и толуол; галогенированные углеводороды, такие как дихлорметан, хлороформ, тетрахлорид углерода и 1,2-дихлорэтан; простые эфиры, такие как тетрагидрофуран, 1,2-диметоксиэтан и 1,4-диоксан; и алкилнитрилы, такие как ацетонитрил. С другой стороны, в качестве растворителя может быть использован их смешанный растворитель.
Примеры фторирующего агента включают алкиламиносера-трифториды, такие как (диметиламино)сератрифторид (DAST) и бис(2-метоксиэтил)аминосератрифторид.
Количество используемого фторирующего агента предпочтительно составляет от 0,25 до 20 молей, более предпочтительно от 0,5 до 4 молей из расчета на 1 моль соединения (Ii).
Реакционная температура процесса фторирования предпочтительно составляет от -20 до 150°С, более предпочтительно от 0 до 100°С.
Реакционное время процесса фторирования меняется в зависимости от реакционных условий и предпочтительно составляет от 5 минут до 72 часов, более предпочтительно от 30 минут до 48 часов.
Способ получения 4: Способ получения соединения (Ik) и соединения (Il)
где символы имеют те же значения, что и определенные выше.
Соединение (Ik) и соединение (Il) могут быть получены восстановлением соединения (Ii).
Стадия 7
Реакцию восстановления соединения (Ii) обычно проводят путем введения в реакцию соединения (Ii) с восстанавливающим агентом в растворителе. В качестве растворителя соответствующим образом выбирают растворитель, который не ингибирует реакцию. Примеры растворителя, который не ингибирует реакцию, включают углеводороды, такие как октан, гексан, бензол и толуол; простые эфиры, такие как тетрагидрофуран, 1,4-диоксан, диметиловый эфир этиленгликоля и диэтиловый эфир; и спирты, такие как метанол, этанол и изопропиловый спирт. В качестве растворителя также может быть использован их смешанный растворитель.
Примеры восстанавливающего агента включают боргидрид натрия, боргидрид лития, гидрид диизобутилалюминия, алюминийгидрид лития, триэтилгидрид лития, бис(2-метоксиэтокси)алюминийгидрид натрия и борановые комплексы.
Количество используемого восстанавливающего агента предпочтительно составляет от 0,25 до 100 молей, более предпочтительно от 0,5 до 20 молей из расчета на 1 моль соединения (Ii).
Реакционная температура процесса восстановления предпочтительно составляет от -78 до 150°С, более предпочтительно от -78 до 100°С.
Реакционное время процесса восстановления меняется в зависимости от реакционных условий, таких как температура процесса, количество восстанавливающего агента и т.д., и предпочтительно составляет от 5 минут до 72 часов, более предпочтительно от 30 минут до 24 часов.
Способ получения 5: Способ получения соединения (Im) и соединения (In)
где символы имеют те же значения, что и определенные выше.
Соединение (Im) и соединение (In) могут быть получены трифторметилированием соединения (Ii).
Стадия 8
Примеры трифторметилирующего агента включают кремнийорганические соединения, такие как (трифторметил)-триметилсилан. Реакция трифторметилирования с использованием кремнийорганического соединения может быть проведена в соответствии со способом, описанным в документе предшествующего уровня техники (Journal of the American Chemical Society, 1989, Vol. 39, pp. 393-395), или аналогичным способом.
Способ получения 6: Способ получения соединения (Io)
где символы имеют те же значения, что и определенные выше.
Соединение (SI) может быть получено, если дать возможность реагенту Виттига (LI) подействовать на соединение (Ii), а затем гидролизовать полученное соединение. В качестве реагента Виттига можно использовать коммерчески доступные соединения, или реагент может быть синтезирован в соответствии со способом, очевидным для специалиста в данной области техники. Соединение (Io) может быть получено окислением соединения (SI).
Стадия 9
Реакцию Виттига соединения (Ii) обычно проводят путем введения в реакцию соединения (Ii) с реагентом Виттига в растворителе в присутствии основания. В качестве растворителя соответствующим образом выбирают растворитель, который не ингибирует реакцию. Примеры растворителя, который не ингибирует реакцию, включают углеводороды, такие как октан, гексан, бензол и толуол; и простые эфиры, такие как тетрагидрофуран, 1,4-диоксан, диметиловый эфир этиленгликоля и диэтиловый эфир. В качестве растворителя также может быть использован их смешанный растворитель.
Примеры основания включают диизопропиламид лития, трет-бутоксид калия, гидрид натрия, фениллитий и трет-бутиллитий.
Количество используемого основания предпочтительно составляет от 0,5 до 3 молей, более предпочтительно от 0,8 до 2 молей из расчета на 1 моль соединения (Ii).
Количество используемого соединения (LI) предпочтительно составляет от 0,5 до 3 молей, более предпочтительно от 0,8 до 2 молей из расчета на 1 моль соединения (Ii).
Температура реакции Виттига предпочтительно составляет от -78 до 100°С, более предпочтительно от -78 до 50°С.
Время реакции Виттига меняется в зависимости от реакционных условий, таких как температура процесса, и предпочтительно составляет от 5 минут до 48 часов, более предпочтительно от 30 минут до 24 часов.
Реакцию гидролиза для получения соединения (SI) проводят в соответствующим образом выбранном растворителе, который не ингибирует реакцию. Примеры растворителя, который не ингибирует реакцию, включают простые эфиры, такие как тетрагидрофуран, 1,4-диоксан и диметиловый эфир этиленгликоля; спирты, такие как метанол, этанол и трет-бутанол; ацетонитрил; и воду. В качестве растворителя также может быть использован их смешанный растворитель.
Концентрация кислоты, которую используют в реакции гидролиза, предпочтительно составляет от 0,1 до 12 М, и количество используемой кислоты предпочтительно составляет от 1 моля до избыточного количества из расчета на 1 моль соединения (Ii).
Примерами кислоты, которую используют в реакции гидролиза, являются неорганические кислоты, такие как соляная кислота и серная кислота; и органические кислоты, такие как уксусная кислота.
Реакционная температура процесса гидролиза предпочтительно составляет от -20 до 200°С, более предпочтительно от 0 до 100°С.
Реакционное время процесса гидролиза меняется в зависимости от реакционных условий и предпочтительно составляет от 5 минут до 48 часов, более предпочтительно от 30 минут до 24 часов.
Стадия 10
Примеры окисляющего агента, который используют в реакции окисления соединения (SI), включают (оксид хрома(VI))-(уксусная кислота), реагент Джонса, хлорит натрия и подобные агенты. Реакция окисления может быть проведена в соответствии со способом, очевидным для специалиста в данной области техники.
Способ получения 7: Способ получения соединения (Ii)
где заместители R9 и R10 каждый независимо друг от друга представляет собой метильную группу, этильную группу, н-пропильную группу, изопропильную группу, н-бутильную группу, втор-бутильную группу или трет-бутильную группу или подобные группы; или заместители R9 и R10 могут вместе образовывать этиленовую группу (-СН2-СН2-), пропиленовую группу (-СН2-СН2-СН2-) или подобные группы; а другие символы имеют те же значения, что и определенные выше.
Соединение (Ii) может быть получено путем снятия защитной группы соединения (Ip).
Стадия 11
Реакция снятия защитной группы соединения (Ip) может быть проведена в соответствии со способом, который описан в документе предшествующего уровня техники (Protective groups in organic synthesis, Wiley-Interscience), или аналогичным способом.
Способ получения 8: Способ получения соединения (IIIb)
где символы имеют те же значения, что и определенные выше.
Соединение (IIIb) может быть получено путем хлорирования соединения (IIIa).
Стадия 12
Реакцию хлорирования соединения (IIIa) обычно проводят путем введения в реакцию соединения (IIIa) с хлорирующим агентом в растворителе. В качестве растворителя соответствующим образом выбирают растворитель, который не ингибирует реакцию. Примеры растворителя, который не ингибирует реакцию, включают галогенированные углеводороды, такие как дихлорметан, хлороформ, тетрахлорид углерода и 1,2-дихлорэтан; ацетонитрил; и этилацетат. В качестве растворителя также может быть использован их смешанный растворитель.
Примеры хлорирующего агента включают N-хлорсукцинимид (NCS).
Количество используемого хлорирующего агента предпочтительно составляет от 0,5 до 2 молей, более предпочтительно от 0,8 до 1,2 молей из расчета на 1 моль соединения (IIIa).
Реакционная температура процесса хлорирования предпочтительно составляет от 0 до 200°С, более предпочтительно от 0 до 120°С.
Реакционное время процесса хлорирования меняется в зависимости от реакционных условий, таких как температура процесса, и предпочтительно составляет от 5 минут до 72 часов, более предпочтительно от 30 минут до 48 часов.
Способ получения 9: Способ получения соединения (IIIa)
где символы имеют те же значения, что и определенные выше.
Соединение (IIIa) может быть получено циклизацией соединения (LII) с помощью соединения (SII). В качестве соединения (LII) можно использовать коммерчески доступное соединение, или это соединение может быть синтезировано способом, очевидным для специалиста в данной области техники.
Стадия 13
Реакцию циклизации соединения (LII) с помощью соединения (SII) обычно проводят в, соответствующим образом выбранном, растворителе, который не ингибирует реакцию. Примеры растворителя, который не ингибирует реакцию, включают спирты, такие как метанол, этанол и изопропиловый спирт; галогенированные углеводороды, такие как дихлорметан, хлороформ, тетрахлорид углерода и 1,2-дихлорэтан; простые эфиры, такие как тетрагидрофуран, 1,2-диметоксиэтан и 1,4-диоксан; бензол; толуол; уксусную кислоту и воду. В качестве растворителя также может быть использован их смешанный растворитель.
Количество используемого соединения (LII) предпочтительно составляет от 0,5 до 1,5 молей, более предпочтительно от 0,8 до 1,2 молей из расчета на 1 моль соединения (SII).
В реакции циклизации может быть использован катализатор, и примеры катализатора включают органические основания, такие как триэтиламин и пиридин; неорганические кислоты, такие как соляная кислота и серная кислота; и органические кислоты, такие как уксусная кислота.
Количество используемого катализатора предпочтительно составляет от 0,1 до 3 молей из расчета на 1 моль соединения (SII).
Реакционная температура процесса циклизации предпочтительно составляет от 0 до 200°С, более предпочтительно от 0 до 120°С.
Реакционное время процесса циклизации меняется в зависимости от реакционных условий, таких как температура процесса, и предпочтительно составляет от 5 минут до 72 часов, более предпочтительно от 30 минут до 48 часов.
Способ получения 10: Способ получения соединения (IV)
где символы имеют те же значения, что и определенные выше.
Соединение (IV) может быть получено путем снятия защитной группы и окисления соединения (SIII). Реакция окисления может быть проведена в соответствии со способом, описанным в документе предшествующего уровня техники (Tetrahedron, 1989, Vol. 45, pp. 5703-5742), или аналогичным способом.
Стадия 14
Реакцию снятия защитной группы и реакцию окисления соединения (SIII) обычно проводят путем введения в реакцию соединения (SIII) с основанием и окисляющим агентом в безводном растворителе. В качестве растворителя соответствующим образом выбирают растворитель, который не ингибирует реакции. Примеры растворителя, который не ингибирует реакции, включают углеводороды, такие как октан, гексан и гептан; и простые эфиры, такие как тетрагидрофуран, 1,4-диоксан, диметиловый эфир этиленгликоля и диэтиловый эфир. В качестве растворителя также может быть использован их смешанный растворитель.
Примеры основания включают бутиллитии, такие как н-бутил-литий, втор-бутиллитий и трет-бутиллитий.
Количество используемого основания предпочтительно составляет от 0,8 до 5 молей, более предпочтительно от 0,9 до 3 молей из расчета на 1 моль соединения (SIII).
Количество используемого соединения (LIII) предпочтительно составляет от 0,8 до 5 молей, более предпочтительно от 0,9 до 3 молей из расчета на 1 моль соединения (SIII).
Примеры окисляющего агента, который используют в реакции окисления, включают 3-фенил-2-(фенилсульфонил)-1,2-оксазиридин.
Реакционная температура процесса снятия защитной группы и реакции окисления предпочтительно составляет от -78 до 150°С, более предпочтительно от 0 до 50°С.
Реакционное время процесса снятия защитной группы и реакции окисления меняется в зависимости от реакционных условий и предпочтительно составляет от 5 минут до 72 часов, более предпочтительно от 30 минут до 48 часов.
Способ получения 11: Способ получения промежуточного соединения (VI)
где символы имеют те же значения, что и определенные выше.
Соединение (VI) может быть получено сольволизом соединения (V), которое получено введением в реакцию соединения (LIV) и соединения (LV). В качестве соединения (LIV) и соединения (LV) можно использовать коммерчески доступные соединения, или эти соединения могут быть синтезированы в соответствии со способами, очевидными для специалиста в данной области техники.
Стадия 15
Реакцию между соединением (LIV) и соединением (LV) обычно проводят в безводном растворителе в присутствии основания; и в качестве растворителя соответствующим образом выбирают растворитель,