Агломераты оксигидроксидов металлов и их применение
Иллюстрации
Показать всеИзобретение относится к области неорганической химии. Предложен продукт в виде агломератов оксигидроксидов металлов, выбранных из группы, состоящей из Al, Fe, Mg, Ti или их смеси. Агломераты образованы множеством элементов, имеющих размеры от 200 до 500 нм и представляющих собой низкоразмерные складчатые структуры, имеющие складки и грани неправильной формы. Структуры обладают локально высоким уровнем напряженности электрического поля на упомянутых складках, гранях и ребрах граней, составляющим 106-107 В/м. Изобретение обеспечивает получение агломератов оксигидратов, которые могут быть использованы в качестве сорбентов или в качестве средства, обладающего ранозаживляющей и антибактериальной активностью, а также для угнетения пролиферативной активности опухолевых клеток. 4 н. и 10 з.п. ф-лы, 12 ил., 5 табл., 11 пр.
Реферат
Изобретение относится к области неорганической химии, а именно к оксигидроксидам металлов, синтезированных из металлов группы, состоящей из Al, Fe, Mg, Ti. Изобретение может быть использовано в биологии, фармакологии, биохимии, медицине и ветеринарии.
Известно использование нано- и микроструктурированных гидроксидов и оксигидроксидов в различных материалах и технологических процессах, в том числе в биологии и медицине.
Известен Способ получения усовершенствованного волокнистого фильтрующего материала [заявка RU №2011116705, опубл. 10.11.2012], в результате которого на поверхности волокнистого материала формируют слой из оксигидроксидов алюминия и кремния с положительным поверхностным зарядом. С этой целью приготовляли раствор алюмосиликагеля и осуществляли обработку волокнистого керамического материала полученным составом.
К недостаткам можно отнести то, что для создания положительного заряда поверхности используются известные свойства структурированного кремния, покрытия из которого создаются при обработке волокнистого керамического материала.
Известен наноразмерный электроположительный волокнистый адсорбент, раскрытый в [RU 2304463 С2, опубл. 20.08.2007], состоящий из несферических частиц гидроксида алюминия, в виде волокон с диаметром менее 50 нм и отношением длины к толщине более пяти к одному, полученный в результате преобразования исходного алюминиевого компонента в водном растворе при температуре до 100°С, и непосредственно нанесенный на поверхность волокнистой структуры, характеризующийся возможностью адсорбции, по крайней мере, одной электроотрицательной частицы из жидкости. Известен [RU 2328447 С1, опубл. 10.07.2008], в котором раскрыт способ получения волокон оксидно-гидроксидных фаз со структурой бемита, который может быть использован для получения адсорбентов для тонкой очистки питьевой воды, а также промышленных и сточных вод. Получение нановолокон оксидно-гидроксидных фаз алюминия осуществляют гидролизом порошка, полученного методом электрического взрыва алюминиевой проволоки диаметром 0,3<d≤0,4 мм в атмосфере азота при давлении Р<3 атм и значении энергии, введенной в проволоку, 19,8 Дж/мм3 <Е≤66 Дж/мм3. При этом последующий гидролиз порошка проводят при температуре не более 70°С. Полученные нановолокна оксидно-гидроксидных фаз алюминия имеют длину 0,1-0,2 мкм, диаметр 0,001-0,013 мкм и удельную поверхность до 500 м2/г. Известен также патент США [US 8,033,400 В2, опубл. 11.10.2011], в котором раскрыт фильтрующий материал, содержащий в качестве основы нетканое органическое синтетическое полотно и положительно заряженные агломераты нановолокон гидроксида алюминия. Известен [RU 2397781 С1, опубл.: 27.08.2010] Нетканый материал медицинского назначения, обладающий ранозаживляющей, антибактериальной и противовирусной активностью, и перевязочное средство на его основе, содержащий волокнистую основу на волокнах которого закреплены высокопористые частицы гидрата оксида алюминия, образованные нановолокнами. В работе [Н.А. Яворовский, Г.Г. Савельев, А.И. Галанов, Л.Н. Шиян, Т.А. Юрмазова, Г.Л. Лобанова. Получение нановолокон оксогидроксидов алюминия из порошков металлического алюминия // ПЕРСПЕКТИВНЫЕ МАТЕРИАЛЫ, 2008, №4, с. 74-80.] исследовалось окисление частиц алюминия с размером 20-500 нм в дистиллированной воде при исходной температуре 60°С с последующим саморазогревом реагирующей системы до 90-98°С. По данным РФА образец соответствует фазе псевдобемита (AlOOH) с примесями гиббсита (Al(ОН)3) и γ-Al2O3. По данным электронной микроскопии продукт окисления представляет собой нановолокона, имеющие толщину 5-8 нм и соотношение длины к толщине 50-100. Волокна агломерированы в виде обособленных рыхлых клубков с размерами 1-5 мкм. Удельная поверхность порошка после окисления и сушки составляет 350-370 м2/г.
В качестве недостатков известных вышеприведенных наноразмерных волокнистых сорбентов, раскрытых в [RU 2304463 С2 и RU 2328447 С1, RU 2397781 С1, US 8033400 В2] и работе [Н.А. Яворовский, Г.Г. Савельев, А.И. Галанов, Л.Н. Шиян, Т.А. Юрмазова, Г.Л. Лобанова. Получение нановолокон оксогидроксидов алюминия из порошков металлического алюминия // ПЕРСПЕКТИВНЫЕ МАТЕРИАЛЫ, 2008, №4, с. 74-80.] можно отнести относительно низкую сорбционную емкость, обусловленную формой и расположением волокон или нановолокон. Это подтверждают данные приведенные в статье Tepper Fred and Kaledin Leonid «Virus and Protein Separation Using Nano Alumina Fiber Media», http://www.argonide.com/publications/laboratory.pdf. В статье приведены микрофотографии нановолокон, которые формируют плотноупакованные структуры. Вследствие этого, поровое пространство сорбционного материала, состоящего из нановолокон, менее доступно для сорбата (бактерий, коллоидных частиц и т.д.), чем поровое пространство агломератов низкоразмерных складчатых структур. Кроме того, на микрофотографиях видно, что сорбция коллоидных частиц, в основном, происходит на торцах нановолокон. При этом коллоидные частицы не сорбируются между нановолокнами в объеме материала. Таким образом, нановолокна с достаточно высокой удельной поверхностью обладают небольшой сорбционной емкостью по сравнению с агломератами низкоразмерных складчатых структур.
В работе [Ларичев М.Н., Шайтура И.С., Колокольников В.Н., Ларичева О.О., Школьников Е.И., Артемов В.В. Получение наноструктурных продуктов при окислении микронного порошка алюминия водой в ультразвуковом поле // Перспективные материалы, 2010, с. 290-294.] исследовался процесс гидролиза порошков алюминия марки порошок АСД-4, серийно производимый российской промышленностью, со средним размером частиц около 4 мкм. Окисление алюминия изучалось в дистиллированной воде и в водном насыщенном растворе Са(ОН)2 (буферный активатор) в присутствии и отсутствии УЗ поля. Без наложения ультразвукового поля степень окисления АСД-4 дистиллированной водой за разумное время (нескольких суток) не превышает 30%. На поверхности исходных частиц алюминия образуется ячеистая структура из продуктов окисления. Применение ультразвуковой активации в сочетании с буферной позволяет существенно изменить процесс, степень окисления достигает 100%. При этом образуются наноразмерные палочкообразые структуры. Удельная поверхность таких продуктов (измеренная методом БЭТ) составляет всего 40 м2/г.
Критика: В процессе были синтезированы палочкобразные структуры с низкой удельной поверхностью, поэтому следует ожидать, что сорбционные свойства таких частиц невелики.
Также в статье не указанно, способны ли полученные нановолокна формировать электрическое поле в водных средах.
Известен процесс приготовления адсорбента, содержащего оксигидроксид железа - FeO(OH), адсорбент и его применение, раскрытый в [WO 2006032727 (А1), опубл. 2006-03-30]. Изобретение относится к процессам для приготовления адсорбционных материалов. Процесс для производства адсорбента, содержащего оксигидроксид железа, характеризуется тем, производят гранулированный гидроксид железа который включает в количестве 5-15% по массе, имеющей влагу, в расчете на массу адсорбента. И где упомянутая масса гранулирована компактированием и просеиванием компактированного продукта, чтобы получить гранулы размером от 0.5 до 4 мм.
Раскрытый адсорбент представляет собой гранулы с размером между 0,5 и 4,0 мм. Гранулы такого размера не будут создавать электрическое поле с высокой напряженностью, необходимой для эффективной сорбции заряженных частиц и воздействия на клеточные мембраны.
Известен СПОСОБ ПОЛУЧЕНИЯ БИОПРЕПАРАТА “ФЕРРИГЕЛЬ” [RU 2466713, опубл. 20.11.2012] на основе наноразмерного оксигидроксида железа. Способ получения биопрепарата включает смешивание оксигидроксида железа, выделенного на станциях обезжелезивания подземных вод, с водорастворимым полимером и глицерином.
В описании к патенту не указана форма частиц оксигидроксида железа, и не обсуждается с какими свойствами связана их биологическая активность, выражающаяся в ускоренном ранозаживлении. Кроме того, смешивание частиц с водорастворимыми полимерами и глицерином приведет к обволакиванию частиц оксигидроксида железа указанными веществами и блокированию значительной части поверхности доступной для воздействия на биологические объекты.
В патенте [RU 2270663 С2, опубл. 27.02.2006] представлен способ терапии пролиферативных раковых клеток организма, включающий выбор биологически активных точек и последующее воздействие на них, отличающийся тем, что выбирают биологически активную точку, соответствующую органу с патологической пролиферацией клеток, измеряют потенциал выбранной биологически активной точки относительно референтной точки, после чего к выбранным точкам подключают внешний источник постоянного электрического поля, полюса которого противоположны по знаку полюсам точек, к которым его подключают, а абсолютная его величина равна разности абсолютных величин измеренного потенциала и потенциала, соответствующего здоровому органу в выбранной точке, и воздействуют до значения величины мембранного потенциала раковой клетки, равного величине мембранного потенциала соответствующего здорового органа. Таким образом, происходит нормализация биохимических процессов клеток, что приводит к существенному снижению патологической активности раковых клеток, а в пределе - к их возврату в нормальное состояние. В патенте [RU 2253903, опубл. 10.06.2005] предложен способ блокирования деления раковых клеток, включающий воздействие на клетку или группу клеток внешнего источника энергии, отличающийся тем, что перед воздействием вводят, по меньшей мере, два электрода, один из которых - на цитоплазматическую поверхность мембраны клетки, а другой - на наружную поверхность мембраны клетки и измеряют значение мембранного потенциала, после чего к введенным электродам подключают противоположно по полярности внешний источник ЭДС со значением разности потенциалов не меньше значения мембранного потенциала клетки.
Предлагаемые в патентах RU 2270663 и RU 2253903 способы подавления пролиферативной активности раковых клеток основаны на воздействие электрического потенциала на мембраны клеток при введении в опухоль электродов. Эти способы сложны и травматичны. Кроме того, будет подавляться только рост клеток непосредственно контактирующих с поверхностью электродов. Клетки опухоли, не контактирующие с потенциальными электродами, будут активны.
Как можно видеть из вышеприведенных аналогов оксигидроксиды металлов используются как в процессах сорбции, так и в медицине для ранозаживления. Также существуют методы блокирования деления раковых клеток путем изменения их мембранного потенциала при воздействии электрического поля. Однако в настоящее время существует особая потребность в материалах, имеющих как более высокий уровень сорбционной емкости, так и более высокий уровень биологической активности.
Задачей настоящего изобретения является создание локально высокого уровня напряженности электрического поля у частиц оксигидроксидов, синтезированных из металлов группы Al, Fe, Mg, Ti или их композитов, за счет геометрической формы и размерных параметров.
Другой задачей настоящего изобретения является использование упомянутых выше частиц в качестве сорбентов биологических объектов, неорганических коллоидных частиц и ионов металлов.
Еще одной задачей настоящего изобретения является использование упомянутых выше частиц в качестве ранозаживляющих и антибактериальных средств, а также лекарственных средств и изделий на их основе.
Еще одной задачей настоящего изобретения является использование упомянутых выше частиц для подавления пролиферации раковых клеток, а также их применение в составе противоопухолевых средств.
Поставленная задача достигается тем, что разработанный продукт состоит из агломератов оксигидроксидов металлов или композитов, по меньшей мере, двух оксигидроксидов металлов, выбранных из группы металлов, состоящей из Al, Fe, Mg, Ti.
При этом упомянутые агломераты образованны множеством элементов, представляющих собой низкоразмерные складчатые структуры, имеющие складки и грани неправильной формы, и обладающие локально высоким уровнем напряженности электрического поля на упомянутых складках, гранях и ребрах граней.
Кроме того элементы агломератов, представляющие собой низкоразмерные складчатые структуры, имеют, по меньшей мере, один размер определяемый в нанометрах, предпочтительно поперечный размер (толщину) грани не более 10 нм.
Предпочтительно, что поперечный размер (толщину) грани имеет размер 5-8 нм, еще предпочтительней не более 2 нм.
Кроме того, отдельный элемент низкоразмерной складчатой структуры имеет размеры 200-500 нм.
Кроме того локальный уровень напряженности электрического поля, а именно на складках и гранях, образующих структуру агломерата составляет 106-107 В/м.
Кроме того, упомянутые агломераты имеют форму близкую к сферической.
Другая задача изобретения достигается тем, что упомянутые агломераты используют в качестве сорбентов органических частиц (молекулы, бактерии, вирусы, белки, антигены, эндотоксины) и неорганических частиц (ионы металлов, коллоиды).
Предпочтительно, что агломераты для вышеупомянутой сорбции применяют в водной среде, в интервале значений рН упомянутой среды от 5,0 до 9,5 и более предпочтительно в интервале значений рН водной среды от 6 до 8.
Еще одна задача изобретения достигается тем, что упомянутые агломераты применяют в качестве средства, обладающего ранозаживляющей и антибактериальной активностью.
И еще одна задача достигается тем, что упомянутые агломераты применяют для угнетения пролиферативной активности опухолевых клеток.
Упомянутые агломераты применяют либо самостоятельно, либо нанесенными на материал-носитель, выбранный из группы, состоящей из нетканых материалов, волокон, гранул, губок и других пористых материалов и сред, либо в составе композиции, состоящей из агломератов и веществ, обладающих фармакологическим и/или поглощающим действием.
Такое свойство, как высокий локальный уровень напряженности электрического поля, присущий заявляемым агломератам, обеспечивается:
- поверхностным зарядом, присущим оксигидроксидам металлов группы Al, Fe, Mg, Ti в водных средах и
- складчатой формой низкоразмерных структур, формирующих агломераты упомянутых оксигидроксидов металлов, вследствие малой толщины или радиуса кривизны ребер и складок электрически заряженных граней элементов, образующих агломераты.
В данном изобретении под оксидами и оксигидроксидами металлов понимают химические соединения, имеющие общую формулу AlOOH, Al2O3×nH2O, где n=0,8-3, FeOOH, Fe2O3, Fe3O4, TiO2, Mg(OH)2, MgO.
Известно [Савельев И.В. Курс общей физики, том II. Электричество // Издательство: «Наука», Москва, 1970, 501 с. ], что поверхностная плотность зарядов δ для заряженного тела, пропорциональна кривизне поверхности k, δ~k, где k~1/r (r - радиус кривизны). Соответственно максимальная плотность зарядов будет наблюдаться на ребрах граней и складках низкоразмерных складчатых структур, составляющих агломераты/агрегаты и имеющих максимальное значение k. Таким образом, вследствие малого радиуса кривизны поверхности электрически заряженных ребер граней и складок оксигидроксидов металлов, создается сильно неоднородное электрическое поле, действующее с силой F на заряженные частицы противоположного знака.
Под действием неоднородного электрического поля с локально высокой напряженностью на складках и ребрах граней агломератов, заряженные частицы движутся в сторону увеличения напряженности электрического поля, т.е. по градиенту модуля напряженности поля. Сила, действующая между зарядом q1 (заряд на гранях, ребрах и складах агломерата) и q2 (Заряд частицы сорбата), определяется законом Кулона:
где, х - расстояние между сорбентом и сорбатом.
С учетом рассчитанной толщины грани одного из элементов, формирующих складчатую структуру можно оценить напряженность ее электрического поля.
Напряженность электрического поля (мВ/нм):
где φ - потенциал агломерата, R - толщина грани.
Сила, действующая на заряженную частицу, находящуюся вблизи агломерата будет определяться выражением:
F=qE,
где q - заряд частицы [Савельев И.В. Курс общей физики, том II. Электричество].
Заявителями было рассчитано (см. примеры), что у непористых частиц правильной сферической формы напряженность приблизительно на 3 порядка меньше, чем на ребре грани складчатой структуры.
Соответственно, при q=const, сила, действующая на частицу, для агломерата, состоящего из низкоразмерных складчатых структур, будет в 600 раз больше, чем для компактных непористых сферических частиц аналогичного размера.
При применении частиц (агломератов), имеющих складчатую форму (фиг.1) и имеющих большое расстояние (до 50 нм) между элементами складчатой структуры образующих указанный агломерат, органические молекулы, ионы, микроорганизмы размером до 50 нм, (вирусы), могут проникать внутрь агломерата и удерживаться электрическим полем, возникающим как на гранях и складках, так и между элементами складчатой структуры.
Указанный выше эффект демонстрирует также фиг.5 и 6. Из фиг.5 и 6 видно, что дисперсные частицы латексные сферы (фиг.5) и частицы коллоидного серебра (рис. 6) сорбируются на гранях и проникают в объем агломерата, образованного складчатыми структурами. Таким образом, агломераты, образованные складчатыми структурами обладают большой сорбционной емкостью.
По данным разных авторов (см. например публикации Marino A., Ilev I., Schwaike M. Association between Cell Membrane Potential and Breast Cancer/Tumor Biol 1994; 15: 82-89; Steve Haltiwanger M.D. The Electrical Properties of Cancer Cells / http://www.royalrife.com/haltiwangerl.pdf) электрический потенциал нормальных клеток составляет минус 60…100 мВ, потенциал раковых клеток приблизительно равен минус 15…20 мВ. Когда нормальные клетки начинают деление их электрический потенциал падает до приблизительно до минус 15 мВ. При завершении деления клетки ее мембранный потенциал возвращается к естественному значению. По существующему мнению ключевым компонентом лечения рака было бы восстановление естественного мембранного потенциала и, как следствие, нормального метаболизма клеток. Таким образом регуляция потенциала клеточных мембран является одним из способов управления функциональным состоянием клеток.
При взаимодействии с клеточными мембранами, имеющими отрицательный заряд поверхности, положительно заряженные складчатые структуры будут притягиваться к поверхности клетки. При этом отрицательный заряд клеточной мембраны будет компенсироваться под воздействием положительного заряда складчатых структур. Увеличение потенциала клеточной мембраны, вследствие воздействия электроположительных складчатых структур, приведет с одной стороны к активному делению нормальных клеток и к ускоренному ранозаживлению, с другой, к подавлению пролиферации раковых клеток.
На фиг. 1 приведено ПЭМ-изображение агломерата оксигидроксида алюминия с заявляемой складчатой структурой и показаны ребра грани и складки: 1 - ребра грани, 2 - складки.
На фиг. 2 приведено СЭМ-изображение агломератов складчатых структур оксигидроксида алюминия.
На фиг. 3 приведены:
а) СЭМ-изображение агломератов складчатых структур оксигидроксида железа;
б) СЭМ-изображение агломерата композита FeOOH/AlOOH.
На фиг. 4 приведено СЭМ-изображение агломератов складчатых структур оксида титана.
На фиг. 5 приведена микрофотография (ПЭМ-изображение) низкоразмерных структур Mg(OH)2, полученных с помощью просвечивающего микроскопа JEM 2100.
На фиг. 6 приведена микрофотография (ПЭМ-изображение) низкоразмерных структур композита Mg(OH)2/AlOOH, полученных с помощью просвечивающего микроскопа JEM 2100.
На фиг. 7 приведено ПЭМ-изображение агломератов складчатых структур с латексными сферами на ребрах граней и между складчатыми элементами агломерата оксигидроксида алюминия.
На фиг. 8 приведено ПЭМ-изображение агломератов складчатых структур с частицами коллоидного серебра на ребрах граней и между складчатыми элементами агломерата оксигидроксида алюминия.
На фиг. 9 приведены результаты экспериментов на клетках линии Hos: количество живых клеток Hos, %, в зависимости от содержания оксигидроксида алюминия в 2 мл среды роста: 1 - 0,005 г, 2 - 0,01 г, 3 - 0,03 г.
На фиг. 10 приведены результаты на клетках линий HELA, MCF-7, UM-SCC-14C: количество живых раковых клеток (%) через 24 часа (а) и через 48 часов (б).
На фиг. 11 приведены результаты на клетках линий HELA, MCF-7, UM-SCC-14C: пролиферация раковых клеток (%) через 24 часа (а) и через 48 часов (б).
На фиг. 12 приведены результаты экспериментов на клетках нейробластомы мыши линии Neuro-2a, количество живых клеток через 48 и 72 часа при воздействии низкоразмерных структур: К - контроль, 1 - оксид титана, 2 - гидроксид магния, 3 - композит железа/алюминия оксигидроксидов, 4 - композит магния/алюминия гидроксидов, 5 - оксигидроксид алюминия.
ПРИМЕРЫ КОНКРЕТНОГО ВЫПОЛНЕНИЯ
Пример 1. Получение агломерата электроположительных низкоразмерных складчатых структур оксигидроксида алюминия (AlOOH).
Для получения агломератов с заявляемой формой и характеристиками проводили реакцию взаимодействия с водой исходного сырья, в качестве которого использовали порошок состава Al/AlN, полученный методом электрического взрыва алюминиевой проволоки в атмосфере азота, с размером частиц 80-100 нм, удельной поверхностью 21 м /г и содержанием фазы AlN - 70% масс.
Для проведения реакции 100 г порошка заливали 10,0 л воды, добавляли наночастицы оксида алюминия со средним размером 70 нм, в количестве 0,1% масс относительно массы порошка, выступающих затравкой для увеличения скорости образования зародышей на частицах затравки и кристаллизации продуктов превращения, полученную суспензию нагревали от 25°C до 60°C при интенсивном перемешивании механической мешалкой при скорости 200 об/мин.
Реакцию проводили при pH=9,4 в течение 60 мин. до установления постоянного значения pH.
Полученный продукт - высушивали при температуре 90°C до постоянной массы в течение 4 часов.
Масса полученного продукта составила 150 г. Удельную поверхность продукта, измеренная на приборе «Сорбтометр-М», составила 330 м2/г. Рентгенофазовый анализ проведенный с помощью дифрактометра ДРОН-7 показал, что продукт представляет собой AlOOH.
На фиг. 1 приведена микрофотография агломератов низкоразмерных складчатых структур оксигидроксида алюминия, полученных с помощью просвечивающего микроскопа JEM 2100, которая демонстрирует наличие граней и складок.
На фиг. 2 приведена микрофотография агломератов низкоразмерных складчатых структур, полученных с помощью сканирующего микроскопа LEO EVO 50.
Размер агломератов составил от 0,5 мкм до 7 (в среднем 3,0 мкм), размер отдельного элемента складчатой структуры составил - в среднем 250 нм. Толщина грани- в среднем 5 нм.
Дзета-потенциал агломератов определялся с помощью прибора ZetaSizer Nano ZS и составил около 60 мВ. С учетом толщины граней в среднем 5 нм можно оценить напряженность электрического поля на ребре грани. Напряженность электрического поля:
где φ - потенциал агломерата, R - толщина грани.
Напряженность электрического поля на ребре грани составляет Е=12 мВ/нм или 1,2·107 В/м. Напряженность электрического поля на поверхности непористой сферической частицы оксигидроксида алюминия размером 3 мкм составляла бы 20 мВ/мкм или 2·104 В/м, т.е. приблизительно на 3 порядка меньше, чем на ребре грани.
Сила, действующая на заряженную частицу, находящуюся вблизи агломерата будет определяться выражением:
F=qE,
где q - заряд частицы [Савельев И.В. Курс общей физики, том II. Электричество // Издательство: «Наука», Москва, 1970, 501 с].
Соответственно, при q=const, сила, действующая на частицу, для агломерата, состоящего из низкоразмерных складчатых структур, будет в 600 раз больше, чем для непористой сферической частицы с аналогичным размером и химическим составом.
Пример 2. Получение агломератов низкоразмерных складчатых структур оксигидроксида железа (FeOOH).
Для получения агломератов низкоразмерных складчатых структур оксигидроксида железа использовали биметаллические наночастицы Fe-Al с примесью алюминия не более 10% масс. Биметаллический нанопорошок Fe-Al с размером частиц около 100 нм получали параллельным электрическим взрывом железной и алюминиевой проволоки в атмосфере азота при соотношении Fe:Al=90:10% масс. 20 г порошка заливали 2000 мл дистиллированной воды и нагревали при постоянном перемешивании до 60°C. Контролировали и поддерживали pH реагирующей смеси на уровне 9,0 раствором аммиака. Реакцию проводили в течение 60 мин. Затем суспензию отфильтровывали, промывали дистиллированной водой до нейтральной реакции промывных вод и сушили при температуре 90°C в течение 4 часов.
Масса полученного продукта составила 25,4 г. Удельная поверхность продукта измерялась прибором «Сорбтометр-М» и составляла 220 м2/г. Рентгенофазовый анализ проведенный с помощью дифрактометра ДРОН-7 показал наличие в продукте, в основном, гетита FeOOH и небольшого содержания бемита AlOOH. Полученный продукт содержал примесь AlOOH в количестве не более 10% масс.
На фиг. 3 а приведена микрофотография агломерата FeOOH с примесью бемита AlOOH не более 10% масс, полученная с помощью сканирующего микроскопа LEO EVO 50, которая демонстрирует, что агломераты образованы из множества низкоразмерных складчатых структур.
Размер агломератов составлял от 1,0 мкм до 12,0 (в среднем 6,0 мкм). Дзета-потенциал агломератов определенный с помощью прибора ZetaSizer Nano ZS составил около 50 мВ. Размер отдельного элемента складчатой структуры составил - в среднем 500 нм, толщина грани - в среднем 2 нм.
Далее проводили расчеты, аналогичные указанным в примере 1. Напряженность электрического поля на торце (ребре см. пример 1 и 2)) грани составила E=2,5·107 В/м.
Для сравнения напряженность электрического поля на поверхности непористой сферической частицы с аналогичным химическим составом размером 1 мкм E=5·104 В/м.
Для получения агломератов композита FeOOH/AlOOH использовали биметаллические частицы Fe-Al с соотношением Fe/Al=50/50. Биметаллический нанопорошок Fe-Al с размером частиц около 100 нм получали параллельным электрическим взрывом железной и алюминиевой проволоки в атмосфере азота при соотношении Fe:Al=50:50% масс. 20 г порошка заливали 2000 мл дистиллированной воды и нагревали при постоянном перемешивании до 60°C. Контролировали и поддерживали pH реагирующей смеси на уровне 9,0 раствором аммиака. Реакцию проводили в течение 60 мин. Затем суспензию отфильтровывали, промывали дистиллированной водой до нейтральной реакции промывных вод и сушили при температуре 90°C в течение 4 часов.
Масса полученного продукта составила 27,1 г. Удельная поверхность продукта измерялась прибором «Сорбтометр-М» и составляла 253 м2/г. Рентгенофазовый анализ проведенный с помощью дифрактометра ДРОН-7 показал наличие в продукте гетита FeOOH, интерметаллидов и бемита AlOOH.
На фиг. 3б приведена микрофотография агломерата композита FeOOH/AlOOH, полученная с помощью сканирующего микроскопа LEO EVO 50, которая демонстрирует, что агломераты образованы из множества низкоразмерных складчатых структур двух типов - низкоразмерных складчатых структур бемита размером в среднем 250 нм и низкоразмерных складчатых структур оксигидроксида железа FeOOH размером в среднем 500 нм. Средний размер агломератов - 8,0 мкм, удельная поверхность - 253 м /г, дзета-потенциал агломератов - около 31 мВ, толщина граней, соответственно, AlOOH в среднем 5 нм, FeOOH - в среднем 2 нм, напряженность электрического поля на торце грани AlOOH составила Е=1,2×107 В/м, напряженность электрического поля на торце грани FeOOH составила Е=2,5×107 В/м.
Пример 3. Получение агломерата низкоразмерных складчатых структур оксида Ti.
Агломераты низкоразмерных складчатых структур оксида Ti получали гидротермальным синтезом при температуре 130°C в течение 12 часов. Для этого к 100 г бутилата титана приливали 30 мл ацетилацетона и 10 мл дистиллированной воды при постоянном перемешивании. Затем добавляли 10 мл концентрированного раствора аммиака. Смесь нагревали до 130°C и проводили гидротермальную обработку в течение 12 часов при постоянном перемешивании. Полученную суспензию отфильтровывали и промывали изопропиловым спиртом и дистиллированной водой. Влажный порок сушили на воздухе при температуре 105°C в течение 10 часов.
Получено 18 г низкоразмерных складчатых структур оксида титана. Удельная поверхность оксида титана, измеренная аналогично примерам 1 и 2, составила 380 м2/г.
На фиг. 4 приведена микрофотография агломератов оксида титана, полученных с помощью сканирующего микроскопа LEO EVO 50, которая демонстрирует, что агломераты образованы из множества низкоразмерных складчатых структур.
Размер агломератов составлял от 0,3 мкм до 5,0 (в среднем 0,5 мкм.) Размер отдельного элемента складчатой структуры составлял в среднем 100 нм, толщина грани в среднем 3 нм.
Дзета-потенциал агломератов, определенный с помощью прибора ZetaSizer Nano ZS, составил около -40 мВ.
Далее проводили расчеты, аналогичные приведенным в примере 1. Напряженность электрического поля на торце грани составила Е=1,3·107 В/м.
Для сравнения напряженность электрического поля на поверхности непористой сферической частицы размером 0,3 мкм E=1,3·105 В/м.
Пример 4. Получение низкоразмерных структур гидроксида магния Mg(OH)2. Низкоразмерные структуры гидроксида магния Mg(OH)2 получали гидротермальным синтезом при температуре 200°C в течение 6 часов. Для этого навеску цитрата магния 5 г растворяли в дистиллированной воде, приливали 2 М раствор NaOH по каплям до достижения pH≈9,7. Реакцию проводили при постоянном перемешивании до полного осаждения гидроксида магния. Получившийся золь помещали в автоклав, нагревали до 200°C и проводили гидротермальную обработку в течение 6 часов. Осадок отфильтровывали, промывали тремя порциями дистиллированной воды, а затем этиловым спиртом (2-3 раза). Осадок сушили в сушильном шкафу при температуре 80°C в течение 2-3 часов. Получено 0,8 г низкоразмерных структур гидроксида магния. Удельная поверхность оксида магния измерялась прибором «Сорбтометр-М» и составляла 157 м2/г. Рентгенофазовый анализ проведенный с помощью дифрактометра ДРОН-7 показал, что продукт представляет собой Mg(OH)2. На фиг. 5 приведена микрофотография низкоразмерных структур Mg(OH)2, полученных с помощью просвечивающего микроскопа JEM 2100. Размер отдельных элементов складчатых структур составил в среднем 30 нм, размер агломератов в среднем 0,5 мкм. Дзета-потенциал агломератов определялся с помощью прибора ZetaSizer Nano ZS и составил около 6 мВ. С учетом толщины граней в среднем 2 нм можно оценить напряженность электрического поля на ребре грани.
Напряженность электрического поля: Е=φ/R, где φ - потенциал агломерата, R - толщина грани. Напряженность электрического поля на ребре грани составляет E=3·106 В/м.
Пример 5. Получение агломератов композита Mg(OH)2/AlOOH.
Композит Mg(OH)2/AlOOH получали совместным осаждением из солей алюминия и магния с последующей гидротермальной обработкой образовавшегося геля. Для этого 30 г нитрата алюминия девятиводного и 23 г нитрата магния шестиводного растворяли в 150 мл дистиллированной воды. Совместное осаждение гидроксидов магния/алюминия проводили при pH≈10,5. Для этого в раствор солей вводили по каплям 2 М раствор NaOH при постоянном перемешивании. Получившийся золь помещали в автоклав при 200°C на 6 часов. Осадок отфильтровывали, 3 раза промывали дистиллированной водой, далее промывали этиловым спиртом 2 раза. Затем сушили в сушильном шкафу при температуре 80°C в течение 2 часов.
Дзета-потенциал полученного образца +37 мВ. Размер отдельных элементов складчатых структур составил в среднем 200 нм размер агломератов в среднем 1,0 мкм, удельная поверхность 227 м2/г, толщина граней в среднем 5 нм, напряженность электрического поля на ребре грани составляет Е=7,4×106 В/м.
На фиг. 6 приведена микрофотография низкоразмерных структур композита Mg(OH)2AlOOH, полученных с помощью просвечивающего микроскопа JEM 2100.
Пример 6. Сорбция микроорганизмов оксигидроксидами металлов.
Сорбцию микроорганизмов, проводили на образцах оксигидроксида алюминия, полученного по примеру 1, оксигидроксида Fe, полученного по примеру 2 и оксида титана, полученного по примеру 3. Все характеристики используемых изучения сорбции агломератов приведены в соответствующих примерах их получения.
Культуры микроорганизмов E.coli 7935, St.aureus 209, P.aeruginosa 27583, культивировали на МП А в течение 24 часов в термостате при температуре 37±1°C, затем готовили взвесь микроорганизмов в концентрации 1,0×103 КОЕ/мл. E.coli 7935 - это короткие (длина 1-3 мкм, ширина 0,5-0,8 мкм) полиморфные подвижные и неподвижные грамотрицательные палочки; St.aureus 209 - грамположительные шаровидные клетки диаметром 0,5-1,5 мкм; P.aeruginosa 27583 - грамотрицательная прямая палочка длиной 1-3 мкм, шириной 0,5-0,7 мкм.
Измерение эффективности сорбции поводили на бактериях E.coli, St.aureus и P.aeruginosa согласно рекомендациям [Ворошилова А.А., Дианова Е.Д. Окисляющие нефть бактерии показатели интенсивности биологического окисления нефти в природных условиях // Микробиология, 1952. - т. 21. - вып. 4. - С. 408-415.]. Для определения эффективности сорбции, образцы стерилизованного в автоклаве продукта с массой 100 мг помещали в стерильные колбы и добавляли 30 мл бактериальной суспензии с концентрацией 1,0×103 КОЕ/мл. Адсорбцию микроорганизмов на образцах проводили при постоянном перемешивании суспензии в течение 30 мин на магнитной мешалке со скоростью 500 об/мин. Далее пробы центрифугировали в течение 3 минут при скорости вращения 1300 об/мин и осуществляли посев 1 мл надосадочной жидкости на МПА, посевы инкубировали в термостате при температуре 37±1°C в течение 24 ч. Через сутки после инкубирования проводили подсчет колоний.
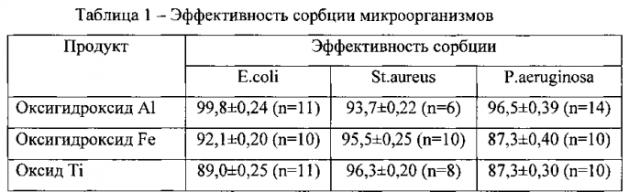
Значения эффективности сорбции приведены в таблице 1.
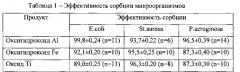
Аналогично проводили эксперименты по сорбции микроорганизмов в зависимости от величины pH (таблица 2).
Пример 7. Антибактериальная активность гидроксида магния с полученными формой и характеристиками в примере 4.
Измерение антибактериальной активности поводили на бактериях E.coli, St.aureus и P.aeruginosa. Для этого культуры микроорганизмов E.coli 7935, St.aureus 209, P.aeruginosa 27583, культивировали на МПА в течение 24 часов в термостате при температуре 37±1°C, затем готовили взвесь микроорганизмов в концентрации 1,0×103 КОЕ/мл. Для определения эффективности антимикробного действия, образцы стерилизованного в автоклаве гидроксида магния с массой 100 мг помещали в стерильные колбы и добавляли 30 мл бактериальной суспензии с концентрацией 1,0×103 КОЕ/мл. Время экспозиции составляло 24 часа. Далее пробы центрифугировали в течение 3 минут при скорости вращения 1300 об/мин и осуществляли посев 1 мл надосадочной жидкости на МПА, посевы инкубировали в термостате при температуре 37±1°C в течение 24 ч. Через сутки после инкубирования проводили подсчет колоний.
Гибель микроорганизмов под действием гидроксида магния через 24 часа экспозиции, % составила при (n=5) составила: для E.coli - 98,7±0,21; для St.aureus - 99,1±0,25 и для P.aeruginosa - 97,1±0,24.
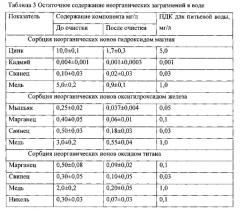
Пример 8. Исследование сорбции неорганических ионов предлагаемыми агломератами оксигидроксидов металлов.
Для исследования сорбции неорганических ионов были выбраны гидроксид магния, оксигидроксид железа, оксид титана с заявляемой формой и характеристиками, полученными в соответствующих примерах их синтезирования, а именно в примере 4, примере 2 и примере 3.
Для исследования сорбции неорганических ионов гидроксидом магния готовили модельный раствор ионов металлов, содержащий 10,0 мг/л цинка, 0,004 мг/л кадмия, 0,1 мг/ л свинца и 5,0 мг/л меди. К 100 мл модельного раствора прибавляли 1 г агломератов складчатых структур гидроксида магния, полученную смесь перемешивали в течение 1 часа при комнатной температуре. Определяли содержание ионов металлов после адсорбции.
Для исследования сорбции неорганических ионов оксигидроксидом железа готовили модельный раствор ионов металлов, содержащий 0,25