Способ получения 9-(бета-d-арабинофуранозил)-6-(nα-l-сериламидо)-2-хлорпурина
Иллюстрации
Показать всеИзобретение относится к новому способу получения противоопухолевого препарата - 9-(бета-D-арабинофуранозил)-6-(Nα-L-сериламидо)-2-хлорпурина. Способ заключается в том, что 9-(бета-D-арабинофуранозил)-6-(Nα-L-сериламидо)-2-хлорпурин получают посредством конденсации метилового эфира L-серина с 2,6-дихлор-9-(2′,3′,5′-три-O-ацетил-бета-D-рибофуранозил)пурином с последующим удалением защитных групп и реакции транс-арабинозилирования полученного нуклеозида с 1-бета-D-арабинофуранозилурацилом в присутствии каталитических количеств уридин фосфорилазы и пуриннуклеозидфосфорилазы. Предложен эффективный способ ценного противоопухолевого препарата. 3 пр., 2 ил.
Реферат
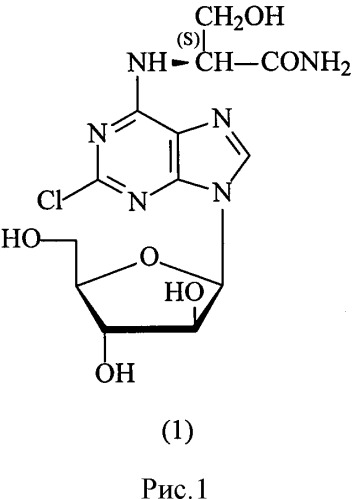
Изобретение относится к биотехнологии, в частности к получению противоопухолевого пуринового нуклеозида бета-D-арабинофуранозы, содержащий по С2 положению атом хлора, по С6 положению пуринового основания остаток природной аминокислоты L-серина (соединение (1), рис. 1) - 9-(бета-D-арабинофуранозил)-6-(Nα-L-сериламидо)-2-хлорпурина (САП).
Модифицированный нуклеозид САП (1) синтезирован впервые, в литературе не описан. Относится к классу антиметаболитов. Исследования резистентности опухолевых клеток линии MOLT-4 и U937 к препарату САП показали, что данное соединение обладает дозозависимым цитотоксическим эффектом in vitro. Цитотоксическая активность препарата САП сопоставима с активностью коммерчески доступного препарата неларабина, используемого для терапии Т-лимфобластных лейкозов.
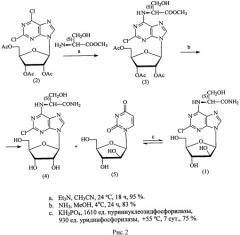
Изобретение решает задачу разработки эффективного способа синтеза САП за счет использования химико-ферментативного подхода, приведенного на схеме 1 (рис. 2). В качестве исходного соединения был выбран 2,6-дихлор-9-(2′,3′,5′-три-O-ацетил-β-D-рибофуранозил)пурин (соединение 2, рис. 2), синтез которого описан в патенте [Берзин В.Б., Дорофеева Е.В., Леонов В.К, Лутонина О.И., Мирошников А.И. Способ получения 2,6-дихлор-9-(2′,3′,5′-три-O-ацетил-β-D-рибофуранозил)пурина. Патент РФ №2324699 от 05.02.2008 г.].
На первой стадии синтеза проводили конденсацию нуклеозида (2) (рис. 2)с метиловым эфиром L-серина [Синтез пептидов. Реагенты и методы. А.А. Гершкович, Кибирев В.К. Изд. «Наукова думка», Киев, 1987, с. 171-172]. В отличие от описанных ранее способов конденсации аминокислот, синтез проводили в ацетонитриле при комнатной температуре без нагревания реакционной смеси, чтобы избежать изомеризации L-серина в D-серин. После удаления защитных групп нуклеозида (3) (рис. 2) получали рибозид (4) (рис. 2). На следующей стадии синтеза использовали генно-инженерные ферменты нуклеозидфосфорилазы, которые осуществляют перенос остатка арабинозы с 1-бета-D-арабинофуранозилурацила (соединение (5), рис. 2) на основание, полученное при фосфоролизе нуклеозида (4). В качестве генно-инженерных ферментов используют пуриннуклеозидфосфорилазу (ПНФ, КФ 2.4.2.1) и уридинфосфорилазу (УФ, КФ 2.4.2.3).
Изобретение иллюстрируют рисунки:
Рисунок 1. Структурная формула 9-(бета-D-арабинофуранозил)-6-(Nα-L-сериламидо)-2-хлорпурина (САП).
Рисунок 2. Схема получения 9-(бета-D-арабинофуранозил)-6-(Nα-L-сериламидо)-2-хлорпурина.
Изобретение иллюстрируют примеры.
Пример 1.
Синтез 9-(2′,3′,5′-три-O-ацетил-бета-D-рибофуранозил)-6-(Nα-L-метоксисерил)-2-хлорпурина (соединение 3, рис. 2).
К раствору 2.00 г (4.5 ммоль) 2,6-дихлор-защищенного нуклеозида (2) и метилового эфира L-серина 0.996 г (6.4 ммоль) в 60 мл ацетонитрила при перемешивании на магнитной мешалке добавляют 1.76 мл (12.8 ммоль) триэтиламина, смесь перемешивают при комнатной температуре 18 ч. Контроль прохождения реакции осуществляют по ТСХ на силуфоле в системе хлороформ-метанол, 20:1. После окончания реакции отфильтровывают кристаллы хлоргидрата Et3N. Растворитель удаляют в вакууме при 40°C, полученный маслообразный продукт распределяют между 100 мл хлороформа и 100 мл воды. Органический слой промывают 60 мл воды, сушат над сульфатом магния безв., растворитель удаляют в вакууме. Получают продукт (3) в количестве 2.25 г (95%), чистотой 95.14%, Rt=6.86 мин (метод 30-100% В за 20 мин, далее во всех случаях: хроматограф Waters, Breeze (США), колонка Nova-Pak С18, 4.6×150 мм, 4 мкм, детекцию осуществляют при 254 нм, элюент А - вода с 0.1% ТФУ, элюент В - 70% ацетонитрила в воде с 0.1% ТФУ). Масс-спектр (3), m/z: [М+Н]+=530.1293, расч.=530.1284; Cl37 [М+Н]+=532.1258; [основание +Н]+=272.0543, расч.=272.0545, Cl37 [М+Н]+=274.0513.
Пример 2.
Синтез 9-(бета-D)-рибофуранозил)-6-(Nα-L-сериламидо)-2-хлорпурина (соединение 4, рис. 2).
2.25 г (4.0 ммоль) нуклеозида (3) растворяют в 60 мл абс. метанола, охлаждают в ледяной бане до +4°C, насыщенной NH3, оставляют на 24 ч при +4°C. Контроль - ТСХ хлороформ-метанол, 10:1. Реакционную смесь концентрируют до 5 мл, остаток кипятят с 20 мл смеси хлороформ-метанол (3:2). Осадок отфильтровают, получают 1.53 г технического продукта нуклеозида (4) (93%) с чистотой 91%, Rt=9.041 мин (метод 0-30% В за 20 мин). Далее технический продукт кристаллизуют из смеси ацетонитрил-метанол (8:1), получают 1.35 г продукта (83%) с чистотой 95.86%, Rt=8.872 мин (метод 0-30% В за 20 мин, 254 нм), т.пл. 168-170°C. Масс-спектр, m/z: [М+Н]+=389.0953, расч. 389.0971; Cl37 [М+Н]+=391.0927.
Пример 3.
Синтез 9-(бета-D-арабинофуранозил)-6-(Nα-L-сериламидо)-2-хлор-пурина (соединение 1, рис. 2).
Рибозид (4) 0.8 г (20.0 ммоль) растворяют в 1 л воды в полученном растворе при небольшом нагревании растворяют 2.5 г (0.1 моль) 1-бета-0-арабинофуранозилурацила (соед. 5, рис. 1) и 1.4 г (0.1 моль) дигидроортофосфата калия. Доводят рН реакционной смеси до 7.0. В реакционную смесь добавляют 1610 ед. пуриннуклеозидфосфорилазы и 930 ед. уридинфосфорилазы. Раствор термостатируют при 55°C. Реакцию проводят до тех пор пока конверсия нуклеозида (4) в целевое соединение (1) не составит 81%. По окончании процесса реакционную смесь концентрируют в вакууме (15 мм.рт.ст.) до объема 30 мл и хроматографируют на обращеннофазовом сорбенте Octadecyl=Si 100polyol (0.03 mm), размеры колонки: 30×220 мм. Целевое соединение элюируют 10% ацетонитрила в воде. Фракции содержащие продукт объединяют, растворитель удаляют в вакууме (15 мм.рт.ст.). Продукт сушат в вакууме (5 мм.рт.ст.) над пятиокисью фосфора. Выход: 0.58 г (75%). Чистота продукта по данным ВЭЖХ 99.27% (Rt=4.624 мин, градиент элюента В 0-100% за 20 минут).
λmax249 нм, 204 нм. Масс-спектр, m/z: [М+Н]+=389.1007, расч. 389.0971; [ α ] D 25 43.6 (с 0.5, H2O).
1Н-ЯМР (WM-700 Bruker, США, dmso-d6, 30°C): 8.27, (с, 1Н, Н8), 7.54 (д, 1H, NH (J=6.2 Гц)), 7.47 (м, 2Н2, NH2), 6.17 (д, 1Н, H1, (J=5.1 Гц)), 4.51 (м, 1Н, Н2 ,), 4.12 (м, 1Н, H3 ,), 3.8 (м, 1Н, Н4 ,), 3.68, 3.64 (2 м, 2Н, Н5), 5.64 (уш. д, 1Н, 2′-ОН), 5.51 (уш. д, 1Н, 3′-ОН), 5.05 (м, 1H, 5′-ОН), 4.62 (т, 1Н, NHCH), 3.80 (м, 2Н, СН2ОН);
13С-ЯМР: 171.85 (CONH2), 150.21 (С4), 141.37 (С8), 118.41 (С5), 84.55 (С4 ,), 84.17 (С1 ,), 75.95 (С2 ,), 75.07 (С3 ,), 62.02 (СН2ОН), 61.08 (С5 ,), 56.35 (NHCH),
15N-ЯМР: 104.62 (NH2), 90.67 (NH).
Способ получения противоопухолевого препарата нуклеозидной природы 9-(бета-D-арабинофуранозил)-6-(Nα-L-сериламидо)-2-хлорпурина, включающий конденсацию метилового эфира L-серина с 2,6-дихлор-9-(2′,3′,5′-три-O-ацетил-бета-D-рибофуранозил)пурином с последующим удалением защитных групп и реакцию транс-арабинозилирования полученного нуклеозида с 1-бета-D-арабинофуранозилурацилом в присутствии каталитических количеств уридин фосфорилазы и пуриннуклеозидфосфорилазы.