Растительный пептид гамма-зеин для доставки биомолекул в растительные клетки
Иллюстрации
Показать всеИзобретение относится к области биохимии, в частности к способу введения нуклеиновой кислоты в растительную клетку, имеющую интактную клеточную стенку. Также раскрыты способ экспрессии гена и способ переноса плазмидной ДНК в растительную клетку. При этом способы включают: взаимодействие пептида гамма-зеина с плазмидной ДНК для образования гамма-зеин связанной структуры; и контактирование гамма-зеин связанной структуры с интактной имеющей стенку растительной клеткой для предоставления возможности захвата гамма-зеин связанной структуры клеткой, имеющей интактную клеточную стенку. Изобретение позволяет эффективно вводить нуклеиновую кислоту, представляющую интерес, в растительную клетку, имеющую интактную клеточную стенку. 3 н. и 16 з.п. ф-лы, 6 ил., 8 пр.
Реферат
ПРИТЯЗАНИЕ НА ПРИОРИТЕТ
Настоящая заявка заявляет приоритет даты регистрации предварительной патентной заявки США, серийный номер 61/319764, зарегистрированной 31 марта 2010 года для заявки "РАСТИТЕЛЬНЫЙ ПЕПТИД ГАММА-ЗЕИН ДЛЯ ДОСТАВКИ БИОМОЛЕКУЛ В РАСТИТЕЛЬНЫЕ КЛЕТКИ".
УРОВЕНЬ ТЕХНИКИ
Традиционные стратегии растениеводства для разработки новых линий растений, проявляющих конкретные признаки, являются трудоемкими и иногда непрогнозируемыми. Существующие стратегии, такие как трансформация с помощью Agrobacterium и бомбардировка частицами, в значительной степени зависят от ткани и генотипа. Пептиды, проникающие в клетки (CPP), представляют собой новый и быстро развивающийся класс коротких пептидов, которые играют важную роль в перемещении широкого диапазона транспортируемых комплексов, включающих в себя ДНК, РНК и белки, через клеточные мембраны в линиях клеток млекопитающих и человека (Schwartz and Zhang, 2000; Langel, 2002; Vives, 2002).
Несмотря на то, что CPP облегчают доставку груза в клетки млекопитающих, использование CPP в растительных клетках для изучения трансфекции ограничено многими факторами. Основное препятствие для адаптации этой технологии для растений состоит в том, что, в отличие от животных клеток, в растительных клетках существует система двойного барьера (клеточная стенка и плазматическая мембрана) для интернализации пептидов CPP и их груза. Поэтому для эффективного перемещения транспортируемых молекул в интактные растительные клетки CPP должны преодолеть два упомянутых барьера. В растительных клетках использовались CPP, но их применение основывалось на использовании агентов проницаемости для осуществления доставки транспортируемых молекул в интактные растительные клетки. CPP-опосредованная доставка маленьких молекул, нуклеиновых кислот и белков в интактные растительные клетки остается в значительной степени неисследованной и имеет преимущества для генетических и биохимических манипуляций в растительных системах in vivo и in vitro.
Наночастицы обладают уникальными свойствами, которые задействуют для использования при доставке ДНК в клетки. Наночастицы металлов, такие как наночастицы золота (Au), применяют для доставки ДНК в силу их низкой цитотоксичности и легкой функционализации с различными биологически важными лигандами. В дополнение к наночастицам металлов, для доставки молекул в клетки в качестве носителей также используют полупроводниковые наночастицы (например, квантовые точки - "QD") с размером в диапазоне 3-5 нм. ДНК и белки могут быть связаны с лигандом, присоединенным к QD посредством различных поверхностных функциональных групп (см., например, Patolsky F. Et al., J. Chem. Soc. 125, 13918 (2003)).
Наночастицы используют для доставки плазмидной ДНК в различные клетки животных. Было выявлено, что при инкубировании покрытых ДНК наночастиц с клетками, не имеющими клеточной стенки, клетки захватывают наночастицы и начинают экспрессировать любые гены, кодируемые на ДНК. Вместе с тем, на современном этапе существуют проблемы доставки растительных генов, обусловленные наличием стенок в растительных клетках, что приводит к традиционной зависимости от инвазивных способов доставки в целях генетической трансформации растений. Если желательна доставка наночастиц к клеткам, обычно имеющим клеточную стенку, то перед добавлением частиц к растительным прототипам клеточную стенку удаляют (см. Torney, F. Et al, Nature Nanotechnol. 2, (2007)). Клеточная стенка растительных клеток представляет собой труднопреодолимый барьер для доставки экзогенно находящихся молекул. Для осуществления доставки генов и маленьких молекул в растительные клетки со стенкой применялось множество инвазивных способов, таких как генная пушка (биолистика), микроинъекция, электропорация и Agrobacterium, но доставка белков достигалась только с помощью микроинъекции.
На фоне постоянно растущего объема информации о разработках в области последовательности генома растений существует острая потребность в быстром, универсальном (независимым от ткани/генотипа) способе функциональных исследований генома растений для широкого разнообразия генов и для разработки трансгенных растений, экспрессирующих важные агрономические признаки.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Описание следующих вариантов осуществления приведено совместно с системами, инструментами и способами, которые предназначены служить примерами, выполнять иллюстративные задачи и не ограничивать объем изобретения.
Один вариант осуществления настоящего изобретения относится к способу введения молекулы, представляющей интерес, в растительную клетку, имеющую клеточную стенку. Способ включает в себя предоставление растительной клетки, имеющей клеточную стенку, и взаимодействие пептида гамма-зеина с рассматриваемой молекулой для образования связанной структуры гамма-зеина. Затем клетку, имеющую клеточную стенку, и связанную структуру гамма-зеина располагают так, чтобы они контактировали друг с другом, и была возможность захвата рассматриваемой гамма-зеин связанной молекулы в клетку, имеющую клеточную стенку.
Другой вариант осуществления изобретения относится к способу экспрессии гена, и указанный способ включает в себя предоставление растительной клетки, имеющей клеточную стенку, и взаимодействие пептида гамма-зеина с рассматриваемым геном для образования гамма-зеин связанной генной структуры. Растительную клетку, имеющую клеточную стенку, и гамма-зеин связанную структуру располагают так, чтобы они контактировали друг с другом, и была возможность захвата пептида гамма-зеина и гена в растительную клетку, содержащую клеточную стенку. Затем в потомстве растения, несущего эту растительную клетку, происходит экспрессия гена.
Еще в одном варианте осуществления изобретения в растительную клетку переносится молекулярная субстанция. Способ включает в себя взаимодействие пептида гамма-зеина с плазмидной ДНК для образования гамма-зеин связанной структуры. Гамма-зеин связанная структура располагается так, чтобы она контактировала с интактной растительной клеткой, имеющей клеточную стенку, при условиях, позволяющих захватывать растительную клетку пептид гамма-зеин и ген из плазмидной ДНК.
В дополнение к примерам аспектов и вариантов осуществления, описанным выше, дополнительные аспекты и варианты осуществления станут очевидными в свете последующего описания.
КРАТКОЕ ОПИСАНИЕ ФИГУР
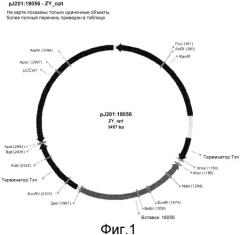
Фиг. 1 представляет карту плазмиды слитого гена гамма-зеин/YFP.
Фиг. 2 представляет Ni хелирующую хроматографию очистки слитого пептида гамма-зеин/YFP.
Фиг. 3 показывает профиль элюирования гамма-зеина/YFP в анализе SDS-PAGE (электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия).
Фиг. 4 показывает масс-спектры пептида гамма-зеина/YFP при время-пролетной ионизации лазерной десорбцией с использованием матрицы Maldi-TOF.
Фиг. 5 показывает конфокальные микроскопные изображения, иллюстрирующие клеточный захват и интернализацию слитого пептида: A. Одиночная клетка моркови, окрашенная Хехст 33342 с показом ядра; B. Одиночная клетка моркови, показывающая локализацию флюоресценции гамма-зеин/YFP в ядре и цитоплазме; C. Клетки табака JTNTI, окрашенные Хехст 33342 с показом ядра; D. Клетки табака JTNTl, показывающие флюоресценцию гамма-зеин/YFP в ядре и цитоплазме вместе с окрашиванием ядер синим цветом красителем Хехст 33342; E. Конфокальное изображение, показывающее слитый пептид гамма-зеин/YFP, нацеленный и на плазматическую мембрану и на ядро клеток JTNTl; и F и G, показывающие соответствующие изображения в светлом поле и наложения конфокальных/светлопольных изображений, соответственно.
Фиг. 6 показывает карту плазмиды pDAB3831.
СПОСОБ (СПОСОБЫ) ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
В нижеследующем описании и таблицах применяется ряд терминов. Для достижения ясного и последовательного понимания описания и формулы изобретения, включающих в себя область применения таких терминов, представлены следующие определения:
обратное скрещивание. Обратное скрещивание представляет собой способ, при котором селекционер неоднократно скрещивает гибридное потомство обратно с одним из родителей, например, гибрид F1 первого поколения скрещивает с одним из родительских генотипов гибрида F1.
Зародыш. Зародыш может представлять собой маленькое растение, содержащееся в зрелом семени.
Зеин. Зеин представляет собой кукурузный белок, получаемый из кукурузной глютеновой муки. В нем не содержится аминокислот лизина и триптофана, таким образом, он не подходит в качестве единственного источника пищевого белка. Зеин нерастворим в воде и спиртах, но является растворимым в водных спиртах, гликолях и гликолевых эфирах. Зеин присутствует в виде пленки и покрытия для обеспечения влагоустойчивого барьера в орехах и зерновых продуктах. Он также используется как покрытие для кондитерских изделий и для глазури на формовых изделиях.
Наночастица. Микроскопическая частица, имеющая по меньшей мере один размер в наномасштабе, обычно меньше чем 100 нм. Наночастица, подходящая для использования в настоящем изобретении, может иметь размер в диапазоне от 1 нм до 0,4 мкм. Квантовая точка может иметь средний диаметр в пределах от 1 нм до 10 нм, предпочтительно от 2 до 4 нм. Наночастицу можно выбирать из: наночастицы золота, покрытой золотом наночастицы, пористой наночастицы, мезопористой наночастицы, кварцевой наночастицы, полимерной наночастицы, вольфрамовой наночастицы, желатиновой наночастицы, нанооболочек, наноядер, наносфер, наностержней, магнитных наночастиц и их комбинаций.
Квантовая точка. Квантовая точка представляет собой полупроводниковую наноструктуру, которая ограничивает движение электронов зоны проводимости, дырки зоны валентности или экситоны (связанные пары электронов зоны проводимости и дырки зоны валентности) во всех трех пространственных измерениях. Удержание может осуществляться благодаря электростатическим потенциалам (генерируемым внешними электродами, допированием, посторонними напряжениями), наличием пространства между различными полупроводниковыми материалами (например, в нанокристаллической системе ядро-оболочка), наличием полупроводниковой поверхности (например, полупроводникого нанокристалла) или их комбинацией. Квантовая точка может иметь дискретный квантованный спектр энергии. Соответствующие волновые функции пространственно локализованы в квантовой точке, но распространяются через многочисленные периоды кристаллической решетки. Квантовая точка содержит малое конечное число электронов зоны проводимости (порядка 1-100), дырок валентной зоны, или экситонов (то есть, конечное число элементарных электрических зарядов).
Стабильные или устойчивые трансформанты. Термины «стабильные или устойчивые трансформанты» относятся к растению, геном которого репродуктируемо передается от одного поколения к следующему поколению.
Захват. Захват относится к перемещению частицы, такой как гамма-зеин, через клеточную стенку или клеточную мембрану, при этом перемещение не происходит исключительно в результате момента, который передается частице чем-либо отличным от клетки, в которую захватывается частица. Для сравнения, примерами устройств или способов, которые вызывают перемещение частицы через клеточную стенку или клеточную мембрану исключительно в результате момента, передаваемого частице, является генная пушка, технологии биолистики, микроинъекции и/или импалефекции.
В конкретном варианте осуществления изобретение относится к использованию гамма-зеина в качестве CPP для эффективной доставки полезных грузов в интактные растительные клетки, для применения при доставке маленьких молекул, доставке биомолекул, доставке генов, визуализации и различных задач биотехнологической диагностики и функций индикации в растительных системах.
В других вариантах осуществления изобретения к молекуле гамма-зеина можно присоединять "добавочную" или "гостевую" молекулу. Это свойство можно задействовать, например, для специфичного нацеливания и редактирования молекулярных участков в клетках, в таких областях данной техники, как биомиметики, направленная доставка, для вариантов негенетически модифицированных организмов и вариантов неустойчивой трансформации у многих древесных, овощных и зерновых культур в целях достижения признака и устойчивости к болезням. Варианты осуществления изобретения можно применять также для разработки подходящих биосенсоров в растениях.
Согласно вариантам осуществления изобретения может быть представлен способ введения молекулы, представляющей интерес, в растительную клетку, содержащую клеточную стенку, и указанный способ содержит приведение гамма-зеина, содержащего молекулу, представляющую интерес, в контакт с растительный клеткой, и предоставление возможности захвата гамма-зеина через клеточную стенку растительной клетки. В конкретных аспектах изобретения гамма-зеин может обратимо или необратимо содержать молекулу, представляющую интерес, может взаимодействовать или иным образом быть связанным с молекулой, представляющей интерес, и/или нести ее.
Согласно вариантам осуществления настоящего изобретения, растительная клетка, имеющая клеточную стенку, может представлять собой любую растительную клетку, содержащую интактную и целую клеточную стенку. Примеры клеток, имеющих клеточную стенку, включают в себя без ограничения водоросли, табак, морковь, кукурузу, канолу, рапс, хлопок, пальму, арахис, сою, сахарный тростник, Oryza sp., Arabidopsis sp., и Ricinus sp., предпочтительно, табак, кукурузу, морковь, хлопок, канолу, сою и сахарный тростник; более предпочтительно табак и морковь. Варианты осуществления изобретения могут включать в себя содержащие клеточную стенку клетки из любой ткани или из любого места их выявления, включая в себя без ограничения зародыши, меристематические клетки, каллюс, пыльцу, листья, пыльники, корни, корневые кончики, цветы, семена, стручки, стебли, культуру тканей и суспензии интактных одиночных растительных клеток.
В вариантах осуществления изобретения рассматриваемая молекула может представлять собой любую молекулу, которую можно доставлять в растительную клетку согласно настоящему изобретению. Молекулы, представляющие интерес, или компоненты молекул, представляющие интерес, могут включать в себя без ограничения любые маленькие молекулы, нуклеиновые кислоты, молекулы ДНК, РНК, iРНК, miРНК, гены, плазмиды, космиды, YAC, BAC, полипептиды, ферменты, гормоны, гликопептиды, сахара, жиры, сигнальные пептиды, антитела, витамины, мессенджеры, вторичные мессенджеры, аминокислоты, цАМФ, лекарства, гербициды, фунгициды, антибиотики и/или их комбинации.
Варианты осуществления изобретения включают в себя способы профилактики или лечения болезни. Неограничивающие примеры вариантов осуществления включают в себя доставку фунгицидов, антибиотиков, и/или других лекарственных веществ в клетки, нуждающиеся в такой доставке, с помощью способов настоящего изобретения.
В аспектах изобретения связанная структура гамма-зеина может захватываться во множество органел растительной клетки. Примеры локализаций, в которые могут захватываться связанные структуры гамма-зеина, включают в себя без ограничения цитозоль, ядро, тонопласты, пластиды, этиопласты, хромопласты, лейкопласты, элайопласты, протеинопласты, амилопласты, хлоропласты и просвет двойных мембран. В других вариантах осуществления изобретения захват связанных структур гамма-зеина в клетку, содержащую клеточную стенку, может происходить посредством симпластического или апопластического пути.
Дополнительные варианты осуществления изобретения включают в себя генетически модифицированные растительные клетки и способы их получения, при этом растительные клетки имеют одну или более нуклеиновых кислот, внедренных в эти клетки посредством способов настоящего изобретения. В одном примере вариантов осуществления с помощью гамма-зеина согласно настоящему изобретению в растительную клетку, имеющую клеточную стенку, можно вводить плазмиду, содержащую ген, представляющий интерес, и селектируемый маркер. В дополнительных вариантах осуществления можно выбирать устойчивые трансформанты, в которые устойчиво внедрили ген, представляющий интерес, и/или селектируемый маркер. В альтернативных вариантах осуществления можно размножать растительную клетку, уже содержащую ген, представляющий интерес, чтобы получить другие клетки, содержащие молекулу, представляющую интерес. В других вариантах осуществления растительные клетки, уже содержащие молекулу, представляющую интерес, могут представлять собой регенерируемую клетку, которую можно использовать для регенерации целого растения, включающего в себя молекулу, представляющую интерес.
В другом аспекте настоящее изобретение относится к способам создания регенерируемых растительных клеток, содержащих молекулу, представляющую интерес, для использования в тканевой культуре. Тканевая культура предпочтительно будет способна к регенерации растений, имеющих по существу тот же генотип, что и регенерируемые клетки. Регенерируемые клетки в таких тканевых культурах могут представлять собой зародыши, прототипы, меристематические клетки, каллюс, пыльцу, листья, пыльники, корни, корневые кончики, цветы, семена, стручки или стебли. Еще один дополнительный вариант осуществления изобретения относится к растениям, регенерированным из тканевых культур по изобретению.
Альтернативно, настоящее изобретение относится к способу введения желательного признака в растительную клетку, имеющую клеточную стенку, при этом способ содержит: введение способного обеспечить желательный признак гена гамма-зеина, представляющего интерес, в растительную клетку, имеющую клеточную стенку и предоставление возможности захвата гамма-зеин связанного гена, представляющего интерес, через клеточную стенку. Примеры желательных признаков включают в себя без ограничения признаки, выбираемые из следующего: мужская стерильность, устойчивость к гербицидам, устойчивость к насекомым, устойчивость к бактериальному, грибковому и/или вирусному заболеванию, и признаки, дающие преимущества для конечного пользователя, такие как модифицированные масляные профили, измененное содержание крахмала и волокон, увеличенное содержание витаминов и аминокислот и тому подобное.
Дополнительные аспекты изобретения представляют способы создания устойчивых линий растений, содержащих целевую молекулу или ген, представляющих интерес, при этом целевая молекула или ген, представляющие интерес, сначала могут вводиться через стенку растительной клетки путем гамма-зеин опосредованной транслокации. Способы стабилизации растительных линий, измененных генетически или другим способом, известны рядовым специалистам в данной области и включают в себя без ограничения такие методики, как самовоспроизводство, обратные скрещивания, гибридное производство, скрещивание с устойчивыми популяциями и тому подобное. Все растения и растительные клетки, содержащие целевую молекулу или ген, представляющие интерес, вначале вводятся в растительную клетку (или ее предшественники) путем опосредуемого гамма-зеином переноса через клеточную стенку согласно настоящему изобретению. Преимущество состоит в том, что растительные клетки, содержащие молекулу или ген, представляющие интерес, которые сначала вводят в растение или клетку (или ее предшественники) путем опосредуемого гамма-зеином переноса через клеточную стенку, можно использовать в кросс-бридинге с другими различными растениями для получения гибридных клеток первого поколения (F1), семян и/или растений с более хорошими характеристиками и фенотипами.
В вариантах осуществления, в которых рассматриваемая молекула содержит один или более генов, ген (гены) может быть доминантной или рецессивной аллелью. Как пример, ген (гены) будет придавать такие признаки, как устойчивость к гербицидам, устойчивость к насекомым, устойчивость к бактериальной устойчивости, устойчивость к грибковым заболеваниям, устойчивость к вирусным заболеваниям, мужская фертильность, мужская стерильность, улучшенные пищевые качества и промышленное применение.
С появлением технологий молекулярной биологии, которые позволили выделять и оценивать гены, кодирующие конкретный белок или РНК-продукты (например, iРНК), у ученых в области биологии растений возник сильный интерес к созданию генома клеток, в которых могут содержаться и экспрессироваться чужие гены, или дополнительные или модифицированные версии нативных или эндогенных генов (возможно, с помощью различных промоторов), в целях изменения признаков клетки конкретным образом. Такие чужие дополнительные и/или модифицированные гены в настоящем изобретении обобщенно называются "трансгенами". За последние пятнадцать - двадцать лет были разработаны несколько способов получения трансгенных растительных клеток, и в конкретных вариантах осуществления настоящее изобретение относится к трансформированным версиям клеток и способам их получения посредством введения трансгена в растительную клетку, имеющую клеточную стенку, путем захвата связанной структуры гамма-зеина через стенку растительной клетки и мембрану. В вариантах осуществления изобретения трансген может содержаться в векторе экспрессии.
Клеточная трансформация может охватывать конструирование вектора экспрессии, кодирующего конструкцию, которая будет функционировать в конкретной клетке. Такой вектор может содержать ДНК, которая включает в себя ген под контролем регуляторного элемента, или функционально связана с регуляторным элементом (например, промотором). Вектор экспрессии может содержать один или более таких комбинаций из функционально связанного гена/регуляторного элемента. Вектор (векторы) может быть в форме плазмиды и может использоваться единственным или в комбинации с другими плазмидами для получения трансформированных клеток с помощью описанных в изобретении способов трансформации, с целью введения трансгена (трангенов) в генетический материал растительной клетки, содержащей клеточную стенку.
Векторы экспрессии для захвата посредством гамма-зеина: маркерные или репортерные гены
Векторы экспрессии могут включать в себя по меньшей мере один генетический маркер, функционально связанный с регуляторным элементом (например, промотором), который позволяет восстанавливать несущие маркер трансформированные клетки или путем отрицательной селекции (то есть, ингибированием роста клеток, которые не содержат селектируемый маркерный ген), или путем положительной селекции (то есть скринингом продукта, кодируемого генетическим маркером). В методиках трансформации известно множество селектируемых маркерных генов для трансформации, и они включают в себя, например, гены, кодирующие ферменты, которые метаболически детоксифицируют селективный химический агент, который может представлять собой антибиотик или гербицид, или гены, кодирующие измененную мишень, которая может быть нечувствительной к ингибитору. В данной области также известен ряд способов положительной селекции.
Один широко используемый селектируемый маркерный ген, подходящий для трансформации растений, может включать в себя ген неомицин-фосфотрансферазы II (nptll) под контролем растительных регуляторных сигналов, которые придают устойчивость к канамицину. См., например, Fraley et al,, Proc. Natl. Acad. Sci. USA, 80:4803 (1983). Другим обычно используемым селектируемым маркерным геном может быть ген гигромицин-фосфотрансферазы, который придает устойчивость к антибиотику гигромицину. См., например, Vanden Elzen et al., Plant Mol. Biol, 5:299 (1985). Дополнительные селектируемые маркерные гены бактериального происхождения, которые придают устойчивость к антибиотикам, включают в себя гентамицин-ацетилтрансферазу, стрептомицин-фосфотрансферазу, аминогликозид-3'-аденил-трансферазу и детерминанту устойчивости к блеомицину. См. публикации: Hayford et al., Plant Physiol. 86: 1216 (1988), Jones et al., Mol. Gen. Genet., 210:86 (1987), Svab et al., Plant Mol. Biol. 14: 197 (1990), Hille et al., Plant Mol. Biol. 7: 171 (1986). Другие селектируемые маркерные гены придают устойчивость к гербицидам, таким как глифосфат, глюфосинат или бромоксинил. См. публикации Comai et al., Nature 317:741-744 (1985), Gordon-Kamm et al., Plant Cell 2:603-618 (1990) and Stalker et al., Science 242:419-423 (1988). Селектируемые маркеры, которые придают толерантность к гербицидам, включают в себя фосфинотрицин-ацетилтрансферазу (PAT).
Другие селектируемые маркерные гены, подходящие для трансформации растений, не имеют бактериального происхождения. Эти гены включают в себя, например, мышиную дигидрофолат-редуктазу, растительную 5-энолпирувилшикимат-3-фосфат-синтазу и растительную ацетолактат-синтазу. См. публикации Eichholtz et al., Somatic Cell Mol. Genet. 13:67 (1987), Shah et al., Science 233:478 (1986), Charest et al., Plant Cell Rep. 8:643 (1990).
Для другого класса маркерных генов, подходящих для трансформации растений, необходим скрининг предположительно трансформированных растительных клеток, а не прямая генетическая селекция трансформированных клеток на устойчивость к токсичному веществу, например, к антибиотику. Эти гены особенно полезны для количественного определения или визуализации пространственной характеристики экспрессии гена в конкретных тканях, и часто их называют репортерными генами, поскольку для изучения генной экспрессии их можно сливать с геном или регуляторной последовательностью гена. Обычно используемые гены для скрининга трансформированных клеток включают в себя β-глюкуронидазу (GUS), β-галактозидазу, люциферазу и хлорамфеникол-ацетилтрансферазу. См. публикации Jefferson, R. A., Plant Mol. Biol. Rep. 5:387 (1987), Teeri et al., EMBO J. 8:343 (1989), Koncz et al Proc. Natl. Acad. Sci U.S.A. 84: 131 (1987), DeBlock et al EMBO J. 3: 1681 (1984).
В последнее время стали доступными способы визуализации активности GUS in vivo, которые не требуют разрушения растительной ткани. См. публикация Molecular Probes publication 2908, Imagene Green.TM., p. 1-4(1993) и Aleway et al., J. Cell Biol. 115: 151a (1991). Вместе с тем, эти способы in vivo для визуализации активности GUS не доказали свою полезность для восстановления трансформированных клеток из-за низкой чувствительности, высоких исходных уровней флуоресцентности и ограничений, связанных с использованием генов люциферазы в качестве селектируемых маркеров.
Позднее в качестве маркеров генной экспрессии в прокариотических и эукариотических клетках были использованы гены, кодирующие флуоресцентные белки (например, GFP, EGFP, EBFP, ECFP и YFP). См. Chalfie et al., Science 263:802 (1994). В качестве возможных для скрининга маркеров можно использовать флуоресцентные белки и мутации флуоресцентных белков.
Векторы экспрессии для захвата посредством гамма-зеина: промоторы
Гены, включенные в векторы экспрессии, должны запускаться нуклеотидными последовательностями, содержащими регуляторный элемент, например, промоторы. В настоящее время в области трансформации известны несколько типов промоторов, а также другие регуляторные элементы, которые можно использовать единственными или в комбинации с промоторами.
Используемый в изобретении термин "промотор" относится к области ДНК, которая может располагаться в 3'-5' направлении от начала транскрипции, и может участвовать в распознавании и связывании РНК-полимеразы и других белков для инициации транскрипции. "Растительным промотором" может быть промотор, способный к инициации транскрипции в растительных клетках. Примеры промоторов под контролем индивидуального развития включают в себя промоторы, которые предпочтительно инициируют транскрипцию в конкретных тканях, таких как листья, корни, семена, волокна, сосуды ксилемы, трахеиды или склеренхима. Такие промоторы называют "тканепредпочтительными". Промоторы, которые инициируют транскрипцию только в определенных тканях, называются "тканеспецифичными". Промотор, специфичный по "типу клетки", осуществляет экспрессию преимущественно в определенных типах клеток в одном или более органах, например, в сосудистых клетках корней или листьев. "Индуцибельным" промотором может быть промотор, который может регулироваться окружающей средой. Примеры условий окружающей среды, при которых может проходить транскрипция индуцибельными промоторами, включают в себя анаэробные условия или присутствие света. Тканеспецифичные, тканепредпочтительные, специфичные по типу клетки и индуцибельные промоторы составляют класс "неконститутивных" промоторов. "Конститутивный" промотор представляет собой промотор, который может быть активным в большинстве условий окружающей среды.
A. Индуцибельные промоторы
Индуцибельный промотор может быть функционально связан с геном для экспрессии в клетке. Необязательно, индуцибельный промотор может быть функционально связан с нуклеотидной последовательностью, кодирующей сигнальную последовательность, которая может быть функционально связана с геном для экспрессии в клетке. При наличии индуцибельного промотора скорость транскрипции увеличивается в ответ на индуцирующий агент.
В настоящем изобретении можно использовать любой индуцибельный промотор. См. Ward et al, Plant Mol. Biol. 22:361-366 (1993). Примеры индуцибельных промоторов включают в себя без ограничения: промоторы из системы ACEI, которые реагируют на медь (Mett et al., PNAS 90:4567-4571 (1993)); ген In2 из кукурузы, который реагирует на антидоты бензолсульфонамидного гербицида (Hershey et al, Mol. Gen Genetics 227:229-237 (1991) и Gatz et al, Mol. Gen. Genetics 243:32-38 (1994)); и ген - репрессор Tet из Tnl0 (Gatz et al., Mol. Gen. Genetics 227:229-237 (1991)). Особенно полезным индуцибельным промотором может быть промотор, который реагирует на индуцирующий агент, на который растение обычно не реагирует. Примером индуцибельного промотора может быть индуцибельный промотор из гена стероидного гормона, транскрипционную активность которого можно индуцировать глюкокортикостероидным гормоном. Schena et al., Proc. Natl. Acad. Sci. USA 88:0421 (1991).
B. Конститутивные промоторы
Конститутивный промотор может быть функционально связан с геном для экспрессии в клетке, или конститутивный промотор может быть функционально связан с нуклеотидной последовательностью, кодирующей сигнальную последовательность, которая может быть функционально связана с геном для экспрессии в клетке.
В настоящем изобретении можно использовать различные конститутивные промоторы. Примеры конститутивных промоторов включают в себя без ограничения: промоторы из вирусов растений, например, промотор 35S из CaMV (Odell et al., Nature 313:810-812 (1985)) и промотор из вируса прожилковой мозаики маниоки (CsVMV) (см., например, патенты США 7053205 и 6664384); промоторы из гена риса actin (McElroy et al, Plant Cell 2: 163-171 (1990)); убиквитин (Christensen et al., Plant Mol. Biol. 12:619-632 (1989) и Christensen et al., Plant Mol. Biol. 18:675-689 (1992)); pEMU (Last et al., Theor. Appl. Genet. 81:581-588 (1991)); MAS (Velten et al., EMBO J. 3:2723-2730 (1984)); и гистон H3 кукурузы (Lepetit et al, Mol. Gen. Genetics 231:276-285 (1992) и Atanassova et al., Plant Journal 2 (3): 291-300 (1992)). Особенно полезным конститутивным промотором является промотор ALS, фрагмент 5' Xbal/Ncol к структурному гену Brassica napus ALS3 (или нуклеотидная последовательность, подобная указанному фрагменту Xbal/Ncol). См. PCT заявку WO 96/30530.
C. Тканеспецифичные или тканепредпочтительные промоторы
Тканеспецифичный промотор может быть функционально связан с геном для экспрессии в клетке. Необязательно, тканеспецифичный промотор может быть функционально связан с нуклеотидной последовательностью, кодирующей сигнальную последовательность, которая может быть функционально связана с геном для экспрессии в клетке. Растения, трансформированные рассматриваемым геном, функционально связанным с тканеспецифичным промотором, могут продуцировать белковый продукт трансгена исключительно или предпочтительно в конкретной ткани.
В настоящем изобретении можно использовать любой тканеспецифичный или тканепредпочтительный промотор. Примеры тканеспецифичных или тканепредпочтительных промоторов включают в себя без ограничения промотор, предпочтительный для корней, например, промотор из гена фазеолина (Murai et al., Science 23:476-482 (1983) и Sengupta-Gopalan et al., Proc. Natl. Acad. Sci. USA 82:3320-3324 (1985)); специфичный для листьев и индуцируемый светом промотор, такой как промотор из cab или rubisco (Simpson et al., EMBO J. 4(11):2723-2729 (1985) и Timko et al., Nature 318:579-582 (1985)); промотор, специфичный для пыльника, например, промотор из LAT52 (Twell et al., Mol. Gen. Genetics 217:240-245 (1989)); специфичный для пыльцы промотор, такой как Zm13 (Guerrero et al, Mol. Gen. Genetics 244: 161-168 (1993)) или предпочтительный для микроспор промотор, такой как промотор из apg (Twell et al., Sex. Plant Reprod. 6:217-224 (1993)).
Транспорт белка, продуцируемого трансгенами, в субклеточное пространство, например, в хлоропласт, вакуолю, пероксисому, глиоксисому, клеточную стенку или митохондрию, или для секреции в апопласт, может осуществляться посредством функционального присоединения нуклеотидной последовательности, кодирующей сигнальную последовательность, к 5' и/или 3'-областям гена, кодирующего рассматриваемый белок. Нацеливание последовательностей на 5' и/или 3' концах структурного гена во время синтеза и процессинга белка может определить, где может произойти окончательная компартментализация кодируемого белка. Альтернативно, такие белки, нацеленные на субклеточное пространство, могут непосредственно связываться с гамма-зеином для нацеливания молекулы, на желательное субклеточное пространство.
Присутствие сигнальной последовательности направляет полипептид или к внутриклеточному органоиду или в субклеточное пространство, или для секреции в апопласте. В данной области известно множество сигнальных последовательностей. См., например, Becker et al., Plant Mol. Biol. 20:49 (1992), Close, P. S., Master's Thesis, Iowa State University (1993), Knox, С et al., "Structure and Organization of Two Divergent Alpha-Amylase Genes from Barley", Plant Mol. Biol. 9:3-17 (1987), Lerncr ct al., Plant Physiol. 91:124-129 (1989), Fontes ct al., Plant Cell 3:483-496 (1991), Matsuoka et al., Proc. Natl. Acad. Sci. 88:834 (1991), Gould et al., J. Cell. Biol. 108:1657 (1989), Creissen et al., Plant J. 2; 129 (1991), Kalderon et al., A short amino acid sequence able to specify nuclear location, Cell 39:499-509 (1984), Steifel et al., Expression of a maize cell wall hydroxyproline-rich glycoprotein gene in early leaf and root vascular differentiation, Plant Cell 2:785-793 (1990).
Гены чужих белков и гены, представляющие агрономический интерес
С помощью трансгенных растений согласно настоящему изобретению чужой белок может быть произведен в коммерческих количествах. Таким образом, технологии селекции и размножения трансформированных растений, которые широко распространены в данной области, в результате дают множество трансгенных растений, сбор которых проводят общепринятыми способами, и затем из рассматриваемой ткани или из общей биомассы можно извлекать чужой белок. Извлечение белка из растительной биомассы можно осуществлять известными способами, которые рассмотрены, например, авторами Heney and Orr, Anal. Biochem. 114:92-6 (1981).
В аспектах изобретения трансгенное растение, предназначенное для коммерческого получения чужого белка, может представлять собой клетку или растение. В других аспектах рассматриваемая биомасса может быть семенами. Для относительно небольшого количества трансгенных растений, которые проявляют более высокие уровни экспрессии, можно создавать генетическую карту прежде всего посредством общепринятых анализов ПДРФ (полиморфизма длин рестрикционных фрагментов), ПЦР (полимеразно-цепной реакцией) и SSR (простых повторяющихся последовательностей), которые определяют приблизительную хромосомную локализацию интегрированной молекулы ДНК. В этом плане примеры методик см. в публикациях Glick and Thompson, Methods in Plant Molecular Biology and Biotechnology CRC Press, Boca Raton 269:284 (1993). Информация по картированию в отношении хромосомной локализации может быть полезной для собственной защиты рассматриваемого трансгенного растения. Если может произойти непредусмотренное размножение и скрещивание с другой зародышевой плазмой, карту области интеграции можно сравнивать с подобными картами подозрительных растений, чтобы определить наличие у последних общего происхождения с рассматриваемым растением. Сравнения карт будут охватывать гибридизации, ПДРФ, ПЦР, SSR и секвенирование, все из которых являются общепринятыми методиками.
Аналогично, в трансформированных клетках или в их потомстве можно экспрессировать гены, представляющие агрономический интерес. Более подробно, растения можно генетически конструировать с помощью способов по изобретению для экспрессии разнообразных фенотипов, представляющих агрономический интерес. Примеры генов, которые можно использовать в этом отношении, включают в себя без ограничения гены с