Способ прогнозирования обострения бронхиальной астмы
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к болезням внутренних органов, и предназначено для прогнозирования обострения бронхиальной астмы. Проводят забор периферической крови на стадии ремиссии заболевания. Полученную кровь делят на две пробы. Проводят ультрафиолетовое облучение одной из проб в течение 60 секунд. Получают из них образцы сыворотки крови, которые исследуют методом краевой дегидратации в поляризованном свете. При обнаружении агрегаций кристалла-сферолита и внедренного в него шаровидного скопления мелких слабоанизотропных гранул в пробе, облучению не подвергавшейся, и кристаллов-сферолитов, окруженных рыхло расположенными скоплениями слабоанизотропных гранул, в пробе, подвергшейся облучению, прогнозируют обострение бронхиальной астмы. Способ прост, объективен, точен и доступен, безопасен для пациента, позволяет достоверно прогнозировать обострение бронхиальной астмы на доклинической стадии, когда проведение профилактических мероприятий будет своевременным и не даст возможности перейти заболеванию в стадию обострения. 2 пр., 2 ил.
Реферат
Изобретение относится к медицине, а именно к болезням внутренних органов, и может быть использовано для прогнозирования обострения бронхиальной астмы (БА).
Несмотря на значительные успехи в исследовании проблемы БА, до сих пор отсутствуют точные диагностические критерии для определения периода БА и прогнозирования обострения заболевания. В настоящее время диагностика обострения и ремиссии БА основывается преимущественно на клинических проявлениях заболевания и данных анамнеза и зачастую носит субъективный характер, так как определенная часть больных БА плохо ощущает выраженность симптомов, и такие больные могут не жаловаться на ухудшение даже при значительном снижении функции легких, что чаще наблюдается у пациентов с угрожающими жизни обострениями БА в анамнезе. С другой стороны, снижение пиковой скорости выдоха при обострении БА может появляться позже, чем увеличение выраженности симптомов БА (Chan-Yeung M, Changes in peak flow, symptom score and the use of medications during acute exacerbations of asthma, Am. J. Respir. Crit. Care Med., 1996, Vol. 154, p. 889-893). Разработка объективных критериев для прогнозирования обострения заболевания представляет научный и практический интерес, поскольку обострения БА отражают высокую активность воспалительного процесса в дыхательных путях, прогрессирование воспаления, исходом которого является ремоделирование морфологической структуры бронхов с последующим развитием хронической дыхательной недостаточности, а целью лечения БА является достижение ремиссии, поддержание контроля над заболеванием и предупреждение обострений.
Известен способ прогнозирования нестабильного течения БА (RU 2262891 С1, 17.03.2004), заключающийся в том, что определяют показатель скорости бронхиального мукоцилиарного клиренса радиофармпрепарата радиоаэрозольным методом в % за 1 час, с помощью величины данного показателя определяют дискриминантную функцию, и при ее значении выше определенного порогового значения прогнозируют нестабильное течение БА. Недостатками данного способа являются необходимость дорогостоящего оборудования и радиофармпрепаратов, лучевая нагрузка на организм обследуемого, возможность развития аллергических реакций, наличие общих противопоказаний к проведению сцинтиграфии.
Наиболее близким к заявленному способу является способ прогнозирования обострения БА (Антонович Ж.В., Прогнозирование обострения бронхиальной астмы на основе исследования показателей клеточного иммунитета, апоптоза лимфоцитов периферической крови и концентрации цитокинов интерлейкина-4 и интерферона-γ. Медицинский журнал: научно-практический рецензируемый журнал, 2010 г., №1, с. 28-32), заключающийся в заборе и исследовании периферической крови на стадии ремиссии заболевания, а именно в цитофлюорометрическом определении показателя процентного содержания в крови естественных регуляторных Т-клеток (CD4+CD25hi), показателя процентного содержания лимфоцитов, находящихся на ранней стадии индуцированного ФГА апоптоза в 72-часовых культурах лимфоцитов, показателей «IFN-γ/IL-4 и СД25+», показателей «СД8+и СД25+», определении показателя ОВФ1 и последующем построении и анализе 5 моделей логит-регрессии. Однако данный способ имеет ряд недостатков: он требует дорогостоящего оборудования и реактивов, сложен, неточность в определении одного из множества показателей, участвующих в расчетах, может повлечь за собой ошибки в прогнозировании обострения БА.
Таким образом, существует потребность в простом, доступном, достоверном и безопасном для пациента способе прогнозирования БА.
Задачей изобретения является устранение указанных недостатков и получение объективных оценочных характеристик в условиях in vitro, позволяющих на доклинической стадии заболевания прогнозировать у больных обострение бронхиальной астмы при исследовании их биологического материала, а именно по изменению структуры неклеточной ткани - сыворотки крови, способной передавать диагностическую информацию на уровне молекулярных нарушений при воздействии на нее светового облучения. Это позволит точно и объективно прогнозировать обострение бронхиальной астмы, когда проведение профилактических мероприятий будет своевременным и не даст возможности перейти заболеванию в стадию обострения.
В настоящее время установлено, что при облучении светом биологического вещества возникают эффекты, связанные с его селективным поглощением. Поглощение кванта энергии сопровождается переходом молекул в электронно-возбужденное состояние. При поглощении света происходит взаимодействие электрического вектора световой волны с электронным облаком молекулы, в результате чего молекулам передается квант энергии и происходит переход с пассивного на возбужденный электронно-колебательно-вращательный уровень. Эта энергия мигрирует при соударениях с другими молекулами, пока не произойдет химическая реакция, требующая определенных затрат энергии. Такие реакции биологически целесообразны и необходимы для осуществления механизмов регуляции (Карандашов В.И., Петухов Е.Б., Зродников B.C. Квантовая терапия. М., 2004, с. 8-12).
Взяв за основу это положение, нами был проведен теоретический анализ механизмов действия света различных длин волн на биологические объекты и в качестве источника внешнего воздействия на кровь больных БА с контролируемым лечением было выбрано ультрафиолетовое облучение.
Известно, что в результате ультрафиолетового облучения крови (УФОК) происходит изменение свойств органических макромолекул: снижается активность факторов свертывания, увеличивается фагоцитарная активность нейтрофилов, происходит разрушение тромбоцитов. Образуются сложные химические соединения (пероксиды, активный озон, озониды и др.), которые, вместе с продуктами распада тромбоцитов и других клеток крови обладают высокой биологической активностью, способной вызвать дисрегуляцию биологических процессов (Карандашов В.И., Петухов Е.Б., Зродников B.C. Квантовая терапия. М., 2004, с. 36-50). При прочных связях межмолекулярных структур, характерных для организма больных с устойчивой ремиссией БА, провоцирование в крови «хаоса» путем создания макроэргических связей, не способно перевести «шары» из слабоанизотропных гранул в состояние дегрануляции (россыпи). Если ремиссия заболевания неустойчива, то провоцирующее УФОК способно вызвать соответствующий отклик в клеточном составе крови (дегрануляция базофилов, эозинофилов), который может быть оценен по морфологической картине сыворотки крови в виде эффекта дегрануляции структур, которое дает картину рыхло расположенных скоплений слабоанизотропных гранул.
Для этого в способе прогнозирования обострения бронхиальной астмы, включающем забор и исследование периферической крови на стадии ремиссии заболевания, предложено полученную кровь делить на две пробы, при этом проводят ультрафиолетовое облучение одной из проб в течение 60 секунд, получают из них образцы сыворотки крови, которые исследуют методом краевой дегидратации в поляризованном свете, и при обнаружении агрегаций кристалла-сферолита и внедренного в него шаровидного скопления мелких слабоанизотропных гранул в пробе, облучению не подвергавшейся, и кристаллов-сферолитов, окруженных рыхло расположенными скоплениями слабоанизотропных гранул, в пробе, подвергшейся облучению, прогнозируют обострение бронхиальной астмы.
Способ осуществляют следующим образом.
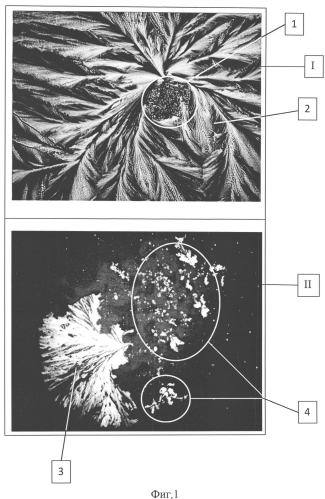
У пациента с БА на стадии ремиссии забирают 5 мл крови из вены или мякоти пальца утром, строго натощак. Кровь разделяют по 2,5 мл в две пробирки: проба I (контроль) и проба II. Пробу II облучают ультрафиолетом с помощью аппарата УФО «Надежда» длиной волны 254 нм в течение 60 с. Затем из обеих проб получают сыворотку крови путем центрифугирования в течение 10 мин при 1500 об/мин, создают аналитические ячейки методом краевой дегидратации, т.е. сыворотку крови каждой пробы наносят на поверхность предметного стекла в количестве 0,02 мл, накрывают покровным стеклом и дегидратируют при +20-25°C при относительной влажности 55-60% (аналитических ячеек для каждой пробы должно быть не менее трех). После трех суток краевой дегидратации проводят сравнительную микроскопию структур сыворотки крови обеих проб в поляризованном свете. При этом если в первой пробе (I) выявляют агрегации кристалла-сферолита (1) и внедренного в него шаровидного скопления мелких слабоанизотропных гранул (2), а во второй пробе (II) - кристаллы-сферолиты (3), окруженных рыхло расположенными скоплениями слабоанизотропных гранул (4), прогнозируют обострение БА (фиг. 1). Отрицательный прогноз обострения БА отмечают при наличии в обеих пробах (I, II) однотипных агрегаций кристалла-сферолита (1) и внедренного в него шаровидного скопления мелких слабоанизотропных гранул (2) (фиг. 2).
Пример 1.
Пациент Р., 37 лет с диагнозом: «Бронхиальная астма, стадия ремиссии». Исследование крови предлагаемым способом показало, что при сравнительной микроскопии структур обеих проб сыворотки крови в поляризованном свете в пробе I определяются агрегации кристалла-сферолита и внедренного в него шаровидного скопления мелких слабоанизотропных гранул, а в пробе II - кристаллы-сферолиты, окруженные рыхло расположенными скоплениями слабоанизотропных гранул (фиг. 1).
Заключение: прогнозируется обострение БА.
Пациент не имел возможности пройти курс профилактики обострения заболевания. Через месяц он поступил в стационар с обострением заболевания.
Пример 2.
Пациент И., 42 лет с диагнозом: «Бронхиальная астма, стадия ремиссии». Исследование крови предлагаемым способом показало, что при сравнительной микроскопии структур обеих проб сыворотки крови в поляризованном свете отмечалась идентичная картина. В обеих пробах (I, II) определялись агрегации кристалла-сферолита и внедренного в него шаровидного скопления мелких слабоанизотропных гранул (фиг. 2).
Заключение: обострение БА не прогнозируется.
Наблюдение за пациентом в течение 6 месяцев показало отсутствие обострения заболевания, т.е. заболевание характеризовалось устойчивой ремиссией.
Предлагаемый способ прост, объективен, точен и доступен, безопасен для пациента, позволяет достоверно прогнозировать обострение бронхиальной астмы на доклинической стадии, когда проведение профилактических мероприятий будет своевременным и не даст возможности перейти заболеванию в стадию обострения.
Способ прогнозирования обострения бронхиальной астмы, включающий забор и исследование периферической крови на стадии ремиссии заболевания, отличающийся тем, что полученную кровь делят на две пробы, при этом проводят ультрафиолетовое облучение одной из проб в течение 60 секунд, получают из них образцы сыворотки крови, которые исследуют методом краевой дегидратации в поляризованном свете, и при обнаружении агрегаций кристалла-сферолита и внедренного в него шаровидного скопления мелких слабоанизотропных гранул в пробе, облучению не подвергавшейся, и кристаллов-сферолитов, окруженных рыхло расположенными скоплениями слабоанизотропных гранул, в пробе, подвергшейся облучению, прогнозируют обострение бронхиальной астмы.