Способ и набор для диагностики гломерулонефрита у кошки
Иллюстрации
Показать всеГруппа изобретений относится к области биотехнологии. Способ диагностики наличия гломерулонефрита у кошки предусматривает измерение уровня экспрессии одного или нескольких биомаркеров, выбранных из группы, состоящей из люмикана; цепи коллагена альфа 1 (III), варианта 12; декорина; секретируемого родственного frizzled белка 2; ретинол-связывающего белка 5; MMP-2; MMP-7 и MMP-19, в биологическом образце, полученном от кошки. При этом значимое отличие в экспрессии одного или нескольких биомаркеров в образце по сравнению с контрольным значением для экспрессии в образце, полученном от здорового животного, свидетельствует о наличии расстройства почек. В группу изобретений также входит набор для осуществления указанного способа, с возможным использованием для диагностики нуклеотидных последовательностей комплементарных указанным выше генам. Проведение диагностика гломерулонефрита с использованием данной группы изобретений позволяет выявлять и прогнозировать развитие гломерулонефрита на ранних стадиях. 3 н. и 19 з.п. ф-лы, 16 ил., 4 табл., 6 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к композициям, веществам и способам диагностики и/или мониторинга заболеваний и расстройств почек у кошачьих, включая способы диагностики, выработки и контролирования плана лечения и мониторинга состояния в случае расстройства почек, характеризуемого аномальной утратой функции почек, почечной недостаточностью, пониженной скоростью клубочковой фильтрации или гломерулонефритом, у кошачьих, посредством измерения экспрессии выбранных генов.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка содержит список последовательностей, который был представлен в EFS-Web и включен в настоящее описание в виде ссылки в полном объеме. Указанная копия ASCII, созданная 30 марта 2010 г., названа 8888POUS.txt и имеет размер 7809 байт.
УРОВЕНЬ ТЕХНИКИ
Нефрит является общим термином воспаления почек, которое может представлять собой очаговое или диффузное пролиферативное или деструктивное заболевание, в которое вовлечены клубочки, почечные канальцы или интерстициальная (или соединительная) ткань почек. Нефрит может прогрессировать, проходя ряд стадий, заканчивающихся терминальной стадией заболевания почек или терминальной стадией почечной недостаточности. Наиболее распространенной формой нефрита является гломерулонефрит.
Гломерулонефрит или гломерулярный нефрит («GN») является состоянием, характеризуемым воспалением клубочков или капиллярных петель почки. Состояние встречается в острой, подострой и хронической формах и может быть идиопатическим или вторичным после инфекции, заболевания или воздействия токсина.
Почечная недостаточность означает неспособность почек поддерживать свои нормальные функции. В результате конечные продукты обмена веществ и метаболиты накапливаются в крови. Такие конечные продукты обмена веществ и метаболиты могут отрицательно влиять на большинство систем организма. Нарушения в поддержании водно-электролитного баланса являются характерными в случае почечной недостаточности.
Острая почечная недостаточность может возникать внезапно вследствие травмы, инфекции, воспаления или воздействия нефротоксических веществ. Такое состояние может приводить к обезвоживанию, гипотонии и циркуляторному коллапсу. Острую почечную недостаточность часто делят на три категории: (1) преренальную недостаточность, которая ассоциирована с пониженным почечным кровотоком; (2) интраренальную недостаточность, которая ассоциирована с ишемией и токсинами; и (3) постренальную недостаточность, которая является результатом обструкции мочевыводящих путей.
Хроническая почечная недостаточность заключается в прогрессирующей утрате функции почек, которая в конечном итоге может прогрессировать до терминальной стадии заболевания почек или почечной недостаточности. Вначале хроническая почечная недостаточность проявляется в виде снижения функции почек без ощутимого накопления конечных продуктов метаболизма в крови. По мере замедления скорости клубочковой фильтрации вследствие воспаления конечные продукты начинают накапливаться. Заболевание прогрессирует до уремии вследствие пониженной функции почек, и высокие уровни белковых конечных продуктов начинают накапливаться и нарушать функции организма. Распространенные причины хронической почечной недостаточности включают: воспаление, инфекцию, обструкцию мочевых путей и некоторые системные заболевания и токсические явления, включая гиперкальцемию, красную волчанку, сахарный диабет и гипертонию.
Для терминальной стадии заболевания почек характерна необратимая хроническая почечная недостаточность. Уровни креатинина в сыворотке и азота мочевины в крови продолжают повышаться, и в результате уремия нарушает все системы организма. Почка может подвергаться непрерывной и почти полной потере функции, порядка 10% или меньше от нормальной функции почки. Одной из причин терминальной стадии заболевания почек является гломерулонефрит. Другие причины включают причины, указанные для хронической почечной недостаточности.
Клубочки являются одним из структурных компонентов нефрона почки и состоят из мелких кровеносных сосудов, часто описываемых как капиллярный пучок или гроздь. Нефрон является основной структурной и функциональной единицей почки, которая также состоит из структуры, известной как мальпигиева капсула или капсула Боумена, а также содержит артериолы и канальцы. Капсула Боумена содержит клубочковые петли и почечный каналец. Клубочки содержат очень мелкие капилляры, поэтому поток крови через такие сосуды является очень медленным, и молекулы крови могут легко осаждаться на стенках таких тонких капилляров. Почечные канальцы состоят из базальной мембраны и эпителиальной выстилки и служат для секреции, сбора и проведения мочи.
Клубочек функционирует в качестве фильтра в нефроне. Вода и небольшие молекулы в крови проходят через клубочек и фильтруются через структуру, называемую базальной мембраной, которая образована базальными мембранами клубочка и капсулы Боумена. Фильтрат, содержащий воду и небольшие молекулы, проходит через почечный каналец, подвергаясь абсорбции и реабсорбции перед тем как, наконец, превратиться в мочу. Базальная мембрана имеет поры разного размера, которые служат для фильтрации небольших молекул и предотвращения прохождения через базальную мембрану более крупных молекул. Специальной функцией нефрона является удаление из плазмы некоторых конечных продуктов метаболизма, таких как мочевая кислота, мочевина и креатинин, а также электролиты, например, ионы натрия, хлора и калия. Благодаря реабсорбции воды и электролитов нефрон играет важную роль в поддержании нормального водного баланса в организме.
Креатинин является азотсодержащим соединением, образуемым в результате метаболизма креатина. Креатин, в свою очередь, является небелковым веществом, которое синтезируется в организме из трех аминокислот, аргинина, глицина и метионина. Молекула встречается в мышцах в небольших количествах и в сочетании с фосфатом в виде фосфокреатина служит в качестве формы запасания высокоэнергетического фосфата, используемого в различных метаболических процессах. Креатинин всасывается в кровь и, в конце концов, экскретируется в мочу. Таким образом, простой лабораторный тест для измерения креатинина в крови можно использовать для определения функции почек. Тест часто называют тестом клиренса креатинина, и в таком тесте измеряют количество креатинина, выводимого из плазмы в течение заданного промежутка времени. Поскольку креатинин образуется из фосфокреатина в относительно постоянных количествах, повышение уровней креатинина в крови является показателем нарушения почек, т.е., утраты функции почек.
Гломерулонефрит может возникать в результате биологического поражения иммунной системы. Чужеродные вещества могут налипать на базальной мембране и вызывать иммунную реакцию, приводящую к продукции антител. Такие антитела могут объединяться с чужеродными веществами, образуя иммунные комплексы, которые откалываются на стенках тонких клубочковых капилляров, приводя к повреждению нефрона. Альтернативно, у некоторых индивидуумов иммунная система может образовывать аутоантитела, которые представляют собой иммуноглобулины, которые могут атаковать клетки почек, приводя к так называемой аутоиммунной реакции. Если белки в организме изменены, то может возникать ответ в виде аутоантител, поскольку аутоантитела распознают измененные белки как чужие. Такие комплексы аутоантитело-белок, вероятно, могут откладываться на базальной мембране клубочка, вызывая нарушение функционирования нефрона.
Гломерулонефрит является распространенной причиной протеинурии у кошек и может быть в форме либо идиотипического, либо вторичного состояния. В последнем случае состояние может развиваться вторично вследствие неоплазии, воспалительных заболеваний, эндокринных проявлений, инфекций или наследственной нефропатии. Как и у людей, гломерулонефрит у кошек часто опосредован иммунологически с вовлечением иммуноглобулинов и факторов комплемента в организме животного. В клубочках почки возникает повреждение, приводящее к морфологическим изменениям клубочков. В конечном итоге повреждение становится необратимым и приводит к нарушению функции нефрона.
Гломерулонефрит охарактеризован в научной литературе в различных формах на основе имеющих место гистопатологических изменений. Мембранозный гломерулонефрит заключается в утолщении базальной мембраны клубочков. Пролиферативный или мезангиальный пролиферативный гломерулонефрит характеризуется пролиферацией клеток в мезангиальном матриксе. Мембранозно-пролиферативный гломерулонефрит заключается в сочетании указанных выше изменений. Гломерулосклероз характеризуется повышенным образованием и рубцеванием матрикса. В некоторых случаях имеются минимальные изменения клубочков и только небольшое повышение пролиферации мезангиальных клеток.
Был разработан ряд способов для исследования дифференциальной экспрессии генов, например, микроматрицы ДНК, секвенирование с использованием маркерных экспрессируемых последовательностей (EST), серийный анализ экспрессии генов (SAGE), вычитающая гибридизация, вычитающее клонирование и дифференциальный дисплей (DD) мРНК, произвольно РНК-праймируемая ПЦР (RAP-ПЦР), ПЦР в реальном времени (РВ-ПЦР), репрезентативный дифференциальный анализ (RDA), двумерный гель-электрофорез, масс-спектрометрия и основанное на микроматрице белков связывание антител к белкам.
Из-за сложности биологических путей, вовлеченных в заболевание почек, и имеющихся молекулярных взаимодействий и процессов межклеточной передачи сигналов, весьма желательно понять взаимодействия, которые имеют место, на генетическом уровне. Определение генов с нарушенной регуляцией на ранних стадиях утраты функции почек у кошачьих полезно для понимания биологии почечного заболевания, особенно гломерулонефрита на основе анализа всего генома. Тот факт, что нарушение регуляции генов можно выявить на ранней стадии развития заболевания у животных, подвергаемых повторному ишемическому поражению, полезен для разработки способов диагностики, и выработки плана и мониторинга лечения аномальной утраты функции почек, почечной недостаточности, пониженной скорости клубочковой фильтрации или гломерулонефрита у кошек.
Более детальное понимание вовлеченных биологических путей с использованием получения профилей экспрессии генов поможет разработать диагностические способы, реагенты и наборы для тестирования, а также полезные средства фармацевтического, нутрицевтического и пищевого (диетарного) вмешательства в патологические пути. Такие способы могут обеспечить возможность раннего выявления и потенциального предотвращения или лечения лежащего в основе заболевания почек, в частности, гломерулонефрита, а также мониторинга прогноза почечной недостаточности и гломерулонефрита на ранней стадии, особенно у кошачьих. Гены с нарушенной регуляцией, вовлеченные в патологию таких расстройств, могут служить в качестве важных биомаркеров для диагностики и возможного предотвращения или лечения расстройства и для оптимизации подбора подходящих средств для фармацевтического, нутрицевтического и пищевого (диетарного) вмешательства.
Уровень экспрессии генов и/или определение уровня функционирования экспрессированного генного продукта у кошек можно использовать для подбора соответствующего средства для терапевтического или профилактического применения. Такие данные могут быть использованы специалистом для выбора подходящих лекарств в качестве средств профилактики или лечения почечных заболеваний у кошек посредством определения профиля экспрессии генов. Данные и анализ экспрессии генов также можно применять для подбора состава кормов, пищевых добавок и нутрицевтиков, оказывающих благотворное действие на эффективность работы почек, посредством использования биомаркеров, являющихся показателями нормального функционирования почек.
До настоящего времени была проведена очень ограниченная работа по скринингу генома кошек в отношении профилей экспрессии генов в связи с диагностикой заболеваний у кошек. Исследования на здоровых популяциях кошек по сравнению с популяциями, имеющими заболевание, такое как заболевание почек и утрата функции почек, которые описаны в настоящей публикации, ранее широко не проводились. Имеется мало данных в отношении профиля экспрессии генома кошек, особенно в отношении развития заболеваний почек у кошек с течением времени.
Почечная недостаточность является лидирующей причиной смертности у кошек. Чтобы эффективно лечить заболевание почек, важно решать проблему раньше того, как почка будет серьезно повреждена. К тому моменту, когда у субъекта наблюдаются признаки почечной недостаточности, повреждение вполне может быть необратимым. Это может являться проблематичным, поскольку заболевание почек на таких ранних стадиях может не иметь никаких явных симптомов. Соответственно, существует потребность в улучшенных способах идентификации животных на ранних стадиях заболевания почек, так чтобы их можно было соответствующим образом лечить, например, обеспечивая им соответствующее питание в случае идиопатических состояний и/или условия лечения, например, инфекции или аутоиммунного заболевания, которые могут вносить вклад в проблему, чтобы помочь обратить или, по меньшей мере, замедлить и подавить прогрессирование состояния.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к композициям и способам диагностики, выработки и контролирования плана лечения и мониторинга состояния расстройства почек, характеризуемого аномальной утратой почечной функции, почечной недостаточностью, пониженной скоростью клубочковой фильтрации или гломерулонефритом у кошек, при этом расстройство почек можно выявить с использованием, по меньшей мере, одного релевантного биомаркера, выделенного и измеренного из биологического тестируемого образца, взятого у такой кошки, при этом экспрессия биомаркера положительно или отрицательно коррелирует с заболеванием. Биомаркер, подходящий для практического осуществления композиций и способов согласно настоящему изобретению, включает полинуклеотид или белок, присутствующий в таком биологическом тестируемом образце от такой кошки. Биологический тестируемый образец для практического осуществления способа согласно изобретению может содержать, например, образец ткани почки такой кошки. Биомаркеры также выбирали на основе их секреции, так чтобы их можно было выявлять в сыворотке или плазме крови или в моче. Соответственно биологическим тестируемым образцом также может быть образец биологической жидкости, взятый у такой кошки, например, крови или мочи.
Изобретение отчасти основано на открытии того, что конкретные профили экспрессии генов у кошек коррелируют с изменением у такого животного биологического процесса в почке от нормального до аномального, что может приводить к снижению функции почек с течением времени. Корреляция конкретного профиля экспрессии генов со снижением почечной функции может быть предсказана, выявлена и диагностирована у кошки без осуществления обычной клинической диагностики на основе известных в данной области клинических признаков и симптомов заболевания почек. Следовательно, измененный профиль экспрессии генов у кошки является прогностическим признаком снижения почечной функции, которое в ином случае может быть диагностировано в более поздний период времени благодаря известным в данной области измерениям функции почек. Такие известные в данной области измерения функции почек обычно могут включать, например, одно из следующих измерений: скорости клубочковой фильтрации, скорости клиренса креатинина, уровней белков в моче, уровней креатинина в сыворотке, уровней креатинина в моче, уровней азота мочевины в крови (BUN), мечения метаболитов радиоактивными изотопами, томографию мягких тканей, включая сонографию, магнитно-резонансную томографию и/или компьютерную томографию. Неинтрузивные анализы, такие как анализы креатинина в сыворотке и уровней BUN, обычно плохо коррелируют с гистопатологией почек и, в общем, не могут быть прогностическим признаком будущих изменений в почке.
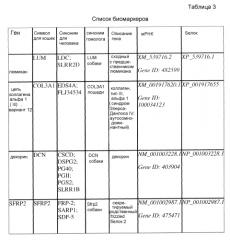
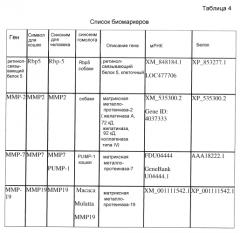
Изобретение относится, например, к способам измерения наличия расстройства почек, характеризуемого аномальной утратой почечной функции, почечной недостаточностью, пониженной скоростью клубочковой фильтрации или гломерулонефритом, включающим в себя оценку уровня генной экспрессии или активности, по меньшей мере, одного гомологичного гена кошек или продукта трансляции такого гена, выбранного из группы, состоящей из секретируемого родственного frizzle белка-2 (SFRP2); ретинол-связывающего белка 5 (rbp5); люмикана (LUM); декорина (DCN); цепи коллагена альфа 1 (III), варианта 12 (COL3A1); и матриксной металлопротеиназы-2, -7 и -19 (MMP2, MMP7 и MMP19).
Изобретение относится, например, к способам измерения наличия расстройства почек, характеризуемого аномальной утратой почечной функции, почечной недостаточностью, пониженной скоростью клубочковой фильтрации или гломерулонефритом, включающим в себя оценку уровня генной экспрессии или активности, по меньшей мере, одного гомологичного гена кошек или продукта трансляции такого гена, выбранного из группы, состоящей из секретируемого родственного frizzle белка-2 (SFRP2) и ретинол-связывающего белка 5 (rbp5); и, необязательно, второй группы, по меньшей мере, одного гомологичного гена кошек или продукта трансляции такого гена, выбранного из группы, состоящей из люмикана (LUM); декорина (DCN); цепи коллагена альфа 1 (III), варианта 12 (COL3A1); и матриксной металлопротеиназы-2, -7 и -19 (MMP2, MMP7 и MMP19).
В одном варианте настоящее изобретение относится к одному или нескольким генам или участкам генов («гены» имеют значение, которое определено в настоящем описании), которые по-другому экспрессируются у отклоняющихся от нормы животных по сравнению с нормальными животными. Изобретение основано на открытии полинуклеотидов, которые по-другому экспрессируются у животных с отклонениями от нормы по сравнению с нормальными животными. Гены идентифицировали посредством сравнения экспрессии генов в образцах ткани, взятых у животных, которых диагностировали как животных с отклонениями от нормы, с генами в образцах ткани от животных, которые диагностированы как нормальные, с использованием методики Affymetrix GeneChip®.
Полинуклеотиды и гены идентифицировали, измеряя различия в экспрессии генов в образцах тканей, взятых от кошек, которых диагностировали как животных с отклонениями от нормы и имеющих расстройство почек, и экспрессии генов в образцах тканей от кошек, которые диагностировали как нормальных. Изменения в экспрессии генов можно определять любым способом, известным специалистам в данной области. В общем, изменения в экспрессии генов определяют, измеряя транскрипцию (определяя количество мРНК, продуцируемой геном) или измеряя трансляцию (определяя количество белка, продуцируемого геном). Количество РНК или белка, продуцируемого геном, можно определить, используя любой способ, известный специалистам в данной области для количественной оценки полинуклеотидов и белков.
Обычно экспрессию мРНК определяют, используя полимеразную цепную реакцию (ПЦР) (включая без ограничения ПЦР с обратной транскрипцией (ОТ-ПЦР) и количественную ПЦР в реальном времени (кПЦР)), матрицы коротких и длинных олигонуклеотидов, матрицы кДНК, EST-секвенирование, Нозерн-блоттинг, SAGE, MPSS, MC, матрицы на шариках и другие способы гибридизации. Измеряемая РНК обычно находится в форме мРНК или обратно транскрибированной мРНК.
Экспрессию белка или полипептида определяют, используя различные колориметрические и спектроскопические анализы и способы, такие как количественные Вестерн-блоты, ELISA, двумерные гели, газовая или жидкостная хроматография, масс-спектроскопия, анализ по Лоури, биуретовый анализ, флуоресцентные анализы, турбидиметрические способы, бицинхониновый анализ, методику белковых чипов, поглощение инфракрасного излучения, нингидриновый анализ, анализ по Бредфорду и поглощение ультрафиолетового излучения.
Генные чипы обеспечивают возможность крупномасштабного исследования биологических процессов и измерения активности в клетке в определенной временной точке. Анализ микроматриц позволяет оценивать различия в фенотипах на генетической основе в крупном масштабе. Фактическое измерение продуктов экспрессии генов является более точным показателем функционирования гена, чем определение последовательностей как таковых. Анализ на микроматрицах основан на количественном определении концентрации РНК-транскрипта гена в клетке в данный момент времени. ДНК иммобилизуют на среде и меченую мРНК-мишень гибридизуют с зондами на матрице. Связывание меченой мРНК с зондами измеряют, используя лазерный анализ. Измерение представляет собой подсчет испускаемых фотонов. Весь чип сканируют и получают цифровые изображения. Изображение обрабатывают, чтобы определить положение зондов и получить измерения интенсивности для каждого зонда. Таким образом можно определить подвергаемые повышающей и понижающей регуляции гены. Анализ позволяет специалисту найти группы генов со сходными профилями экспрессии и определить ткани со сходными профилями экспрессии. Таким образом можно идентифицировать гены, которые объясняют наблюдаемые различия.
Для генных чипов Affymetrix обычно используют зонды длиной 25 п.н. и наборы зондов, состоящие из 11-20 зондов, соответствующих конкретному гену или EST. Чип конструируют с идеально совпадающим и несовпадающим зондом, каждый из которых имеет длину 25 п.н., при этом первый является абсолютно комплементарным конкретной области гена, а последний имеет замену 13-ой п.н. для получения ошибочного спаривания. Используют алгоритм суммирования зондов, чтобы определить поправку на фон, осуществить нормализацию и суммирование зондов, который представляет собой преобразование значений, полученных для зондов с получением значений экспрессии для набора зондов. RMA является одним из алгоритмов, который можно использовать для такой цели. Алгоритм осуществляет две последние стадии анализа, нормализацию и суммирование измерений интенсивности на уровне зондов. Следовательно, идеально совпадающие значения являются скорректированными относительно фона, нормализованы и суммированы с получением набора измерений экспрессии.
Исходные данные анализируют, используя компьютерную программу GeneSpring версии 7.0 (GS) (Agilent Corporation), и подтверждают, используя бесплатное программное обеспечение R-Bioconductor (RB). Оба пакета компьютерных программ использовали для расчета интенсивностей для зондов из CEL-файлов, созданных на приборе Affymetrix. Наличие/отсутствие/пограничные сигналы на зонд и P-значения оценивали, используя компьютерные программы R-Bioconductor и GeneSpring по отдельности.
В общем, по-разному экспрессируемые гены у животных с отклонениями от нормы по сравнению с нормальными животными определяют, измеряя экспрессию, по меньшей мере, одного гена. Предпочтительно измеряют экспрессию двух или более дифференциально экспрессируемых генов, чтобы получить картину экспрессии генов или профиль экспрессии генов. Более предпочтительно измеряют экспрессию множества дифференциально экспрессируемых генов, чтобы получить дополнительную информацию для более значимой картины или профиля экспрессии генов.
Настоящее изобретение относится к множеству маркеров, которые вместе или в отдельности являются или могут быть использованы в качестве маркеров заболевания почек. В особенно применимых вариантах осуществления изобретения можно выбрать множество таких маркеров, и экспрессия их мРНК может быть измерена одновременно, чтобы получить профили экспрессии для применения в различных аспектах изобретений, описанных в настоящей заявке. В предпочтительном варианте предлагаемых способов и композиций, по меньшей мере, 2, 3, 4, 5, 6, 7 или 8 маркеров выбраны из группы, состоящей из: секретируемого родственного frizzle белка-2 (SFRP2) или кошачьего гомолога или его фрагмента (SEQ ID NO: 9); ретинол-связывающего белка 5 (rbp5) или кошачьего гомолога или его фрагмента (SEQ ID NO: 10); люмикана (LUM) или кошачьего гомолога или его фрагмента (SEQ ID NO: 11); декорина (DCN) или кошачьего гомолога или его фрагмента (SEQ ID NO: 12); цепи коллагена альфа 1 (III), варианта 12 (COL3A1) или кошачьего гомолога или ее фрагмента (SEQ ID NO: 13); матриксной металлопротеиназы-2 (MMP2) или кошачьего гомолога или ее фрагмента (SEQ ID NO: 14); матриксной металлопротеиназы-7 (MMP7, PUMP-1) или кошачьего гомолога или ее фрагмента (SEQ ID NO: 15); и матриксной металлопротеиназы-19 (MMP19) или кошачьего гомолога или ее фрагмента (SEQ ID NO: 16), и могут быть использованы для определения профилей экспрессии генов, применяемых при практическом осуществлении способов согласно изобретению. Каждый маркер может быть, в частности, связан с определенными аспектами заболевания почек.
Настоящее изобретение относится к множеству маркеров, которые вместе или в отдельности являются или могут быть использованы в качестве маркеров заболевания почек. В другом особенно применимом варианте осуществления изобретения может быть выбрано множество таких маркеров, и экспрессия их мРНК может быть измерена одновременно для получения профилей экспрессии для применения в различных аспектах изобретений, описанных в настоящей заявке. В предпочтительном варианте предлагаемых в настоящем изобретении способов и композиций, по меньшей мере, 2, 3, 4, 5, 6, 7 или 8 маркеров выбраны из группы, состоящей из секретируемого родственного frizzle белка-2 (SFRP2) или кошачьего гомолога или его фрагмента (SEQ ID NO: 9) и ретинол-связывающего белка 5 (rbp5) или кошачьего гомолога или его фрагмента (SEQ ID NO: 10); и, необязательно, второй группы, состоящей из, по меньшей мере, одного полинуклеотида, выбранного из группы, состоящей из люмикана (LUM) или кошачьего гомолога или его фрагмента (SEQ ID NO: 11); декорина (DCN) или кошачьего гомолога или его фрагмента (SEQ ID NO: 12); цепи коллагена альфа 1 (III), варианта 12 (COL3A1) или кошачьего гомолога или его фрагмента (SEQ ID NO: 13); матриксной металлопротеиназы-2 (MMP2) или кошачьего гомолога или ее фрагмента (SEQ ID NO: 14); матриксной металлопротеиназы-7 (MMP7, PUMP-1) или кошачьего гомолога или ее фрагмента (SEQ ID NO: 15); и матриксной металлопротеиназы-19 (MMP19) или кошачьего гомолога или ее фрагмента (SEQ ID NO: 16), и могут быть использованы для определения профилей экспрессии генов, применяемых при практическом осуществлении способов согласно изобретению. Каждый маркер может быть, в частности, связан с некоторыми аспектами заболевания почек.
В другом аспекте изобретение относится к устройству, подходящему для детекции экспрессии множества генов, по-разному экспрессируемых у кошек с отклонениями от нормы по сравнению с нормальными кошками. Устройство включает в себя подложку, имеющую множество олигонуклеотидных или полинуклеотидных зондов согласно настоящему изобретению, фиксированных на подложке в известных положениях. Устройство по существу представляет собой иммобилизованный вариант олигонуклеотидных или полинуклеотидных зондов, описанных в настоящей публикации. Устройство применимо для быстрой и специфичной детекции генов и полинуклеотидов и картин и профилей их экспрессии. Обычно такие зонды связаны с подложкой или сходным твердым носителем, и образец, содержащий один или несколько полинуклеотидов (например, ген, продукт ПЦР, продукт лигазной цепной реакции (LCR), последовательность ДНК, которая была синтезирована с использованием способов амплификации, или их смесь) подвергают воздействию зондов, чтобы полинуклеотид(-ы) в образце мог гибридизоваться с зондами. Зонды, полинуклеотид(-ы) в образце, или и то и другое метят, обычно флуорофором или другой меткой, такой как стрептавидин, и выявляют, используя способы, известные специалистам в данной области. Если метят полинуклеотид(-ы) в образце, то гибридизацию можно выявлять, регистрируя связанную флуоресценцию. Если метят зонды, то гибридизацию обычно выявляют, используя гашение метки. Если метят и зонд и полинуклеотид(-ы) в образце, то гибридизацию обычно выявляют, наблюдая за сдвигом окраски, возникающим в результате близости двух связанных меток. Множество методик мечения и меток известны специалистам в данной области, в частности, в случае флуоресцирующих меток. Предпочтительно зонды иммобилизуют на подложках, подходящих для создания матрицы (известных под несколькими названиями, включая микроматрицу ДНК, генный чип, биочип, ДНК-чип и генную матрицу), сравнимых с подложками, известными в данной области.
Способы определения количества или концентрации белка в образце известны специалистам в данной области. Такие способы включают радиоиммуноанализы, анализы конкурентного связывания, Вестерн-блот-анализ и анализы ELISA. В случае способов, в которых используют антитела, подходящими являются поликлональные и моноклональные антитела. Такие антитела могут быть иммунологически специфичными для белка, эпитопа белка или фрагмента белка.
В некоторых вариантах осуществления изобретения используют антитела для выявления и количественной оценки белков, продуцируемых при экспрессии полинуклеотидов согласно настоящему изобретению. Хотя белки можно выявлять с использованием иммунопреципитации, аффинного разделения, Вестерн-блот-анализа, белковых матриц и тому подобного, при этом в предпочтительном способе используют методику ELISA, в которой антитело иммобилизуют на твердой подложке, и белок-мишень или пептид подвергают взаимодействию с иммобилизованным антителом. Либо зонд, либо мишень, либо и то и другое можно метить, используя известные способы.
В следующем аспекте изобретение относится к способу выявления в образце дифференциальной экспрессии одного или нескольких генов, по-разному экспрессируемых у кошек с отклонениями от нормы по сравнению с нормальными кошками. Способ включает в себя (a) гибридизацию сочетания, содержащего множество полинуклеотидных зондов, которые по-разному экспрессируются у кошек с отклонениями от нормы по сравнению с нормальными кошками, с полинуклеотидами в образце с образованием одного или нескольких гибридизационных комплексов; (b) необязательно гибридизацию сочетания, содержащего множество полинуклеотидных зондов, которые по-разному экспрессируются у кошек с отклонениями от нормы по сравнению с нормальными кошками, с полинуклеотидами в стандарте с образованием одного или нескольких гибридизационных комплексов; (c) выявление гибридизационных комплексов в образце и, необязательно, в стандарте со стадии (b); и (d) сравнение гибридизационных комплексов в образце с гибридизационными комплексами в стандарте, при этом различие в количестве гибридизационных комплексов между стандартом и образцом свидетельствует о дифференциальной экспрессии в образце генов, по-другому экспрессируемых у животных с отклонениями от нормы по сравнению с нормальными животными.
Стадия (b) и часть стадии (c) являются необязательными, и их используют в том случае, если необходимо осуществить относительно одновременное сравнение двух или более тест-систем. Однако в предпочтительном варианте стандарт, используемый для сравнения, основан на данных, полученных ранее с применением такого способа.
Указанные зонды выдерживают с образцом для образования гибридизационных комплексов, которые выявляют и сравнивают с гибридизационными комплексами стандарта. Различия между гибридизационными комплексами в образце и стандарте свидетельствуют о дифференциальной экспрессии в образце полинуклеотидов и, следовательно, генов, по-разному экспрессируемых у кошек с отклонениями от нормы по сравнению с нормальными кошками. В предпочтительном варианте получают зонды для специфичного выявления полинуклеотидов или их фрагментов, продуцируемых одним или несколькими генами или фрагментами генов, идентифицированными в настоящем изобретении. Способы выявления гибридизационных комплексов известны специалистам в данной области.
В другом аспекте изобретение относится к способу выявления в образце дифференциальной экспрессия генов, по-разному экспрессируемых у кошек с отклонениями от нормы по сравнению с нормальными кошками. Способ включает в себя (a) взаимодействие сочетания, содержащего множество полипептидных зондов с белками в образце в условиях, которые обеспечивают возможность осуществления специфичного связывания между зондами и белками, при этом белки, связываемые зондами по-разному экспрессируются у кошки с отклонениями от нормы по сравнению с нормальной кошкой; (b) необязательно взаимодействие сочетания, содержащего множество полипептидных зондов с белками в стандарте в условиях, которые обеспечивают возможность осуществления специфичного связывания между зондами и белками, при этом белки, связываемые зондами, по разному экспрессируются у кошки с отклонениями от нормы по сравнению с нормальной кошкой; (c) выявление специфичного связывания в образце и необязательно в стандарте со стадии (b); и (d) сравнение специфичного связывания в образце со специфичным связыванием в стандарте, при этом различия между специфичным связыванием в стандарте и образце свидетельствуют о дифференциальной экспрессии в образце генов, по-разному экспрессируемых у кошек с отклонениями от нормы по сравнению с нормальными кошками.
Указанные зонды подвергают взаимодействию с образцом, чтобы происходило специфичное связывание, которое выявляют и сравнивают со специфичным связыванием в стандарте. Различия между специфичным связыванием в образце и стандарте свидетельствуют о дифференциальной экспрессии в образце белков и, следовательно, генов, по-разному экспрессируемых у кошек с отклонениями от нормы по сравнению с нормальными кошками, особенно генов, ассоциированных с отклонениями от нормы. В предпочтительном варианте получают зонды для специфичного выявления белков или их фрагментов, продуцируемых одним или несколькими генами или фрагментами генов, идентифицированными в настоящем изобретении.
В одном варианте способ дополнительно включает в себя воздействие на кошку или образец тестируемым веществом перед взаимодействием полипептидов с белками. Затем сравнение является показателем того, изменяет ли тестируемое вещество экспрессию в образце генов, по-разному экспрессированных у кошек с отклонениями от нормы по сравнению с нормальными кошками, особенно генов, ассоциированных с отклонениями от нормы.
Животных, у которых способами согласно настоящему изобретению диагностировано наличие заболеваний почек, например, таких как гломерулонефрит, предпочтительно содержат на защищающем почки рационе. Защищающие почки рационы включают, например, рационы, которые описаны выше и в WO 20067119049 A2, WO 2006/071952, содержание которых включено в настоящее описание в виде ссылки.
Таким образом, изобретение относится к способу (способу 1) диагностики наличия заболевания почек у кошек, включающему в себя измерение уровня экспрессии одного или нескольких биомаркеров, выбранных из группы, состоящей из люмикана (LUM); цепи коллагена альфа 1 (III), варианта 12 (COL3A1); декорина (DCN); секретируемого родственного frizzled белка 2 (SFRP2); ретинол-связывающего белка 5 (rbp5); MMP-2; MMP-7 и MMP-19, в биологическом образце, взятом у кошки, при этом различия в экспрессии одного или нескольких биомаркеров в образце по сравнению с контрольным значением для экспрессии в образце от нормального животного свидетельствует о наличии заболевания почек, например, согласно любому из следующих способов:
1.1. Способ 1, в котором уровень экспрессии одного или нескольких биомаркеров определяют измерением экспрессии генов одного или нескольких биомаркеров с использованием либо (i) ДНК-микроматрицы, содержащей один или несколько олигонуклеотидов, комплементарных мРНК или кДНК, соответствующей одному или нескольким биомаркерам, которые необходимо измерить, либо (ii) количественной полимеразной цепной реакции с олигонуклеотидными праймерами для мРНК или кДНК, соответствующим одному или нескольким биомаркерам, которы