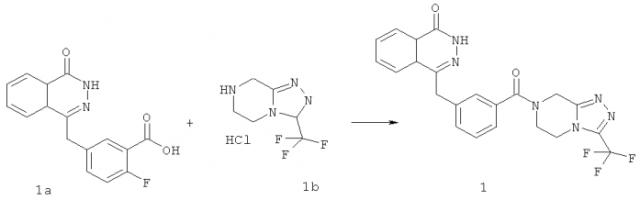
Производное фталазинонкетона, способ его получения и его фармацевтическое применение
Иллюстрации
Показать всеИзобретение относится к производному фталазинонкетона, представленному формулой (I), в которой радикалы и символы имеют значения, приведенные в формуле изобретения, способу его получения, фармацевтической композиции, содержащей это производное, его применению в качестве ингибитора поли(АДФ-рибоза)полимеразы (PARP). 6 н. и 7 з.п. ф-лы, 26 пр.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новому производному фталазинонкетона формулы (I), к способам его получения, к фармацевтической композиции, содержащей это производное, и к его применению в качестве терапевтического агента, в частности, в качестве ингибитора поли(АДФ-рибоза)полимеразы (PARP).
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Химиотерапия и радиотерапия являются двумя общепринятыми способами лечения рака. Оба способа лечения могут индуцировать однонитевой и/или двунитевой разрыв ДНК, что приводит к цитотоксичности, следовательно, целевые раковые клетки будут погибать вследствие хромосомного повреждения. Важным результатом в ответ на сигнал повреждения ДНК является активация сигнала в регуляторном сайте, цель которого состоит в том, чтобы защитить клетки от митоза в случае повреждения ДНК, предотвращая посредством этого повреждение клетки. В большинстве случаев опухолевые клетки проявляют дефекты сигнала регуляции в клеточном цикле и обладают высокой скоростью пролиферации. Поэтому можно предсказать, что опухолевые клетки обладают специфичными механизмами репарации ДНК, которые могут реагировать быстро, чтобы репарировать хромосомное повреждение, релевантное для регуляции пролиферации, посредством этого спасая клетки от цитотоксических эффектов некоторых способов лечения и поддерживая их жизнь.
В клиническом применении эффективная концентрация химиотерапевтического лекарственного средства или терапевтическая интенсивность излучения может бороться с этим механизмом репарации ДНК, чтобы обеспечить эффект уничтожения в отношении целевых опухолевых клеток. Однако в опухолевых клетках может развиваться толерантность к лечению за счет усиления их механизмов репарации повреждений ДНК, и они выживают после летального повреждения ДНК. В целях преодоления этой толерантности обычно необходимо увеличить дозировку терапевтического лекарственного средства или интенсивность излучения. Данный подход приведет к побочным эффектам в отношении нормальной ткани вблизи повреждений, и, следовательно, сделает курс лечения осложненным тяжелыми побочными реакциями, в результате, повышая риск лечения. В то же время, постоянно возрастающая толерантность снизит терапевтический эффект, поэтому можно сделать вывод, что цитотоксичность агентов, повреждающих ДНК, можно улучшить на пути специфичности к опухолевым клеткам посредством контроля механизма репарации, стимулируемого сигналом повреждения ДНК.
PARP (поли(АДФ-рибоза)полимеразы), характеризующиеся активностью поли-АДФ-рибозилирования, состоят из надсемейства 18 ядерных ферментов и цитоплазматических ферментов. Такой эффект поли-АДФ-рибозилирования может регулировать активность белка-мишени и взаимодействие между белками, а также регулировать многие другие фундаментальные биологические процессы, включая репарацию ДНК и клеточную гибель. Кроме того, геномная стабильность также связана с поли-АДФ-рибозилированием (см. D'Amours et al. Biochem. J, 1999, 342, 249).
Активность PARP-1 составляет примерно 80% суммарной клеточной активности PARP. PARP-1 вместе с PARP-2, который является наиболее сходным с PARP-1, являются членами семейства PAPR, обладающими способностью к репарации повреждения ДНК. Как сенсорный и сигнальный белок повреждения ДНК, PARP-1 может быстро обнаруживать сайты повреждения ДНК и непосредственно связываться с ними, а затем индуцировать агрегацию различных белков, необходимых для репарации ДНК, обеспечивая посредством этого репарацию повреждения ДНК. Когда в клетках отсутствует PARP-1, PARP-2 может осуществлять репарацию повреждения ДНК вместо PARP-1.
Исследования показали, что по сравнению с нормальными клетками экспрессия белков семейства PARP в солидных опухолях в целом усилена. Кроме того, показано, что опухоли (такие как рак молочной железы и рак яичника), в которых отсутствует ген, связанный с репарацией ДНК (такой как BRCA-1 или BRCA-2), крайне чувствительны к ингибиторам PARP-1. Это позволяет предположить потенциальное применение ингибиторов PARP в качестве единственного агента, который может быть назван трижды негативным раком молочной железы (см. Plummer, E.R. Curr. Opin. Pharmacol. 2006, 6, 364; Ratnam, et al; Clin. Cancer Res. 2007, 13, 1383). В то же время, поскольку механизм репарации повреждения ДНК является основным механизмом ответа опухолевых клеток на толерантность, производимую лечением химиотерапевтическими лекарственными средствами и ионизирующим излечением, PARP-1 считают эффективной мишенью для освоения новых способов терапии рака.
Ингибиторы PARP прежде разработаны и сконструированы с использованием никотинамида NAD+, который можно использовать в качестве каталитического субстрата PARP, в качестве матрицы для разработки их аналогов. Как конкурентные ингибиторы NAD+, эти ингибиторы конкурируют с NAD+ за каталитические сайты PARP, посредством этого предотвращая синтез цепи поли(АДФ-рибоза). PARP без модификации поли(АДФ-рибозилирование) не может диссоциировать из сайтов повреждения ДНК, что приведет другие белки, вовлеченные в репарацию, в сайт повреждения, предотвращая посредством этого осуществление процесса репарации. Следовательно, под действием цитотоксических лекарственных средств или излучения ингибитор PARP, в конечном счете, уничтожит опухолевые клетки с повреждением ДНК.
Кроме того, NAD+, который потребляется в качестве каталитического субстрата PARP, является существенным фактором в процессе синтеза АТФ клеток. При высоком уровне активности PARP внутриклеточные уровни NAD+ значительно снизятся, воздействуя посредством этого на внутриклеточный уровень АТФ. Вследствие недостатка внутриклеточного содержания АТФ клетки не могут достигать программируемого АТФ-зависимого процесса клеточной гибели и могут только переходить к некрозу, специфичному механизму апоптоза. В процессе некроза будет высвобождаться множество воспалительных цитокинов, производя посредством этого токсические эффекты в отношении других органов и тканей (Horvath ЕМ et al. Drug News Perspect, 2007, 20, 171-181). Следовательно, ингибиторы PARP можно также применять для лечения ряда заболеваний, обусловленных этим механизмом, включая нейродегенеративные заболевания (такие как болезнь Альцгеймера, болезнь Гентингтона, болезнь Паркинсона), диабет, сопутствующие заболевания при ишемии или процессе ишемии-реперфузии, таком как инфаркт миокарда и острая почечная недостаточность, заболевания системы кровообращения, такие как септический шок, и воспалительные заболевания, такие как хронический ревматизм, и т.д. (см. Tentori L, et al. Pharmacol. Res., 2002, 45, 73-85; Horvath ЕМ et al. Drug News Perspect., 2007, 20, 171; Faro R, et al. Ann. Thorac. Surg., 2002, 73, 575.; Kumaran D, et al. Brain Res., 2008, 192, 178).
В настоящее время существует серия заявок на патенты в отношении фталазинонкетонового ингибитора PARP, включающая WO 2002036576, WO 2004080976 и WO2006021801.
Хотя раскрыта серия ингибиторов PARP для лечения опухолей, все еще существует потребность в разработке новых соединений с лучшими результатами эффективности и фармакокинетики. После продолжительных исследований авторы настоящего изобретения разработали серию соединений формулы (I) и обнаружили, что соединение, имеющее такую структуру, проявляет отличный эффект и функцию.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение было направлено на разработку производных фталазинонкетона формулы (I) и их таутомеров, энантиомеров, диастереомеров, рацематов и фармацевтически приемлемых солей, а также их метаболитов, метаболических предшественников или пролекарств:
где:
А и В вместе с присоединенными атомами углерода образуют циклоалкил, гетероциклил, арил или гетероарил, где циклоалкил, гетероциклил, арил или гетероарил каждый независимо и необязательно замещен одной или более чем одной группой, выбранной из группы, состоящей из алкила, галогена, гидроксила, алкоксила, циклоалкила, гетероциклила, арила, гетероарила, -C(O)OR5, -OC(O)R5, -O(СН2)nC(O)OR5, -C(O)R5, -NHC(O)R5, -NR6R7, -OC(O)NR6R7 и -C(O)NR6R7;
R1, R2, R3 или R4 каждый независимо выбран из группы, состоящей из водорода, галогена, алкила, циано и алкоксила, где алкил или алкоксил каждый независимо и необязательно замещен одной или более чем одной группой, выбранной из группы, состоящей из галогена, гидроксила, алкила и алкоксила;
D, Е или G каждый независимо выбран из группы, состоящей из азота и C(R8);
R5 выбран из группы, состоящей из водорода, алкила, циклоалкила, гетероциклила, арила и гетероарила, где алкил, циклоалкил, гетероциклил, арил или гетероарил каждый независимо и необязательно замещен одной или более чем одной группой, выбранной из группы, состоящей из алкила, галогена, гидроксила, алкоксила, циклоалкила, гетероциклила, арила, гетероарила, карбоксила и алкоксикарбонила;
R6 или R7 каждый независимо выбран из группы, состоящей из водорода, алкила, циклоалкила, гетероциклила, арила и гетероарила, где алкил, циклоалкил, гетероциклил, арил или гетероарил каждый независимо и необязательно замещен одной или более чем одной группой, выбранной из группы, состоящей из алкила, галогена, гидроксила, алкоксила, циклоалкила, гетероциклила, арила, гетероарила, карбоксила и алкоксикарбонила;
либо R6 и R7 вместе с присоединенным атомом N образуют гетероциклил, где гетероциклил содержит один или более чем один гетероатом N, О или S(O)m, и гетероциклил необязательно замещен одной или более чем одной группой, выбранной из группы, состоящей из алкила, галогена, гидроксила, алкоксила, циклоалкила, гетероциклила, арила, гетероарила, карбоксила и алкоксикарбонила;
R8 выбран из группы, состоящей из водорода, алкила, галогена, гидроксила, циано, алкоксила, циклоалкила, гетероциклила, арила, гетероарила, бензила, -C(O)OR5, -OC(O)R5, -O(CH2)nC(O)OR5, -(CH2)nNR6R7, -C(O)R5, -NHC(O)R5, -NR6R7, -OC(O)NR6R7 и -C(O)NR6R7, где алкил, алкоксил, циклоалкил, гетероциклил, арил, гетероарил или бензил каждый независимо и необязательно замещен одной или более чем одной группой, выбранной из группы, состоящей из алкила, галогена, гидроксила, алкоксила, циклоалкила, гетероциклила, арила, гетероарила, оксо, -C(O)OR5, -OC(O)R5, -O(CH2)nC(O)OR5, -C(O)R5, -NHC(O)R5, -NR6R7, -ОС(O)NR6R7 и -C(O)NR6R7;
m выбрано из группы, состоящей из 0, 1 и 2; и
n выбрано из группы, состоящей из 0, 1 и 2.
Предпочтительной формой осуществления является соединение формулы (I) или его фармацевтически приемлемая соль, где А и В вместе с присоединенными атомами углерода образуют арил, где предпочтительно арил представляет собой фенил.
Предпочтительно соединение формулы (I) или его фармацевтически приемлемая соль, где R1 представляет собой атом водорода.
Предпочтительно соединение формулы (I) или его фармацевтически приемлемая соль, где R1 представляет собой атом галогена, предпочтительно атом фтора.
Предпочтительно соединение формулы (I) или его фармацевтически приемлемая соль, где R1 представляет собой атом галогена, предпочтительно атом фтора.
Предпочтительно соединение формулы (I) или его фармацевтически приемлемая соль, где R1, R2, R3 или R4 каждый независимо выбран из водорода.
Предпочтительно соединение формулы (I) или его фармацевтически приемлемая соль, где R8 выбран из группы, состоящей из водорода, алкила, галогена, циано, -C(O)OR5, -(CH2)nNR6R7 и -C(O)NR6R7, где алкил необязательно замещен одним или более чем одним атомом галогена.
Предпочтительно соединение формулы (I) или его фармацевтически приемлемая соль, где R8 представляет собой трифторметил.
Соединение формулы (I) может содержать асимметрические атомы углерода, следовательно, оно может существовать в форме оптически чистого диастереомера, диастереомерной смеси, диастереомерного рацемата, смеси диастереомерного рацемата или в виде мезосоединения. Настоящее изобретение включает все эти формы. Диастереомерную смесь, диастереомерный рацемат или смесь диастереомерного рацемата можно выделить общепринятыми способами, такими как колоночная хроматография, тонкослойная хроматография и высокоэффективная жидкостная хроматография.
Эквивалент может быть понят обычным специалистом в данной области техники таким образом, что соединение формулы (I) может также иметь таутомеры. Таутомерные формы соединения (I) включают, но не ограничены, структуру представленную приведенной ниже формулой (II):
Соединения по изобретению включают, но не ограничены ими, приведенные ниже:
| Пример № | Структура и название |
| 1 | |
| 4-[[4-фтор-3-[3-(трифторметил)-6,8-дигидро-5H-[1,2,4]триазоло[4,3-а]пиразин-7-карбонил]-фенил]метил]-2H-фталазин-1-он | |
| 2 | |
| 4-[[3-(3,4-дигидро-1H-пирроло[1,2-а]пиразин-2-карбонил)-4-фтор-фенил]метил]-2H-фталазин-1-он | |
| 3 | |
| метил-7-[2-фтор-5-[(4-оксо-3H-фталазин-1-ил)метил]бензоил]-3-(трифторметил)-6,8-дигидро-5H-имидазо[1,5-а]пиразин-1-карбоксилат | |
| 4 | |
| 4-[[3-(6,8-дигидро-5H-имидазо[1,2-а]пиразин-7-карбонил)-4-фтор-фенил]метил]-2H-фталазин-1-он | |
| 5 | |
| 4-[[4-фтор-3-[3-(трифторметил)-6,8-дигидро-5H-имидазо[1,5-а]пиразин -7-карбонил]фенил]метил]-2H-фталазин-1-он | |
| 6 | |
| 4-[[4-фтор-3-[1-(гидроксиметил)-3-(трифторметил)-6,8-дигидро-5H-имидазо[1,5-а]пиразин-7-карбонил]фенил]метил]-2H-фталазин-1-он | |
| 7 | |
| N-этил-7-[2-фтор-5-[(4-оксо-3H-фталазин-1-ил)метил]бензоил]-3-(трифторметил)-6,8-дигидро-5H-имидазо[1,5-а]пиразин-1-карбоксамид | |
| 8 | |
| 7-[2-фтор-5-[(4-оксо-3H-фталазин-1-ил)метил]бензоил]-3-(трифторметил)-6,8-дигидро-5H-имидазо[1,5-а]пиразин-1-карбоновая кислота | |
| 9 | |
| 4-[[4-фтор-3-[1-(метиламинометил)-3-(трифторметил)-6,8-дигидро-5Н-имидазо[1,5-а]пиразин-7-карбонил]фенил]метил]-2Н-фталазин-1-он | |
| 10 | |
| 7-[2-фтор-5-[(4-оксо-3Н-фталазин-1-ил)метил]бензоил]-3-(трифторметил)-6,8-дигидро-5H-имидазо[1,5-а]пиразин-1-карбоксамид | |
| 11 | |
| 4-[[3-[1-бром-3-(трифторметил)-6,8-дигидро-5H-имидазо[1,5-а]пиразин-7-карбонил]-4-фтор-фенил]метил]-2H-фталазин-1-он | |
| 12 | |
| 4-[[4-фтор-3-[2-(трифторметил)-6,8-дигидро-5H-имидазо[1,2-а]пиразин-7-карбонил]фенил]метил]-2H-фталазин-1-он | |
| 13 | |
| 7-[2-фтор-5-[(4-оксо-3H-фталазин-1-ил)метил]бензоил]-N-метил-3-(трифторметил)-6,8-дигидро-5H-имидазо[1,5-а]пиразин-1-карбоксамид | |
| 14 | |
| этил-7-[2-фтор-5-[(4-оксо-3H-фталазин-1-ил)метил]бензоил]-6,8-дигидро-5H-имидазо[1,2-а]пиразин-3-карбоксилат | |
| 15 | |
| 4-[[3-[3-(трифторметил)-6,8-дигидро-5H-[1,2,4]триазоло[4,3-а]пиразин-7-карбонил]фенил]метил]-2H-фталазин-1-он | |
| 16 | |
| 4-[[3-(6,8-дигидро-5H-[1,2,4]триазоло[1,5-а]пиразин-7-карбонил)-4-фтор-фенил]метил]-2H-фталазин-1-он | |
| 17 | |
| 4-[[3-(6,8-дигидро-5Н-[1,2,4]триазоло[4,3-а]пиразин-7-карбонил)-4-фтор-фенил]метил]-2H-фталазин-1-он | |
| 18 | |
| 4-[[4-фтор-3-[1-(пирролидин-1-карбонил)-3-(трифторметил)-6,8-дигидро-5Н-имидазо[1,5-а]пиразин-7-карбонил]фенил]метил]-2H-фталазин-1-он | |
| 19 | |
| 4-[[4-фтор-3-[2-(трифторметил)-6,8-дигидро-5H-[1,2,4]триазоло[1,5-а]пиразин-7-карбонил]фенил]метил]-2H-фталазин-1-он | |
| 20 | |
| 4-[[4-фтор-3-[1-(морфолин-4-карбонил)-3-(трифторметил)-6,8-дигидро-5H-имидазо[1,5-а]пиразин-7-карбонил]фенил]метил]-2Н-фталазин-1-он |
| 21 | |
| N-метил-7-[3-[(4-оксо-3H-фталазин-1-ил)метил]бензоил]-3-(трифторметил)-6,8-дигидро-5H-имидазо[1,5-а]пиразин-1-карбоксамид | |
| 22 | |
| 7-[2-фтор-5-[(4-оксо-3H-фталазин-1-ил)метил]бензоил]-N,N-диметил-3-(трифторметил)-6,8-дигидро-5H-имидазо[1,5-а]пиразин-1-карбоксамид | |
| 23 | |
| 4-[[3-[3-(дифторметил)-6,8-дигидро-5H-[1,2,4]триазоло[4,3-а]пиразин-7-карбонил]-4-фтор-фенил]метил]-2H-фталазин-1-он | |
| 24 | |
| N-(циклопропилметил)-7-[2-фтор-5-[(4-оксо-3H-фталазин-1-ил)метил]бензоил]-3-(трифторметил)-6,8-дигидро-5H-имидазо[1,5-а]пиразин-1-карбоксамид | |
| 25 | |
| 7-[2-фтор-5-[(4-оксо-3H-фталазин-1-ил)метил]бензоил]-3-(трифторметил)-6,8-дигидро-5H-имидазо[1,5-а]пиразин-1-карбонитрил | |
| 26 | |
| 4-[[4-фтор-3-[3-(2,2,2-трифторэтил)-6,8-дигидро-5H-[1,2,4]триазоло[4,3-а]пиразин-7-карбонил]фенил]метил]-2H-фталазин-1-он |
или их фармацевтически приемлемые соли.
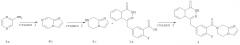
Данное изобретение также относится к способу получения соединения формулы (I) или его фармацевтически приемлемой соли, включающему стадии:
необязательного гидролиза соединения формулы (IA) до карбоновой кислоты, взаимодействия карбоновой кислоты с соединением формулы (IB) или его солью в присутствии конденсирующего агента, такого как бензотриазол-N,N,N',N'-тетраметилмочевины гексафторфосфат, в щелочных условиях с получением соединения формулы (I);
где:
R3 выбран из группы, состоящей из гидроксила, галогена и алкоксила;
А, В, D, Е, G и R1-R4 являются такими, как указано для формулы (I). В другом аспекте настоящее изобретение относится к применению соединений формулы (I) или их фармацевтически приемлемых солей для получения ингибиторов PARP.
В другом аспекте настоящее изобретение относится к способу ингибирования PARP, включающему введение субъекту, нуждающемуся в этом, терапевтически эффективного количества соединений формулы (I) или их фармацевтически приемлемых солей.
В другом аспекте настоящее изобретение относится к применению соединений формулы (I) или их фармацевтически приемлемых солей для получения адъюванта при лечении рака или лекарственного средства, вызывающего чувствительность опухолевых клеток к ионизирующему излучению или химиотерапии.
В другом аспекте настоящее изобретение относится к соединениям формулы (I) или их фармацевтически приемлемым солям для применения в качестве адъюванта при лечении рака или лекарственного средства, вызывающего чувствительность опухолевых клеток к ионизирующему излучению или химиотерапии.
В другом аспекте настоящее изобретение относится к соединениям формулы (I) или их фармацевтически приемлемым солям для применения в качестве ингибиторов PARP.
В другом аспекте настоящее изобретение относится к применению соединений формулы (I) или их фармацевтически приемлемых солей для получения лекарственного средства для лечения рака, где рак выбран из группы, состоящей из рака молочной железы, рака яичника, рака поджелудочной железы, рака простаты, рака печени и рака толстой кишки, где лекарственное средство дополнительно вводят совместно с терапевтически эффективным количеством лекарственного средства, выбранного из группы, состоящей из темозоломида, адриамицина, таксола, цисплатина, карбоплатина, дакарбазина, топотекана, иринотекана, гемцитабина и бевацизумаба.
В другом аспекте настоящее изобретение относится к способам лечения рака, включающим введение субъекту, нуждающемуся в этом, терапевтически эффективного количества соединений формулы (I) или их фармацевтически приемлемых солей, где рак выбран из группы, состоящей из рака молочной железы, рака яичника, рака поджелудочной железы, рака простаты, рака печени и рака толстой кишки, где лекарственное средство дополнительно вводят совместно с терапевтически эффективным количеством лекарственного средства, выбранного из группы, состоящей из темозоломида, адриамицина, таксола, цисплатина, карбоплатина, дакарбазина, топотекана, иринотекана, гемцитабина и бевацизумаба.
В другом аспекте настоящее изобретение относится к соединениям формулы (I) или их фармацевтически приемлемым солям для применения в качестве лекарственного средства для лечения рака, где рак выбран из группы, состоящей из рака молочной железы, рака яичника, рака поджелудочной железы, рака простаты, рака печени и рака толстой кишки, где лекарственное средство дополнительно вводят совместно с терапевтически эффективным количеством лекарственного средства, выбранного из группы, состоящей из темозоломида, адриамицина, таксола, цисплатина, карбоплатина, дакарбазина, топотекана, иринотекана, гемцитабина и бевацизумаба.
Кроме того, настоящее изобретение также относится к фармацевтической композиции, содержащей терапевтически эффективное количество соединений формулы (I) или их фармацевтически приемлемых солей по настоящему изобретению и фармацевтически приемлемый носитель или наполнитель. Настоящее изобретение также относится к данной фармацевтической композиции для применения в качестве ингибитора PARP, либо в качестве адъюванта при лечении рака или лекарственного средства, вызывающего чувствительность опухолевых клеток к ионизирующему излучению или химиотерапии, либо в качестве лекарственного средства для лечения рака. Настоящее изобретение также относится к применению данной фармацевтической композиции для получения ингибитора PARP. Настоящее изобретение также относится к применению данной фармацевтической композиции для получения адъюванта при лечении рака или лекарственного средства, вызывающего чувствительность опухолевых клеток к ионизирующему излучению или химиотерапии. Настоящее изобретение также относится к применению данной фармацевтической композиции для получения лекарственного средства для лечения рака, где рак выбран из группы, состоящей из рака молочной железы, рака яичника, рака поджелудочной железы, рака простаты, рака печени и рака толстой кишки, где лекарственное средство дополнительно вводят совместно с терапевтически эффективным количеством лекарственного средства, выбранного из группы, состоящей из темозоломида, адриамицина, таксола, цисплатина, карбоплатина, дакарбазина, топотекана, иринотекана, гемцитабина и бевацизумаба.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Если не указано иное, термины, используемые в описании и формуле изобретения, имеют значения, описанные ниже.
"Алкил" относится к насыщенной алифатической углеводородной группе, включающей С1-С20 прямоцепочечные и разветвленные группы. Предпочтительно алкильная группа представляет собой алкил, имеющий от 1 до 12 атомов углерода. Репрезентативные примеры включают, но не ограничены ими, метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, втop-бутил, н-пентил, 1,1-диметилпропил, 1,2-диметилпропил, 2,2-диметилпропил, 1-этилпропил, 2-метилбутил, 3-метилбутил, н-гексил, 1-этил-2-метилпропил, 1,1,2-триметилпропил, 1,1-диметилбутил, 1,2-диметилбутил, 2,2-диметилбутил, 1,3-диметилбутил, 2-этилбутил, 2-метилпентил, 3-метилпентил, 4-метилпентил, 2,3-диметилбутил, н-гептил, 2-метилгексил, 3-метилгексил, 4-метилгексил, 5-метилгексил, 2,3-диметилпентил, 2,4-диметилпентил, 2,2-диметилпентил, 3,3-диметилпентил, 2-этилпентил, 3-этилпентил, н-октил, 2,3-диметилгексил, 2,4-диметилгексил, 2,5-диметилгексил, 2,2-диметилгексил, 3,3-диметилгексил, 4,4-диметилгексил, 2-этилгексил, 3-этилгексил, 4-этилгексил, 2-метил-2-этилпентил, 2-метил-3-этилпентил, н-нонил, 2-метил-2-этилгексил, 2-метил-3-этилгексил, 2,2-диэтилпентил, н-децил, 3,3-диэтилгексил, 2,2-диэтилгексил и их изомеры разветвленной цепи. Более предпочтительно алкильная группа представляет собой низший алкил, имеющий от 1 до 6 атомов углерода. Репрезентативные примеры включают, но не ограничены ими, метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, втор-бутил, н-пентил, 1,1-диметилпропил, 1,2-диметилпропил, 2,2-диметилпропил, 1-этилпропил, 2-метилбутил, 3-метилбутил, н-гексил, 1-этил-2-метилпропил, 1,1,2-триметилпропил, 1,1-диметилбутил, 1,2-диметилбутил, 2,2-диметилбутил, 1,3-диметилбутил, 2-этилбутил, 2-метилпентил, 3-метилпентил, 4-метилпентил, 2,3-диметилбутил и т.д. Алкильная группа может быть замещенной или незамещенной. Когда она замещена, группа(ы) заместителя могут быть замещены в любой доступной точке присоединения, предпочтительно группа(ы) заместителя предпочтительно представляет собой одну или более чем одну группу, независимо выбранную из группы, состоящей из алкила, алкенила, алкинила, алкоксила, алкилсульфо, алкиламино, галогена, тиола, гидроксила, нитро, циано, циклоалкила, гетероциклического алкила, арила, гетероарила, циклоалкоксила, гетероциклического алкоксила, циклоалкилтио, гетероциклического алкилтио, оксо, -C(O)OR5, -OC(O)R5, -O(CH2)nC(O)OR5, -C(O)R5, -NHC(O)R5, -NR6R7, -ОС(O)NR6R7 и -С(O)NR6R7.
"Циклоалкил" относится к насыщенной и/или частично ненасыщенной моноциклической или полициклической углеводородной группе и имеет от 3 до 20 атомов углерода, предпочтительно от 3 до 12 атомов углерода, более предпочтительно от 3 до 10 атомов углерода. Репрезентативные примеры моноциклического циклоалкила включают, но не ограничены ими, циклопропил, циклобутил, циклопентил, циклопентенил, циклогексил, циклогексенил, циклогексадиенил, циклогептил, циклогептатриенил, циклооктил и т.д. Полициклический циклоалкил включает циклоалкил, имеющий спиро-кольцо, конденсированное кольцо и кольцо с внутренним мостиком.
"Спиро-циклоалкил" относится к 5-20-членной полициклической группе с кольцами, соединенными через один общий атом углерода (называемый спиро-атомом), где одно или более чем одно кольцо может содержать одну или более чем одну двойную связь, но ни одно из колец не имеет полностью конъюгированной пи-электронной системы. Предпочтительно спиро-циклоалкил является 6-14-членным, более предпочтительно является 7-10-членным. В соответствии с числом общих спиро-атомов спиро-циклоалкил делят на моно-спироциклическое кольцо, ди-спироциклическое кольцо или поли-спироциклическое кольцо, предпочтительно он относится к моно-спироциклическому кольцу или ди-спироциклическому кольцу. Более предпочтительно спиро-циклоалкил представляет собой 4-членное/4-членное, 4-членное/5-членное, 4-членное/6-членное, 5-членное/5-членное, or 5-членное/6-членное моноциклическое спиро-кольцо. Репрезентативные примеры спиро-циклоалкила включают, но не ограничены ими, приведенные ниже группы:
и .
"Конденсированный циклоалкил" относится к 5-20-членной полициклической углеводородной группе, где каждое кольцо в системе имеет общую пару соседних атомов углерода с другим кольцом, где одно или более чем одно кольцо может содержать одну или более чем одну двойную связь, но ни одно из колец не имеет полностью конъюгированной пи-электронной системы. Предпочтительно конденсированная циклоалкильная группа является 6-14-членной, более предпочтительно 7-10-членной. В соответствии с числом колец-членов конденсированный циклоалкил делят на конденсированный циклоалкил с бициклическим кольцом, трициклическим кольцом, тетрациклическим кольцом или пол и циклическим кольцом, предпочтительно он относится к конденсированному циклоалкилу с бициклическим кольцом или трициклическим кольцом. Более предпочтительно конденсированный циклоалкил представляет собой конденсированный циклоалкил с 5-членным/6-членным или 5-членным/6-членным бициклическим кольцом. Репрезентативные примеры конденсированного циклоалкила включают, но не ограничены ими, приведенные ниже группы:
и .
"Циклоалкил с внутренним мостиком" относится к 5-20-членной полициклической углеводородной группе, где каждые два кольца в системе имеют два общих разъединенных атома углерода. Эти кольца могут иметь одну или более чем одну двойную связь, но не имеют полностью конъюгированной пи-электронной системы. Предпочтительно циклоалкил с внутренним мостиком является 6-14-членным, более предпочтительно 7-10-членным. В соответствии с числом колец-членов циклоалкил с внутренним мостиком делят на бициклическое кольцо, трициклическое кольцо, тетрациклическое кольцо или полициклическое кольцо с внутренним мостиком, предпочтительно он относится к бициклическому, трициклическому или тетрациклическому циклоалкилу с внутренним мостиком, более предпочтительно относится к бициклическому или трициклическому циклоалкилу с внутренним мостиком. Репрезентативные примеры циклоалкила с внутренним мостиком включают, но не ограничены ими, приведенные ниже группы:
и .
Циклоалкил может быть конденсирован с кольцом арила, гетероарила или гетероциклического алкила, где кольцом, соединенным с исходной структурой, является циклоалкил. Репрезентативные примеры циклоалкила с внутренним мостиком включают, но не ограничены ими, инданилуксусную кислоту, тетрагидронафталин, бензоциклогептил и т.д. Циклоалкил может быть необязательно замещенным или незамещенным. Когда он замещен, группа(ы) заместителя предпочтительно представляют собой одну или более чем одну группу, независимо выбранную из группы, состоящей из алкила, алкенила, алкинила, алкоксила, алкилсульфо, алкиламино, галогена, тиола, гидроксила, нитро, циано, циклоалкила, гетероциклического алкила, арила, гетероарила, циклоалкоксила, гетероциклического алкоксила, циклоалкилтио, гетероциклического алкилтио, оксо, -C(O)OR5, -OC(O)R5, -O(CH2)nC(O)OR5, -C(O)R5, -NHC(O)R5, -NR6R7, -OC(O)NR6R7 и -C(O)NR6R7.
"Алкенил" относится к алкилу, определенному, как описано выше, который имеет по меньшей мере два атома углерода и по меньшей мере одну углерод-углеродную двойную связь, например, винил, 1-пропенил, 2-пропенил, 1-, 2- или 3-бутенил и т.д. Алкенильная группа может быть замещенной или незамещенной. Когда она замещена, группа(ы) заместителя предпочтительно представляют собой одну или более чем одну группу независимо выбранную из группы, состоящей из алкила, алкенила, алкинила, алкоксила, алкилсульфо, алкиламино, галогена, тиола, гидроксила, нитро, циано, циклоалкила, гетероциклического алкила, арила, гетероарила, циклоалкоксила, гетероциклического алкоксила, циклоалкилтио, гетероциклического алкилтио, -C(O)OR5, -OC(O)R5, -O(CH2)nC(O)OR5, -C(O)R5, -NHC(O)R5, -NR6R7, -ОС(O)NR6R7 и -С(O)NR6R7.
"Алкинил" относится к алкилу, определенному, как описано выше, который имеет по меньшей мере два атома углерода и по меньшей мере одну углерод-углеродную тройную связь, например, этинил, 1-пропинил, 2-пропинил, 1-, 2- или 3-бутинил и т.д. Алкинильная группа может быть замещенной или незамещенной. Когда она замещена, группа(ы) заместителя предпочтительно представляют собой одну или более чем одну группу независимо выбранную из группы, состоящей из алкила, алкенила, алкинила, алкоксила, алкилсульфо, алкиламино, галогена, тиола, гидроксила, нитро, циано, циклоалкила, гетероциклического алкила, арила, гетероарила, циклоалкоксила, гетероциклического алкоксила, циклоалкилтио, гетероциклического алкилтио, -C(O)OR5, -OC(O)R5, -O(CH2)nC(O)OR5, -C(O)R5, -NHC(O)R5, -NR6R7, -ОС(O)NR6R7 и -C(O)NR6R7.
"Гетероциклил" относится к 3-20-членной насыщенной и/или частично ненасыщенной моноциклической или полициклической углеводородной группе, имеющей один или более чем один гетероатом, выбранный из группы, состоящей из N, О или S(O)m (где m равно 0, 1 или 2), в качестве кольцевых атомов, но исключая -O-O-, -O-S- или -S-S-в кольце, где остальными кольцевыми атомами являются атомы С. Предпочтительно гетероциклил является 3-12-членным, имеющим от 1 до 4 гетероатомов, более предпочтительно 3-10-членным. Репрезентативные примеры моноциклического гетероциклила включают, но не ограничены ими, пирролидил, пиперидил, пиперазинил, морфолинил, сульфоморфолинил, гомопиперазинил и т.д. Полициклический гетероциклил включает гетероциклил, имеющий спиро-кольцо, конденсированное кольцо и кольцо с внутренним мостиком. "Спиро-гетероциклил" относится к 5-20-членному полициклическому гетероциклилу с кольцами, соединенными через один общий атом углерода (называемый спиро-атомом), где кольца имеют один или более чем один гетероатом, выбранный из группы, состоящей из N, О или S(O)p (где p равно 0, 1 или 2) в качестве кольцевых атомов, где остальными кольцевыми атомами являются атомы С, где одно или более чем одно кольцо может содержать одну или более чем одну двойную связь, но ни одно из колец не имеет полностью конъюгированной пи-электронной системы. Предпочтительно спиро-гетероциклил является 6-14-членным, более предпочтительно 7-10-членным. В соответствии с числом общих спиро-атомов спиро-гетероциклил делят на моно-спиро-гетероциклил, ди-спиро-гетероциклил или поли-спиро-гетероциклил, предпочтительно он относится к моно-спиро-гетероциклилу и ди-спиро-гетероциклилу. Более предпочтительно спиро-гетероциклил представляет собой 4-членный/4-членный, 4-членный/5-членный, 4-членный/6-членный, 6-членный/5-членный или 5-членный/6-членный моно-спиро-гетероциклил. Репрезентативные примеры спиро-гетероциклила включают, но не ограничены ими, приведенные ниже группы:
и .
"Конденсированный гетероциклил" относится к 5-20-членной полициклической гетероциклильной группе, где каждое кольцо в системе имеет общую пару соседних атомов углерода с другим кольцом, где одно или более чем одно кольцо может содержать одну или более чем одну двойную связь, но ни одно из колец не имеет полностью конъюгированной пи-электронной системы, и где кольца имеют один или более чем один гетероатом, выбранный из группы, состоящей из N, О или S(O)p (где p равно 0, 1 или 2) в качестве кольцевых атомов, где ос