Способ флотации руд
Иллюстрации
Показать всеИзобретение относится к области обогащения полезных ископаемых, в частности к выбору флотационных реагентов для руд. Способ флотации руд с использованием смеси собирателей включает предварительный подбор флотореагентов, для которого используют компьютерную химическую программу. С помощью программы предварительно виртуально прикрепляют смеси реагентов к атому металла модели флотируемого минерала, определяют для полученного комплекса компьютерные параметры и с учетом содержания металлов в руде определяют мольность металла во флотируемой руде, при этом для используемых реагентов должно быть - диполь/дипольное взаимодействие в пределах от -2.7717 до 0.4956, 1/4 ван-дер-ваальсово взаимодействие в пределах от 2.2390 до 8.8701, не 1/4 ван-дер-ваальсово взаимодействие от -0.3746 до 1.7483, изгиб валентных углов от 2.4600 до 3.1866, растяжением валентных связей от 0.2580 до 0.7430 и рассчитывают величину стерической энергии с учетом вычисленной мольности извлекаемого металла от 6.1198 до 8.6639 ккал/моль. Технический результат - повышение эффективности подбора флотационных реагентов для максимального извлечения ценных компонентов. 1 з.п. ф-лы, 2 ил., 3 табл., 3 пр.
Реферат
Изобретение относится к области обогащения полезных ископаемых, в частности к выбору флотационных реагентов для флотации руд.
Известен способ обогащения сульфидных руд, в котором дополнительно к основному сульфгидрильному собирателю используют реагент, снижающий флотируемость минералов [Игнаткина В.А. Развитие теории селективности действия сочетаний собирателей при флотации труднообогатимых руд цветных металлов. Автореферат доктора техн. наук. Москва. НАТУ МИСиС, 2011 г.].
Недостатком способа является то, что подбор реагентов осуществляется без достаточного научного обоснования.
Известный способ флотации сульфидных руд цветных металлов можно признать [Патент РФ №2379116 C1. Способ флотации сульфидных руд цветных металлов. Бочаров В.А., Игнаткина В.А. и др. Опубл. 20.01.2010, бюл. №2 и Игнаткина В.А. Выбор селективных собирателей для флотации сульфидных минералов. Цветные металлы. 2009, №6. С.4-7].
Наиболее близкими по технической сущности и достигаемому результату является способ флотации медных сульфидных руд с использованием смеси собирателей, а именно бутилового и изопропилового ксантогенатов при соотношении 2:1 и при общем расходе реагентов 70 г/т гексилового и бутилового ксантогенатов при соотношениях 1:1,5 или 2:1 при расходе 50 г/т, а также с использованием одного гексилового ксантогената при расходе 70 г/т [Отрожденнова Л.А., Рябой В.И., Кучаев В.А., Малиновская Н.Д. Флотация медных сульфидных руд гексиловым ксантогенатом фирмы «Хехст. Обогащение руд. 2010, №4. С.9-12 /1/] и который является наиболее близким аналогом к предложенному способу по совокупности признаков и назначению и может быть принят в качестве прототипа.
Недостатком способа является низкая эффективность при подборе смеси реагентов.
Целью изобретения является повышение эффективности при подборе смеси реагентов.
Технический результат, получаемый при реализации способа, состоит в обеспечении подбора композитов реагентов для максимального извлечения ценных компонентов, основанный на изменении строения известных функциональной группировки введением в нее различных атомов и заместителей или использовании композиции реагентов.
Для хорошей селекции при флотации полиметаллических руд следует использовать:
- химическую активность собирателя (прочность связи его терминальной группы с катионом флотируемого минерала);
- дисперсионное взаимодействие углеводородных цепей;
- действие модификаторов (депрессоров и активаторов).
Предлагается составлять композиции на основе современных представлений и квантово-химических расчетов при использовании химических программ и специальных коэффициентов.
Для компьютерного моделирование реагентов использовали программу Chem Bio 3D специализированного комплекса Chem Office корпорации Cambridge Soft. Компьютерные данные получали после минимизации ММ2.
Для подтверждения эффективности разработанного способа было проведено сравнение его со способом, выбранным в качестве ближайшего аналога.
Способ позволяет заранее подбирать расход реагентов для максимального извлечения металлов.
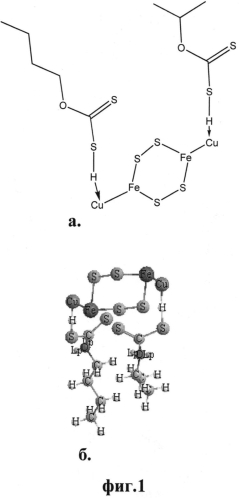
Сущность изобретения поясняется чертежами, где на Фиг.1 приведена схема прикрепления бутилового КхН и изо-пропилового КхН к поверхности циклического халькопирита (а) и шаростержневая модель созданного соединения(б); на Фиг.2 показана схема прикрепления гексилового ксантогената КхН и бутилового КхН к поверхности циклического халькопирита (а) и шаростержневая модель созданного соединения (б).
Для анализа химической активности собирателя (прочность связи его терминальной группы с катионом флотируемого минерала) и дисперсионного взаимодействия углеводородных цепей предложен коэффициент, который представляет собой сумму двух величин энергии:
1. энергии компьютерных параметров, применяемых собирателей полученных с помощью химической программы, умноженных на соответствующую долю расходов используемых собирателей во флотации, выраженных в молях;
2. энергии компьютерных параметров, специально созданного комплекса путем прикрепления собирателя к атому модели минерала. Затем определяют количество (содержание) меди в полученном комплексе с учетом молекулярного веса соединения, определяют количество молей меди комплекса, количество(содержанию) меди в халькопирите-минерале - 24,57% меди, затем количество молей меди комплекса в руде с целью установления доли исходной мольности, выраженных в молях, и определения энергии путем умножения компьютерных параметров на установленную мольность.
Ниже приведены расчеты необходимой композиции реагентов для максимального извлечения меди из руд и определены основные компьютерные параметры общей стерической энергии ряда флотационных реагентов, распределения электронной плотности (заряда) на отдельных атомах, ван-дер-ваальское и дипольное взаимодействия, построены молекулярные орбитали и вычислена энергия их уровня.
В табл.1 представлены компьютерные параметры флотореагентов - бутиловая ксантогеновая кислота (Бутиловый КхН), изопропиловая ксантогеновая кислота(Изопропиловый КхН), гексиловая ксантогеновая кислота (Гексиловый КхН), которые используются при флотации медных руд.
| Таблица 1 | |||
| Компьютерные параметры флотореагентов | |||
| Параметры | Сульфгидрильные реагенты | ||
| Бутиловый КхНИтерация 44 (1) | Изопропиловый КхНИтерация 165 (2) | Гексиловый КхН Итерация 41 (3) | |
| Растяжение валентных связей n1 | 0.4563 | 0.5090 | 0.5937 |
| Изгиб валентных углов n2 | 2.2180 | 2.7544 | 2.6131 |
| Поправки изгиб-растяжение n3 | 0.1797 | 0.2243 | 0.2286 |
| Внутреннее вращение n4 | 0.0074 | -2.7544 | 0.0140 |
| Не ¼ ван-дер-ваальсовские взаимодействия n5 | -0.5533 | -0.6989 | -0.8169 |
| ¼ ван-дер-ваальсовские взаимодействия n6 | 5.1367 | 4.3641 | 6.5109 |
| Диполь/дипольное взаимодействие | 0.5266 | 0.7969 | 0.4181 |
| Общая стерическая энергия, ккал/моль n7 | 7.9714 | 5.1953 | 9.5615 |
Для получения необходимой концентрации реагентов для максимального извлечения металла из руд предварительно создают комплекс, включающий минерал и прикрепленный к нему собиратель (собиратели), и определяют общую энергию комплекса и количество металла (меди) в созданном комплексном соединении. Например, при прикреплении Бутилового КхН к минералу - халькопириту энергия соединения составляет 4,4598 ккал/моль, а содержание меди в соединении 24,57% или отношения меди соединения по отношению к содержанию меди в халькопирите-минерале 24,57/34,63=0,71.
Определяют необходимые параметры с учетом содержания металлов в исследуемой руде.
1. Определим общую энергию собирателя с учетом расхода используемого реагента в молях, Ml
Е=n1×M1+n2×M1+n3×M1+n4M1+n5×M1
(n1+n2+n3+n4+n5) - компьютерные параметры исследуемых собирателей в ккал /моль.
M1 - расход реагентов в молях.
Для расчетов используем только ¼ ван-дер-ваальсово взаимодействие n6 и диполь/дипольное взаимодействие.
Полученная величина является приведенным коэффициентом А1. Определяют соотношение между медью в руде и медью в созданном комплексе.
Установлено содержание меди в соединении 19,45%, а молекулярный вес соединения составляет 653,54.
Определяют весовое количество меди в комплексе:
М=19,45X653,54/100=127,11 или в молях 127,11/653,54=0,18 М.
Содержание меди в руде 1,059% и определяют количество молей меди соединении в руде: Х=1,059Х0,18/127,11=0,0015 М.
Рассчитывают общую энергию Е используемых реагентов в комплексе с учетом установленной мольности (0,0015М2), М2:
n1×M2+n2×M2+n3×M2+n4M2+n5×М2=А2 прив. (приведенный коэффициент), ккал/моль (коэффициент комплекса);
(n1+n2+n3+n4+n5) - компьютерные параметры для соединения комплекса, ккал/моль.
Предлагаемый коэффициент представляет сумму A1+А2 прив.
Сущность изобретения показана на примерах оптимальной флотации медной руды с различным соотношением ксантогенатов.
Пример 1. При флотации медной руды использовали смесь бутилового и изопропилового ксантогенатов при отношении 2:1 и общем расходе 70 г/т.
Молекулярные веса бутилового ксантогената - 150,02, изопропилового - 136,24 и гексилового ксантогената - 178,05. Долю бутилового ксантогената составила при. использовании расхода 70/3=23,3×2=46,66 г/т или в молях 46,66:150,02=0,31 М (БКх), а изопропилового ксантогената 23,3 г/т или в молях 23,33:136,24=0,17 М (изо-ПКх).
В табл.2 представлены компьютерные параметры ксантогенатов с учетом их мольности.
| Таблица 2 | ||||
| Компьютерные параметры с учетом мольности используемыхРеагентов | ||||
| Параметры | Сульфгидрильные реагенты | |||
| Бутиловый КхН | Изопропиловый КхН | Бутиловый КхН с учетом 0,31М (расход 46,6 г/т) | Изопропиловый КхН с учетом 0,17 М(расход 23.3 г/т) | |
| Итерация 44 (1) | Итерация 165 (2) | Итерация 44(3) | Итерация 165 (4) | |
| Растяжение валентных связей n1 | 0.4563 | 0.5090 | 0,14 | |
| Изгиб валентных угловn2 | 2.2180 | 2.7544 | 0,69 | |
| Поправки изгиб-растяжение n3 | 0.1797 | 0.2243 | ||
| Внутреннее вращениеn4 | 0.0074 | -2.7544 | ||
| Не ¼ ван-дер-ваальсовские взаимодействия n5 | -0.5533 | -0.6989 | ||
| ¼ ван-дер-ваальсовскиевзаимодействия n6 | 5.1367 | 4.3641 | 1,59 | 0,742 |
| Диполь/дипольное взаимодействие | 0.5266 | 0.7969 | 0,16 | 0,136 |
| Общая стерическая энергия, ккал/мол n7 | 7.9714 | 5.1953 | 2,47 | 0,88 |
| Коэффициент | 1,75 | 0.878 | ||
| Суммакоэффициентов | 2,408 |
Установлено, что для бутилового КхН величина ¼ ВДВ и Д/Д составляют 5,1367 и 0,5266 соответственно. С учетом использованного расхода реагентов (БКх) ¼ ВДВ равно - 1,59 и Д/Д - 0,16 соответственно, т.е. сумма коэффициентов составила - 1,75.
Установлено, что для изопропилового КхН величина ¼ ВДВ и Д/Д составляют 4,3641 и 0,7969 соответственно. С учетом использованного расхода реагентов изо-ПКх ¼ ВДВ равно - 0,742 и Д/Д - 0,136, соответственно, т.е. сумма коэффициентов составила - 0,878.
Прикрепим молекулы бутилового БКхН и изо-пропилового КхН к поверхности циклического халькопирита.
На Фиг.1 показана схема прикрепления молекул бутилового КхН и изопропилового КхН к поверхности двух атомов Сu циклического халькопирита.
Схема показывает прикрепления бутилового КхН и изопропилового КхН к поверхности циклического халькопирита (а) и шаростержневая модель созданного соединения (б).
В табл.3 показаны компьютерные параметры созданного комплекса.
| Таблица 3 | ||||
| Компьютерные параметры созданного комплекса | ||||
| Параметры | Сульфгидрильные реагенты | |||
| Соединения бутилового КхН и изопропилового КхН, связанные с халькопиритом Итерация (438) | Соединение, связанное с халькопиритом применительно с величиной 0,0015 М (содержанием меди в руде) | Соединение, гексиловый КхН связанное с халькопиритом применительно с величиной 0,0019 М | Соединение гексиловый КхН и бутиловый КхН с халькопиритом Итерация 401 | |
| (1) | (2) | (3) | (4) | |
| Растяжение валентных связей n1 | 1.1104 | 0,0017 | 0.6125×0,0019 | 1.0980 |
| Изгиб валентных углов n2 | 3.9670 | 0.006 | 1.4003×0,0019 | 2.5526 |
| Поправки изгиб-растяжение n3 | 0.1251 | 0.1812×0,0019 | 0.2760 | |
| Внутреннее вращение n4 | -2.4180 | -0.1073×0,0019 | -0.1178 | |
| Не ¼ ван-дер-ваальсовские взаимодействия n5 | -5.5868 | -3.2972× 0.0019 | -5.7245 | |
| ¼ ван-дер-ваальсовские взаимодействия n6 | 8.3533 | 0,013 | 5.6060×0,0019 0.01065 | 10.6714×0,0015 0,016 |
| Диполь/дипольное взаимодействие | 1.5475 | 0.002 | 0.8212×0,0019 0.0016 | 1.5320×0,0015 0,002 |
| Общая стерическая энергия, ккал/мол n7 | 7.0984 | 0,106 | 5.2167×0,0019 | 10.2877 |
| Коэффициент | 0,015 | 0.012 | 0.0162 | |
| Сумма коэффициентов | 2,408+0,015=2,423 |
Энергия соединения, связанного с халькопиритом 7.0984 ккал/моль.
Ниже предлагается метод расчета необходимой концентрации реагентов для максимального извлечения металла из руд.
Определяет общую энергию и количество металла в созданном соединении. Например, при связывании бутилового КхН и изопропилового КхН с поверхностью халькопирита энергия составляет 7.0984 ккал/моль, а содержание меди в соединении 19,45% или молей меди в соединений по отношению к содержанию меди в халькопирите 19,45/34,63=0,56 М. Устанавливают количество молей меди в созданном соединений по отношению к меди в руде.
Химическая формула C9H18Cu2Fe2O2S8; молекулярный вес 653,54.
Элементный анализ C 16,54; H 2,78: Cu 19, 45; Fe l7,09; O 4,90; S 39,25.
Содержание меди в созданном (с прикрепленными собирателями) соединении определено 19,45%, а молекулярный вес составляет 653,54.
Весовое количество меди в созданном соединении составляет:
100-19,45
653,54-X
Вес=127,11.
Определяют количество молей меди в соединении, моль=127,11/653,54=0,18 М.
Содержание меди в руде 1,059% и определяют количество молей меди соединении в руде:
127,11-0,18
1,059-X
молей Х=0,0015.
Количество молей определяют компьютерные параметры (табл.3, столбец 2).
Предлагаемый коэффициент равен 2,408+0,015=2,423.
При извлечении меди 89,39% предлагаемый коэффициент равен 2,423.
Пример 2. Флотацию медной руды проводили смесью гексилового КхН и бутилового ксантогенатов КхН при отношении 1:1,5 при расходе 50 г/т.
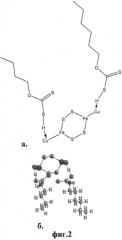
На Фиг.2 представлены схема прикрепления смеси гексилового ксантогената КхН и бутилового ксантогената КхН к поверхности циклического халькопирита (а) и шаростержневая модель созданного соединения (б).
С учетом использованного расхода гексилового ксантогената КхН (0,1М) ¼ ВДВ равно - 0,65 и Д/Д - 0,04 соответственно, т.е. сумма коэффициентов составила - 0,69.
С учетом использованного расхода бутилового ксантогената КхН (0,17М) ¼ ВДВ равно - 1,11 и Д/Д - 0,09 соответственно, т.е. сумма коэффициентов составила - 1,2.
На Фиг.2 показана схема прикрепления гексилового ксантогената ГКхН и бутилового ксантогената БКхН к поверхности циклического халькопирита (а) и шаростержневая модель созданного соединения (б).
Химическая формула C12H24Cu2Fe2O2S8, молекулярный вес 695,62, энергия 10,2877. Элементный анализ C 20,72; H 3,48: Cu 18,27; Fe 16,06; O 4,60; S 36,88.
Весовое количество меди
100-18,27
695,62-X
Вес=127,09
Моль=127,09/695,62=0,183 М (табл.3, столбец 3).
Содержание меди в руде 1,059% и определяют количество молей меди соединении в руде:
127,09-0,183
1,059-X
молей Х=0,0015 (табл.3, столбец 4).
При извлечении меди 89,74% предлагаемый коэффициент равен 1,89+0,0162=1,9062.
Пример 3. Флотации медной руды проводили смесью гексилового КхН и бутилового КхН ксантогенатов при отношении 2:1 при расходе 50 г/т.
С учетом использованного расхода гексилового КхН (0,17 М) ¼ ВДВ равно - 1,11 и Д/Д - 0,07 соответственно, т.е. сумма коэффициентов составила - 1,18.
С учетом использованного расхода бутилового КхН (0,1 М) ¼ ВДВ равно - 0,65 и Д/Д - 0,05 соответственно, т.е. сумма коэффициентов составила - 0,7.
При извлечении меди 89,84% предлагаемый коэффициент равен 1,88+0,0162=1,896.
Полученные суммарные данные для композиций на основе алкилксантогенатов можно представить:
| извлечение меди, % | предлагаемый коэффициент |
| 89,39 | 2,31 |
| 89,90 | 2,442 |
| 89,74 | 1,9062 |
| 89,84 | 1,896 |
При извлечении меди в пределах 89,39-89,90% величина предлагаемого коэффициента изменяется от 1,896 до 2,442 при различном соотношении смеси бутилового ксантогената изопропилового и гексилового ксантогенатов.
Было установлено:
- коэффициент равен 2,442 при флотации медных руд смесью бутилового и изопропилового ксантогенатов при отношении 2:1, коэффициент 1,89 для флотации смесью гексилового (ГКх) и бутилового ксентогенатов(БКх) при отношении 1:1,5, коэффициент 1,896, для флотации смесью гексилового (ГКх) и бутилового (БКх) ксантогенатов при отношении 2:1;
- соотношение смесей флотореагентов для максимального извлечения меди из медных руд определяется коэффициентом в пределах от 1,896 до 2,442;
- у смеси реагентов при флотации медных руд растяжение валентных связей от 0.4563 до 0.5937; изгиб валентных углов от 2.2180 до 2.7544 и коэффициент для растяжения валентных связей равен 0,749, а изгиба валентных углов коэффициент 3,367;
- общая стерическая энергия реагентов при флотации руд при максимальном извлечении металлов должна в пределах от 5.1953 до 9.5615 ккал/моль;
- отношение общей энергии соединения с прикрепленным собирателем к энергии суммы бутилового и изопропилового собирателей (собирателей), гексилового ксантогената (9.5615) должно быть от - 0,78 (10.2877/7.9714+5.1953=13,1667) до 1,076 (10.2 877/9.5615);
- в случае смеси бутилового и изопропилового ксантогенатов при отношении 2:1 и расходе реагентов 70 г/т, предлагаемый коэффициент равен 2,31 для извлечения меди 89,39%.
Работа способа
Определяют подачу бутилового ксантогената. Энергия для ¼ ван-дер-ваальсово взаимодействия равно 5.1367 и для диполь/диполь взаимодействия 0.5266.
5,1367×М+0,5266×М=коэффициент 1,75 М=1,75/5,6633=0.309 М, т.е нужно подавать 0,309 М или X 150,02 (мол. вес.)=46,36 г/т.
1. Способ флотации руд с использованием смеси собирателей, отличающийся тем, что для подбора реагентов в качестве флотореагентов используют компьютерную химическую программу, предварительно виртуально прикрепляют смеси реагентов к атому металла модели флотируемого минерала, определяют для полученного комплекса компьютерные параметры и с учетом содержания металлов в руде определяют мольность металла во флотируемой руде, при этом для используемых реагентов должно быть - диполь/дипольное взаимодействие в пределах от -2.7717 до 0.4956, 1/4 ван-дер-ваальсово взаимодействие в пределах от 2.2390 до 8.8701, не 1/4 ван-дер-ваальсово взаимодействие от -0.3746 до 1.7483, изгиб валентных углов от 2.4600 до 3.1866, растяжением валентных связей от 0.2580 до 0.7430 и рассчитывают величину стерической энергии с учетом вычисленной мольности извлекаемого металла от 6.1198 до 8.6639 ккал/моль.
2. Способ флотации руд по п. 1, отличающийся тем, что стерическая энергия созданных моделей без учета мольности извлекаемого металла соединений с прикрепленными к халькопириту изопропилового ксантогената и бутилового ксантогената составляет 7.0984 ккал/моль, а гексилового ксантогената и бутилового ксантогената составляет 10.2877 ккал/моль.