Ртн-содержащий терапевтический/профилактический агент против остеопороза, характеризующийся тем, что ртн вводят один раз в неделю в стандартной дозе 100-200 единиц
Иллюстрации
Показать всеИзобретение относится к медицине и касается способа лечения или предотвращения остеопороза, включающего введение субъекту, которому это необходимо, лекарственного средства, содержащего РТН в качестве активного ингредиента, где РТН вводят один раз в неделю в стандартной дозе 200 единиц, и субъект удовлетворяет всем из следующих условий: возраст 65 лет или более, преобладающие переломы костей, плотность костей менее 80% средней плотности молодого взрослого и/или степень атрофии костей I или более высокая. Изобретение обеспечивает безопасность и высокую эффективность способа лечения остеопороза. 1 з.п. ф-лы, 2 пр., 5 ил., 35 табл.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Данное изобретение относится к терапевтическому или профилактическому агенту против остеопороза, который содержит PTH в качестве активного ингредиента. Данное изобретение относится также к агенту для ингибирования или предупреждения переломов костей, который содержит PTH в качестве активного ингредиента. В частности, данное изобретение относится к вышеуказанному лекарственному средству, характеризующемуся тем, что PTH вводят один раз в неделю в стандартной дозе 100-200 единиц.
УРОВЕНЬ ТЕХНИКИ
Остеопороз является “заболеванием, характеризующимся уменьшением прочности кости, которое создает увеличенный риск переломов костей”. Препараты PTH (гормона паращитовидной железы) известны в настоящее время в качестве одного агента для лечения остеопороза.
PTH является гормоном, который способствует регуляции концентрации кальция крови, вместе с кальцитонинами и витамином D. Например, известно, что PTH стимулирует абсорбцию кальция в кишечнике увеличением продуцирования активного витамина D3 в почке in vivo (непатентная ссылка 1).
Патентная ссылка 1 описывает способ лечения остеопороза, который увеличивает плотность костной ткани губчатого вещества кости имеющего остеопороз пациента без уменьшения плотности костной ткани кортикального слоя кости подкожным введением стандартной дозы 100 или 200 единиц PTH имеющему остеопороз пациенту один раз в неделю на протяжении периода 26 недель.
Таким образом, хотя патентная ссылка 1 утверждает, что эти способы лечения приводят лишь к увеличению плотности костной ткани, она не демонстрирует, способен или не способен этот способ лечения увеличивать прочность кости имеющего остеопороз пациента или уменьшать риск переломов костей. Кроме того, PTH вводят только отдельно, не в комбинации с кальцийсодержащими агентами.
Непатентная ссылка 1 описывает, что гиперкальциемию наблюдали у 11% пациентов и что стойкую гиперкальциемию наблюдали у 3% из них при взятии проб крови при 4-6 часах после введения PTH (20 мкг/день) пациентам в клиническом исследовании PTH при лечении остеопороза. Кроме того, непатентная ссылка 1 описывает также, что лечение прекращали вследствие стойкого повышения кальция сыворотки у одного из 541 пациентов, даже хотя кальций сыворотки возвращался к нормальному уровню фактически у всех пациентов перед следующим введением PTH.
Хотя непатентная ссылка 2 описывает, что не было клинической проблемы с сывороточным кальцием после введения этого лекарственного средства при ежедневном введении подкожного препарата PTH вместе с кальцийсодержащим агентом, она сообщает также, что кальций сыворотки повышался после введения. Непатентная ссылка 3 является вкладышем упаковки вводимого один раз в день подкожного препарата, описанного в непатентной ссылке 2. Этот вкладыш сообщает в описании различных вредных побочных событий после введения этого препарата, что наблюдали транзиторную гиперкальциемию после введения этого препарата. Кроме того, непатентная ссылка 3 описывает, что имелись сообщения о вредной побочной реакции на это лекарственное средство в виде гиперкальциемии в постмаркетинговых исследованиях этого препарата.
Таким образом, непатентные ссылки 1-3 описывают случаи гиперкальциемии в качестве вредной побочной реакции лекарственного средства при лечении остеопороза с использованием PTH и т.п., и описанные в них способы не могут быть названы адекватными в отношении безопасности.
При таком уровне техники, желательным является высоко безопасный и эффективный способ лечения остеопороза при помощи PTH.
ССЫЛКИ ИЗВЕСТНОГО УРОВНЯ ТЕХНИКИ
ПАТЕНТНЫЕ ССЫЛКИ
Патентная ссылка 1: JP Kokai H08-77376
Патентная ссылка 2: WO00/10596
Патентная ссылка 3: JP Kokai Н05-306235
Патентная ссылка 4: JP Kokai S64-16799
Патентная ссылка 5: WO02/002136
Патентная ссылка 6: JP Kokai 2003-095974
НЕПАТЕНТНЫЕ ССЫЛКИ
Непатентная ссылка 1: Paul D. Miller, MD, Current Osteoporosis reports, Vol. 6, 12-16, 2008
Непатентная ссылка 2: CLINICAL CALCIUM, Vol. 17, No. 1, 48-55, 2007
Непатентная ссылка 3: FORTEO (registered trademark) teriparatide (rDNA origin) injection 750 mcg/3 ml, 2008
Непатентная ссылка 4: ADVANCES IN ENZYMOLOGY, 32, 221-296, 1969
Непатентная ссылка 5: Hoppe Seyler's Z. Physiol Chem., 355, 415, 1974
Непатентная ссылка 6: J. Biol. Chem., Vol. 259, No. 5, 3320, 1984
Непатентная ссылка 7: Pthobiology annual, 11, 53, 1981
Непатентная ссылка 8: J. Biol. Chem., Vol. 266, 2831-2835, 1991
Непатентная ссылка 9: Marcus. & Aurbach, G.D., Endocrinology 85, 801-810, 1969
Непатентная ссылка 10: “2006 Ostroporosis Prevention and Treatment Guidelines” (Life Sciences Publishing Co., Ltd.)
Непатентная ссылка 11: M. Takai et al., Peptide Chemistry 1979, 187-192, 1980
Непатентная ссылка 12: H. Orimo, et al., Diagnostic criteria for primary osteoporosis (1996 revised edition) (1997) Journal of Bone And Mineral Metabolism 14; 219-233
Непатентная ссылка 13: Diagnostic criteria for primary osteoporosis and osteoporosis prevention and treatment guidelines (H. Orimo, et al., 2006 Osteoporosis prevention and treatment guidelines (2006) 34-35)
Непатентная ссылка 14: Genant H.K. et al., J. Bone Miner. Res., 8, 1137-1148, 1993
Непатентная ссылка 15: N. Engl. J. Med., Vol. 344, No. 19, 1434-1441, 2001
Непатентная ссылка 16: Clinical Diabetes, Vol. 22, No. 1, 10-20, 2004
Непатентная ссылка 17: Kawasaki Medical Journal, 36(1), 23-33, 2010
Непатентная ссылка 18: Bone, Vol. 32, 86-95, 2003
Непатентная ссылка 19: Reports on Dentistry, 102(11): 853-868, 2002
Непатентная ссылка 20: Miner. Electrolyte Metab. 1995; 21(1-3); 201-4
Непатентная ссылка 21: Nippon Seikeigeka Gakkai Zasshi 1995 Oct; 69 (10): 1027-36
Непатентная ссылка 22: Calcif. Tissue Int. 2000 Mar; 66(3): 229-33
Непатентная ссылка 23: N. Engl. J. Med., Vol. 358, No. 12, 1302-1304, 2008
Непатентная ссылка 24: N. Engl. J. Med., Vol. 357, No. 20, 2028-2039, 2007
Непатентная ссылка 25: Osteoporos. Int. 2003 Jan; 14(1): 77-81
Непатентная ссылка 26: Osteoporos. Int. 2000; 11(5): 434-42
Непатентная ссылка 27: J. Bone Miner. Res. 2000 May; 15(5): 944-51
Непатентная ссылка 28: J. Clin. Invest. 1998 Oct 15; 102(8): 1627-33
Непатентная ссылка 29: J. Clin. Endocrinol. Metab. 2001 Feb; 86(2): 511-6
Непатентная ссылка 30: J. Bone Miner. Res. 2004 May; 19(5): 745-51. Epub 2004 Jan 19
Непатентная ссылка 31: J. Clin. Endocrinol. Metab. 2009 Oct; 94(10): 3772-80. Epub 2009 Jul 7
Непатентная ссылка 32: Osteoporos. Int. 2007; 18; 59-68
Непатентная ссылка 33: J. Bone Miner. Res., Vol. 25, No. 3, 472-481 (2010)
Непатентная ссылка 34: Osteoporos. Int. 1999; 9; 296-306
Непатентная ссылка 35: T. Inoue et al., Diagnostic criteria for osteoporosis-Assessment of degree of bone loss and vertebral deformity by simple vertebral roentgenogram, Ministry of Health and Welfare Life Science Research Fund Silver Science Research 1988 report, 1990, 3
Непатентная ссылка 36: J. Bone Miner. Metab. 1998; 16(1): 27-33
Непатентная ссылка 37: Proceedings of the 26th Meeting of the Japanese Society for Bone and Mineral Research, O-025, 147 (Oct. 2008)
Непатентная ссылка 38: ASBMR 31st Annual Meeting, “Weekly treatment with human parathyroid hormone (1-34) for 18 months increases bone strength via the amelioration of microarchitecture, degree of mineralization, enzymatic and non-enzymatic cross-links formation in ovariectomized cynomolgus monkeys” (Sa0044, FR0044).
Непатентная ссылка 39: IOF World Congress on Osteoporosis & 10th European Congress on Clinical and Economic Aspects of Osteoporosis and Osteoarthritis “ONCE-WEEKLY TREATMENT WITH TERIPARATIDE FOR 18 MONTHS INCREASES BONE STRENGTH VIA AMELIORATE TRABECULAR ARCHITECTURE, COLLAGEN ENZYMATIC AND NON-ENZYMATIC CROSS-LINK FORMATION IN OVARIECTOMIZED CYNOMOLGUS MONKEYS”
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
ПРОБЛЕМЫ, РЕШАЕМЫЕ ПОСРЕДСТВОМ ЭТОГО ИЗОБРЕТЕНИЯ
Данное изобретение обеспечивает высоко безопасный и эффективный способ для лечения или предотвращения остеопороза при помощи PTH. Кроме того, данное изобретение обеспечивает высоко безопасный способ ингибирования или предотвращения переломов костей при помощи PTH.
СРЕДСТВА ДЛЯ РЕШЕНИЯ ЭТИХ ПРОБЛЕМ
В результате интенсивного исследования и развития, осуществленных для решения вышеуказанных проблем, авторы этого изобретения изобрели высоко безопасный и эффективный способ лечения или предотвращения остеопороза, довольно неожиданно, ограничением дозы и интервала введения PTH. Они изобрели также высоко безопасный способ ингибирования/предотвращения переломов костей, описав эти дозу и интервал введения PTH. Кроме того, они обнаружили также, что эти способы особенно эффективны у пациентов с высоким риском.
Конкретно, данное изобретение раскрывает следующее.
[1] Агент для лечения или предотвращения остеопороза, который содержит PTH в качестве активного ингредиента, характеризующийся тем, что его используют вместе с кальцийсодержащим агентом, и PTH вводят один раз в неделю в стандартной дозе 100-200 единиц.
[2] Агент для лечения или предотвращения остеопороза по [1] выше, характеризующийся тем, что кальцийсодержащий агент, используемый в комбинации, вводят один или несколько раз в неделю.
[3] Агент для лечения или предотвращения остеопороза по [1] или [2] выше, характеризующийся тем, что кальцийсодержащий агент, используемый в комбинации, вводят в дозе 200-800 мг/день в виде кальция.
[4] Агент для лечения или предотвращения остеопороза по любому из [1]-[3] выше, где вышеуказанный PTH является PTH человека (1-34).
[5] Агент для лечения или предотвращения остеопороза по любому из [1]-[4] выше для введения на протяжении периода, превышающего 24 недели или 48 недель.
[6] Агент для лечения или предотвращения остеопороза по любому из [1]-[5] выше для лечения пациентов с остеопорозом, которые удовлетворяют всем из следующих условий (1)-(3) ниже:
(1) Возраст 65 лет или более,
(2) Преобладающие переломы костей,
(3) Плотность костей менее 80% средней плотности молодого взрослого и/или степень атрофии костей I или более высокая.
[7] Агент для лечения или предотвращения остеопороза по любому из [1]-[6] выше для лечения или предотвращения вторичного остеопороза, вызываемого глюкокортикоидом, или диабетического остеопороза.
[8] Агент для лечения или предотвращения остеопороза по любому из [1]-[6] выше для лечения или предотвращения остеопороза у пациентов, имеющих по меньшей мере одно из заболеваний (1)-(8) ниже в качестве осложнения:
(1) Диабет,
(2) Гипертензию,
(3) Гиперлипидемию,
(4) Артралгию,
(5) Остеоартрит позвоночника,
(6) Метатипическую боль в нижней части спины,
(7) Остеоартрит бедра,
(8) Остеоартрит челюсти.
[9] Агент для лечения или предотвращения остеопороза по любому из [1]-[6] выше для введения пациенту с остеопорозом, имеющим историю введения по меньшей мере одного из терапевтических агентов остеопороза по (1) - (6) ниже:
(1) L-аспартата кальция,
(2) Альфакальцидола,
(3) Элкатонина,
(4) Гидрохлорида ралоксифена,
(5) Менатетренона,
(6) Лактата кальция.
[10] Агент для лечения или предотвращения остеопороза по любому из [1]-[6] выше для введения пациенту с остеопорозом, имеющим легкую почечную дисфункцию или умеренную почечную дисфункцию.
[11] Агент для лечения или предотвращения остеопороза по любому из [6]-[10] выше, где вышеуказанный PTH является PTH человека (1-34).
[12] Агент для лечения или предотвращения остеопороза по любому из [6]-[11] выше, где вышеуказанный терапевтический агент против остеопороза, содержащий PTH в качестве активного ингредиента, является подкожным инъекционным раствором.
[13] Комбинированный препарат или набор для лечения, состоящий из агента для лечения или предотвращения остеопороза, указанного в любом из [1]-[12] выше, и по меньшей мере одного лекарственного средства по (1)-(6) ниже:
(1) Метоклопрамида,
(2) Домперидона,
(3) Фамотидина,
(4) Цитрата мозаприда,
(5) Лансопразола,
(6) Рокушингана.
[14] Агент для лечения или предотвращения остеопороза, который содержит PTH в качестве активного ингредиента, характеризующийся тем, что PTH вводят один раз в неделю в стандартной дозе 100-200 единиц, причем этот агент для лечения или предотвращения остеопороза используют для лечения пациентов с остеопорозом, которые удовлетворяют всем из следующих условий (1)-(3):
(1) Возраст 65 лет или более,
(2) Преобладающие переломы костей,
(3) Плотность костей менее 80% средней плотности молодого взрослого и/или степень атрофии костей I или более высокая.
[15] Агент для лечения или предотвращения остеопороза при высоком риске в отношении переломов костей, который содержит PTH в качестве активного ингредиента, характеризующийся тем, что PTH вводят один раз в неделю в стандартной дозе 100-200 единиц.
[16] Агент для лечения или предотвращения остеопороза, который содержит PTH в качестве активного ингредиента, характеризующийся тем, что PTH вводят один раз в неделю в стандартной дозе 100-200 единиц, причем этот агент для лечения или предотвращения остеопороза используют для лечения или предотвращения вторичного остеопороза, вызываемого глюкокортикоидом, или диабетического остеопороза.
[17] Агент для лечения или предотвращения остеопороза, который содержит PTH в качестве активного ингредиента, характеризующийся тем, что PTH вводят один раз в неделю в стандартной дозе 100-200 единиц, причем этот агент для лечения или предотвращения остеопороза вводят пациентам с остеопорозом, имеющим легкую почечную дисфункцию или умеренную почечную дисфункцию.
[18] Агент для ингибирования или предотвращения переломов костей, который содержит PTH в качестве активного ингредиента, характеризующийся тем, что его используют вместе с кальцийсодержащим агентом и PTH вводят один раз в неделю в стандартной дозе 100-200 единиц.
[19] Агент для ингибирования или предотвращения переломов костей по [18] выше, характеризующийся тем, что кальцийсодержащий агент, используемый в комбинации, вводят один или несколько раз в неделю.
[20] Агент для ингибирования или предотвращения переломов костей по [18] или [19] выше, характеризующийся тем, что кальцийсодержащий агент, используемый в комбинации, вводят в дозе 200-800 мг/день в виде кальция.
[21] Агент для ингибирования или предотвращения переломов костей по [18]-[20] выше, где вышеуказанный PTH является PTH человека (1-34).
[22] Агент для ингибирования или предотвращения переломов костей по [18]-[21] выше для введения субъектам, которые удовлетворяют всем из следующих условий (1)-(3):
(1) Возраст 65 лет или более,
(2) Преобладающие переломы костей,
(3) Плотность костей менее 80% средней плотности молодого взрослого и/или степень атрофии костей I или более высокая.
[23] Агент для ингибирования или предотвращения переломов костей по [22] выше, где этот вышеуказанный PTH является PTH человека (1-34).
[24] Агент для ингибирования или предотвращения переломов костей по [22] или [23] выше, где вышеуказанный агент для ингибирования или предотвращения переломов костей, который содержит PTH в качестве активного ингредиента, является подкожным инъекционным раствором.
[25] Агент для ингибирования или предотвращения переломов костей по любому из [18]-[24] выше, где вышеуказанный агент для ингибирования или предотвращения переломов костей является агентом для ингибирования множественных переломов костей или предотвращения множественных переломов костей.
[26] Агент для ингибирования или предотвращения переломов костей по любому из [18]-[25] выше, где вышеуказанный агент для ингибирования или предотвращения переломов костей является агентом для ингибирования ухудшения переломов или предотвращения ухудшения переломов.
[27] Агент для лечения или предотвращения остеопороза по [14] или [15] выше, причем этот агент для лечения или предотвращения остеопороза используют для лечения или предотвращения вторичного остеопороза, вызываемого глюкокортикоидом, или диабетического остеопороза.
[28] Агент для лечения или предотвращения остеопороза по [14] или [15] выше, причем этот агент для лечения или предотвращения остеопороза вводят пациентам с остеопорозом, имеющим легкую почечную дисфункцию или умеренную почечную дисфункцию.
[29] Агент для лечения или предотвращения остеопороза по [27] выше, причем этот агент для лечения или предотвращения остеопороза вводят пациентам с остеопорозом, имеющим легкую почечную дисфункцию или умеренную почечную дисфункцию.
[30] Агент для лечения или предотвращения остеопороза по [16] выше, причем этот агент для лечения или предотвращения остеопороза вводят пациентам с остеопорозом, имеющим легкую почечную дисфункцию или умеренную почечную дисфункцию.
[31] Способ предотвращения или лечения с использованием агента лечения, агента предотвращения, лекарственного средства, комбинации лекарственного средства или набора по любому из [1]-[30] выше.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Терапевтический агент для использования при остеопорозе, согласно данному изобретению, является высоко безопасным и имеет превосходную эффективность. Агент для ингибирования или предотвращения переломов костей согласно данному изобретению является также высоко безопасным и полезным.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Фиг.1 является графиком, показывающим изменения в сывороточной концентрации кальция в группе введения (пациентов высокого риска, пациентов низкого риска);
Фиг.2 показывает действия введения тестируемого лекарственного средства на протяжении времени в случае новых позвоночных переломов. Эта тест-группа лекарственного средства указана в списке как “группа PTH200” и контрольная группа указана как “Р-группа”;
Фиг.3 показывает действия тестируемого лекарственного средства на изменения на протяжении времени в случае новых позвоночных переломов. Эта тест-группа лекарственного средства указана в списке как “группа PTH200” и контрольная группа указана как “Р-группа”;
Фиг.4 показывает результаты на изменениях величины кальция мочи, при введении тестируемого лекарственного средства (“группы PTH200”) и контроля (“Р-группы”) пациентам один раз в неделю в течение 72 недель. Отношение величина кальция мочи/величина креатинина мочи сравнивали перед началом введения и во время недель наблюдения. Кальций мочи измеряли в начале (на старте), после 12 недель, после 24 недель, после 48 недель и после 72 недель. Стандартное сопутствующее лекарственное средство (610 мг кальция, 400 МЕ витамина D3 и 30 мг магния) принимали один раз в день после обеда со времени согласия пациента до конца этого исследования; и
Фиг.5 показывает результаты на изменениях в корректированной величине сывороточного кальция при введении тестируемого лекарственного средства (“группе PTH200”) или контроля (“Р-группе”) пациентам один раз в неделю в течение 72 недель. Сывороточный кальций измеряли на старте, после 12 недель, после 24 недель, после 48 недель и после 72 недель. Стандартная величина сывороточного кальция: 8,4-10,4 мг/дл. Стандартное сопутствующее лекарственное средство (610 мг кальция, 400 МЕ витамина D3 и 30 мг магния) принимали один раз в день после обеда со времени согласия пациентов до конца этого исследования.
СПОСОБ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Данное изобретение подробно объясняется ниже.
Данное изобретение предоставляет способ для лечения или предотвращения остеопороза или способ для ингибирования или предотвращения переломов костей с использованием PTH, характеризующийся тем, что PTH вводят один раз в неделю в стандартной дозе 100-200 единиц (вместо “один раз в неделю” здесь иногда употребляется “каждую неделю”). Данное изобретение также предоставляет агент для лечения или предотвращения остеопороза или агент для ингибирования или предотвращения переломов костей, имеющий PTH в качестве активного ингредиента, характеризующийся тем, что PTH вводят каждую неделю в стандартной дозе 100-200 единиц. Кроме того, данное изобретение обеспечивает применение PTH для получения вышеуказанного агента для лечения или предотвращения остеопороза или вышеуказанного агента для ингибирования или предотвращения переломов костей.
I. Активный ингредиент
PTH, который является активным ингредиентом согласно данному изобретению (иногда называемый здесь далее просто “PTH”), включает в себя PTH человека (1-84), который является паращитовидным (паратиреоидным) гормоном человека и пептидами с молекулярной массой приблизительно 4000-10000, имеющими активность, эквивалентную PTH человека (1-84).
PTH включает в себя все из природного PTH, PTH, продуцируемого способами генетической инженерии, и PTH, синтезированного способами химического синтеза. PTH может быть получен способами генетической инженерии, которые сами по себе являются известными (непатентная ссылка 8). Альтернативно, PTH может быть синтезирован способами пептидного синтеза, которые сами по себе являются известными (непатентная ссылка 11). Например, он может быть синтезирован твердофазным способом, который удлиняет пептидную цепь от С-конца на нерастворимом полимерном носителе (непатентная ссылка 4). Кроме того, происхождение PTH данного изобретения не ограничивается человеком и может включать в себя PTH крысы, коровы, свиньи и т.п.
В этом описании, PTH человека (n-m) обозначает пептид, показанный частичной аминокислотной последовательностью от номера n до номера m в аминокислотной последовательности PTH человека (1-84). Например, PTH (1-34) человека обозначает пептид, показанный частичной аминокислотной последовательностью, состоящей из части от 1 до 34 в аминокислотной последовательности PTH человека (1-84).
PTH, который является активным ингредиентом в соответствии с данным изобретением, может быть также солью, образованной с одним, двумя или более типами летучих органических кислот. Примеры летучих органических кислот включают в себя трифторуксусную кислоту, муравьиную кислоту, уксусную кислоту и т.п. Уксусная кислота может быть представлена в качестве предпочтительного примера. Отношение этих двух компонентов, когда свободный PTH и летучая органическая кислота образуют соль, особо не ограничивается, пока образуется соль. Например, поскольку PTH (1-34) человека имеет девять основных аминокислотных остатков и четыре кислых аминокислотных остатка в его молекуле, с учетом образования соли в этих молекулах, основный аминокислотный остаток 5 может быть превращен в химический эквивалент уксусной кислоты. Например, если содержание уксусной кислоты, представленное отношением масса уксусной кислоты × 100 (%)/масса пептида PTH человека (1-34), используется в качестве количества уксусной кислоты, по одной теории, химический эквивалент уксусной кислоты против свободного PTH человека (1-34) становится приблизительно 7,3% (% масс.). В этом описании, свободный PTH человека (1-34) называют иногда терипаратидом и ацетат терипаратида также называют иногда терипаратидацетатом. Содержание уксусной кислоты в терипаратидацетате не ограничивается особо, пока этот терипаратид и уксусная кислота образуют соль. Например, это содержание может быть равно 7,3%, что выше теоретического химического эквивалента, или более высоким, или оно может быть 0-1%. Более конкретные примеры содержания уксусной кислоты в терипаратиде равны 1-7%, предпочтительно 2-6%. Эти соли могут быть получены способами, которые сами по себе известны (патентные ссылки 4 и 5).
Примеры PTH включают в себя PTH человека (1-84), PTH человека (1-34), PTH человека (1-38), hPTH (непатентная ссылка 5), PTH человека (1-34) NH2, [Nle8,18]PTH человека (1-34), [Nle8,18, Tyr34]PTH человека (1-34), [Nle8,18]PTH человека (1-34) NH2, [Nle8,18, Tyr34]PTH человека (1-34) NH2, мышиный PTH (1-84), мышиный PTH (1-34), бычий PTH (1-84), бычий PTH (1-34), бычий PTH (1-34) NH2 и т.п. Примерами предпочтительных PTH являются PTH человека (1-84), PTH человека (1-38), PTH человека (1-34) и PTH человека (1-34) NH2 (патентная ссылка 3, и т.д.). PTH человека (1-34) является примером особенно предпочтительного PTH. PTH человека (1-34), полученный химическим синтезом, является примером даже более предпочтительного PTH, а терипаратидацетат (Рабочий Пример 1) является примером наиболее предпочтительного PTH.
II. Объединенное применение с другими лекарственными средствами
В результатах двойного слепого сравнительного клинического исследования PTH, используемого в комбинации с кальцийсодержащими агентами, проводимого авторами данного изобретения, с присутствием переломов костей в качестве первичной точки, это действие проявлялось рано (после 24 или 26 недель), и гиперкальциемия не подтверждалась в качестве вредного побочного события (рабочие примеры 1 и 2). Таким образом, комбинированное применение с другими лекарственными средствами является одной характеристикой этого терапевтического агента против остеопороза или агента для ингибирования/предотвращения переломов костей согласно данному изобретению. Комбинированное применение с другими лекарственными средствами означает, что этот терапевтический агент против остеопороза или агент для ингибирования/предотвращения переломов костей согласно данному изобретению используется в комбинации с другим лекарственным средством (другими лекарственными средствами).
Кальций может рассматриваться в качестве предпочтительного примера другого лекарственного средства в данном изобретении. Однако утверждение о комбинированном применении с другими лекарственными средствами в данном изобретении не исключает дополнительного комбинированного применения с лекарственными средствами, отличными от указанных здесь. Таким образом, предпочтительные примеры комбинированного применения с кальцием включают в себя:
комбинированное применение только с кальцием и
комбинированное применение с кальцием и витамином D (в том числе его производными) и/или только магнием.
Кальцийсодержащие агенты могут рассматриваться в качестве примеров конкретных вариантов других лекарственных средств, и предпочтительные примеры включают в себя:
(1) Кальцийсодержащий агент, содержащий кальций в качестве активного фармацевтического ингредиента, и
(2) Кальцийсодержащий агент, содержащий кальций, витамин D (в том числе его производные) и магний в качестве активных фармацевтических ингредиентов.
Способ вышеуказанного комбинированного применения терапевтического агента против остеопороза или агента для ингибирования/предотвращения переломов костей согласно данному изобретению и других лекарственных средств (частота введения, способ введения, место введения, доза и т.п.) не являются ограниченными и могут определяться предписанием доктора и т.п. в согласии с пациентом.
Например, при применении кальцийсодержащего агента в комбинации с вышеуказанным другим лекарственным средством, этот кальцийсодержащий агент может вводиться одновременно с терапевтическим агентом против остеопороза или агентом для ингибирования/предотвращения переломов костей согласно данному изобретению, имеющим PTH в качестве активного ингредиента (другими словами, один раз в неделю) или может вводиться более часто от одного до нескольких раз в день. Таким образом, вышеуказанное другое лекарственное средство может быть приготовлено в виде комбинированного препарата в комбинации с терапевтическим/профилактическим агентом против остеопороза или агентом для ингибирования/предотвращения переломов костей согласно данному изобретению или может быть отдельным препаратом от терапевтического/профилактического агента против остеопороза или агента для ингибирования/предотвращения переломов костей согласно данному изобретению. Примеры таких кальцийсодержащих агентов включают в себя “New Calcichew (trademark) D3” (продаваемый: Daiichi Sankyo Health Care, изготовляемый и продаваемый: Nitto Pharmaceutical Industries, Ltd.).
Другие лекарственные средства могут также вводиться тем же самым или отличным способом введения вместе или последовательно (то есть, в разное время) с терапевтическим/профилактическим агентом против остеопороза или агентом для ингибирования/предотвращения переломов костей согласно данному изобретению. Таким образом, форма этих других лекарственных средств конкретно не ограничивается. Примеры включают в себя таблетки, капсулы, гранулы и т.п. Когда этим другим лекарственным средством является кальцийсодержащий агент, он является предпочтительно кальцийсодержащим агентом, содержащим стандартную дозу 100-400 (предпочтительно 150-350) мг кальция. Если вводится кальцийсодержащий агент, содержащий стандартную дозу 100-400 мг в виде кальция, например, в дозе двух таблеток в день в соответствии с рабочим примером данного изобретения, 200-800 мг в день будут введены в виде кальция. Однако возможности не ограничиваются этим.
Конкретные примеры вышеуказанных других лекарственных средств, например, в случае кальцийсодержащих агентов, включают в себя известные лекарственные средства, имеющие в качестве активного ингредиента осажденный карбонат кальция, лактат кальция, карбонат кальция, хлорид кальция, глюконат кальция, аспартат кальция, фосфат кальция, гидрофосфат кальция, цитрат кальция и т.п. Предпочтительными являются лекарственные средства, которые содержат осажденный карбонат кальция. Кроме того, это лекарственное средство может содержать, в случае необходимости, эксципиенты, связывающие агенты, дезинтегрирующие агенты, матирующие агенты, антациды и т.п.
Известно, что рвота, тошнота, недомогание, ощущение тупости в желудке, желудочный дискомфорт, изжога и другие подобные желудочно-кишечные симптомы наблюдались транзиторно у некоторого процента пациентов, которым вводили PTH (патентная ссылка 6).
В результате тестирования количества точек времени введения и эффективности различных противорвотных средств для противодействия тошноте и рвоте, ассоциированным с введением этого тестируемого лекарственного средства, авторы данного изобретения подтвердили, что Примперан (родовое название этого активного ингредиента: метоклопрамид), Наузелин (родовое название этого активного ингредиента: домперидон), Гастер D (родовое название этого активного ингредиента: фамотидин), гасмотин (родовое название этого активного ингредиента: мозаприда цитрат), Такепрон OD (родовое название этого активного ингредиента: лансопразол) и рокушинган являются эффективными против тошноты и рвоты, ассоциированными с введением PTH (рабочий пример 2). Таким образом, эти противорвотные средства являются предпочтительными в качестве других лекарственных средств, и Наузелин (родовое название этого активного ингредиента: домперидон), гасмотин (родовое название этого активного ингредиента: мозаприда цитрат) и/или рокушинган могут рассматриваться как предпочтительные примеры. Доза и введение этих противорвотных средств могут устанавливаться подходящим способом лечащим врачом или другим медицинским персоналом в соответствии с симптомами пациента и другими подобными факторами.
III. Период введения
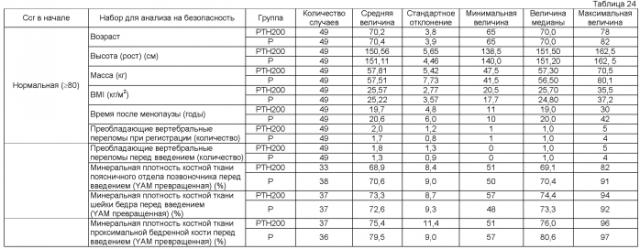
Период введения терапевтического/профилактического агента против остеопороза или агента для ингибирования/предотвращения переломов костей согласно данному изобретению не ограничивается конкретно и может определяться соответствующим образом лечащим врачом или подобным медицинским персоналом в соответствии с конкретным пациентом. Авторы этого изобретения проводили двойное слепое сравнительное клиническое исследование с появлением переломов костей в качестве первичной точки с использованием периодов введения 156 недель или 72 недель. Удалось подтвердить значимое ингибирующее действие на переломы костей таким введением в этом исследовании, и это действие проявлялось рано (спустя 24 недели или спустя 26 недель) (рабочие примеры 1 и 2). Кроме того, не обнаруживали новых позвоночных переломов при продолжении введения в течение более 48 недель (рабочий пример 2). Таким образом, примеры периодов введения включают в себя 24 недели или более, 26 недель или более, 48 недель или более, 52 недели или более, 72 недели или более и 78 недель или более. Наиболее предпочтительным является введение в течение семидесяти восьми недель или более. В этом исследовании не наблюдали гиперкальциемии в качестве вредного побочного события (рабочий пример 1).
IV. Доза
В результате двойного слепого сравнительного клинического исследования с использованием стандартной дозы 100 или 200 единиц PTH, авторы этого изобретения обнаружили значимое ингибирующее действие на переломах костей, вызываемое этим введением, и показали, что этот эффект появлялся рано (спустя 24 недели или 26 недель) и что не было гиперкальциемии в качестве побочного вредного события (рабочие примеры 1 и 2).
Таким образом, одним из признаков данного изобретения является то, что стандартная доза равна 100-200 единицам. Здесь, одна единица PTH может измеряться способами измерения активности, которые сами по себе известны (непатентная ссылка 9). Эта стандартная доза предпочтительно равна 100 или 200 единицам, наиболее предпочтительно 200 единицам.
V. Интервал введения
В результате двойного слепого сравнительного клинического исследования, в котором PTH вводили один раз в неделю, авторы этого изобретения обнаружили значимое ингибирующее действие на переломах костей, вызываемое этим введением, и показали, что это действие появлялся рано (спустя 24 недели или 26 недель) и что не было гиперкальциемии в качестве побочного вредного события (рабочие примеры 1 и 2). Таким образом, интервал введения один раз в неделю является одним из признаков данного изобретения.
VI. Способ введения
Терапевтический/профилактический агент против остеопороза и агент для ингибирования/предотвращения переломов костей согласно данному изобретению могут вводиться способом введения, который соответствует форме этого препарата. Например, когда терапевтический или профилактический агент против остеопороза или агент для ингибирования или предотвращения переломов костей согласно данному изобретению является инъекционным раствором, он может вводиться внутривенно, внутриартериально, подкожно, внутримышечно и т.п. Авторы этого изобретения установили, что подкожная инъекция PTH имеет превосходную эффективность и безопасность (рабочие примеры 1 и 2). Таким образом, подкожное введение может рассматриваться как предпочтительный пример способа введения в данном изобретении.
VII. Заболевания-мишени
Остеопороз в данном изобретении не является конкретно ограниченным и включает в себя как первичный остеопороз, так и вторичный остеопороз. Примеры первичного остеопороза включают в себя инволюционный остеопороз (постменопаузальный остеопороз и возрастной (старческий) остеопороз)) и идиопатический остеопороз (остеопороз после беременности, ювенильный остеопороз и т.п.). Вторичный остеопороз является остеопорозом, вызываемым конкретным заболеванием, конкретным лекарственным средством или другой подобной причиной. Примеры причин включают в себя конкретные лекарственные средства, ревматоидный артрит, диабет, гипертиреоидизм, половую дисфункцию, неподвижность, питание, наследственные заболевания и т.п. Примером конкретного лекарственного средства является глюкокортикоид. Остеопороз, который создает высокий риск переломов костей, является предпочтительным примером остеопороза в данном изобретении. Показание данного изобретения против остеопороза, создающего высокий риск переломов костей, означает, что данное изобретение показано для следующих пациентов высокого риска.
Авторы данного изобретения подтвердили эффективность и безопасность данного изобретения в клиническом исследовании, проводимом у пациентов с первичным остеопорозом (рабочие примеры 1 и 2). Таким образом, первичный остеопороз может считаться предпочтительным примером остеопороза в данном изобретении, и инволюционный остеопороз может считаться особенно предпочтительным примером.
Авторы данного изобретения подтвердили действие данного изобретения в клиническом исследовании, проводимом у пациентов с первичным остеопорозом, которые принимали глюкокортикоид, который вызывает вторичный остеопороз (рабочий пример 2). Таким образом, пациенты с первичным остеопорозом, которые принимают глюкокортикоид, вызывающий вторичный остеопороз, могут считаться предпочтительным примером пациентов с первичным остеопорозом в данном изобретении.
Авторы данного изобретения подтвердили действие данного изобретения в клиническом исследовании, проводимом у пациентов с первичным остеопорозом, имеющих осложнения (диабет, гипертензию или гиперлипидемию) (рабочий пример 2). Таким образом, пациенты с остеопорозом, имеющие по меньшей мере одно осложнение из диабета, гипертензии и гиперлипидемии, могут рассматриваться как предпочтительный пример пациентов с остеопорозом в данном изобретении, и пациенты с первичным остеопорозом, имеющие по меньшей мере одно осложнение из диабета, гипертензии и гиперлипидемии, могут рассматриваться как более предпочтительный пример.
Известно, что диабет является, очень вероятно, фактором риска остеопорозных переломов костей (непатентная ссылка 16).
Следующие сообщения взаимосвязи между диабетическим остеопорозом и PTH основаны на исследованиях с использованием животных.
1) Сообщается, что введение PTH получающим стрептозотоцин крысам, которые обнаруживали диабетическую потерю костей, увеличивает “объем костей”, “толщину костных трабекул”, “остеоидную поверхность”, “минерализованную поверхность”, “скорость аппозиции минеральных веществ” и скорость образования