Оптическая гиперполяризация на основе света, обладающего оптическим угловым моментом
Иллюстрации
Показать всеИзобретение относится к измерительной технике, представляет собой распылитель для получения контрастного вещества с гиперполяризованными ядрами и предназначено для использования в магнитно-резонансных исследованиях. Распылитель содержит камеру для приема соединения и систему гиперполяризации фотонов для создания пучка фотонов с орбитальным угловым моментом (ОУМ) и направления пучок фотонов с ОУМ в камеру для создания гиперполяризации ядер в соединении. Камера имеет выход, через который можно выпускать гиперполяризованное соединение. 2 н. и 6 з.п. ф-лы, 3 ил.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Изобретение относится к созданию гиперполяризованного контрастного вещества. Оптическая система создает пучок света с ОУМ, обладающий орбитальным угловым моментом (ОУМ). Этот пучок фотонов с ОУМ создает гиперполяризацию ядер в соединении, которое затем можно использовать в качестве гиперполяризованного контрастного вещества в магнитно-резонансном исследовании.
УРОВЕНЬ ТЕХНИКИ
Такая система гиперполяризации на основе фотонов известна из международной заявки WO2009/081360.
Известная система гиперполяризации на основе фотонов содержит поверхностный зонд со световым выходом, который направляет свет, обладающий орбитальным угловым моментом, для проникновения через ткань пациента, подлежащую исследованию. В альтернативном варианте осуществления известной системы гиперполяризации на основе света предусмотрен катетер. Эти известные приложения гиперполяризации на основе фотонов создают гиперполяризованное контрастное вещество в биологическом материале и имеют лишь небольшую глубину проникновения в биологическую (т. е. человеческую или животную) ткань. Таким образом, эти известные применения ограничены эндоскопическими, инвазивными и хирургическими применениями.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Цель изобретения состоит в том, чтобы предоставить распылитель с системой гиперполяризации на основе фотонов, который подходит для нехирургического применения.
Эта цель достигается с помощью распылителя, содержащего:
камеру для приема соединения; и
систему гиперполяризации фотонов, выполненную с возможностью создавать пучок фотонов с орбитальным угловым моментом (ОУМ) и направлять пучок фотонов с ОУМ в камеру для создания гиперполяризации ядер в соединении;
при этом камера имеет выход, через который можно выпускать гиперполяризованное соединение.
Изобретение основано на идеи использования фотонного пучка, обладающего орбитальным угловым моментом (световой пучок с ОУМ), для гиперполяризации соединения, например флюида (текучего вещества), в камере. Гиперполяризованное соединение выполняет роль контрастного вещества в эксперименте по ядерному магнитному резонансу (ЯМР) или магнитно-резонансной томографии (МРТ) и его вводят в объект, например, пациенту, подлежащему исследованию. Путь пучка для пучка фотонов с ОУМ и ЯМР- или МРТ-эксперимента разделяют. Таким образом, какие-либо ограничения по глубине проникновения света с ОУМ принимают во внимание в размерах камеры. Гиперполяризация соединения происходит в камере, которая легко доступна для пучка фотонов с ОУМ, т.е. через прозрачное окно, которое сохраняет орбитальный угловой момент пучка фотонов. Затем гиперполяризованное соединение выпускают через выход камеры, и его можно вводить в качестве контрастного вещества пациенту, подлежащему исследованию. В другой реализации гиперполяризацию переносят с первого гиперполяризованного соединения на второе целевое соединение, которое используют в качестве контрастного вещества. Поскольку гиперполяризацию создают ex vivo, глубина проникновения пучка фотонов с ОУМ в биологическую ткань не имеет значения для настоящего изобретения. Камеру можно реализовать в виде отдельного контейнера, который вмещает соединение, в которой соединение гиперполяризуют посредством пучка фотонов с ОУМ и впоследствии распыляют в качестве контрастного вещества. Альтернативно, камера может быть составной частью инфузионной системы, вдоль которой соединение переносят, гиперполяризуют пучком фотонов с ОУМ и распыляют в качестве контрастного вещества. Камера или в виде отдельного контейнера, или в виде составной части инфузионной системы предпочтительно имеет размеры в несколько миллиметров во всех направлениях. Камеру такого размера легко облучать с использованием приблизительно тысячи (1000) пятен пучка(ов) фотонов с ОУМ. Например 30×30 пятен по 1 мм2 можно использовать для гиперполяризации соединения на глубине 1 мм. Таким образом, можно получать от 1 до 10 мл/с гиперполяризованного соединения. Эти и другие аспекты изобретения будут дополнительно конкретизированы со ссылкой на варианты осуществления, определяемые в зависимых пунктах формулы изобретения.
В дополнительном аспекте изобретения распылитель содержит систему передачи поляризации. Соединение в камере представляет собой исходное соединение, в котором гиперполяризацию ядер или электронов создают с помощью пучка фотонов с ОУМ. В системе передачи поляризации с этого гиперполяризованного исходного соединения гиперполяризацию ядер или электронов передают целевому соединению. Это целевое соединение необязательно должно присутствовать, когда исходное соединение гиперполяризуют с помощью пучка фотонов с ОУМ, и может быть добавлено позже. Обычно, гиперполяризованное ядро в исходном соединении отличается от гиперполяризованного ядра в целевом соединении. В частности, протоны (1H) исходного соединения гиперполяризуют с помощью пучка фотонов с ОУМ, и эту гиперполяризацию переносят, например, на ядра 13C, 15N, 17O или 19F целевого соединения. В частности, исходное соединение может представлять собой воду, протоны (1H) которой можно эффективно поляризовать с помощью пучка фотонов с ОУМ. Эти ядра могут и будут поляризованы непосредственно с сохранением углового момента, если присутствуют в смеси во время взаимодействия с пучком фотонов с ОУМ.
Передача гиперполяризации из исходного соединения на целевое соединение происходит посредством системы передачи поляризации, основанной, например, на эффекте Оверхаузера или динамической ядерной поляризации (ДЯР). Альтернативно, для передачи поляризацию можно осуществлять через обменные взаимодействия в одной и той же молекуле, т.е., например, усиливать уже усиленный сигнал 13C посредством дополнительной передачи также усиленных сигналов 1H. В этой альтернативе исходное соединение и целевое соединение фактически представляют собой одно и то же, но передача поляризации происходит внутри от исходного ядра реципиенту в одном и том же соединении. Например, пучок фотонов с ОУМ поляризует протоны (1H) в глюкозе, и затем созданную поляризацию переносят на ядро углерода-13 (13C) в глюкозе. Затем глюкозу с гиперполяризованным 13C разводят в растворе, который подходит для введения в качестве контрастного вещества. В такой передаче поляризации используются последовательности импульсов ЯМР, такие как INEPT и другие последовательности, известные специалистам в данной области (см., например, Spin Dynamics. Basis of Nuclear Magnetic Resonance, M.H. Levitt, Wiley 2008). В особенно подходящем варианте осуществления эти последовательности модифицируют с тем, чтобы исключить РЧ импульс(ы), создающий(ие) когерентность (поперечное намагничивание) на целевых ядрах (например, 13C) в последовательности передачи поляризации. Применение РЧ импульса к целевым ядрам задерживают до тех пор, пока гиперполяризованная частица не достигнет целевого местоположения для МРТ-эксперимента или регистрации данных визуализации. Таким образом, поляризацию сохраняют вдоль оси намагничивания z, и на нее влияет только время продольной релаксации T1. Чтобы избежать асимметричных сигналов ЯМР, можно применять схемы периодического изменения фазы во время регистрации данных МРТ.
Гиперполяризация ядер целевого соединения имеет более длительное (продольное) время жизни (T1), чем таковая у ядер исходного соединения, с тем, чтобы было доступно больше времени между гиперполяризацией целевого соединения и введением пациенту, подлежащему исследованию, в качестве контрастного вещества.
Согласно одному аспекту изобретения, исходное соединение растворяют с высокой концентрацией в подходящем, нетоксичном растворителе для эффективной гиперполяризации посредством взаимодействия с пучком фотонов с ОУМ. Здесь квантовое число орбитального углового момента пучка фотонов с ОУМ можно выбирать для оптимизации передачи орбитального углового момента с фотонов на исходное соединение, содержащее спины с высоким гиромагнитным отношением. Поляризацию спина на исходном соединении передают посредством ЯМР-системы передачи поляризации на растворенное целевое соединение, которое может иметь низкое гиромагнитное отношение. Таким образом, можно гиперполяризовать большое количество растворителя или растворенного вещества, передать гиперполяризацию на меньшее количество растворенного вещества с тем, чтобы получить гиперполяризованное растворенное вещество, но с низкой концентрацией в растворителе с тем, чтобы не достигать токсичных концентраций. Затем гиперполяризованный раствор используют в качестве контрастного вещества. В смежном подходе соединение гиперполяризуют посредством взаимодействия с пучком фотонов с ОУМ при повышенной температуре, чтобы повысить максимальную концентрацию растворенного исходного соединения и/или целевого соединения при облучении пучком фотонов с ОУМ.
В еще одной другой реализации пучок фотонов с ОУМ сначала поляризует исходные ядра в соединении, и затем поляризацию передают на целевые ядра в том же соединении. В этом примере исходное соединение и целевое соединение совпадают.
В дополнительной реализации нет необходимости передавать гиперполяризацию, где соединение гиперполяризуют посредством взаимодействия с пучком фотонов с ОУМ при высокой концентрации и затем просто разводят в инертном растворенном веществе с тем, чтобы избежать превышения токсической концентрации.
В другом варианте осуществления изобретения камера представляет собой проточную кювету или плоскую кювету. Проточная кювета может функционировать в режиме непрерывного потока, в котором создают постоянное течение гиперполяризованного соединения. В другом примере в проточной кювете предусмотрен выпускной клапан на выпускном отверстии для управления гиперполяризованным соединением, которое нужно предоставлять дискретными порциями. Предпочтительно, также предусмотрен впускной клапан на впускном отверстии проточной кюветы, чтобы более точно управлять доставкой дискретных порций гиперполяризованного соединения. Например, проточная кювета может быть организована в виде так называемой лаборатории на чипе. Этот подход допускает радикальную миниатюризацию оборудования для распыления гиперполяризованных веществ. Лаборатория на чипе представляет собой концепцию, основанную на микроструйной технике, для манипуляции малыми количествами флюидов (от нанолитров 10-9 л до аттолитров 10-18 л) с использованием каналов размерами 10-100 мкм. Лабораторию на чипе можно применять с использованием очень малых количеств образцов и реактивов для осуществления анализа, для осуществления разделения и обнаружения с высоким разрешением и чувствительностью. Дополнительные подробности относительно лаборатории на чипе находятся в публикации «The origins and the future of microfluidics», G.M. Whitesides, Nature 442(2006)368-373. Интеграция гиперполяризации пучком фотонов с ОУМ и ЯМР-лаборатории на чипе допускает избирательное определение спектроскопических характеристик химических или биологических образцов с высокой чувствительностью.
После взаимодействия с пучком фотонов с ОУМ гиперполяризованное соединение можно вводить пациенту, подлежащему исследованию, используя способы, которые также используют в стандартной контрастной визуализации (компьютерная томография с контрастом, МРТ с контрастом). В одном из вариантов осуществления проточная кювета соединена с распыляющим блоком посредством клапанной системы, которой можно управлять для приведения в действие в порционном режиме или в режиме непрерывного потока. В порционном режиме болюс гиперполяризованного вещества вводят, например инъецируют, подобно стандартной процедуре контрастной МР-визуализации. Например, распыляющий блок соединен с выпускным отверстием проточной кюветы. Затем распыляющий блок, такой как насосная инъекционная или инфузионная система, вводит гиперполяризованное соединение в объект, например пациенту, подлежащему исследованию. Альтернативно, распыляющий блок может быть соединен с впускным отверстием проточной кюветы. Затем распыляющий блок доставляет соединение контролируемым образом в проточную кювету, где пучок фотонов с ОУМ создает гиперполяризацию, а затем гиперполяризованное соединение вводят пациенту, подлежащему исследованию.
В дополнительном примере предусмотрено несколько проточных кювет, работающих параллельно, для увеличения объемной скорости потока гиперполяризованного вещества.
Дополнительное преимущество настоящего изобретения состоит в том, что процесс гиперполяризации на основе пучка фотонов с ОУМ, особенно когда его применяют к соединению 13C, почти не чувствителен к положению специфического мечения ядер 13C в соединении 13C. Соответственно, этот аспект изобретения снимает ограничения с конкретных соединений, которые можно гиперполяризовать. Другими словами, настоящее изобретение не налагает ограничения на конкретные метаболически значимые соединения, которые можно метить гиперполяризованным ядром 13C. Примерами таких метаболически значимых соединений являются глюкоза, пируват, бикарбонат, лактат, глутамин, холин и т.д. Дополнительно, перед инъекцией можно гиперполяризовать лекарственные средства или искусственные вещества крови, такие как перфторуглероды и ПФОБ (перфтороктилбромид). Таким образом, настоящее изобретение делает возможным исследование посредством гиперполяризованной контрастной магнитно-резонансной визуализации широкого спектра метаболических и физиологических процессов.
Изобретение также относится к системе магнитно-резонансного исследования, в которой предусмотрен распылитель по изобретению. Согласно соответствующему аспекту, в системе магнитно-резонансного исследования и распылителе предусмотрено управление синхронизацией для синхронизации работы РЧ и градиентной системы в системе магнитно-резонансного исследования с работой подсистемы РЧ поляризатора распылителя. Синхронизация организована с тем, чтобы РЧ (B1) поле блока поляризатора активировать для возбуждения гиперполяризованных целевых ядер в распыляющем блоке, когда отсутствуют возбуждающие РЧ и импульс градиентного магнитного поля системы магнитно-резонансного исследования. Альтернативно, РЧ и/или градиентный экран, например из алюминия или меди, можно предусмотреть для защиты гиперполяризованных вторичных ядер от RF и/или градиентных магнитных полей системы магнитно-резонансного исследования.
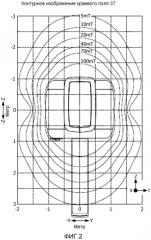
В дополнительном аспекте изобретения в распылителе применяют магнитное поле. Стоит отметить, что в этом аспекте изобретения путь передачи проходит через это магнитное поле из камеры, в которой имеется пучок фотонов с ОУМ, в (необязательную) систему передачи поляризации, в которой гиперполяризацию передают с исходного соединения на целевое соединение. Это направление магнитного поля является предпочтительным направлением поляризации, создаваемой пучком фотонов с ОУМ. Этого достигают, например, когда распылитель расположен в краевом поле основного магнита системы магнитно-резонансного исследования. Стоит отметить, что магнитное поле от 0,2 T до 0,5 T или даже 1,0 Т сохраняет созданную поляризацию, и его легко достичь в системе магнитно-резонансного исследования. Эти напряженности поля доступны в краевом поле основного магнита, как проиллюстрировано в примере на Фиг. 2. Магнитное поле в распылителе сохраняет гиперполяризацию, сохраняемую, когда гиперполяризованное соединение переносят из пучка фотонов с ОУМ. Для варианта осуществления, в котором последовательности импульсов ЯМР используют для передачи поляризации спина со спинов с высоким гиромагнитным отношением на спины с низким гиромагнитным отношением, использование небольших объемов полезно для того, чтобы избежать эффектов пространственной неоднородности магнитного поля в ЯМР-последовательности передачи поляризации. На практике пучок фотонов с ОУМ, например, имеет падающее пятно 20-50 мкм и вплоть до 1000 пятен можно использовать параллельно для достижения поляризации в отдельном местоположении в объеме приблизительно 10 см3. В таком небольшом объеме пространственные неоднородности магнитного поля не имеют значения и краевое поле основного магнита можно использовать для ЯМР-передачи поляризации после ОУМ-гиперполяризации. Альтернативно, в распылителе предусмотрена своя собственная магнитная система, которая создает магнитное поле в камере.
В дополнительном применении изобретения воду гиперполяризуют пучком фотонов с ОУМ с подходящими длинами оптических волн, например в ближнем красном спектре, и вводят, например инъецируют или вливают, в виде болюса. Обнаружение функции артериального ввода и количественное определение T1 позволяет количественно определять перфузию в ткани. Множественные инъекции болюсов можно использовать для улучшения отношения сигнала к ошибке (SNR), поскольку сигнал воды затухает с T1 или может быть разрушен последовательностями импульсов МРТ. Способ можно легко комбинировать с динамической контрастной МРТ (после инъекции гиперполяризованной воды), и таким образом можно получать комбинированные карты перфузии и проницаемости.
Инъектор используют для внутривенного введения изотонических физиологических растворов, которые гиперполяризованы на основе ОУМ-поляризации. Можно легко достигать объемную скорость потока 10 мл/с при подходящей степени поляризации (>20%). Первая реализация включает в себя: регистрацию динамического сканирования области, представляющей интерес, двухмерной или трехмерной, мониторинг прохождения болюса гиперполяризованной воды; использование последовательности трехмерного градиентного эха с малым углом отклонения вектора намагниченности для предотвращения быстрого затухания намагниченности; комбинацию со способами совместного использования профилей, подобно замочной скважине и VIPR, и реконструирование с использованием Compressed Sensing, чтобы сделать возможными четырехмерные изображения высокого разрешения. Опорные изображения(е) можно получать в двух моделях: несколько болюсов воды и регистрация времени относительно инъекции, чтобы обеспечить равные уровни сигналов, или полустационарная инъекция поляризованной воды.
Дополнительное применение этого способа допускает количественное определение функции ввода: использование отметок времени для инъектора и устройства визуализации, чтобы получить точную информацию о времени прибытия и рассеивании болюса.
Вторая реализация включает в себя способы вычитания, в частности, для визуализации перфузии, например:
1. Гиперполяризованная вода с намагниченностью вдоль B0 (положительный (усиленный) сигнал) против базового сигнала (МРТ теплового равновесия).
2. Гиперполяризованная вода с намагниченностью вдоль B0 (положительный усиленный сигнал) против намагниченности против B0 (отрицательный усиленный сигнал). Последнее возможно благодаря эффекту полярности способа ОУМ-поляризации. Типичные стратегии считывания включают в себя однократный EPI с порядком срезов, противоположным направлению потока.
Оба способа можно применять в режиме повторных болюсов («импульсный») или с использованием стационарной подачи поляризованной воды («непрерывный») подобно способам, используемым для артериального спинового мечения.
Типичное время переноса от руки в область, представляющую интерес (головной мозг, почки), составляет 6-12 секунд. Таким образом и предполагая T1=1,5 секунды, можно достичь уровня остаточного сигнала 3-10× намагничивания теплового равновесия (не поляризованного). Для исследований перфузии в головном мозге, используя инверсию (и вычитание) намагниченности теплового равновесия, измеряют разницы сигналов приблизительно в 1%, и необходимо множество средних, чтобы получить приемлемые уровни SNR (время сканирования 3-4 минуты). ОУМ-гиперполяризация допускает уменьшение времени сканирования приблизительно на 1 порядок величины, таким образом, снижая чувствительность к артефактам движения или позволяя увеличить SNR посредством дополнительного усреднения.
Подобно известным способам, таким как PULSAR (X. Golay et al. Magnetic Resonance in Medicine 2005, 53: 15-21), можно получать множество временных точек, чтобы сделать возможным количественное определение перфузии без модели. Регионарную перфузию можно оценивать посредством избирательного применения импульсов насыщения к питающим артериям.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Эти и другие аспекты изобретения будут объяснены со ссылкой на варианты осуществления, описанные далее в настоящем документе, и со ссылкой на сопроводительные чертежи, на которых:
на Фиг. 1 показано схематическое представление распылителя изобретения, совместно работающего с системой магнитно-резонансного исследования;
на Фиг. 2 показано графическое представление последовательностей импульсов, используемых в системе передачи поляризации в распылителе изобретения;
на Фиг. 3 показан пример модифицированной последовательности INEPT для передачи поляризации со спина I (например, 1H) на S (например, 13C).
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
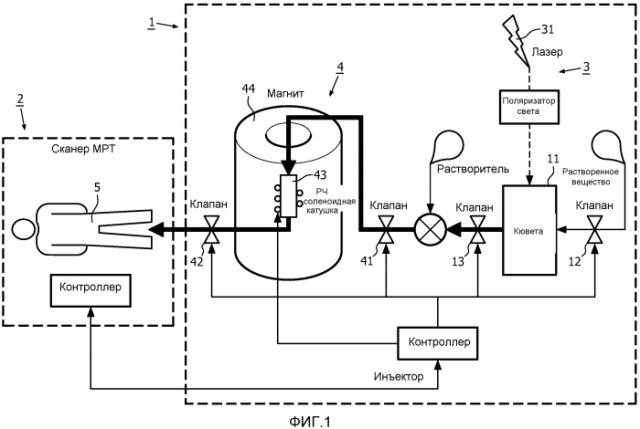
На Фиг. 1 показано схематическое представление распылителя 1 изобретения, совместно работающего с системой 2 магнитно-резонансного исследования. Камера 11 распылителя 1 сформирована в виде кюветы 11. Система 3 гиперполяризации фотонов содержит лазер 31 и поляризатор 33 света, который формирует пучок 32 фотонов, который имеет орбитальный угловой момент. Этот пучок фотонов с ОУМ направлен в кювету 11, которая содержит исходное соединение в форме растворенного вещества, с тем, чтобы сформировать в кювете гиперполяризованное исходное соединение. Затем это гиперполяризованное исходное соединение подают в систему 4 передачи поляризатора. В системе 4 передачи поляризатора гиперполяризацию растворенного вещества исходного соединения передают, например посредством передачи поляризации ядер, целевому соединению, которое добавляют в виде растворенного вещества в растворитель. Затем гиперполяризованный раствор с гиперполяризованным растворенным веществом целевого соединения подают в распыляющий блок (не показан) для введения пациенту 5, подлежащему исследованию. Вместо пациента-человека также можно исследовать животных, особенно грызунов. Система 4 передачи поляризации из данного примера оснащена своим собственным магнитом 44 для создания стационарного магнитного поля для сохранения ориентации спинов для гиперполяризованных молекул или ядер гиперполяризованного соединения после выключения поляризующего пучка фотонов с ОУМ или перемещения гиперполяризованного соединения за пределы области, в которой происходит взаимодействие с пучком фотонов с ОУМ. РЧ подсистема, содержащая РЧ соленоидную катушку 43, может генерировать РЧ электромагнитные поля для передачи поляризации с исходного соединения на целевое соединение или с исходных ядер на целевые ядра в том же соединении, например, с 1H на 13C в глюкозе.
Распылитель изобретения, как показано на Фиг. 1, оснащен несколькими клапанами 12, 13, 41, 42 для управления потоком соединений. Впускной клапан 12 кюветы управляет входным потоком растворенного вещества в кювету, где гиперполяризацию создают посредством взаимодействия с пучком фотонов с ОУМ. Выпускной клапан 13 кюветы управляет выходным потоком гиперполяризованного растворенного вещества в систему передачи поляризации. Система передачи поляризации также имеет впускной клапан 41 на своем впускном отверстии и выпускной клапан 42 на своем выпускном отверстии.
Система 2 магнитно-резонансного исследования имеет свой собственный МР-контроллер 21 для выполнения нескольких функций для работы системы магнитно-резонансного исследования, например, для управления наложением импульсов градиентов магнитных полей, РЧ возбуждением, инверсией или перефокусированием импульсов, т.е. выполнением регистрационных последовательностей. Также МР-контроллер управляет сбором магнитно-резонансных сигналов, передачей и обработкой этих магнитно-резонансных сигналов и реконструированием магнитно-резонансного изображения по сигналам. Распылитель 1 предоставлен с контроллером 14 поляризации, который управляет различными функциями распылителя 1. МР-контроллер 21 и контроллер 14 поляризации связаны с тем, чтобы обеспечить временную синхронизацию между системой 2 магнитно-резонансного исследования и распылителем 1 с тем, чтобы избежать помех, особенно со стороны РЧ поля системы 4 поляризации, в регистрационных последовательностях и считывании сигнала системы магнитно-резонансного исследования. Один вариант состоит в том, чтобы работа системы магнитно-резонансного исследования, управляемой МР-контроллером, также управляла распылителем. Альтернативно, контроллер поляризации можно использовать для запуска работы системы магнитно-резонансного исследования.
Система поляризации работает на основе способов передачи поляризации ядер, таких как модифицированный INEPT, см. Фиг. 3. Модификация заключается в мерах по сохранению поляризации целевого соединения, например в ядре 13C, вдоль продольной оси, т.е. вдоль направления магнитного поля в камере. Только при применении в качестве контрастного вещества в системе магнитно-резонансного исследования гиперполяризованное ядро переключается на поперечный компонент. Модифицированная последовательность INEPT, для которой первый пример последовательности импульсов показан на чертеже Фиг. 3, использует намагничивание ядра с высоким гиромагнитным отношением, например, 1H, 19F или 31P, чтобы усилить слабые магнитно-резонансные сигналы ядра с низким гиромагнитным отношением, например 31C, 15N, 17O. Ядерный спин исходного соединения, который имеет высокое гиромагнитное отношение (например, 1H), ориентирован вдоль оси z и затем поворачивается на 90° вокруг оси x, таким образом, создавая поперечное намагничивание исходного соединения. Посредством непрямого диполь-дипольного взаимодействия между ядром с высоким гиромагнитным отношением исходного соединения и ядром с низким гиромагнитным отношением целевого соединения намагничивание передают с этого соединения на целевое соединение. Эту передачу усиливают посредством модифицированной последовательности INEPT. После начального возбуждения посредством 90× импульса, спиновую систему оставляют формироваться в течение интервала свободной прецессии τ, равного J/4, а затем ядерные спины этого соединения и целевого соединения перефокусируют посредством 180× импульсов, которые сохраняют перефокусированное намагничивание целевого соединения вдоль оси z. В альтернативной модифицированной последовательности импульсов INEPT применяют повторные восстанавливающие импульсы, возбуждающие намагничивание, как исходного соединения, так и целевого соединения в возбужденном равновесном состоянии.
1. Распылитель для получения контрастного вещества с гиперполяризованными ядрами, причем распылитель содержит:камеру для приема соединения;систему гиперполяризации фотонов, выполненную с возможностью создавать пучок фотонов с орбитальным угловым моментом (ОУМ) и направлять пучок фотонов с ОУМ в камеру для создания гиперполяризации ядер в соединении; имагнит для создания магнитного поля в камере;при этом камера имеет выход, через который можно выпускать гиперполяризованное соединение.
2. Распылитель по п.1, содержащий:систему передачи поляризации, выполненную с возможностью:принимать соединение, в котором была создана гиперполяризация ядер в камере, в качестве гиперполяризованного исходного соединения из камеры,принимать целевое соединение ипередавать гиперполяризацию с исходного соединения на целевое соединение.
3. Распылитель по п.1 или 2, в котором камера представляет собой проточную кювету для прохождения флюида.
4. Распылитель по п.1 или 2, в котором камера представляет собой плоскую кювету.
5. Распылитель по п.3, в котором проточная кювета имеет впускное отверстие с впускным клапаном и/или выпускное отверстие с выпускным клапаном.
6. Система магнитно-резонансного исследования, содержащая:основной магнит для создания статического магнитного поля;РЧ систему для создания РЧ импульсов;градиентную систему для получения импульсов градиента магнитного поля;при этом система магнитно-резонансного исследования дополнительно содержит:распылитель по п.2, в котором система передачи поляризации содержит подсистему РЧ поляризатора для создания РЧ электромагнитных полей для передачи поляризации иустройство управления синхронизацией для синхронизации работы подсистемы РЧ поляризатора с градиентной системой и РЧ системой.
7. Система магнитно-резонансного исследования по п.6, содержащая распылитель по п.5, при этом камера распылителя расположена в основном магнитном поле или в магнитном поле рассеяния основного магнита.
8. Система магнитно-резонансного исследования по п.6, снабженная градиентным экраном, расположенным между градиентной системой и распылителем.