Внутрикамерные имплантаты с пролонгированным высвобождением терапевтического агента
Иллюстрации
Показать всеИзобретение относится к медицине, а именно офтальмологии, и может быть использовано для лечения повышенного внутриглазного давления. Для этого в переднюю камеру глаза при помощи аппликатора имплантируют по меньшей мере два биоразлагаемых внутрикамерных имплантатата с пролонгированным высвобождением, каждый из которых содержит по меньшей мере один простамид, при этом каждый из указанных по меньшей мере двух биоразлагаемых имплантатов с пролонгированным высвобождением высвобождает от 100 нг в день до 900 нг в день по меньшей мере одного указанного простамида в течение жизни имплантата, причем каждый из указанных по меньшей мере двух биоразлагаемых имплантатов с пролонгированным высвобождением содержит 5-40% по меньшей мере один простамид, 10-60% R203S, который является поли(D,L-лактидом), обладающим собственной вязкостью 0,25-0,35 дл/г, 5-20% R202H, который является поли(D,L-лактидом), обладающим собственной вязкостью 0,16-0,24 дл/г, 5-40% RG752S, который является поли(D,L-лактид-ко-гликолидом), имеющим молярное соотношение D,L-лактид:гликолид от 73:27 до 77:23 и собственную вязкость 0,16-0,24 дл/г, и 5-15% полиэтиленгликоля (ПЭГ) 3350. Способ позволяет повысить эффективность лечения повышенного внутриглазного давления за счет инъекции имплантов в переднюю часть стекловидного тела через плоскую часть ресничного тела при эффективном обходе транссклеральных барьеров. 4 з.п. ф-лы, 3 табл., 2 пр., 6 ил.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Данная заявка претендует на приоритет предварительной заявки на патент США Номер 61/297,660, поданной 22 января 2010 года, полное раскрытие каждой из которых полностью включено в настоящий документ посредством ссылки.
Область техники
[0002] Настоящее изобретение относится к внутрикамерным имплантатам с пролонгированным высвобождением и способам их изготовления и использования.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0003] Здесь описаны внутриглазные системы и способы лечения заболеваний глаз. В частности, описывается местное введение системы доставки с пролонгированным высвобождением терапевтического агента в переднюю камеру и/или в передней камере стекловидного тела глаза для лечения повышенного внутриглазного давления в передней камере глаза.
[0004] Далее здесь описываются способы лечения глазных заболеваний, включающие следующие этапы: обеспечение, по меньшей мере, двумя биоразлагаемыми имплантатами с пролонгированным высвобождением, содержащими, по меньшей мере, один терапевтический агент; имплантация, по меньшей мере, двух биоразлагаемых имплантатов с пролонгированным высвобождением в переднюю камеру глаза; и лечение заболевания глаз, где, по меньшей мере, два биоразлагаемых имплантата с пролонгированным высвобождением высвобождают, приблизительно, 100 нг в день, по меньшей мере, одного биоактивного агента в течение, приблизительно, более 1 месяца.
[0005] Более того, здесь описываются способы лечения глаукомы в глазу, включающие следующие этапы: обеспечение, по меньшей мере, двумя биоразлагаемыми имплантатами с пролонгированным высвобождением, содержащими, по меньшей мере, один терапевтический агент; имплантация, по меньшей мере, двух биоразлагаемых имплантатов с пролонгированным высвобождением в переднюю камеру глаза; обеспечение достаточного времени для устанавливания в нижнем углу, по меньшей мере, двух биоразлагаемых имплантатов с пролонгированным высвобождением; обеспечение достаточного времени для высвобождения, по крайней мере, двумя биоразлагаемыми имплантатами с пролонгированным высвобождением, по меньшей мере, одного терапевтического агента; и лечении глаукомы, где, по меньшей мере, два биоразлагаемых имплантата с пролонгированным высвобождением высвобождают, приблизительно, 100 нг в день, по меньшей мере, одного биоактивного агента в течение, приблизительно, более 1 месяца.
[0006] В одном варианте воплощения заболеванием глаз является глаукома и/или повышенное внутриглазное давление. Имплантаты с пролонгированным высвобождением могут высвобождать, приблизительно, 70%, по меньшей мере, одного терапевтического агента в течение первого месяца. В некоторых вариантах воплощения, по меньшей мере, один терапевтический агент может составлять, приблизительно, 30%, по меньшей мере, двух биоразлагаемых имплантатов с пролонгированным высвобождением, и он отбирается из группы, состоящей из латанопроста, биматопроста и травопроста, а также их солей, эфиров и неактивных форм лекарств.
[0007] В другом варианте воплощения, по меньшей мере, два имплантата с пролонгированным высвобождением содержат, приблизительно, от 5% до, приблизительно, 70% поли(DL-лактида). В других вариантах воплощения, по меньшей мере, два имплантата с пролонгированным высвобождением содержат, приблизительно, от 5% до, приблизительно, 40% поли(DL-лактида-ко-гликолида). В других, помимо этого, вариантах воплощениях, по меньшей мере, два имплантата с пролонгированным высвобождением содержат, приблизительно, от 5% до, приблизительно, 40% полиэтилен гликоля.
[0008] Кроме этого, в других вариантах воплощениях, по меньшей мере, два имплантата с пролонгированным высвобождением содержат, приблизительно, 30% терапевтического агента, 65% поли(D,L-лактида) и 5% полиэтилен гликоля или, приблизительно, 20% терапевтического агента, 55% поли(D,L-лактида), 10% поли(DL-лактида-ко-гликолида) и 5% полиэтилен гликоля.
[0009] Сами имплантаты могут быть введены в ткань глаза с использованием соответствующего аппликатора. После имплантации, по меньшей мере, два имплантата с пролонгированным высвобождением могут установиться в нижнем углу в течение 24 часов после имплантации в переднюю камеру.
[0010] В одном варианте воплощения время, достаточное для высвобождения, по меньшей мере, двумя имплантатами, по меньшей мере, одного терапевтического агента, более, приблизительно, 42 дней.
КРАТКОЕ ОПИСАНИЕ ФИГУР
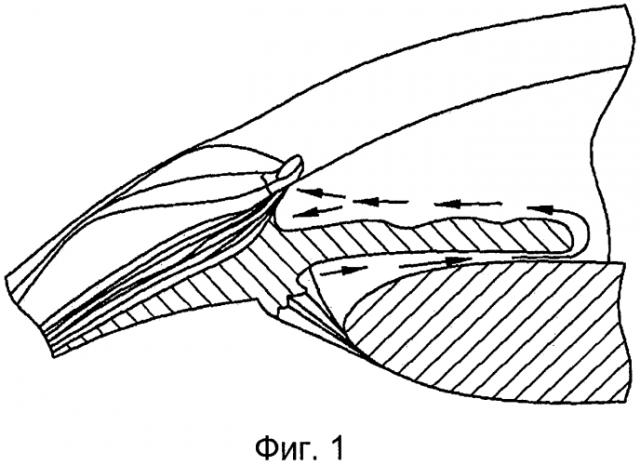
[0011] Фигура 1 иллюстрирует два различных пути оттока внутриглазной жидкости из передней камеры глаза, оба они расположены в иридокорнеальном углу.
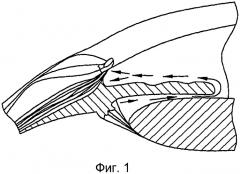
[0012] Фигура 2 иллюстрирует помещение имплантата, как было здесь описано, в месте оттока внутриглазной жидкости из передней камеры.
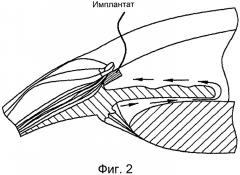
[0013] Фигура 3 иллюстрирует потоки, распложенные в передней камере глаза, наряду с возможным расположением имплантата или имплантатов, как здесь описано.
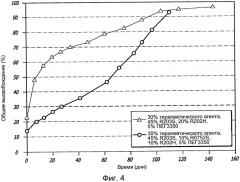
[0014] Фигура 4 графически иллюстрирует профиль высвобождения у имплантатов в настоящем описании.
[0015] Фигура 5 графически иллюстрирует профиль высвобождения у имплантатов в настоящем описании.
[0016] Фигура 6 иллюстрирует помещение имплантата в соответствии с настоящим описанием.
Определение терминов
[0017] "Приблизительно" означает плюс или минус десять процентов от числа, параметра или характеристики, определенных таким образом.
[0018] "Биоразлагаемый полимер" означает полимер или полимеры, которые разлагаются in vivo, и где со временем происходит эрозия полимера или полимеров, происходящая одновременно или последовательно с высвобождением терапевтического агента. Использованные здесь термины "биоразлагаемый" и "биоразрушаемый" взаимозаменяемы. Биоразлагаемый полимер может быть гомополимером, сополимером или полимером, содержащим более двух различных полимерных единиц. Полимер может быть типа гелевого или гидрогелевого полимера, полимером молочной кислоты или сополимером молочной и гликолевой кислот, полимером полиэтилен гликоля или смесью их производных.
[0019] "Заболевание глаз" означает заболевание, нездоровье или состояние, которое поражает или затрагивает область глаза. В наиболее широком смысле, глаз включает в себя глазное яблоко и ткани, и жидкости, которые входят в состав глаза, окологлазные мышцы (такие, как косая и прямая мышцы) и часть глазного нерва в составе глазного яблока или прилегающую к нему.
[0020] Заболевание передней части глаза - это заболевание, нездоровье или состояние, которое поражает или затрагивает переднюю сторону (то есть переднюю часть глаза) глазной области или участок, такой, как окологлазная мышца, веко или ткань глазного яблока, или жидкость, которые расположены спереди от задней стенки капсулы хрусталика или ресничной мышцы. Таким образом, заболевание передней части глаза поражает или затрагивает конъюнктиву, роговицу, переднюю камеру, радужку, заднюю камеру (за сетчаткой, но перед задней стенкой капсулы хрусталика), хрусталик или капсулу хрусталика и кровеносные сосуды, и нервы, снабжающие кровью или иннервирующие область или участок глаза.
[0021] Таким образом, заболевание передней части глаза может включать заболевание, нездоровье или состояние, такое как, например, афакия, псевдофакия, астигматизм, блефароспазм, катаракта, заболевания конъюнктивы; конъюнктивит; заболевания роговицы; язву роговицы; синдромы сухого глаза; заболевания века; заболевания слезного аппарата; закупорка слезного протока; миопия; пресбиопия; нарушения зрачка; нарушения рефракции и страбизм. Глаукома также может считаться заболеванием передней части глаза, так как клинической целью лечения глаукомы может явиться снижение повышенного давления внутриглазной жидкости в передней камере глаза (то есть снижение внутриглазного давления).
[0022] Заболевание задней части глаза - это заболевание, нездоровье или состояние, которое первоначально поражает или включает заднюю часть глаза или участок, такой, как сосудистая оболочка глаза или склера (в положении позади плоскости, проходящей через заднюю стенку капсулы хрусталика), стекловидное тело, камеру стекловидного тела, сетчатую оболочку, зрительный нерв (то есть диск зрительного нерва) и кровеносные сосуды и нервы, которые снабжают кровью или иннервируют заднюю область или участок глаза.
[0023] Таким образом, заболевание задней части глаза может включать заболевание, нездоровье или состояние, такое как, например, острая макулярная нейроретинопатия, Болезнь Бехчета, неоваскуляризация хороидеи, диабетический увеит, гистоплазмоз, инфекции, такие как грибковые или вирус-индуцированные; макулярная дегенерация, такая как острая макулярная дегенерация, не-экссудативная возрастная макулярная дегенерация и экссудативная возрастная макулярная дегенерация; отек, такой как макулярный отек, цистоидный макулярный отек и диабетический макулярный отек; мультифокальный хороидит; травма глаза, поражающая задний участок глаза или область; глазные опухоли; нарушения сетчатки, такие как окклюзия центральной вены сетчатки, диабетическая ретинопатия (включая пролиферативную диабетическую ретинопатию), пролиферативная витроретинопатия (ПВР), окклюзивное заболевание ретинальной артерии, отслоение сетчатки, воспаление сосудистой оболочки сетчатки; симпатическая офтальмия; синдром Фогта-Коянаги-Харада (ФКХ); увеальная диффузия; состояние задней части глаза, вызванное или связанное с лазерной терапией глаза; состояние задней части глаза, вызванное или связанное с фотодинамической терапией, фотокоагуляцией, радиационной ретинопатией, расстройства эпиретинальных мембран, закупорка боковой ретинальной вены, передняя ишемическая нейропатия глазного нерва, диабетическая ретинальная дисфункция неретинопатического происхождения; пигментная дистрофия сетчатки и глаукома. Глаукома может рассматриваться как заболевание задней части глаза, так как целью лечения является предотвращение или снижение случаев потери зрения из-за повреждения или утраты клеток сетчатки или клеток зрительного нерва (то есть нейропротекторное действие).
[0024] "Область глаза" или "участок глаза" означает любую зону глазного яблока, включая передние и задние сегменты глаза, и которые, в основном, включают любые функциональные (например, для зрения) или структурные ткани, обнаруживаемые в глазном яблоке, или тканях, или в клеточных слоях, которые полностью или частично выстилают внутреннюю или наружную часть глазного яблока, но не ограничиваются этим. Индивидуальные примеры зон глазного яблока включают переднюю (глазную) камеру, заднюю камеру, полость стекловидного тела, сосудистую оболочку глаза, супрахороидальное пространство, конъюнктиву, субконъюнктивальное пространство, эписклеральное пространство, интракорнеальное пространство, эпикорнеальное пространство, склеру, плоскую часть ресничного тела, аваскулярные участки, образовавшиеся в результате операции, макулу и сетчатку.
[0025] "Пролонгированное высвобождение" или "контролируемое высвобождение" относится к высвобождению, по меньшей мере, одного терапевтического биоактивного агента или препарата из имплантата с заранее предопределенной скоростью. Пролонгированное высвобождение предполагает, что терапевтический биоактивный агент не высвобождается из имплантата спорадично, непредсказуемым способом, и не «прорывается» из имплантата при контакте с биологическим окружением (что также здесь называется кинетикой первого порядка), кроме тех случаев, когда это намеревались произвести специально. Однако термин «пролонгированное высвобождение», используемый здесь, не исключает «прорывного явления», связанного с выпуском агента. В некоторых примерных вариантах воплощения согласно настоящему описанию может быть желателен первоначальный прорыв, по меньшей мере, одного терапевтического агента, сопровождающийся впоследствии более постепенным высвобождением. Скорость высвобождения может быть постоянной (в большинстве случаев называется «рассчитанное по времени высвобождение» или кинетика нулевого порядка), так что, по меньшей мере, один терапевтический агент высвобождается в равных количествах в течение предопределенного времени (с начальной прорывной фазой или без нее), или может происходить равномерное высвобождение. Например, у пролонгированного высвобождения могут, в основном, отсутствовать колебания при доставке терапевтического агента по сравнению с топическим введением.
[0026] "Терапевтически эффективное количество" означает уровень или количество агента, необходимое для лечения состояния глаз или для снижения, или предотвращения повреждения или нарушения глаза без индукции значительных негативных или нежелательных побочных эффектов для глаза, или для глазной зоны. С учетом вышеизложенного, терапевтически эффективное количество терапевтического агента, такого, как латанопрост, - это количество, эффективное для снижения, по меньшей мере, одного симптома глазного заболевания.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0027] Здесь описываются внутрикамерные имплантаты, включающие, по меньшей мере, один терапевтический агент. Описанные здесь имплантаты размещаются в передней камере глаза, однако они не закреплены в ткани глаза. В большей мере, имплантаты удерживаются на месте потоками и силой тяжести, присутствующими в передней камере глаза. Имплантаты предпочтительно имеют полимерную природу, они биоразлагаемые и обеспечивают высвобождение, по меньшей мере, одного терапевтического агента как в трабекулярную сеть (ТС), так и в связанные с ней ткани глаза и жидкости в передней камере глаза, куда помещается имплантат.
[0028] Прямое введение в камеру или в переднюю часть стекловидного тела имплантатов с пролонгированным высвобождением или систем доставки терапевтического агента, как здесь изложено, эффективно для лечения ряда указанных здесь глазных заболеваний. В таких состояниях глаукома характеризуется повышенным внутриглазным давлением, которое можно лечить описанным здесь способом путем обхода сложных склеральных механизмов выведения лекарственных веществ (например, топических капель).
[0029] Изменение внутриглазного давления (ВГД) является независимым фактором риска глаукоматозного повреждения. Традиционнее лечение повышенного глазного давления или глаукомы состоит в применении анти-гипертензивных топических глазных капель для снижения ВГД. К сожалению, болюсное дозирование топическими глазными каплями приводит к пиковым и минимальным значениям уровней терапевтического агента в передней камере, что приводит к вариабельности контролирования ВГД во времени. Это колебание ВГД может приводить к прогрессированию глаукоматозного поля, особенно у пациентов с развитой глаукомой. Описываемые здесь внутрикамерные имплантаты с пролонгированным высвобождением предназначены для обеспечения этой неудовлетворенной потребности пациентов с повышенным внутриглазным давлением, требующим медицинского лечения. Данные имплантаты могут обеспечивать низкие колебания ВГД в течение дня и ночи, когда применение топических капель не представляется удобным. Ночной пик ВГД происходит между 23 часами ночи и 6 часами утра у пациентов с открытоугольной глаукомой, и это может способствовать прогрессирующей потере поля зрения у некоторых пациентов. Дополнительным ограничением топической терапии является отсутствие равновесных концентраций препарата в передней камере глаза при болюсным дозировании, которое не контролирует ночные повышения ВГД у ряда пациентов. Описываемые здесь имплантаты устанавливают низкие колебания ВГД также в течение ночи, тем самым смягчая осложнения топического введения в ночные часы.
[0030] Несоблюдение медицинского режима, включающего одни топические глазные капли или более для лечения повышенного глазного давления, происходит у более 50% пациентов, и это может иметь отношение к колебаниям ВГД в течение дня, когда капли не используются в соответствии с регулярным расписанием. Описываемые здесь имплантаты не требуют такого соблюдения, и поэтому они более благоприятны для пациентов.
[0031] Здесь описываются внутрикамерные имплантаты с пролонгированным высвобождением терапевтического агента, которые обеспечивают постоянное высвобождение терапевтического агента, тем самым избегая пиковых и минимальных уровней терапевтического агента, которые имеют место во внутриглазной жидкости при топическом дозировании. Равновесные концентрации препарата, достигаемые во внутриглазной жидкости с описываемыми здесь имплантатами, могут значительно снизить колебания ВГД в течение дня и ночи, в отличие от традиционного топического введения препаратов.
[0032] Передняя и задняя камеры глаза наполнены внутриглазной жидкостью, жидкость постоянно выделяется ресничным телом и имеет ионный состав, подобный составу крови. Внутриглазная жидкость имеет двойную функцию: 1) снабжение питательными веществами аваскулярных структур глаза, таких как хрусталик и роговица, 2) поддерживает ВГД в физиологическом диапазоне. Поддержание ВГД и снабжение питательными веществами переднего сегмента являются определяющими факторами для поддержания нормальной остроты зрения.
[0033] Внутриглазная жидкость, в основном, выделяется в заднюю камеру глаза при помощи мерцательных процессов ресничного тела и путем второстепенного механизма образования внутриглазной жидкости через ультрафильтрацию из артериальной крови (Фигура 1). Внутриглазная жидкость затем достигает передней камеры, пересекая зрачок, и здесь существуют конвекционные потоки, где течение жидкости, прилегающей к радужной оболочке, направлено вверх, а течение жидкости, прилегающей в роговице, направлено вниз (Фигура 2).
[0034] Существуют два различных пути оттока внутриглазной жидкости, оба они расположены в иридокорнеальном углу глаза (Фигура 1). Увеосклеральный или нетрадиционный путь относится к оттоку внутриглазной жидкости из передней камеры путем диффузии через межклеточные пространства между волокнами цилиарных мышц. Хотя это представляется второстепенным путем оттока у человека, увеосклеральный или нетрадиционный путь является мишенью специфических анти-гипертензивных препаратов, таких как гипотензивные липиды, увеличивающие функциональность данного пути путем ре-моделирования внеклеточного матрикса.
[0035] Внутриглазная жидкость дренирует пространство в 360 градусов в трабекулярную сеть, которая первоначально имеет у человека поры диаметром от 10 до менее 30 микрон. Внутриглазная жидкость просачивается через канал Шлема и выходит из глаза через 25-30 коллекторных каналов в водянистые вены и, в конечном счете, в эписклеральные сосуды и вены глазницы (см. Фигуру 3). Фигура 3 представляет собой схему, где стрелками обозначены конвекционные течения внутриглазной жидкости в передней камере глаза. Имплантат, который, как здесь описывается, высвобождает, по меньшей мере, один терапевтический агент, показан расположенным ниже. Свободные терапевтические агенты, элиюруемые из имплантата, вливаются в конвекционные потоки внутриглазной жидкости (стрелки). Затем терапевтические агенты рассеиваются по передней камере и поступают в таргетную ткань, такую как трабекулярная сеть и участок ресничного тела, через зону корня радужки.
[0036] Преимущество внутрикамерного впрыскивания и размещения описываемого здесь биоразлагаемого имплантата состоит в том, что передняя камера является иммунологически привилегированным местом в организме и менее склонна реагировать на чужеродный материал, такой как полимерные системы доставки терапевтического агента. Это не относится к субтенонову пространству, где широко распространены воспалительные реакции на чужеродные материалы. В дополнение к передней камере, содержащей иммунорегуляторные факторы, которые обеспечивают иммунологическую привилегированность, частицы с диаметром более 30 микрон являются менее иммуногенными и имеют меньшую склонность вызывать воспаление глаза. Оседлые макрофаги глаза являются первой линией защиты от чужеродных тел или инфекционных агентов; однако им трудно фагоцитировать частицы размером более 30 микрон. Поэтому частицы размером более 30 микрон менее склонны активировать макрофаги и запускать последующий каскад воспалительных реакций. Это снижение воспалительного ответа для пациента является преимуществом.
[0037] Эффективность доставки терапевтических агентов или препаратов во внутриглазную жидкость с полимерными системами высвобождения намного выше с внутрикамерным расположением по сравнению с использованием субтенонова пространства. Так, менее 1% терапевтического агента, доставленного в субтеноново пространство, попадет во внутриглазную жидкость, в то время как 100% препарата, который высвободился внутри камеры, попадет во внутриглазную жидкость. Поэтому для внутрикамерных систем доставки требуются более низкие нагрузки терапевтическими агентами по сравнению с использованием субтенонова пространства.
[0038] Как таковая, при этом будет иметь место более низкая экспозиция конъюнктивы к терапевтическим агентами, и в результате, меньшая склонность к развитию гиперемии конъюнктивы при доставке топических терапевтических агентов, таких, как простагландины и протамины. Наконец, после внутрикамерной имплантации терапевтический(-ие) агент(-ы) напрямую через водянистые вены попадут в конъюнктивальный/эписклеральный кровеносный сосуд. Это минимизирует гиперемию конъюнктивы с, например, аналогами простагландина по сравнению с введением в субтеноново пространство, где многочисленные сосуды подвержены риску расширения из-за наличия высоких концентраций терапевтического агента, диффузно распространившегося по экстраваскулярному пространству конъюнктивы. Прямая внутрикамерная имплантация также устраняет потребность в консервантах, которые, при использовании в топических каплях, могут раздражать поверхность глаза.
[0039] Описываемые здесь имплантаты изготовлены из полимерного материала для обеспечения максимального прилегания имплантата к иридокорнеальному углу. В дополнение, размер имплантата, который находится в диапазоне диаметра, ширины и поперечного среза от, приблизительно, 0,1 мм до, приблизительно, 1 мм, и диапазоне длины от, приблизительно, 0,1 мм до, приблизительно, 6 мм, обеспечивает введение имплантата в переднюю камеру путем использования аппликатора с иглой малого размера, находящегося в диапазоне от, приблизительно, 22G до, приблизительно, 30G.
[0040] Полимерный материал, использованный для формирования описанных здесь имплантатов, может быть любой комбинацией полимолочной кислоты, гликолевой кислоты и/или полиэтилен гликоля, что со временем обеспечивает пролонгированное высвобождение терапевтического агента в систему оттока в глазу. Для снижения ВГД также могут внутрикамерно использоваться системы доставки с пролонгированным высвобождением терапевтического агента, основанные на других полимерных системах.
[0041] Описываемые здесь внутрикамерные имплантаты могут высвобождать загруженные терапевтические агенты в течение различных периодов времени. Эти имплантаты, введенные внутрь камеры, или в переднюю часть стекловидного тела, обеспечивают терапевтические уровни, по меньшей мере, одного терапевтического агента в течение длительных периодов времени. Длительными периодами времени могут быть, приблизительно, 1 неделя, приблизительно, 6 недель, приблизительно, 6 месяцев, приблизительно, 1 год или более.
[0042] Подходящие полимерные материалы или составы для использования в имплантатах включают те материалы, которые обладают совместимостью, обладают биосовместимостью с глазом, так, что они не вызывают значительной помехи для функционирования или для физиологии глаза. Такие материалы, предпочтительно, по меньшей мере, частично, и что более предпочтительно, в значительной степени, подвергаются биоразложению или биоразрушению.
[0043] В одном варианте воплощения примеры пригодных материалов включают, без ограничения, такие материалы, получаемые из органических сложных и простых эфиров, и/или включающие органические сложные и простые эфиры, которые при разложении дают физиологически приемлемые продукты разложения, включая мономеры. Полимерные материалы, полученные из ангидридов, амидов, ортоэфиров и тому подобных, и/или включающие их самих по себе или в комбинации с другими мономерами, также могут найти применение. Полимерными материалами могут быть ступенчатополимеризованные или конденсационные полимеры, предпочтительнее, конденсационные полимеры. Полимерные материалы могут быть поперечно-сшитыми и не поперечно-сшитыми, например, не более, чем слегка поперечно-сшитыми, так, например менее чем приблизительно 5% или менее чем приблизительно 1% поперечно-сшитого полимерного материала. В большинстве случаев, кроме углерода и водорода, полимеры будут включать, по меньшей мере, один кислород и азот, предпочтительнее, кислород. Кислород может быть представлен в форме окси-, например, гидрокси- или эфира, карбонила, например, нон-оксо-карбонил, такой как эфир карбоновой кислоты, и тому подобные. Азот может присутствовать как амидо-, циано- и амино-.
[0044] В одном варианте воплощения для использования в имплантатах пригодны полимеры гидрокси-алифатических карбоновых кислот, гомополимеры или сополимеры, и полисахариды. Полиэфиры могут включать полимеры D-молочной кислоты, L-молочной кислоты, рацемической молочной кислоты, гликолевой кислоты, поликапролактона и их комбинации. В основном, с использованием D-лактата и L-лактата, достигается медленное разрушение полимера или полимерного материала, в то время как разрушение значительно ускоряется с добавление лактата рацемата. Пригодные полисахариды и полиэфиры могут включать без ограничений полиэтилен гликоль (ПЭГ), кальция альгинат и замещенные целлюлозы, в частности, например, эфиры карбоксиметил целлюлозы, характеризующиеся нерастворимостью в воде и имеющие молекулярный вес от, приблизительно, 5кД до, приблизительно, 500 кД.
[0045] Другие представляющие интерес полимеры включают, без ограничений, поливиниловый спирт, полиэфиры и их комбинации, которые являются биосовместимыми и могут подвергаться биоразрушению и/или биоразложению. Некоторые предпочтительные характеристики полимеров или полимерных материалов могут включать биосовместимость, совместимость с избранным терапевтическим агентом, легкость в использовании полимера при изготовлении описываемой здесь системы доставки терапевтического агента, желательный полупериод распада в физиологической среде и нерастворимость в воде.
[0046] В одном варианте воплощения внутрикамерный имплантат в соответствии с настоящим описанием, имеет состав из 30% терапевтического агента, 45% R203S поли(D,L-лактида), 20% R202H поли(D,L-лактида) и 5% ПЭГ 3350. В другом варианте воплощения состав состоит из 20% терапевтического агента, 45% R203S поли(D,L-лактида), 10% R202H поли(D,L-лактида), 20% RG752S поли(DL-лактид-ко-гликолида), и 5% ПЭГ 3350. Диапазоны концентраций составных частей, которые могут быть использованы, составляют от, приблизительно, 5% до, приблизительно, 40% терапевтического агента, от, приблизительно, 10% до, приблизительно, 60% R203S, от, приблизительно, 5% до, приблизительно, 20% R202H, от, приблизительно, 5% до, приблизительно, 40% RG752S и от, приблизительно, 0 до, приблизительно, 15% ПЭГ 3350. Для регулирования скорости высвобождения терапевтического агента отдельные полимеры могут быть исключены и другие типы могут быть добавлены. Использованные полимеры являются коммерчески доступными.
[0047] Полимеры, используемые для формирования имплантата, имеют свои независимые свойства с тем, чтобы в комбинации придавать свойства, необходимые для пролонгированного высвобождения, по меньшей мере, одного терапевтического агента после имплантации. Например, R203S поли(D,L-лактид) обладает собственной вязкостью, или его средняя вязкость составляет, от, приблизительно, 0,25 до, приблизительно, 0,35 дл/г, в то время, как R202H поли(D,L-лактид) обладает меньшей собственной вязкостью, составляющей от, приблизительно, 0,16 до, приблизительно, 0,24 дл/г. Как таковая, описанная здесь полимерная композиция может иметь смесь поли(D,L-лактида) с более низким и более высоким молекулярным весом. Подобным образом, RG752S поли(DL-лактид-ко-гликолид) имеет молекулярное соотношение D,L-лактид : гликолид, от, приблизительно, 73:27 до, приблизительно, 77:23 и собственную вязкость от, приблизительно, 0,16 до, приблизительно, 0,24 дл/г. Используемый здесь полиэтилен гликоль может иметь молекулярный вес, например от, приблизительно, 3000 до, приблизительно, 3500 г/моль, предпочтительно, приблизительно, 3350 г/моль. Полимеры, имеющие различную собственную вязкость и/или молекулярный вес, могут быть скомбинированы для получения полимерной композиции, подходящей для пролонгированного высвобождения определенного терапевтического агента или агентов.
[0048] Биоразлагаемые полимерные материалы, которые включаются для формирования полимерной матрицы имплантата, предпочтительно подвержены нестабильности, связанной с энзиматическим или гидролизным разложением. Водорастворимые полимеры могут быть поперечно-связанными гидролизируемыми или биоразлагаемыми поперечными связями для обеспечения пригодными водо-нерастворимыми полимерами. Уровень стабильности может широко варьировать, в зависимости от выбора мономера, использования гомополимера или сополимера, от применения смесей полимеров и от того, включает ли полимер концевые кислотные группы.
[0049] Одинаково важно контролировать биоразложение полимера и поэтому профиль длительного высвобождения имплантата зависит от среднего молекулярного веса полимерной композиции, использованной в имплантатах. Для модуляции профиля высвобождения, по меньшей мере, одного терапевтического агента, могут быть использованы различные молекулярные веса одного и того же компонента, а также могут быть включены различные полимерные составы.
[0050] Описываемые здесь имплантаты могут быть цельными, то есть несущими, по меньшей мере, один терапевтический агент, равномерно распределенный по полимерному матриксу, или инкапсулированными, когда резервуар с терапевтическим агентом окружен капсулой из полимерного матрикса. Вдобавок, терапевтический агент может быть распределен не-гомогенным образом по матриксу. Например, имплантаты могут включать в себя часть, имеющую большую концентрацию терапевтического агента по сравнению со второй частью имплантата, которая может иметь меньшую концентрацию.
[0051] Общий вес имплантата зависит от объема внешней камеры и от активности и растворимости терапевтического агента. Зачастую, доза терапевтического агента составляет, в основном, от приблизительно, 0,1 мг до, приблизительно, 200 мг имплантата на дозу. Например, имплантат может весить, приблизительно, 1 мг, приблизительно, 3 мг, приблизительно, 5 мг, приблизительно, 8 мг, приблизительно, 10 мг, приблизительно, 100 мг, приблизительно, 150 мг, приблизительно, 175 мг или, приблизительно, 200 мг, включая помещенный внутрь терапевтический агент.
[0052] Нагруженный терапевтический агент, связанный с имплантатом, будет обладать ассоциированным с ним свойством или профилем пролонгированного высвобождения. Например, в течение первых 30 дней после имплантации описываемые здесь имплантаты могут высвобождать, от приблизительно, 1 мкг/день до, приблизительно, 20 мкг/день. В течение жизни имплантата может быть выделено от, приблизительно, 100 нг/день до, приблизительно, 900 нг/день. В других вариантах воплощения высвобождение терапевтического агента составляет, приблизительно, 300 нг/день, приблизительно, 675 нг/день или, приблизительно, 700 нг/день.
[0053] Соотношения терапевтического агента, полимера и других модификаторов могут быть эмпирически определены путем разработки рецептуры нескольких партий имплантата с различными средними соотношениями. Скорости высвобождения можно определить, например, путем использования метода многократных стоков, взвешенный образец имплантатов добавляется к отмеренному объему раствора, содержащего 0,9% NaCl в воде, где объем раствора будет таким, что концентрация терапевтического агента после высвобождения будет составлять менее 5% насыщения. Смесь выдерживают при температуре 37°С с медленным перемешиванием. Появление растворенного терапевтического агента как функции времени можно прослеживать различными известными современными методами, такими как спектрофотометрия, ВЭЖХ, масс-спектрофотометрия и подобными до установления постоянного поглощения, или до тех пор, пока не высвободится более 90% терапевтического агента.
[0054] Терапевтическими агентами, которые могут быть использованы с описываемыми здесь имплантатами, являются простагландины, аналоги простагландинов и простамиды. Примеры включают агонисты рецепторов простагландинов, включая простагландин E1 (альпростадил), простагландин E2 (динопростон), латанопрост и травопрост. Латанопрост и травопрост являются неактивными формами простагландинов (например, 1-изопропиловые эфиры простагландина); однако они относятся к простагландинам, так как действуют на рецептор простагландина F после их гидролиза до 1-карбоновой кислоты. Простамид (также называемый простагландин-этаноламидом) является аналогом простагландина, и представляет собой фармакологически уникальное соединение группы простагландинов (например, поскольку простамиды действуют на другой клеточный рецептор [рецептор простамида], который отличается от рецептора простагландинов), и представляет собой нейтральный липид, образующийся в качестве продукта окисления при помощи фермента цикло-оксигеназы-2 ("ЦОГ-2") эндоканнабиноида (такого, как анандамид). В дополнение к этому, простамиды не гидролизируются in situ до 1-карбоновой кислоты. Примерами простамидов могут служить биматопрост (этил амид 17-фенил простагландина F2α, полученный путем синтеза) и простамид F2α. Другие аналоги простагландинов, которые могут быть использованы в качестве терапевтических агентов, включают унопростон и агонисты рецепторов ЕР2/ЕР4, но не ограничиваются этим.
[0055] Простагландины, используемые здесь, также включают один или более типов производных простагландинов, аналогов простагландинов, включая простамиды и производные простамидов, неактивные формы препаратов, их соли и их смеси. В определенных имплантатах простагландин включает состав, имеющий структуру
где связи, обозначенные пунктиром, представляют собой единичную или двойную связь, которая может иметь конфигурацию cis или trans; А - это алкилен или алкиленовый радикал, имеющий от двух до шести атомов углерода, этот радикал может прерываться одним или более оксидных радикалов и замещаться одним или более гидрокси-, окси-, алкилокси- или алкилкарбокси-группами там, где алкиловый радикал включает от одного до шести атомов углерода; В - это циклоалкиловый радикал, имеющий от трех до шести атомов углерода или ариловый радикал, выбранный из гидрокарбил ариловых и гетероариловых радикалов, имеющих от четырех до десяти атомов углерода, где гетероатом выбран из атомов азота, кислорода и серы; Х - это - OR4 или -N(R4)2 где R4 выбран из водорода, низший алкильный радикал, имеющий от одного до шести атомов углерода,
или
где R5 - низший алкильный радикал, имеющий от одного до шести атомов углерода; Z=0 или представляет собой два водородных радикала; один из R1 и R2=0, -ОН или группа -O(CO)R6, а другой представляет собой -ОН или -O(CO)R6, или R1=0 и R2 - водород, где R6 представляет собой насыщенную или ненасыщенную ациклическую углеводородную группу, имеющую от 1 до, приблизительно, 20 атомов углерода, или -(CH2)mR7, где m равно 0 или целому числу между 1 и 10, и R7 - циклоалькильный радикал, имеющий от трех до семи атомов углерода, или гидрокарбил ариловый или гетероариловый радикал, как определено выше, или его фармакологически приемлемая соль.
[0056] Фармакологически приемлемые соли присоединения кислот описанных соединений - это соли, образованные из кислот, ко