Способ оценки регуляции капиллярного кровотока
Иллюстрации
Показать всеИзобретение относится к области медицины, а именно к функциональной диагностике. Проводят пробы с локальной ишемией одной из рук. После чего определяют относительные изменения средних амплитуд пульсации кровенаполнения до и после пробы. Регуляцию капиллярного кровотока оценивают по изменению пульсаций кровенаполнения только на руке, не подвергаемой ишемии. Способ позволяет учесть нарушения микроциркуляции крови при проведении терапии заболеваний различной этиологии, выявить эндотелиальную дисфункцию коронарных артерий при ишемической болезни сердца, сократить количество измерений до 2-х и исключить необходимость учета исходных амплитуд пульса, что позволит уменьшить погрешность результатов исследования. 5 ил., 3 табл., 3 пр.
Реферат
Изобретение относится к области медицины и может использоваться для оценки нарушений регуляции капиллярного кровотока (состояния микроциркуляции крови) с целью учета данного фактора при проведении терапии.
В настоящее время состояние микроциркуляции крови определяют с помощью методов функциональной диагностики: лазерной допплеровской флоуметрии, биомикроскопии бульбарной конъюнктивы, дуплексного УЗИ с функциональной пробой, периферической артериальной тонометрии (ПАТ) и лабораторных показателей: молекулы межклеточной адгезии 2 типа (intercellular adhesion molecule-2, ICAM-2), молекулы адгезии сосудистого эндотелия 1 типа (vascular cell adhesion molecule-1, VCAM-1), Е-селектин (E-selectin), Р-селектин (P-selectin) и sCD40L (soluble CD40 ligand), цитокины - интерлейкин-6 и 18, высокочувствительный С-реактивный белок (hs-CRP) и эндотелин-1 (ЕТ-1) (Deanfield et al., 2005), фактор фон Виллебранда (vWF), ангиотензин I-превращающий фермент (angiotensin I converting enzyme, АСЕ), препроэндотелин (ЕТ)-1, эндотелии I-превращающий фермент (endothelin I converting enzyme, ЕСЕ-1), В-рецепторы эндотелина, эндотелиальная NO-синтаза (eNOS), фактор транскрипции NF-kB, ICAM-1, VCAM-1 и Е-селектин [Deanfield et al., 2005].
Известный способ оценки нарушения микроциркуляции крови с помощью лазерной допплеровской флоуметрии (ЛДФ) основан на оптическом неинвазивном зондировании тканей лазерным излучением и анализе излучения, рассеиваемого движущимися эритроцитами. Оценивают сигнал наибольшей амплитуды, отраженный от отдельных эритроцитов из более тонкого слоя, около 1 мм [Fagrell В., 1994]. Этот слой зондирования может содержать в зависимости от типа ткани следующие звенья гемомикроциркуляторного русла: артериолы, терминальные артериолы, капилляры, посткапиллярные венулы, венулы и артериоло-венулярные анастомозы [Крупаткин А.И. Лазерная допплеровская флоуметрия микроциркуляции крови: Руководство для врачей / А.И. Крупаткин, В.В. Сидоров. - М.: ОАО «Издательство «Медицина», 2005. - 256 с.; Козлов В.И., Мач Э.С., Литвин Ф.Б. и соавт. Метод лазерной допплеровской флоуметрии: Пособие для врачей. - М., 2001. - 24 с; Маколкин В.И., Бранько В.В., Богданова Э.А. и др. Метод лазерной флоуметрии в кардиологии: Пособие для врачей. - М., 1999. - 48 с].
Недостатком метода ЛДФ является небольшая площадь оценки микроциркуляторного русла, в то время как при проведении терапии необходим учет интегральной оценки нарушений микроциркуляции крови.
Известный способ оценки нарушения микроциркуляции крови с помощью биомикроскопии бульбарной конъюнктивы широко используют в настоящее время для выявления морфологических повреждений микроциркуляторной сети [Волков B.C., Высоцкий Н.Н., Троцюк В.В. и др. Оценка состояния микроциркуляции методом конъюнктивальной биомикроскопии. Клиническая медицина, 1976, № 7, с. 115-119]. Биомикроскопия конъюнктивы глазного яблока позволяет детально оценить как состояние артериол, прекапилляров, капилляров, посткапилляров, венул, так и кровоток в отдельных микрососудах. Кроме того, этот метод дает возможность составить также представление о периваскулярном пространстве [Наумец Л.В. Диагностические возможности метода конъюнктивальной микроскопии. Материалы международной конференции по микроциркуляции. М., 1997; стр. 110-111.; Чернух A.M., Александров П.Н., Алексеев О.В. Микроциркуляция. Медицина. М. 1984. - 432 с.]. К числу преимуществ конъюнктивальной биомикроскопии относится также доступность объекта, отсутствие значительных особенностей анатомического характера, "беспорядочная" архитектоника сосудов конъюнктивы, представляющая собой морфологический субстрат кровотока, не связанного со специфическими органными функциями, а также хорошая контрастируемость эритроцитарного потока на белом фоне склеры [Куприянов В.В., Калмыкова В.Н. Изучение микроциркуляции в эксперименте и клинике // Под ред. В.В. Куприянова, В.Н. Калмыковой. - М., 1979. - С. 67-78].
Однако недостатком метода является наличие состояний, влияющих на регионарную микроциркуляцию крови, локальные воспалительные и другие патологические состояния органа зрения [Francois J., Neetens A. Importance clinique de I′angioscopie conjnctivale. Amm. Oculist 1967; 200, 6:656-663], субъективизм в оценке нарушений микроциркуляции (высокие требования к квалификации эксперта).
Известные способы оценки нарушения микроциркуляции крови лабораторными методами не уступают другим методам, однако, имеют ряд недостатков: инвазивность, высокая стоимость определения некоторых показателей, отсутствие единого показателя, характеризующего нарушения микроциркуляторного русла.
По наиболее близкой технической сущности в качестве прототипа нами выбран способ оценки эндотелийзависимой вазодилатации по методике «Периферическая артериальная тонометрия» (ПАТ) («Peripheral arterial tonometry», PAT), реализуемой комплексом EndoPAT2000.
Методика ПАТ основана на выявлении нарушений микроциркуляции путем оценки реакции системы регуляции кровообращения на окклюзионную стресс-пробу. Проба заключается в пятиминутной ишемии одной из рук, путем пережатия сосудов плеча окклюзионной манжетой давлением, превышающим систолическое артериальное давление (АД). Оценку реакции осуществляют на основании результатов измерений относительного изменения средней амплитуды пульсаций кровенаполнения пальцев рук (R) до и после пробы. Величину R вычисляют по формуле:
R=М2/М1, где
М1 - средняя амплитуда пульса до пробы
М2 - средняя амплитуда пульса после пробы
Измерения выполняют на двух руках - на стороне окклюзии (ROcls на руке, подвергаемой ишемии) и на стороне контроля (RCtrl на руке, не подвергаемой ишемии). Затем вычисляют отношение этих величин RR=ROcls/RCtrl и специальный индекс реактивной гиперемии RHI=RR*f(M1Ocls), где f(M1Ocls) - корректирующая функция, зависящая от исходной амплитуды пульсаций кровенаполнения на стороне окклюзии). При результатах вычисления меньше единицы индексу присваивают значение RHI=1. Для индекса RHI установлен порог RHIпор.=1,67. Значения индекса ниже порога RHIпор.=1,67 считают признаком «дисфункции эндотелия» коронарных артерий (недостаточность эндотелий-зависимой дилатации этих сосудов, обеспечивающей локальную регуляцию капиллярного кровотока в миокарде). Порог установлен экспериментально, путем сопоставления значений индекса RHI с результатами измерения относительного расширения венечной коронарной артерии в ответ на прямое воздействие ацетилхолином.
Известны и другие способы реализации методики ПАТ, не получившие такого распространения, как рассмотренный выше способ-прототип. В них на основании описанного выше показателя RR осуществляется аналогичная оценка эндотелийзависимой дилатации артерий, соответствующая оценке локальной регуляции капиллярного кровотока.
Недостатками способа, выбранного нами в качестве прототипа, являются:
- ограниченная область применения, то есть оптимизация порогового значения индекса реактивной гиперемии RHI только под одну задачу - выявление эндотелиальной дисфункции коронарных артерий при ишемической болезни сердца;
- для вычисления индекса RHI требуется выполнить 4 измерения и дополнительно учесть исходную амплитуду пульса, что может привести к повышенной погрешности результатов исследования.
Техническим результатом изобретения является возможность учета нарушений микроциркуляции крови при проведении терапии заболеваний различной этиологии, а не только для выявления эндотелиальной дисфункции коронарных артерий при ишемической болезни сердца, а также сокращение количества измерений до 2-х и исключение необходимости учитывать исходную амплитуду пульса, что позволит уменьшить погрешность результатов исследования.
Технический результат изобретения достигается тем, что способ оценки регуляции капиллярного кровотока ограничивается выполнением пробы с локальной ишемией одной из рук и последующим определением относительного изменения средних амплитуд пульсации кровенаполнения до и после пробы только на руке, не подвергаемой ишемии.
Способ может быть осуществлен следующим образом:
Исследование проводят в комфортных условиях при исключении воздействия раздражающих факторов (телефонных звонков, других резких звуков и т.п.). Больного просят снять с рук часы, кольца и прочие подобные изделия. Во время всего исследования необходимо воздержаться от разговоров.
Исследование проводят в положении пациента лежа на спине. Плотно надевают на плечевую часть руки манжету для измерения артериального давления. Помещают подставку под локти и предплечье исследуемого. На средние пальцы обеих рук устанавливают датчики пульсации кровенаполнения. Может быть применен либо сфигмографический «датчик ПАТ» (как в способе-прототипе), либо его функциональный аналог (в частности, фото- или электроплетизмографический датчик пульсаций кровенаполнения тканей). Затем запускают таймер, осуществляют 5-ти минутную запись пульсаций кровенаполнения в исходном состоянии (стабилизационный период) и проводят пробу с локальной ишемией в одной из рук - быстро нагнетают воздух в плечевую окклюзионную манжету до давления, превышающего систолическое не менее чем на 60 мм рт.ст. выше систолического давления и не менее 200 мм рт.ст. На руке, подвергаемой ишемии, контролируют отсутствие или наличие минимальной пульсации кровенаполнения. В том случае, если пульсация кровенаполнения соответствует исходному состоянию, то увеличивают давление в манжете. Через 5 минут быстро выпускают воздух из манжеты и в течение последующих 5 минут продолжают запись пульсаций кровенаполнения (постокклюзионный период). По окончании записи останавливают секундомер, снимают датчики и манжету. На основании выполненной записи определяют средние значения амплитуд пульсаций кровенаполнения до окклюзии М1 и после окклюзии М2 в пальце руки, не подвергавшейся ишемии и вычисляют относительное изменение R=М2/М1. Эту величину, определенную на руке, не подвергавшейся ишемии RCtrl, интерпретируют как оценку центральной реакции единой системы регуляции капиллярного кровотока на проведенную пробу с локальной ишемией.
Отличительным существенным признаком изобретения является то, что регуляцию капиллярного кровотока, в отличие от способа прототипа, оценивают по изменению пульсаций кровенаполнения только на руке, не подвергаемой ишемии.
Причинно-следственная связь между отличительным существенным признаком изобретения и достигаемым результатом:
в способе прототипе результатом исследования является индекс RHI, который интерпретируют как оценку локальной реакции системы регуляции кровотока на проведенную пробу. В заявленном способе результатом исследования является величина RCtrl, которую интерпретируют как оценку центральной реакции. Анализ результатов применения методики ПАТ при обследовании пациентов с разной этиологией показал, что оценка центральной реакции более адекватно характеризует состояние периферической микроциркуляторной сети в целом, чем оценка локальной реакции.
Оценка центральной реакции (величина RCtrl) позволяет выявить общий признак нарушения капиллярного кровотока для различных заболеваний. Таким признаком служит критическое отклонение величины RCtrl от единицы. Значения RCtrl близкие к единице соответствуют минимальной центральной реакции, что свидетельствует о сохранности функции локальной регуляции капиллярного кровотока. Указанное положение сохраняется, несмотря на возможный разнонаправленный характер нарушений регуляции капиллярного кровотока при различных заболеваниях.
Оценка локальной реакции (индекс RHI) не позволяет выявить общий признак, так как очень вариативна. Кроме того, для ее вычисления необходимо выполнить большее число измерений, что дополнительно повышает погрешность результатов исследования.
Оценки, полученные заявляемым способом, были сопоставлены с данными прототипа и фактическим состоянием периферической микроциркуляторной сети, оцениваемым методом биомикроскопии бульбарной конъюнктивы. Были обследованы больные с разной нозологией. В частности:
- гипертоническая болезнь (ГБ) II-III стадией, 22 пациента;
- ишемическая болезнь сердца с атеросклеротически измененные коронарными артериями, 17 пациентов;
- ишемическая болезнь сердца с ангиографически неизмененными или малоизмененными коронарными артериями (Кардиальный синдром X), 26 пациентов.
Верификацию фактического состояния кровеносных сосудов на уровне микроциркуляции и нарушений капиллярного кровотока на момент проведения исследований по методике ПАТ осуществляли с помощью биомикроскопии бульбарной конъюнктивы глаза. Выявлялись следующие дефекты микроциркуляторной сети:
1. Извитость сосудов.
2. Неравномерность калибра.
3. Наличие микроаневризм.
4. Наличие микрокровоизлияний.
5. Замедление кровотока.
6. Ретроградный кровоток.
7. Наличие агрегации эритроцитов.
8. «Патологическая пульсация» сосудов.
9. Запустение капилляров.
В рамках проводимого исследования, верификацию общего поражения микроциркуляторной сети осуществляли, исходя из бинарных оценок («да» или «нет») показателя «запустение капилляров». Остальные показатели рассматривали как дополнительные, позволяющие уточнить специфику поражения.
Положительные оценки наличия микроаневризм (п. 3), микрокровоизлияний (п. 4) и особенно агрегации эритроцитов (п. 7) были отнесены к особым факторам риска осложнений. «Патологическая пульсация» сосудов (п. 8) рассматривалась как общий признак повышенного периферического сопротивления.
Извитость сосудов (п. 1) и неравномерность калибра (п. 2) наблюдались почти у всех больных, а ретроградный кровоток (п. 6) был сравнительно редок. Эти обстоятельства не позволили рассматривать значения показателей, соответствующих п. 1, 2 и 6, как признаки особенностей поражения микроциркуляторной сети при различных заболеваниях ССС.
Замедление капиллярного кровотока (п. 5) могло быть связано с разными особенностями системы кровообращения, и поэтому как показатель поражения микроциркуляторной сети тоже не рассматривалось.
Регуляцию капиллярного кровотока оценивали по относительному изменению амплитуды пульсаций кровенаполнения пальцев рук в ответ на пробу с локальной ишемией одной из них. Изменение пульсаций на руке, подвергаемой ишемии, интерпретировали как оценку общей реакции единой системы кровообращения на пробу, изменение на руке, не подвергаемой ишемии - как оценку ее центральной реакции на пробу (заявляемый способ), а отношение указанных изменений - как оценку ее локальной реакции (способ прототип).
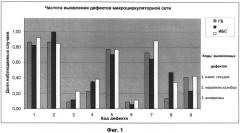
На Фиг. 1 отображена частота верификации различных дефектов периферической микроциркуляторной сети кровеносных сосудов, оцениваемых в каждой из указанных групп методом биомикроскопии бульбарной конъюнктивы. Наиболее выраженные различия между указанными группами больных проявились в отношении дефектов с кодами 4, 7, 8 и 9 (микрокровоизлияния, агрегация эритроцитов, патологическая пульсация и запустевание капилляров). Для верификации оцениваемых нарушений регуляции капиллярного кровотока наиболее представителен показатель 9 - запустевание капилляров. При ИБС этот дефект был верифицирован примерно в 2 раза реже (20%), чем при ГБ и КСХ.
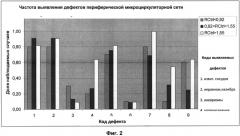
На Фиг. 2 и 3 аналогичным образом показана частота верификации дефектов микроциркуляторной сети среди групп с различной оценкой центральной и локальной реакций на пробу (RCtrl и RR). Как видно, различия между группами, сформированными по оценкам центральной реакции RCtrl, гораздо более выражены, чем между группами, сформированными по оценкам локальной реакции RR. Частота верификации запустевания капилляров при выраженных отклонениях показателя RCtrl от единицы возрастает почти в 3 раза (при разных значениях RR или RHI она была практически одинакова). Важно отметить и то, что на Фиг. 2 выраженное увеличение показателя RCtrl соответствует многократному увеличению частоты верификации микрокровоизлияний (код 4) и 100%-ной верификации агрегации эритроцитов (код 7). Во всем диапазоне наблюдаемых значений показателя RCtrl при его увеличении резко возрастала и частота верификации патологической пульсации артериол. На Фиг. 3 различия между группами с разными значениями показателя RR выражены гораздо слабее и не так специфичны, как на Фиг. 2.
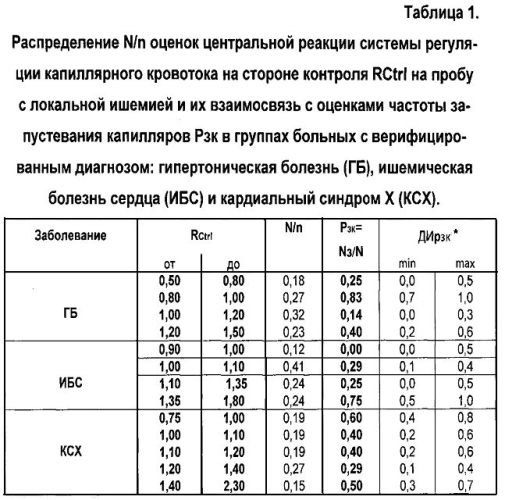
Взаимосвязь распределения N/n оценок реакции системы регуляции капиллярного кровотока на пробу с локальной ишемией (RCtrl, RR, RHI) с оценками частоты запустевания капилляров Рзк группах больных с верифицированным диагнозом гипертоническая болезнь (ГБ), ишемическая болезнь сердца (ИБС) и кардиальный синдром X (КСХ) представлена в таблицах 1, 2 и 3.
На фиг. 4, 5 представлены функции плотности распределения оценок центральной, локальной реакций (RCtrl, RR) и значений индекса реактивной гиперемии RHI, а также графики кусочно-линейной апроксимации зависимости между этими оценками и частотой верификации запустевания капилляров Рзк=Nзк/N. На Фиг. 4 видно, что при умеренной центральной реакции (RCtrl≈1,1) частота верификации запустевания капилляров сравнительно невелика (порядка 25%), а при выраженной (RCtrl≈0,8 или RCtrl>1,4) она достигает значений 60-80%. В зависимости от этиологии заболевания центральная реакция может иметь различную направленность. При ИБС абсолютно преобладают значения RCtrl>1, а при ГБ почти у половины пациентов (45%) наблюдались значения RCtrl<1. На аналогичных графиках Фиг. 5, построенных для оценок локальной реакции RR и индекса RHI, подобные, физиологически объяснимые особенности, выявить труднее.
Таким образом, оценка центральной реакции позволяет учесть специфику заболевания и может использоваться не только у пациентов с ИБС, но и при других нозологиях. Оценка центральной реакции более устойчива, информативна и не требует коррекции (практически не зависит от исходной амплитуды кровенаполнения.
В распределении оценок RCtrl (Фиг. 4) наиболее отчетливо проявляется и ожидаемое различие между группами с ИБС и КСХ. При КСХ распределение оценок RCtrl шире и смещено в сторону более высоких значений. Это вполне соответствует гипотезе о значительном влиянии на патогенез КСХ проявлений «дисфункции эндотелия» (нарушений локальной регуляции капиллярного кровотока), при которых компенсаторно возрастает роль центральной регуляции кровообращения.
Систематически получаемые данные о состоянии и динамике нарушений микроциркуляции позволяют осуществить обоснованный индивидуальный подбор терапии и оперативной его коррекции.
Анализ результатов исследования позволил сделать следующие выводы:
Заявляемый способ оценки регуляции капиллярного кровотока, в отличие от способа прототипа:
- может использоваться не только у пациентов с ИБС, но и при других заболеваниях; позволяет в большей степени учесть специфику заболевания.
- не требует коррекции (практически не зависит от исходной амплитуды кровенаполнения).
В качестве примеров приведены следующие выписки из клинической практики:
Пример 1. Пациент А., диагноз «Гипертоническая болезнь», возраст 57 лет, рабочий.
Повышение артериального давления (АД) отмечает около 4-х лет (до этого АД не измерял), максимальное АД 190/110 мм рт. ст., привычное АД в пределах 120-130/80 мм рт. ст. В 2008 г. перенес острое нарушение мозгового кровообращение, с этого времени принимает постоянную гипотензивную терапию. С июня 2010 г. отмечает одышку, периодически боли за грудиной, обследован амбулаторно по данным стресс-эхокардиографии - проба положительна по клиническим Эхо-данным. Рекомендовано выполнение коронарографии, в связи с чем госпитализирован в отделение кардиологии.
В анамнезе: язвенная болезнь желудка.
На момент осмотра жалоб активно не предъявлял.
При объективном обследовании пациента отмечено состояние удовлетворительное, сознание ясное, тоны сердца приглушены ритмичные, шумов нет; расширение границ сердца влево на 1,5 см. АД 155/90 мм рт. ст. Пульс 64 удара в минуту. Дыхание жесткое, хрипов нет, частота дыхательных движений (ЧДД) 16 в минуту. Живот мягкий, безболезненный во всех отделах при пальпации. Печень не выступает из-под края реберной дуги. Селезенка не пальпируется, размеры селезенки перкуторно не увеличены. Почки не пальпируются. Поколачивание по поясничной области безболезненно с двух сторон. Периферических отеков нет.
При исследовании периферической крови содержание гемоглобина, эритроцитов, лейкоцитов, тромбоцитов, СОЭ не отличалось от нормальных показателей. В биохимическом анализе крови содержание общего белка, глюкозы, КФК общ, липидного спектра, АЛТ, ACT, билирубина, щелочной фосфатазы, ГГТП, мочевины, креатинина, мочевой кислоты, показатель коагулограммы (протромбиновый индекс) соответствовали референтным значениям. При проведении иммуноферментного анализа (ИФА): HbsAg (-), анти-HCV (-).
По данным электрокардиографического исследования: ритм синусовый с частотой сердечных сокращений 60 в мин, признаки гипертрофии левого желудочка. При проведении эхокардиографии обращает на себя внимание умеренное утолщение миокарда левого желудочка, индекс массы миокарда левого желудочка увеличен. Сократительная способность миокарда не снижена. Фракция выброса левого желудочка 70%. Нарушение релаксации миокарда левого желудочка по ригидному типу.
В стационаре повторно проведена стресс Эхо-КГ - проба отрицательная. Выполнена коронарография - тип коронарного кровоснабжения смешанный, гемодинамически значимых стенозов не выявлено.
- При исследовании сосудов бульбарной конъюнктивы определялось: извитость сосудов, неравномерность калибра сосудов, замедление кровотока, наличие агрегациии эритроцитов, наличие запустевших капилляров с отдельными неподвижными эритроцитами. Оценка сосудистых изменений бульбарной конъюнктивы соответствовала 2 баллам.
- При оценке регуляции капиллярного кровотока по способу прототипу получено: RHI 2,25.
- При оценке регуляции капиллярного кровотока по заявляемому способу получено: RCtrl=0,92.
Диагноз:
Основной: Гипертоническая болезнь II ст., АГ 3 ст., риск ССО 4.
Цереброваскулярная болезнь. Последствия ОНМК от 2008 г.
Сопутствующий: Язвенная болезнь желудка, вне обострения.
Осложнение: Хроническая сердечная недостаточность II А стадия, II ф. кл. по NYHA.
Пример 2. Пациент Б., диагноз «Ишемическая болезнь сердца», возраст 57 лет, инженер.
Около 2-х лет беспокоят боли в сердца давящего характера за грудиной без иррадиации, купирующиеся приемом нитратов. Обследован амбулаторно, состояние расценивали как: ИБС, Стенокардия II ф. кл. Последний месяц боли в сердце стали беспокоить чаще, в связи с чем выполнено: CM-ЭКГ от 11.04.2011 г. - выявлены изменения ишемического характера по нижне-диафрагмальной, боковой стенке левого желудочка. 13.04.2011 г. проведен тест с физической нагрузкой - расценен как положительный, в связи с чем госпитализирован в клинику кардиологии в плановом порядке для проведения коронарографии.
В анамнезе: хронический гастродуоденит, подагрический артрит.
На момент осмотра предъявлял жалобы: боли за грудиной давящего характера, одышку при интенсивной физической нагрузке. При объективном обследовании пациента отмечено состояние удовлетворительное, сознание ясное, тоны сердца приглушены ритмичные, шумов нет. АД 120/80 мм рт. ст. Пульс 60 ударов в минуту. Дыхание жесткое, хрипов нет, ЧДД 16 в минуту. Живот мягкий, безболезненный во всех отделах при пальпации. Печень не выступает из-под края реберной дуги. Селезенка не пальпируется. Почки не пальпируются.
Поколачивание по поясничной области безболезненно с двух сторон. Периферических отеков нет.
При исследовании периферической крови содержание гемоглобина, эритроцитов, лейкоцитов, тромбоцитов, СОЭ не отличалось от нормальных показателей. В биохимическом анализе крови содержание общего белка, глюкозы, КФК общ, липидного спектра, АЛТ, ACT, билирубина, мочевины, креатинина, мочевой кислоты, показателя коа-гулограммы (протромбиновый индекс) соответствовали референтным значениям. При проведении ИФА: HbsAg (-), анти-HCV (-).
По данным электрокардиографического исследования: синусовая брадикардия с частотой сердечных сокращений 48 в мин, нарушение межпредсердной проводимости, косвенные признаки гипертрофии левого желудочка. Рентгенография органов грудной клетки патологии не выявила. Пациенту выполнена коронарография - тип коронарного кровообращения левый доминантный, субокклюзия и стеноз 80% в среднем сегменте передней межжелудочковой артерии. Учитывая выявленные изменения по данным коронарографии, пациенту выполнена ангиопластика и стентирование передней межжелудочковой артерии.
- При исследовании сосудов бульбарной конъюнктивы определялось: неравномерность калибра, замедление кровотока, наличие агрегации эритроцитов, запустение капилляров. Оценка сосудистых изменений бульбарной конъюнктивы соответствовала 2 баллам.
- При оценке регуляции капиллярного кровотока по способу прототипу получено: RHI=1,11.
- При оценке регуляции капиллярного кровотока по заявляемому способу получено: RCtrl=1,74.
Диагноз:
Основной: ИБС.Стенокардия напряжения II ф. кл. Ангиопластика и стентирование передней межжелудочковой артерии от 20.06.2011 г.
Сопутствующий: Хронический гастродуоденит, вне обострения.
Осложнение: Хроническая сердечная недостаточность I ст., II ф. кл. по NYHA.
Пример 3. Пациент В., диагноз «Кардиальный синдром X», возраст 62 года, пенсионер.
Госпитализирован в отделение кардиологии в плановом порядке с жалобами на: периодические боли давящего характера в левой половине грудной клетки, возникающие после эмоциональной нагрузки, иногда при физической нагрузке (уровень более, чем бытовая), проходящие самостоятельно, четкого эффекта от нитратов не отмечает, артериальное давление не контролировал, головная боль не беспокоит, при активном расспросе отмечал периодический подъем артериального давления, максимальные цифры 160/90 мм рт. ст. при эмоциональных нагрузках, постоянной гипотензивной терапии не принимал.
Анамнез заболевания: С 2010 года стал отмечать при эмоциональной и физической нагрузке боли давящего характера в левой половине грудной клетки, проходящие самостоятельно, короткодействующими нитратами не пользовался. Обратился в поликлинику по месту жительства, обследован амбулаторно: выполнено суточное мониторирование ЭКГ от 14.09.2010 г.: ЧСС средняя днем 78 уд./мин, минимальная 49 уд./мин, максимальная 132 уд./мин; ЧСС средняя в ночное время 56 уд./мин, минимальная 48 уд./мин, максимальная 74 уд./мин; ЧСС при нагрузках 106 уд./мин, минимальная 81 уд./мин, максимальная 132 уд./мин. В течение всего времени исследования регистрируется синусовый ритм. Нарушения ритма: одиночная наджелудочковая экстрасистолия, 16 за сутки (8 днем, 8 ночью), одиночная желудочковая 5 за сутки (днем), одиночные узловые экстрасистолы, 1 за сутки (ночью). Тредмил-тест от 12.11.2010 г.: проба прекращена в связи с появлением изменений сегмента ST ишемического характера на нижне-боковой стенке левого желудочка, сохраняющиеся в течение 5 минут восстановительного периода, реакция АД адекватная, клинически жалоб нет. Проба положительная, толерантность к физической нагрузке удовлетворительная. Госпитализирован в клинику кардиологии 02.12.10 в плановом порядке в отделение кардиологии для выполнения коронарографии и определения дальнейшей тактики ведения пациента с диагнозом: ИБС: Стенокардия напряжения 2 ф.к. Дислипидемия. Гипертоническая болезнь III стадии, II степени, риск ССО 3.
Анамнез жизни: наследственность отягощена по материнской линии: гипертоническая болезнь.
При объективном обследовании: состояние удовлетворительное, сознание ясное, границы сердца не расширены, тоны сердца приглушены ритмичные, шумов нет. АД 130/80 мм рт.ст. Пульс 57 ударов в минуту. Грудная клетка обычной формы. Дыхание жесткое, хрипов нет, ЧДД 16 в минуту. Живот мягкий, безболезненный во всех отделах при пальпации. Печень не выступает из-под края реберной дуги. Селезенка не пальпируется. Почки не пальпируются. Поколачивание по поясничной области безболезненно с двух сторон. Периферических отеков нет.
При исследовании периферической крови содержание гемоглобина, эритроцитов, лейкоцитов, тромбоцитов, СОЭ не отличалось от нормальных показателей. В биохимическом анализе крови обращало на себя внимание гиперхолестеринемия до 6,8 ммоль/л, гипертриглицеридемия до 2,95 ммоль/л, повышение ЛПНП до 4,31 ммоль/л, снижение ЛПВП до 0,99 ммоль/л.
По данным электрокардиографического исследования: ритм - синусовая брадикардия с частотой сердечных сокращений 57 в минуту, неполная блокада правой ножки пучка Гиса.
Проведена Эхо-КГ от 03.12.2010 г.: ФВ ЛЖ 75%, полости не расширены, стенки левого желудочка не утолщены, глобальная сократимость миокарда левого желудочка нормальная, зон нарушения локальной сократимости не выявлено, аорта не расширена, стенки уплотнены, краевой фиброз полулуний, аортальная недостаточность - приклапанная, аортальный поток нормальный. Митральная регургитация 1 ст. Трикуспидальная регургитация 1 ст. Расчетное систолическое давление в легочной артерии 30 мм рт.ст. Диастолическая дисфункция левого желудочка не нарушена.
Пациенту выполнена коронароангиография 04.12.10 г.: Тип коронарного кровоснабжения - левый доминантный, изменений коронарных артерий не выявлено.
Для верификации состояния пациенту были проведены дополнительные методы диагностики:
- Анализ крови на агрегацию тромбоцитов (без терапии): при исследовании функции тромбоцитов отмечается повышение степени агрегации на малой дозе индуктора АДФ (2,5 мкл), что указывает на повышенную функциональную активность тромбоцитов. При индукции коллагеном степень агрегации повышена.
- При исследовании сосудов бульбарной конъюнктивы определялось: неравномерность калибра сосудов, наличие микроаневризм, замедление кровотока, наличие агрегациии эритроцитов, наличие запустевших капилляров с отдельными неподвижными эритроцитами. Оценка сосудистых изменений бульбарной конъюнктивы соответствовала 2 баллам.
- Позитронно-эмиссионная томография: ПЭТ признаков постинфарктного кардиосклероза не установлено. Стресс-индуцированная ишемия миокарда не зарегистрирована. Проба с дипиридамолом отрицательная. Отмечается уменьшение значений удельного миокардиального кровотока на фоне холодовой пробы (вазоспастическая реакция). Коронарный резерв в пределах нормальных значений.
- При оценке регуляции капиллярного кровотока по способу прототипу получено: RHI=1,11.
- При оценке регуляции капиллярного кровотока по заявляемому способу получено: RCtrl=1,07.
Диагноз:
Основной: ИБС: Кардиальный синдром X. Дислипидемия.
Гипертоническая болезнь II стадии, АГ 2 степени, риск ССО 3.
Осложнение: Хроническая сердечная недостаточность I ф.кл. по NYHA.
Заключение: В примере 2 и 3 у пациентов с ИБС с атеросклеротически измененными и неизмененными коронарными артериями исследование по способу прототипу (учитывая индекс RHI) свидетельствует о нарушении эндотелийзависимой вазодилатации, что подтверждается исследованием по заявленному способу.
В примере 1 у пациента с гипертонической болезнью результат исследования по способу прототипу (учитывая индекс RHI) свидетельствует об отсутствии нарушений эндотелийзависимой вазодилатации, однако данные биомикроскопии бульбарной конъюнктивы свидетельствуют о наличии нарушений микроциркуляции крови, что также подтверждается исследованием по заявленному способу.
Таким образом, разработанный способ оценки регуляции капиллярного кровотока обеспечивает возможность учета нарушений микроциркуляции крови при проведении терапии заболеваний различной этиологии, а не только для выявления эндотелиальной дисфункции коронарных артерий при ишемической болезни сердца. Заявляемый способ позволил также сократить количество измерений до 2-х и исключить необходимость учитывать исходную амплитуду пульса, что уменьшает погрешность результатов исследования.
* Доверительный интервал оценки вероятности запустевания каппиляров ДИркз определялся исходя из биноминального распределения возможных выборочных оценок этой величины с принятым уровнем значимости α≈0,09.
Способ оценки регуляции капиллярного кровотока, включающий выполнение пробы с локальной ишемией одной из рук и последующим определением относительного изменения средних амплитуд пульсации кровенаполнения до и после пробы, отличающийся тем, что регуляцию капиллярного кровотока оценивают по изменению пульсаций кровенаполнения только на руке, не подвергаемой ишемии.