Производное дифенилсульфида и фармацевтический продукт, который содержит его в качестве активного ингредиента
Иллюстрации
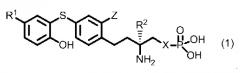
Показать всеИзобретение относится к производному дифенилсульфида, которое может применяться в медицине в качестве антагониста S1P3 рецептора, общей формулы (1)
где R1 представляет собой С1-6-алкоксигруппу, R2 представляет собой пропил или аллил, X представляет собой метилен или атом кислорода и Z представляет собой атом галогена. Предложены новые производные дифенилсульфида, их соли и гидраты, а также композиции на их основе, обладающие превосходной S1P3 антагонистической активностью. 3 н. и 5 з.п. ф-лы, 3 пр., 1 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к новому производному дифенилсульфида, которое является эффективным в качестве лекарственного средства, или к его фармацевтически приемлемой соли или гидрату, и антагонисту рецептора сфингозин-1-фосфата 3 (S1P3), а также к лекарственному средству, содержащему их в качестве активного ингредиента.
Уровень техники
Сфингозин-1-фосфат (S1P) рассматривался только как промежуточный метаболит в метаболизме сфингозина. Однако сообщалось, что S1P обладает стимулирующим действием в отношении роста клеток и регулирующим действием в отношении функции подвижности клеток, и теперь стало ясно, что S1P является новым липидным медиатором, который проявляет различные физиологические действия, такие как апоптозное действие, действие регуляции морфологии клеток и сужение кровеносных сосудов (непатентные документы 1 и 2).
Указанный S1P сочетает два действия, действие в качестве внутриклеточного вторичного мессенджера и действие в качестве межклеточного медиатора. Исследования действия S1P в качестве межклеточного медиатора являются особенно активными. Сообщалось, что информация передается через множество G-белок-связанных рецепторов, присутствующих на поверхности клеточной мембраны (ген дифференцировки эндотелия, EDG) (непатентные документы 1 и 3). В настоящее время известно пять подтипов S1P рецепторов, включающие Edg-1, Edg-3, Edg-5, Edg-6 и Edg-8, которые называются S1P1, S1P3, S1P2, S1P4 и S1P5, соответственно.
В различных исследованиях указанных S1P рецепторов сообщалось, что так называемый регулятор S1P рецептора, который проявляет агонистическое или антагонистическое действие против указанного рецептора, эффективен против широкого спектра заболеваний. В патентном документе 2 и непатентных документах 4-7 сообщается, что антагонист S1P3 эффективен в качестве терапевтического или профилактического лекарственного средства при сужении дыхательных путей, бронхиальной астме, хронической обструктивной болезни легких (ХОБЛ), эмфиземе легких, стенозе трахеи, диффузном панбронхиолите, бронхите в результате инфекции, болезни соединительной ткани или трансплантации, диффузном гамартоангиомиоматозе легких, респираторном дистресс-синдроме взрослых (РДСВ), интерстициальном пневмоните, раке легкого, гиперчувствительной пневмонии, идиопатической интерстициальной пневмонии, фиброзе легких, сепсисе или цитокиновом шторме при инфекции, вызванной вирусом гриппа или респираторным синцитиальным вирусом (RSV).
Кроме того, в патентных документах 3-6 показано, что антагонист S1P3 также эффективен против артериосклероза, гипертрофии интимы кровеносных сосудов, солидных опухолей, диабетической ретинопатии, ревматоидного артрита, остановки сердца, ишемических реперфузионных нарушений, спазмов кровеносных сосудов мозга после субарахноидального кровоизлияния, стенокардии или инфаркта миокарда, вызванного спазмами коронарных сосудов, гломерулонефрита, тромбоза, болезни легких, вызванной отеком легких, такой как РДСВ, сердечной аритмии, болезни глаз, повышенного внутриглазного давления, глаукомы, глаукоматозной ретинопатии, оптической нейропатии, дегенерации желтого пятна и т.п.
Далее, хотя в настоящее время существует рекомбинантная форма человеческого активированного белка C (rhAPC) в лекарственных средствах, эффективных в качестве терапевтических средств при сепсисе, rhAPC также может вызывать геморрагию в качестве побочного эффекта. Таким образом, существует потребность в разработке новых терапевтических или профилактических средств против сепсиса, которые не проявляют таких побочных эффектов. В непатентных документах 5 и 7 сообщается, что рецептор S1P3 способствует полиорганной недостаточности, вызванной сепсисом, на основе анализа с использованием мышей с нокаутом по S1P3, что позволяет, таким образом, предположить, что антагонист S1P3 может быть эффективным в качестве терапевтического или профилактического средства против сепсиса. Кроме того, сообщалось, что антагонист S1P1 повышает проницаемость стенок сосудов и вызывает отек легких (непатентный документ 8). Таким образом, для того чтобы новое терапевтическое или профилактическое средство против сепсиса обладало высоким уровнем безопасности, такое терапевтическое или профилактическое средство должно оказывать слабое антагонистическое действие в отношении S1P1, предпочтительно проявлять агонистическое действие в отношении S1P1 и более предпочтительно не проявлять действия против S1P1 рецептора.
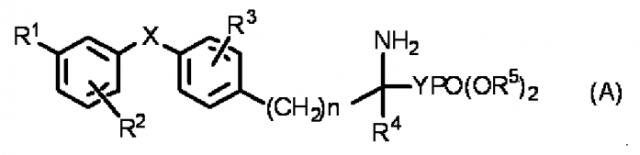
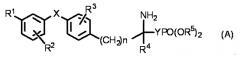
Известные регуляторы S1P рецептора включают, например, соединения, представленные следующей общей формулой (A), описанной в патентном документе 1:
Формула 1
(где в формуле (A) R1 представляет собой атом водорода, атом галогена, галогенированную или негалогенированную низшую алкильную группу, содержащую 1-4 атома углерода, гидроксигруппу, фенильную группу, аралкильную группу, низшую алкоксигруппу, содержащую 1-4 атома углерода, трифторметилоксигруппу, необязательно замещенную аралкилоксигруппу, необязательно замещенную феноксигруппу, циклогексилметилоксигруппу, пиридилметилоксигруппу, циннамилоксигруппу, нафтилметилоксигруппу, феноксиметильную группу, гидроксиметильную группу, гидроксиэтильную группу, низшую алкилтиогруппу, содержащую 1-4 атома углерода, низшую алкилсульфинильную группу, содержащую 1-4 атома углерода, низшую алкилсульфонильную группу, содержащую 1-4 атома углерода, бензилтиогруппу, ацетильную группу, нитрогруппу или цианогруппу; R2 представляет собой атом водорода, атом галогена, галогенированную или негалогенированную низшую алкильную группу, содержащую 1-4 атома углерода, низшую алкоксигруппу, содержащую 1-4 атома углерода, аралкильную группу или аралкилоксигруппу; R3 представляет собой атом водорода, атом галогена, трифторметильную группу, низшую алкильную группу, содержащую 1-4 атома углерода, низшую алкоксигруппу, содержащую 1-4 атома углерода, гидроксигруппу, бензилоксигруппу, фенильную группу, низшую алкоксиметильную группу, содержащую 1-4 атома углерода, или низшую алкилтиогруппу, содержащую 1-4 атома углерода; R4 представляет собой атом водорода, атом галогена, трифторметильную группу, низшую алкильную группу, содержащую 1-4 атома углерода, низшую алкоксиметильную группу, содержащую 1-4 атома углерода, низшую алкилтиометильную группу, содержащую 1-4 атома углерода, гидроксиметильную группу, фенильную группу или аралкильную группу; R5 представляет собой атом водорода или низшую алкильную группу, содержащую 1-4 атома углерода; X представляет собой O, S, SO или SO2; и Y представляет собой -CH2O-, -CH2-, -CH=CH-, -CF=CF-, -CH2CH2-, -CH2CFH-, -CH2CF2- или -CH(О)CF2-).
Однако патентный документ 1 не включает сложные моноэфирные производные 2-аминофосфорной кислоты или производные 3-аминофосфоновой кислоты, имеющие дифенилсульфидный скелет, в котором гидроксильная группа заменяет фенильную группу. Кроме того, тот факт, что сложные моноэфирные производные 2-аминофосфорной кислоты или производные 3-аминофосфоновой кислоты, имеющие такую структуру, демонстрируют превосходное антагонистическое действие в отношении S1P3 рецептора, также не известен.
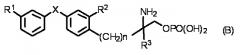
Другие примеры известных регуляторов S1P рецептора включают соединения, представленные следующей общей формулой (B) в патентном документе 6:
Формула 2
(где в формуле (B) R1 представляет собой атом хлора, нормальную алкильную группу, содержащую 1-3 атома углерода, или трифторметильную группу; R2 представляет собой атом фтора или атом хлора; R3 представляет собой нормальную алкильную группу, содержащую 1-3 атома углерода; X представляет собой атом кислорода или атом серы; и n равен целому числу 2 или 3).
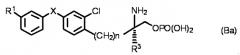
Далее, среди соединений, представленных общей формулой (B), сообщалось, что оптически активные соединения, представленные общей формулой (Ba):
Формула 3
(где в формуле (Ba) R1, R3 и X являются такими, как определено выше).
Сообщалось, что оптически активные соединения, представленные общей формулой (Ba), обладают слабым S1P3 агонистическим действием и превосходным агонистическим действием против S1P1 и/или S1P4. Однако соединения, имеющие инвертированный асимметричный центр по отношению к оптически активным соединениям, представленным общей формулой (Ba), не известны. Кроме того, тот факт, что такие оптически активные соединения демонстрируют превосходное антагонистическое действие в отношении S1P3 рецептора, также не известен.
Патентный документ 1: WO04074297 проспект.
Патентный документ 2: WO03020313 проспект.
Патентный документ 3: выложенная заявка на патент Японии 2005-247691.
Патентный документ 4: WO07043568 проспект.
Патентный документ 5: WO06063033 проспект.
Патентный документ 6: WO08018427 проспект.
Непатентный документ 1: Y. Takuma et al., Mol. Cell. Endocrinol., 177, 3 (2001).
Непатентный документ 2: Y. Igarashi, Ann, N.Y. Acad. Sci., 845, 19 (1998).
Непатентный документ 3: H. Okazaki et al., Biochem. Biophs. Res. Commun., 190, 1104(1993).
Непатентный документ 4: Y. Gon et. al., Proc Natl Acad Sci U S A. 102(26), 9270 (2005).
Непатентный документ 5: F. Nissen et al., Nature, 452, 654(2008).
Непатентный документ 6: D. Christina et al., Am. J. Pathol., 170(1), 281(2007).
Непатентный документ 7: F. Nissen et al., Blood, 113(12), 2859(2009).
Непатентный документ 8: M.G.Sanna et al., Nature Chemical biology, 2, 434 (2006).
Сущность изобретения
Задачи, решаемые настоящим изобретением
Задачей настоящего изобретения является предоставление производного дифенилсульфида, обладающего превосходной S1P3 антагонистической активностью.
Способы решения задач
В результате интенсивных исследований S1P3 антагониста, авторы настоящего изобретения обнаружили, что новое производное дифенилсульфида обладает превосходным S1P3 антагонистическим действием, что составляет сущность настоящего изобретения.
В частности, первый аспект изобретения относится к производному дифенилсульфида или его фармацевтически приемлемой соли или гидрату, представленным общей формулой (1):
Химическая формула 4
(где в формуле (1) R1 представляет собой алкоксигруппу, содержащую 1-6 атомов углерода, R2 представляет собой пропильную группу или аллильную группу, X представляет собой метилен или атом кислорода, и Z представляет собой атом галогена).
Далее, второй аспект изобретения относится к производному дифенилсульфида согласно первому аспекту изобретения или к его фармацевтически приемлемой соли или гидрату, где соединение, представленное общей формулой (1), представлено общей формулой (1a):
Химическая формула 5
(где в формуле (1a) R1 и R2 являются такими, как определено в первом аспекте изобретения).
Третий аспект изобретения относится к производному дифенилсульфида согласно первому аспекту изобретения или к его фармацевтически приемлемой соли или гидрату, где соединением, представленным общей формулой (1), является моноэфир (R)-2-аллил-2-амино-4-{2-хлор-4-(5-этокси-2-гидроксифенилтио)фенил}бутилфосфорной кислоты или моноэфир (S)-2-амино-4-{2-хлор-4-(5-этокси-2-гидроксифенилтио)фенил}-2-пропилбутилфосфорной кислоты.
Четвертый аспект изобретения относится к лекарственному средству, которое включает производное дифенилсульфида согласно любому из аспектов изобретения (1)-(3) или его фармацевтически приемлемую соль или гидрат.
Кроме того, пятый аспект изобретения относится к лекарственному средству согласно четвертому аспекту изобретения, где лекарственное средство является терапевтическим или профилактическим средством при сужении дыхательных путей, бронхиальной астме, хронической обструктивной болезни легких (ХОБЛ), эмфиземе легких, стенозе трахеи, диффузном панбронхиолите, бронхите в результате инфекции, болезни соединительной ткани или трансплантации, диффузном гамартоангиомиоматозе легких, респираторном дистресс-синдроме взрослых (РДСВ), интерстициальном пневмоните, раке легкого, гиперчувствительной пневмонии, идиопатической интерстициальной пневмонии, фиброзе легких, сепсисе или цитокиновом шторме при инфекции, вызванной вирусом гриппа или респираторным синцитиальным вирусом (RSV).
Более того, шестой аспект изобретения относится к лекарственному средству согласно четвертому аспекту изобретения, где лекарственное средство является терапевтическим или профилактическим средством при артериосклерозе, утолщении интимы кровеносных сосудов, солидных опухолях, диабетической ретинопатии, суставном ревматизме, остановке сердца, ишемических реперфузионных нарушениях, спазмах сосудов мозга после субарахноидального кровотечения, стенокардии или инфаркте миокарда, вызванном спазмами коронарных сосудов, гломерулонефрите, тромбозе, болезни легких, вызванной отеком легких, сердечной аритмии, болезни глаз, повышенном внутриглазном давлении, глаукоме, глаукоматозной ретинопатии, оптической нейропатии или дегенерации желтого пятна.
Далее, седьмой аспект изобретения относится к лекарственному средству согласно четвертому аспекту изобретения, где лекарственное средство является терапевтическим или профилактическим средством при сепсисе.
Кроме того, восьмой аспект изобретения относится к фармацевтической композиции, содержащей производное дифенилсульфида согласно любому из аспектов изобретения (1)-(3) или его фармацевтически приемлемую соль или гидрат и фармацевтически приемлемый носитель.
Преимущества изобретения
Согласно настоящему изобретению может быть предложено производное дифенилсульфида, обладающее превосходным S1P3 антагонистическим действием и селективностью в отношении S1P3. Кроме того, производное дифенилсульфида настоящего изобретения может безопасно применяться в качестве лекарственного средства, поскольку оно вызывает слабый гемолиз, повреждение ткани или угнетение ЦНС, или не вызывает их. Кроме того, производное дифенилсульфида настоящего изобретения стабильно в водном растворе. Соединение настоящего изобретения, обладающее указанными превосходными свойствами, эффективно в качестве профилактики или терапии при сепсисе, сужении дыхательных путей, бронхиальной астме, хронической обструктивной болезни легких (ХОБЛ), эмфиземе легких, стенозе трахеи, диффузном панбронхиолите, бронхите в результате инфекции, болезни соединительной ткани или трансплантации, диффузном гамартоангиомиоматозе легких, респираторном дистресс-синдроме взрослых (РДСВ), интерстициальном пневмоните, раке легкого, гиперчувствительной пневмонии, идиопатической интерстициальной пневмонии, фиброзе легких, сепсисе или цитокиновом шторме при инфекции, вызванной вирусом гриппа или респираторным синцитиальным вирусом (RSV), артериосклерозе, утолщении интимы кровеносных сосудов, солидных опухолях, диабетической ретинопатии, ревматоидном артрите, остановке сердца, ишемических реперфузионных нарушениях, спазмах сосудов мозга после субарахноидального кровотечения, стенокардии или инфаркте миокарда, вызванном спазмами коронарных сосудов, гломерулонефрите, тромбозе, болезни легких, вызванной отеком легких, такой как РДСВ, сердечной аритмии, болезни глаз, повышенном внутриглазном давлении, глаукоме, глаукоматозной ретинопатии, оптической нейропатии и дегенерации желтого пятна.
Способ осуществления изобретения
В следующем описании определение функциональных групп в общих формулах может быть опущено при отсылке к уже приведенному определению. Указанные ссылочные определения относятся к определению, приведенному в следующем описании вариантов осуществления. Естественно, следует понимать, что такие ссылочные определения не относятся к определениям функциональных групп соединений, приведенных как предшествующий уровень техники.
"Атомом галогена", используемым в настоящем изобретении, является атом фтора, атом хлора, атом брома или атом йода.
Примеры "алкоксигруппы, содержащей 1-6 атомов углерода" включают метоксигруппу, этоксигруппу, н-пропоксигруппу, н-бутоксигруппу, изопропоксигруппу и трет-бутоксигруппу.
Далее, в настоящем изобретении, для получения превосходного S1P3 антагонистического действия и в целях безопасности для живого организма, R1 предпочтительно представляет собой алкоксигруппу, содержащую 1-6 атомов углерода, при этом этоксигруппы являются наиболее предпочтительными.
Кроме того, R2 предпочтительно представляет собой пропильную группу или аллильную группу.
Более того, X предпочтительно представляет собой метилен или атом кислорода, при этом атом кислорода является наиболее предпочтительным.
Кроме того, Z предпочтительно представляет собой атом галогена, при этом атом хлора является наиболее предпочтительным.
Примеры фармацевтически приемлемой соли в настоящем изобретении включают кислотно-аддитивную соль, такую как гидрохлоридная соль, гидробромидная соль, ацетатная соль, трифторацетатная соль, метансульфонатная соль, цитратная соль или тартратная соль, и аддитивную соль основания, такую как соль натрия, соль калия, соль кальция, соль магния или соль алюминия.
Из соединений, представленных общей формулой (1), соединение, в котором X представляет собой атом кислорода, в частности, соединение, представленное общей формулой (1d), может быть получено, например, на основе следующего способа синтеза A:
Формула 6
(где в формуле (1d) R1 представляет собой алкоксигруппу, содержащую 1-6 атомов углерода, R2 представляет собой пропильную группу или аллильную группу, и Z представляет собой атом галогена).
Способ синтеза A
Формула 7
В способе синтеза A оптически активное соединение, представленное общей формулой (4), может быть получено при взаимодействии оптически активного соединения, представленного общей формулой (2), с соединением, представленным общей формулой (3), в присутствии основания (стадия A-1):
Формула 8
(где в формуле (4) R3 представляет собой алкильную группу, содержащую 1-6 атомов углерода; и R2 является таким, как определено выше).
Формула 9
(где в формуле (2) R3 является таким, как определено выше).
Формула 10
(где в формуле (3), Aa представляет собой обычную уходящую группу, такую как атом галогена, метансульфонилоксигруппа, пара-толуолсульфонилоксигруппа или трифторметансульфонилоксигруппа; и R2 является таким, как определено выше).
В частности, сначала в реакционном растворителе, таком как 1,4-диоксан, тетрагидрофуран или диэтиловый эфир, соединение, представленное общей формулой (2), обрабатывают при -78°C с использованием основания. Затем соединение, представленное общей формулой (3), подвергают взаимодействию при -78°C с полученным анионом соединения, представленного общей формулой (2). Затем температуру постепенно повышают до нормальной температуры, с получением соединения, представленного общей формулой (4). Примеры основания, которое может использоваться в данной реакции, включают н-бутиллитий и диизопропиламид лития, при этом предпочтительным является н-бутиллитий.
В настоящем описании термин "нормальная температура" означает 15-25°C, как определено в Фармакопее Японии.
В способе синтеза A оптически активное соединение, представленное общей формулой (6), может быть получено при взаимодействии оптически активного соединения, представленного общей формулой (4), с соединением, представленным общей формулой (5), в присутствии основания (стадия A-2):
Формула 11
(где в формуле (6) Ab представляет собой обычную уходящую группу, такую как атом галогена, метансульфонилоксигруппа, пара-толуолсульфонилоксигруппа или трифторметансульфонилоксигруппа; и R2, R3 и Z являются такими, как определено выше).
Формула 12
(где в формуле (5) Ac представляет собой обычную уходящую группу, такую как атом галогена, метансульфонилоксигруппа, пара-толуолсульфонилоксигруппа или трифторметансульфонилоксигруппа; и Ab и Z являются такими, как определено выше).
В частности, сначала в реакционном растворителе, таком как 1,4-диоксан, тетрагидрофуран или диэтиловый эфир, соединение, представленное общей формулой (4), обрабатывают при -78°C с использованием основания. Затем соединение, представленное общей формулой (5), подвергают взаимодействию при -78°C с полученным анионом соединения, представленного общей формулой (4). Затем температуру постепенно повышают до нормальной температуры, с получением соединения, представленного общей формулой (6). Примеры основания, которое может использоваться в данной реакции, включают н-бутиллитий и диизопропиламид лития, при этом предпочтительным является н-бутиллитий.
В способе синтеза A соединение, представленное общей формулой (7), может быть получено при кислотном гидролизе соединения, представленного общей формулой (6), с последующей защитой аминогруппы стандартным защитным реагентом.
Формула 13
(где в формуле (7) R4 представляет собой обычную защитную группу для аминогруппы; и Ab, R2, R3 и Z являются такими, как определено выше).
R4 в формуле (7) специально не ограничен, при условии, что он защищает аминогруппу. Например, можно использовать ацильную группу, такую как ацетильная группа, или карбамат, такой как трет-бутоксикарбонил или бензилоксикарбонил (стадия A-3).
В частности, сначала в неорганической или органической кислоте, или в смешанном растворе неорганической или органической кислоты и воды или органического растворителя, соединение, представленное общей формулой (6), подвергают кислотному гидролизу при нормальной температуре. В данном случае, в качестве неорганической кислоты может быть использована хлористоводородная кислота, бромистоводородная кислота или подобные. В качестве органической кислоты может быть использована трифторуксусная кислота или подобные. Далее, в качестве органического растворителя может быть использован метанол, этанол, тетрагидрофуран, 1,4-диоксан, этилацетат или подобные. Из перечисленного, предпочтительно при проведении кислотного гидролиза используют водный раствор трифторуксусной кислоты.
Затем после нейтрализации основанием, с получением сложного аминоэфира, указанный аминоэфир и ацилхлорид или ангидрид кислоты подвергают взаимодействию при температуре от 0°C до нормальной температуры, в растворителе, с получением соединения, представленного общей формулой (7). Примеры растворителя, который может быть использован на данной стадии, включают этилацетат, тетрагидрофуран, N,N-диметилформамид, 1,4-диоксан, метиленхлорид, хлороформ, метанол, этанол и ацетонитрил. В качестве ацилхлорида может быть использован ацетилхлорид, бензилоксикарбонилхлорид или подобные. В качестве ангидрида кислоты может быть использован уксусный ангидрид, ди-трет-бутилдикарбонат или подобные. Из них предпочтительно проводить взаимодействие с использованием ди-трет-бутилдикарбоната.
В способе синтеза A, соединение, представленное общей формулой (8), может быть получено при восстановлении соединения, представленного общей формулой (7) (стадия A-4).
Формула 14
(где в формуле (8) Ab, R2, R4 и Z являются такими, как определено выше).
Например, в реакционном растворителе, таком как тетрагидрофуран, 1,4-диоксан, этанол, метанол или подобные, соединение, представленное общей формулой (7), восстанавливают с использованием восстановителя при температуре от 0°C до температуры кипения с обратным холодильником, и предпочтительно при нормальной температуре. Примеры восстановителя, который может быть использован, включают боран, производные алкилборанов, такие как 9-борабицикло[3.3.1]нонан (9-BBN), металлогидридные комплексы, такие как диизобутилалюминийгидрид ((iBu)2AlH), борогидрид натрия (NaBH4), борогидрид лития (LiBH4), алюмогидрид лития (LiAlH4) или подобные. Предпочтительно восстановителем является борогидрид лития.
В способе синтеза A соединение, представленное общей формулой (10), может быть получено при взаимодействии соединения, представленного общей формулой (8), и соединения, представленного общей формулой (9).
Формула 15
(где в формуле (10) R5 представляет собой атом водорода или обычную защитную группу для фенольной гидроксильной группы; и R1, R2, R4 и Z являются такими, как определено выше).
Формула 16
(где в формуле (9) R1 и R5 являются такими, как определено выше).
Обычная защитная группа для фенольной гидроксильной группы специально не ограничена, при условии, что она защищает фенольную гидроксильную группу. Например, может использоваться метильная группа, бензильная группа, метоксиметильная группа, тетрагидропиранильная группа, трет-бутилдиметилсилильная группа, ацетильная группа или трет-бутоксикарбонильная группа (стадия A-5).
Например, данная реакция может быть проведена в таком реакционном растворителе, как толуол, N,N-диметилформамид, 1,4-диоксан, тетрагидрофуран или диэтиловый эфир, в присутствии неорганического или органического основания, с использованием катализатора, при температуре от нормальной до температуры кипения с обратным холодильником. Примеры неорганических оснований, которые могут быть использованы, включают карбонат натрия или трет-бутоксид калия. Примеры органических оснований, которые могут быть использованы, включают диизопропилэтиламин. Далее, примеры катализатора, который может быть использован, включают соединения палладия, такие как трис(дибензилиденацетон)дипалладий (0) или ацетат палладия (II). Предпочтительно используют трис(дибензилиденацетон)дипалладий (0).
Соединение фосфина, такое как 4,5-бис(дифенилфосфино)-9,9-диметилксантен, бис[2-(дифенилфосфино)фениловый] эфир или 1,1'-бис(ди-трет-бутилфосфино)ферроцен, может быть добавлено к реакционному растворителю в качестве ускорителя реакции.
В способе синтеза A соединение, представленное общей формулой (12), может быть получено при взаимодействии соединения, представленного общей формулой (10), и соединения, представленного общей формулой (11) (стадия A-6).
Формула 17
(где в формуле (12) R1, R2, R3, R4, R5 и Z являются такими, как определено выше).
Формула 18
(где в формуле (11) R3 является таким, как определено выше).
Например, данная реакция может быть проведена в присутствии тетрабромида углерода и пиридина, без растворителя или с использованием такого растворителя, как метиленхлорид, хлороформ, ацетонитрил, этилацетат, тетрагидрофуран или диэтиловый эфир, при температуре от 0°C до нормальной температуры.
В способе синтеза A соединение, представленное общей формулой (1d), может быть получено при кислотном гидролизе или обработке соединения, представленного общей формулой (12), нуклеофильным реагентом, таким как триметилсилилбромид или триметилсилилиодид (стадия A-7).
Что касается реакции кислотного гидролиза, кислотный гидролиз может быть выполнен в неорганической кислоте, такой как хлористоводородная кислота или бромистоводородная кислота, или в смешанном растворе органического растворителя, такого как метанол или этанол, и неорганической кислоты, при температуре кипения с обратным холодильником. Далее, обработка с использованием нуклеофильного реагента может быть осуществлена при взаимодействии с триметилсилилбромидом или триметилсилилиодидом при температуре от 0°C до нормальной температуры, с использованием ацетонитрила или метиленхлорида в качестве предпочтительного реакционного растворителя. Альтернативно, обработка нуклеофильным реагентом может быть также осуществлена при взаимодействии с комбинацией триметилсилилхлорида и бромида натрия или комбинацией триметилсилилхлорида и йодида натрия.
В способе синтеза A соединение, представленное общей формулой (7), может быть также получено, например, на основе следующего способа синтеза B.
Способ синтеза B
Формула 19
В способе синтеза B оптически активное соединение, представленное общей формулой (14), может быть получено на основе такого же способа, как на стадии A-2, с использованием оптически активного соединения, представленного общей формулой (13), и соединения, представленного общей формулой (5) (стадия B-1).
Формула 20
(где в формуле (14), Ab, R3 и Z являются такими, как определено выше).
Формула 21
(где в формуле (13) R3 является таким, как определено выше).
В способе синтеза B оптически активное соединение, представленное общей формулой (15), может быть получено на основе такого же способа, как на стадии A-1, с использованием оптически активного соединения, представленного общей формулой (14), и соединения, представленного общей формулой (3) (стадия B-2).
Формула 22
(где в формуле (15), Ab, R2, R3 и Z являются такими, как определено выше).
В способе синтеза B соединение, представленное общей формулой (7), может быть получено на основе такого же способа, как на стадии A-3, с использованием соединения, представленного общей формулой (15) (стадия B-3).
В способе синтеза A соединение, представленное общей формулой (10), может быть получено, например, на основе следующего способа синтеза C.
Способ синтеза C
Формула 23
В способе синтеза C оптически активное соединение, представленное общей формулой (17), может быть получено на основе такого же способа, как на стадии A-2, с использованием оптически активного соединения, представленного общей формулой (4), и соединения, представленного общей формулой (16) (стадия C-1).
Формула 24
(где в формуле (17) R1, R2, R3, R5 и Z являются такими, как определено выше).
Формула 25
(где в формуле (16) R1, R5, Ac и Z являются такими, как определено выше).
В способе синтеза C соединение, представленное общей формулой (18), может быть получено на основе такого же способа, как на стадии A-3, с использованием соединения, представленного общей формулой (17) (стадия C-2).
Формула 26
(где в формуле (18) R1, R2, R3, R4, R5 и Z являются такими, как определено выше).
В способе синтеза C соединение, представленное общей формулой (10), может быть получено на основе такого же способа, как на стадии A-4, с использованием соединения, представленного общей формулой (18) (стадия C-3).
В способе синтеза C соединение, представленное общей формулой (18), может быть получено, например, на основе следующего способа синтеза D.
Способ синтеза D
Формула 27
В способе синтеза D, оптически активное соединение, представленное общей формулой (19), может быть получено на основе такого же способа, как на стадии A-2, с использованием оптически активного соединения, представленного общей формулой (13), и соединения, представленного общей формулой (16) (стадия D-1).
Формула 28
(где в формуле (19) R1, R3, R5 и Z являются такими, как определено выше).
В способе синтеза D оптически активное соединение, представленное общей формулой (20), может быть получено на основе такого же способа, как на стадии A-1, с использованием оптически активного соединения, представленного общей формулой (19), и соединения, представленного общей формулой (3) (стадия D-2).
Формула 29
(где в формуле (20) R1, R2, R3, R5 и Z являются такими, как определено выше).
В способе синтеза D соединение, представленное общей формулой (18), может быть получено на основе такого же способа, как на стадии A-3, с использованием соединения, представленного общей формулой (20) (стадия D-3).
В способе синтеза A из соединений, представленных общей формулой (10), соединение, в котором R1 представляет собой цианогруппу или ацетильную группу, и R5 представляет собой обычную защитную группу для фенола, в частности, соединение, представленное общей формулой (10a), может быть получено, например, согласно следующему способу синтеза E.
Формула 30
(где в формуле (10a) R1a представляет собой ацетильную группу или цианогруппу, и R5a представляет собой обычную защитную группу для фенольной гидроксильной группы; и R2, R4 и Z являются такими, как определено выше).
R5a специально не ограничен, при условии, что он защищает фенольную гидроксильную группу. Например, может быть использована метильная группа, бензильная группа, метоксиметильная группа, тетрагидропиранильная группа, трет-бутилдиметилсилильная группа, ацетильная группа или трет-бутоксикарбонильная группа.
Способ синтеза E
Формула 31
В способе синтеза E оптически активное соединение, представленное общей формулой (22), может быть получено на основе такого же способа, как на стадии A-5, с использованием оптически активного соединения, представленного общей формулой (8), и соединения, представленного общей формулой (21).
Формула 32
(где в формуле (22) R5b представляет собой обычную защитную группу для фенольной гидроксильной группы; и R2, R4 и Z являются такими, как определено выше).
Формула 33
(где в формуле (21) R5b является таким, как определено выше).
R5b специально не ограничен, при условии, что он защищает фенольную гидроксильную группу. Например, может быть использована метильная группа, бензильная группа, метоксиметильная группа, тетрагидропиранильная группа, трет-бутилдиметилсилильная группа, ацетильная группа или трет-бутоксикарбонильная группа (стадия E-1).
В способе синтеза E соединение, представленное общей формулой (23), может быть получено при защите фенольной гидроксильной группы соединения, представленного общей формулой (22) (стадия E-2).
Формула 34
(где в формуле (23) R2, R4, R5a, R5b и Z являются такими, как определено выше).
Данная реакция может быть проведена согласно любой методике, которая обычно используется для защиты фенольной гидроксильной группы. Например, реакция может быть проведена в таком растворителе, как ацетонитрил, тетрагидрофуран, N,N-диметилформамид, метиленхлорид или хлороформ, в присутствии неорганического или органического основания, при взаимодействии соединения, представленного общей формулой (22), с хлоридом или ацилхлоридом. В качестве неорганического основания могут быть использованы карбонат калия или подобные. В качестве органического основ