Способ определения рения (vii) в водных растворах методом инверсионной вольтамперометрии по пику селективного электроокисления меди из интерметаллического соединения rexcuy
Иллюстрации
Показать всеИзобретение относится к аналитической химии и может быть использовано для анализа вод различного происхождения: питьевые воды, геотермальные источники, смывы хвостов обогащения, а также технологические сливы. Способ определения рения (VII) в водных растворах методом инверсионной вольтамперометрии по пику селективного электроокисления меди из интерметаллического соединения RexCuy заключается в том, что рений осаждают на поверхности графитового электрода вместе с медью, образуя сплав, накопление ионов рения на графитовом электроде в перемешиваемом растворе в присутствии ионов меди (II) проводят в течение 120-180 секунд при потенциале электролиза минус 1,0 В из фонового электролита 1 М HCl с последующей регистрацией анодных пиков селективного электроокисления меди из сплава с рением при скорости развертки потенциала 10-20 мВ/с, концентрацию ионов рения определяют по току анодного пика селективного электроокисления меди в диапазоне потенциалов от -0,4 до -0,1 В отн. нас. х.с.э., используя метод добавок аттестованных смесей. Изобретение обеспечивает возможность количественно определять содержание ионов рения (VII) в интервале содержаний 0,01-1 мг/дм3 по пику селективного электроокисления меди из сплава с рением, полученного на стадии предварительного электроконцентрирования. 2 ил., 1 пр., 2 табл.
Реферат
Изобретение относится к аналитической химии, а именно к способам определения содержания ионов металлов, и может быть использовано для анализа вод различного происхождения (питьевые воды, геотермальные источники, смывы хвостов обогащения), а также технологических сливов методом инверсионной вольтамперометрии (ИВ).
Известен метод полярографического определения рения (VII), впервые изученный в растворах кислот (HCl, H2SO4, H2SO4) и нейтральных растворах (KCl, фосфатном буфере). Определяемая концентрация рения (VII), использованная в исследованиях, составляла 1·10-3 M [Lingan J.J. / J. Am. Chem. Soc. 64, 1001 (1942); Lingan J.J. // J. Am. Chem. Soc. 64, 2182 (1942)]. Недостатком метода является низкая чувствительность и использование больших количеств металлической ртути в ходе полярографических определений рения (VII) в растворе.
Известна методика определения рения (VII) в сернокислых и гидроксонатриевых растворах. Показано, что число волн восстановления и их характер меняются в зависимости от концентрации H2SO4. Потенциал полуволны (E1/2) для рения (VII) в 3,5 M H2SO4 меняется от 0,2 до -0,45 В. В 2 M растворе щелочи E1/2 для рения (VII) равен -1,4 В. Определяемая концентрация рения составляет 1·10-4 M [Geyer R. // Ζ. anorg. u. allgem. Chem., 263, 47 (1950)]. Недостатком методики является низкая чувствительность определяемых содержаний рения; использование металлической ртути, пары которой являются токсичными. При определении рения данным методом мешают анионы Cl-, , , а также ионы металлов Mo, Fe и Ti.
Известен способ восстановления перренат-иона на ртутно-капельном катоде. Величина диффузионного тока в 4 M растворе HClO4 прямо пропорциональна концентрации в растворе в интервале от 1·10-4 до 1·10-3 М. В 2 M и 4,2 M растворах HCl E1/2 равны соответственно -0,45 В и -0,31 В (относительно н.к.э.). [Rulfs C.L., Elving P.J. // J. Am. Chem. Soc. 73, 3284 (1951)]. Недостатком способа является низкая чувствительность определяемых содержаний рения и использование металлической ртути, пары которой ядовиты.
Известна методика определения малых концентраций рения в нейтральных, щелочных и буферных растворах. На скорость каталитического выделения водорода существенное влияние оказывает pH раствора и буферная емкость раствора. В исследованиях использовался ртутно-капельный электрод, а вспомогательным и электродом сравнения служили насыщенные каломельные электроды. Предельный ток достигает максимального значения в интервале pH 7-9. Концентрация перренат-иона, использованная в исследованиях, составляла 8·10-5 моль/л [Рубинская Т.Я., Майрановский С.Г. О восстановлении перренат-иона на ртутном капельном электроде в щелочных и нейтральных средах // Электрохимия, 1971, Т. 7, №10, С. 1403-1408]. Недостатком методики является существенное влияние pH раствора и его буферная емкость. Низкая чувствительность, каталитические волны, пригодные для аналитических целей, находятся в сильно отрицательной области потенциалов -1,6 В, а также использование в анализе высокотоксичного ртутно-капающего электрода.
Известен метод определения рения на фоне раствора NaCl с Na2SO3 (pH=11,3-11,5) E1/2=-0,45 В. Открываемый минимум равен 1·10-5 М. Определение проводят также после подготовки пробы, в ходе которой рений отделяют от молибдена, вольфрама и других сопутствующих элементов [Duca A., Stanescu D., Puscasu M. Studii si cercetari chim. Acad. RPR Fil. Cluj, 6, 123 (1955); 13, 197 (1962)]. При растворении проб, содержащих рений, используется азотная кислота, а нитрат-ионы мешают определению, поэтому необходимо удалять оксиды азота.
Известна методика (прототип), где использовался ртутно-капающий электрод. В качестве фонового электролита использовали раствор, состоящий из 3 M по NH3, 3 M по KSCN, 3 M по ЭДТА и 0,16 M по Na2SO3. Предел обнаружения рения по данному методу составил 0,05 мг/л (2,5·10-7), что позволяет при навеске 2 г и конечном объеме 10 мл определять от 2·10-5% рения. Метод обладает высокой селективностью. Определению не мешает большинство элементов: Mo, W, Fe, Cd, Zn, Sb, Bi, Ag, Al. Полярографирование проводят от -1,0 до -1,5 В [Васильева Л.И., Семенова И.Α., Юстус З.Л. Полярографическое определение рения в сложных продуктах цветной металлургии // Журнал аналитической химии. 1986, т. 41, №2, с. 293-297] (прототип). Недостатком методики является использование ртути. В качестве фонового электролита используется сложный по составу фон, который готовится в день использования. Метод, обладая высокой селективность, однако, уступает в чувствительности определения рения другим методам.
Задача изобретения: разработать методику определения рения (VII) методом инверсионной вольтамперометрии, используя электроконцентрирование рения в сплавы с медью на поверхность графитового электрода с последующим селективным электроокислением меди из интерметаллического соединения с рением.
Электроконцентрирование рения и меди на поверхность графитового электрода проводят при потенциале минус 1 В из фонового электролита 1 M HCl в течение 120-180 секунд с последующей регистрацией анодных пиков электроокисления меди и селективного электроокисления меди из интерметаллического соединения с рением при скорости развертки потенциала 10-20 мВ/с. Концентрацию ионов рения (VII) определяют по току анодного пика селективного электроокисления меди из сплава с рением, наблюдаемого в области потенциалов от -0,4 до -0,1 В отн. нас. х.с.э.
Для количественной оценки содержания рения (VII) используют метод добавок аттестованных смесей. Новым в способе является то, что для получения полезного сигнала, зависящего от концентрации ионов рения (VII) в растворе, используется процесс селективного электроокисления меди из сплава с рением.
В предлагаемом способе впервые установлена способность меди селективно окисляться из сплава с рением при другом потенциале, чем чистая медь. В качестве индикаторного применяли ГЭ, модифицированный медью (в прототипе применяли ртутно-капающий электрод). Использование таких электродов обусловлено высокой химической и электрохимической устойчивостью графита, широкой областью рабочих потенциалов, а также простотой механического обновления поверхности и требованиям техники безопасности. Нижняя граница определяемых содержаний по данному методу составила 0,01 мг/дм3.
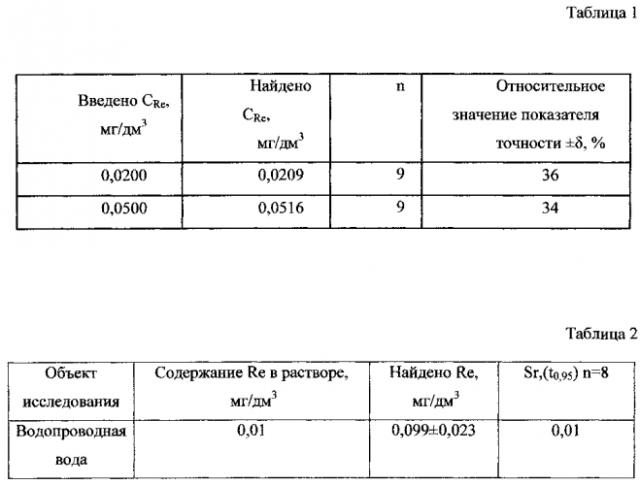
Результаты определения рения из сплава с медью в фоновом электролите 1M HCl с добавкой рения (VII) приведены в таблице 1. Результаты определения рения (VII) в водопроводной воде приведены в таблице 2. Правильность определения рения (VII) оценивалась методом «введено-найдено».
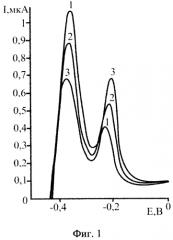
Методика определения рения (VII) в водопроводной воде. Для удаления органических ионов проводят их разрушение путем облучения раствора УФ в течение 1 минуты в присутствии 1 М HCOOH. Электроконцентрирование сплава рения и меди на поверхность графитового электрода проводят в перемешиваемом растворе 1 M HCl, содержащем ионы рения (VII) и меди (VII) в течение 120-180 с при потенциале электролиза минус 1,0 В. Снимают вольт-амперную кривую электроокисления осадка при скорости развертки потенциала 10-20 мВ/с. Концентрацию ионов рения (VII) определяют по высоте анодного пика меди в диапазоне потенциалов от -0,4 до -0,1 В относительно насыщенного хлоридсеребряного электрода (нас. х.с.э). На фиг. 1 представлены вольт-амперные кривые электроокисления меди из сплава с рением. Кривая 1 - фон 1М HCl+CCu(II)=0,2 мг/дм3 и CRe(VII)=0,02 мг/дм3, кривая 2 - фон 1М HCl+CCu(II)=0,2 мг/дм3 и CRe(VII)=0,04 мг/дм3, кривая 3 - фон 1М HCl+CCu(II)=0,2 мг/дм3 и CRe(VII)=0,06 мг/дм3.
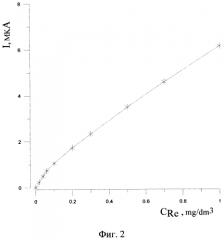
Таким образом, установленные условия впервые позволили количественно определять содержание ионов рения (VII) в интервале содержаний 0,01-1 мг/дм3 по пику селективного электроокисления меди из сплава с рением, полученного на стадии предварительного электроконцентрирования (фиг. 2).
Примеры конкретного выполнения.
Пример 1 (фиг. 1). Измерения были проведены на искусственных смесях. 10 мл фонового электролита (1 М HCl) помещают в кварцевый стаканчик. Не прекращая перемешивания, проводят электролиз раствора, при Eэ=-1,0 В и при τэ=120 с, снимают вольт-амперную кривую электроокисления при скорости развертки 20 мВ/с. Затем добавляют аттестованный раствор Cu (II) 0,02 мл из 100 мг/дм3 и проводят электрохимическое концентрирование осадка при аналогичных условиях. Вносят добавку стандартного образца рения 0,02 мл из 10 мг/дм3, регистрируют аналитический сигнал рения при потенциале накопления -1,0 В. Затем вносят еще одну добавку стандартного образца рения 0,02 мл из 10 мг/дм3 и регистрируют аналитический сигнал рения при аналогичных условиях. По разнице токов пиков меди вычисляют концентрацию рения в растворе. Пик тока меди регистрируют в диапазоне потенциалов от -0,4 до -0,1 В (нас. х.с.э.).
Пример 2. Измерения рения были проведены в водопроводной воде (таблица 2). 100 мл раствора помещают в коническую колбу и выпаривают до минимального объема. Количественно переносят раствор в кварцевый стакан объемом 20 мл и добавляют 37% HCl, чтобы в 10 мл водного раствора концентрация по соляной кислоте составила 1 М, для перевода солей рения в хлориды.
Снимают фоновую кривую: 10 мл фонового электролита (1 М HCl) помещают в кварцевый стаканчик, добавляют аттестованный раствор Cu (II) 0,02 мл из 100 мг/дм3, не прекращая перемешивания, проводят электролиз раствора, при Eэ=-1,0 В и при τэ=120 с, снимают вольт-амперную кривую электроокисления при скорости развертки 20 мВ/с.
Добавляют аликвотную часть 1-2 мл полученного раствора и снимают вольт-амперную кривую электроокисления при потенциале накопления -1,0 В. Затем вносят добавку стандартного образца рения 0,02 мл из 10 мг/дм3 и регистрируют аналитический сигнал при потенциале накопления -1,0 В. По разнице токов пиков меди вычисляют концентрацию рения в растворе. Пик тока меди регистрируют в диапазоне потенциалов от -0,4 до -0,1 В (нас. х.с.э.).
Таким образом, впервые установлена способность количественного анализа рения по пикам селективного электроокисления меди из интерметаллического соединения RexCuy.
Предложенный способ может быть использован для определения рения в водных растворах.
Способ определения рения (VII) в водных растворах методом инверсионной вольтамперометрии по пику селективного электроокисления меди из интерметаллического соединения RexCuy, заключающийся в том, что рений осаждают на поверхности графитового электрода вместе с медью, образуя сплав, накопление ионов рения на графитовом электроде в перемешиваемом растворе в присутствии ионов меди (II) проводят в течение 120-180 секунд при потенциале электролиза минус 1,0 В из фонового электролита 1 М HCl с последующей регистрацией анодных пиков селективного электроокисления меди из сплава с рением при скорости развертки потенциала 10-20 мВ/с, концентрацию ионов рения определяют по току анодного пика селективного электроокисления меди в диапазоне потенциалов от -0,4 до -0,1 В отн. нас. х.с.э., используя метод добавок аттестованных смесей.