Применение инсулин-сенсибилизирующих агентов, вводимых интравагинально
Иллюстрации
Показать всеГруппа изобретений относится к медицине, а именно к гинекологии и эндокринологии, и может быть использована для лечения синдрома поликистозных яичников, гиперандрогении яичникового происхождения и/или связанных расстройств. Применение по изобретению включает инсулин-сенсибилизирующий агент для изготовления вагинального лекарственного средства. Способы по изобретению включают вагинальное введение инсулин-сенсибилизирующего агента. Фармацевтические составы по изобретению содержат инсулин-сенсибилизирующий агент для вагинального введения. Использование изобретений позволяет снизить уровень тестостерона в плазме крови, уменьшить количество атретических фолликулов путем прямого воздействия на ткань яичников при снижении системных побочных эффектов. 6 н. и 7 з.п. ф-лы, 5 табл., 2 ил., 1 пр.
Реферат
Область техники
Настоящее изобретение относится к применению вагинальных инсулин-сенсибилизирующих агентов для профилактики и/или лечения яичниковой гиперандрогении и/или синдрома поликистозных яичников, и/или связанных расстройств.
Предшествующий уровень техники
В общих чертах, гиперандрогения представляет собой любое клиническое или лабораторное проявление избытка андрогенов у женщин. Наиболее частым клиническими проявлением гиперандрогении у женщин репродуктивного возраста является гирсутизм или акне с симптомами ановуляции или без них, такими как аменорея или дисфункциональное маточное кровотечение.
Гиперандрогения у женщин репродуктивного возраста может иметь пять разных причин:
- синдром поликистозных яичников;
- идиопатический гирсутизм;
- недостаточность ферментов в синтезе стероидных гормонов;
- андроген-секретирующие опухоли;
- другие эндокринные нарушения, такие как синдром Кушинга и т.д.
Тем не менее, большинство женщин с симптомами гиперандрогении страдают от синдрома поликистозных яичников (80%).
Синдром поликистозных яичников (или СПКЯ, также называемый синдромом Штейна-Левенталя) представляет собой репродуктивную и гормональную проблему, которая наиболее часто поражает женщин репродуктивного возраста. Согласно оценкам, приблизительно 5% женщин
страдают от данного расстройства.
Согласно Американскому обществу репродуктивной медицины, СПКЯ определяют по наличию любых двух следующих характеристик:
- отсутствие овуляции в течение длительного периода времени;
- высокие уровни андрогенов;
- большое количество мелких кист в яичниках.
Признаки и симптомы СПКЯ связаны с гиперандрогенией и могут включать:
- гирсутизм, акне и выпадение волос;
- избыточный вес или ожирение, особенно в области талии и живота;
- нерегулярные, спорадические менструации или их отсутствие;
- крупные и/или поликистозные яичники;
- бесплодие.
Кроме того, женщины с СПКЯ подвержены более высокому риску развития определенных проблем со здоровьем, включая:
- метаболический синдром: расстройство с несколькими компонентами, среди которых сахарный диабет типа 2 или резистентность к инсулину, высокие уровни холестерина, высокое кровяное давление (особенно вокруг талии и живота), высокие уровни С-реактивного белка и высокие уровни факторов свертывания крови;
- чрезмерное утолщение выстилки эндометрия, обильное или нерегулярное кровотечение и рак эндометрия.
Таким образом, СПКЯ оказывает важное влияние на систему здравоохранения и вызывает беспокойство у женщин, страдающих от него.
Фармакологическое лечение гиперандрогении направлено на устранение связанных с ней симптомов путем уменьшения уровней в сыворотке крови и/или периферического действия андрогенов. Оно должно поддерживаться в течение длительного времени, и удовлетворительные клинические эффекты обычно появляются в течение нескольких месяцев.
Оказалось, что некоторые лекарственные средства, разрешенные для лечения сахарного диабета типа 2, известные как инсулин-сенсибилизирующие агенты, обладают полезным эффектом у пациентов с СПКЯ.
Метформин (N,N-диметилимидодикарбоимиддиамид, Глюкофаж® (Glucophage®)), инсулин-сенсибилизирующий агент бигуанидового типа, доступен для лечения СПКЯ.
Метформин уменьшает клинические признаки гиперандрогении и корректирует нарушения менструального цикла. Если метформин в одиночку не восстанавливает овуляцию, он может улучшать реакцию женщины на фармацевтические продукты при лечении бесплодия. Обычная пероральная доза составляет от 500 до 2500 мг/сутки.
Розиглитазон (Авандия® (Avandia®)) и Пиоглитазон (Актос® (Actos®)), относящиеся к группе тиазолидиндионовых инсулин-сенсибилизирующих агентов, также доступны в Соединенных Штатах для лечения женщин с СПКЯ. Тиазолидиндионы продемонстрировали уменьшение гиперандрогении и восстановление овуляции у некоторых пациентов. Рекомендуемая пероральная доза составляет от 4 до 8 мг/сутки для розиглитазона и от 15 до 30 мг/сутки для пиоглитазона.
Краткое описание изобретения
Однако инсулин-сенсибилизирующие агенты могут вызывать некоторые побочные эффекты при введении перорально, некоторые из которых являются очень серьезными.
В случае метформина наиболее распространенным побочным эффектом, который может приводить к прекращению лечения, является раздражение желудочно-кишечного тракта, что происходит в 5-20% случаев. Диарея представляет собой самый распространенный симптом, сопровождающийся рвотой, болью в животе и неприятным привкусом во рту. Лактацидоз представляет собой редкий, но серьезный побочный эффект, вызываемый данным лекарственным средством.
В случае тиазолидиндионов гепатотоксичность представляет собой редкий эффект, вызывающий сильное беспокойство. При применении данных фармацевтических препаратов необходимо регулярно проводить функциональные пробы печени. Их применение не рекомендуется у пациентов с признаками заболевания печени.
В ходе лечения данными фармацевтическими препаратами может происходить задержка жидкости, которая может усугублять или вызывать застойную сердечную недостаточность. При наблюдении ухудшения сердечной функции необходимо прекратить лечение.
С другой стороны, применение розиглитазона было связано с более высоким риском явлений миокардиальной ишемии. Его применение не рекомендуется у пациентов с ишемической кардиопатией и/или заболеванием периферических артерий.
Также сообщали о случаях возникновения или ухудшения диабетического отека желтого пятна со снижением остроты зрения в ходе лечения данными фармацевтическими препаратами.
У женщин также должен быть учтен риск длительных переломов, связанных с лечением тиазолидиндионами.
Авторы настоящего изобретения обнаружили, что вагинальное введение инсулин-сенсибилизирующих агентов неожиданным образом позволяет достигать достаточных уровней лекарственного средства в яичниках и оказывать терапевтические эффекты при значительном уменьшении системного воздействия, а следовательно, их неблагоприятных эффектов.
Неожиданно оказалось, что данные агенты оказывают антиандрогенное действие без необходимости опосредованного системного действия - за счет повышения чувствительности к инсулину, - но путем прямого действия на клетки яичников.
В частности, авторы настоящего изобретения установили, что вагинальное введение метформина значительно снижает уровни тестостерона (андрогенного гормона) в плазме крови. Подобным образом, авторы настоящего изобретения наблюдали уменьшение атретических (атрофированных) фолликулов в поликистозных яичниках.
Следовательно, вагинальное введение инсулин-сенсибилизирующих агентов может быть полезным при профилактике и/или лечении СПКЯ как у пациентов с высокими уровнями андрогенов (вследствие их влияния на концентрацию тестостерона в плазме крови), так и у пациентов с нормальными уровнями андрогенов (вследствие их прямого действия на ткань яичников).
Оно также может быть подходящим при профилактике и/или лечении других гиперандрогенных состояний, которые возникают при высоких уровнях андрогенов в плазме крови, а также связанных расстройств, таких как гирсутизм, акне и/или выпадение волос.
Следовательно, первый аспект настоящего изобретения относится к вагинальному применению инсулин-сенсибилизирующих агентов для профилактики и/или лечения синдрома поликистозных яичников, и/или гиперандрогенных состояний яичникового происхождения, и/или связанных расстройств.
Второй аспект относится к фармацевтическим составам для вагинального введения, содержащим по меньшей мере один инсулин-сенсибилизирующий агент, для профилактики и/или лечения синдрома поликистозных яичников, и/или гиперандрогенных состояний яичникового происхождения, и/или связанных расстройств.
Третий аспект настоящего изобретения относится к способу предупреждения и/или лечения синдрома поликистозных яичников, и/или гиперандрогенных состояний яичникового происхождения, и/или связанных расстройств, включающему вагинальное введение фармацевтического состава, содержащего по меньшей мере один инсулин-сенсибилизирующий агент.
Краткое описание графических материалов
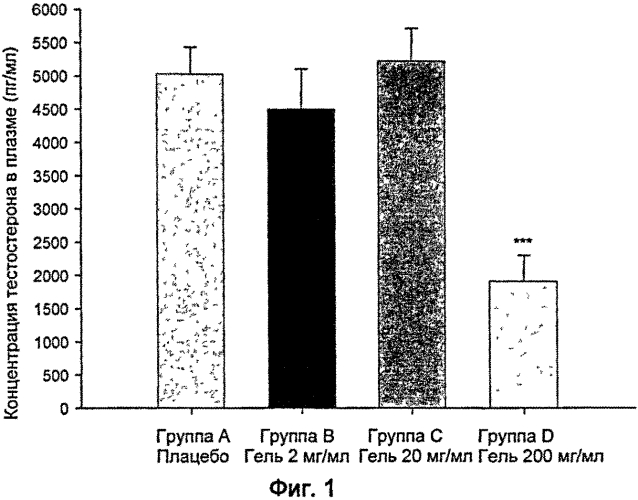
Фиг. 1: Концентрация тестостерона в плазме крови.
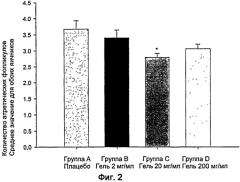
Фиг. 2: Средняя гистологическая оценка обоих яичников (количество атретических фолликулов).
Подробное описание изобретения
Согласно одному воплощению, настоящее изобретение относится к применению метформина или тиазолидиндиона для профилактики и/или лечения синдрома поликистозных яичников.
Согласно другому конкретному воплощению, настоящее изобретение относится к применению метформина или тиазолидиндиона для профилактики и/или лечения других гиперандрогенных состояний яичникового происхождения с высокими уровнями андрогенов в плазме крови.
Настоящее изобретение относится к применению указанных фармацевтических препаратов для профилактики и/или лечения расстройств, связанных с гиперандрогенными состояниями яичникового происхождения, таких как гирсутизм, акне и/или выпадение волос.
Составы инсулин-сенсибилизирующего агента согласно настоящему изобретению могут быть представлены в любой лекарственной форме, подходящей для вагинального введения, например, такой как твердое вещество, полужидкое вещество или жидкость.
Данные составы будут содержать терапевтически эффективное и нетоксичное количество по меньшей мере одного инсулин-сенсибилизирующего агента или одной из его фармацевтически приемлемых солей или пролекарств совместно с по меньшей мере одним фармацевтически приемлемым наполнителем. Наполнители могут быть выбраны из любых наполнителей, известных специалисту в данной области техники, и должны быть подходящими для лекарственной формы, которую требуется изготовить.
Фармацевтические составы согласно настоящему изобретению могут содержаться в любом устройстве, подходящем для вагинального введения, например кольце или пессарии. Материалы для применения в изготовлении указанного устройства могут быть выбраны из любых материалов, известных специалисту в данной области техники, которые являются фармацевтически приемлемыми.
Количество инсулин-сенсибилизирующего агента, которое следует вводить при вагинальном применении для безопасного и эффективного лечения яичниковой гиперандрогении, и/или СПКЯ, и/или родственных расстройств, зависит от многих факторов, включая возраст и состояние пациента, тяжесть заболевания или расстройства, частоту введения состава и т.д.
Согласно конкретному воплощению настоящего изобретения, доза метформина, которую следует вводить при вагинальном применении, будет составлять от 0,01 мг/сутки до 1000 мг/сутки; предпочтительно от 0,1 мг/сутки до 100 мг/сутки; более предпочтительно от 0,5 до 50 мг/сутки, от 1 до 10 мг/сутки.
ПРИМЕР
Следующий тест иллюстрирует настоящее изобретение и не ограничивает объем настоящей заявки.
Цель исследования заключалась в оценке влияния метформина в модели синдрома поликистозных яичников (СПКЯ), индуцированного дегидроэпиандростероном (ДГЭА), у крыс.
Экспериментальный метод
Тестируемые составы представляли собой:
- Гели с Метформином в концентрации, составляющей 2 мг/мл (FT-147), 20 мг/мл (FT-148) и 200 мг/мл (FT-149).
- Гель без Метформина (Плацебо; FT-150).
Указанные гели получали в соответствии со следующими формулами:
| гель 2 мг/мл | гель 20 мг/мл | гель 200 мг/мл | |
| (FT-147) | (FT-148) | (FT-149) | |
| Метформин | 0,1 г | 1 г | 10 г |
| Метилпарабен натрия | 34,3 мг | 34,3 мг | 34,3 мг |
| Лимонная кислота | 1 г | 1 г | 1 г |
| 40% Гидроксид натрия | дост. кол-во, приблизит.pH=5,5 | дост. кол-во, приблизит.pH=5,5 | дост. кол-во, приблизит.pH=5,5 |
| Натросол (Natrosol) | 0,85 г | 0,85 г | 0,85 г |
| Вода | дост. кол-во 50 г | дост. кол-во 50 г | дост. кол-во 50 г |
Использовали 2-3-недельных самок крыс линии Sprague-Dawley.
Животные оставались на карантине в течение 7 дней в тех же условиях, в которых проводили исследование. Определяли их массу после их поступления в лабораторию и каждый день после этого до введения исследуемых веществ и ДГЭА.
Животных держали в клетках из поликарбоната 255×405×197 мм с подстилкой из опилок.
Животных делили на группы по 5 животных в каждой клетке, выбранных случайным образом, и содержали в условиях с контролем температуры (22±2°C), светового периода (12/12 ч свет/темнота), давления воздуха, числа возобновлений и относительной влажности (30-70%).
Животным давали стандартную пищу для грызунов и обеспечивали неограниченный доступ к питьевой воде.
В указанном исследовании использовали четыре экспериментальные группы по 8 животных в каждой:
Группа А: Контроль=Плацебо+ДГЭА
Группа В: Доза 1 исследуемого вещества (0,016 мг/животное)+ДГЭА
Группа С: Доза 2 исследуемого вещества (0,16 мг/животное)+ДГЭА
Группа D: Доза 3 исследуемого вещества (1,6 мг/животное)+ДГЭА
Каждую дозу для животного рассчитывали исходя из концентрации каждого состава и вводимого объема.
Доза 1: состав 2 мг/мл с введением 8 мкл/животное=0,016 мг/животное Доза 2: состав 20 мг/мл с введением 8 мкл/животное=0,16 мг/животное Доза 3: состав 200 мг/мл с введением 8 мкл/животное=1,6 мг/животное.
Исследуемое вещество (дозы, составляющие 0,016, 0,16 и 1,6 мг/животное) и контрольное вещество вводили интравагинально в виде водного геля в объеме, равном 8 мкл/животное.
Перед введением получали раствор ДГЭА в масле семян кунжута и вводили его путем подкожной инъекции в кожную складку в задней грудной области (дорсальная) в объеме, составляющем 0,2 мл.
Введение исследуемого или контрольного вещества начинали в день 0 в дозе, указанной в пункте 7.1.
Также в день 0 сразу после введения исследуемого или контрольного вещества каждому животному вводили путем подкожной инъекции ДГЭА (6 мг/100 г массы тела /0,2 мл кунжутного масла).
Данный режим повторяли с дня 0 по день 14 (всего в течение 15 дней лечения).
У каждого животного забирали образцы крови в день 15 (через 24 часа после последнего лечения) путем пункции брюшной полой вены (с антикоагулянтом гепарином натрия) под анестезией (пентобарбитал натрия).
Из каждого образца крови путем центрифугирования при 5000 g в течение 5 минут получали плазму, которую замораживали для дальнейшей оценки (количественные определения) уровней тестостерона с помощью коммерческих наборов для иммуноанализа (ИФА) для крыс.
После забора крови каждое животное умерщвляли путем смещения шейных позвонков и извлекали оба яичника. Определяли их массу и фиксировали в забуференном формалине для последующей гистологической оценки (путем окрашивания гематоксилином и эозином).
Исследовали три гистологических среза из каждого яичника, взятые из трех репрезентативных областей каждого яичника (начало, центр и конец), определяя количество атретических (атрофических) фолликулов. Фолликул считается атретическим, если наблюдается один из следующих признаков: пикноз тучных клеток, тучные клетки присутствуют в фолликулярной жидкости, гипертрофия текальных клеток.
Результаты
А. Концентрация тестостерона в плазме крови.
Концентрации тестостерона в образцах плазмы крови всех животных определяли в конце исследования (15 День). Результаты представлены в Таблице 1:
| Таблица 1 | |||||||
| Концентрация тестостерона в плазме крови | |||||||
| Исследование FCI/07/05FT - УРОВНИ ТЕСТОСТЕРОНА В ПЛАЗМЕ КРОВИ | |||||||
| ГРУППА A | ГРУППА B | ГРУППА C | ГРУППА D | ||||
| животное | тестостерон (пг/мл) | животное | тестостерон (пг/мл) | животное | тестостерон (пг/мл) | животное | тестостерон (пг/мл) |
| A1 | 3128 | B1 | 2300 | C1 | 6072 | D1 | 2576 |
| A2 | 6164 | B2 | 5474 | C2 | 3450 | D2 | 2622 |
| A3 | 4876 | B3 | 6578 | C3 | 4462 | D3 | 2990 |
| A4 | 3956 | B4 | 2714 | C4 | 3818 | D4 | 736 |
| A5 | 5244 | B5 | 6486 | C5 | 7406 | D5 | 598 |
| A6 | 6670 | B6 | 5336 | C6 | 4554 | D6 | 1518 |
| A7 | 5474 | B7 | 4048 | C7 | 5428 | D7 | 3404 |
| A8 | 4692 | B8 | 3036 | C8 | 6578 | D8 | 828 |
| СРЕД. ЗНАЧЕ НИЕ | 5025,5 | СРЕД. ЗНАЧЕ НИЕ | 4496,5 | СРЕД. ЗНАЧЕ НИЕ | 5221 | СРЕД. ЗНАЧ ЕНИЕ | 1909,000 |
В. Гистологическая оценка
Исследовали три гистологических среза из каждого яичника, взятые из 3 репрезентативных областей (начало, центр и конец), определяя количество атретических фолликулов. Полученные результаты суммированы в Таблицах 2-5:
| Таблица 2 | ||||||||
| Гистологическая оценка яичников животных в группе A | ||||||||
| ИССЛЕДОВАНИЕ FCI/07/05FT - ГИСТОЛОГИЯ | ||||||||
| ГРУППА А | ||||||||
| КОЛИЧЕСТВО АТРЕТИЧЕСКИХ ФОЛЛИКУЛОВ, левый яичник | КОЛИЧЕСТВО АТРЕТИЧЕСКИХ ФОЛЛИКУЛОВ, правый яичник | Среднее значение Атретические фолликулы. Оба яичника | ||||||
| ЖИВОТНОЕ | Срез 1 | Срез 2 | Срез 3 | ЖИВОТНОЕ | Срез 1 | Срез 2 | Срез 3 | |
| А1 | 2 | 3 | 5 | A1 | 1 | 2 | 3 | 2,67 |
| А2 | 2 | 4 | 5 | A2 | 3 | 6 | 7 | 4,50 |
| A3 | 1 | 7 | 3 | A3 | 3 | 5 | 5 | 4,00 |
| А4 | 2 | 2 | 3 | A4 | 2 | 3 | 3 | 2,50 |
| А5 | 6 | 2 | 2 | A5 | 6 | 5 | 4 | 4,17 |
| А6 | 3 | 3 | 2 | A6 | 3 | 6 | 5 | 3,67 |
| А7 | 1 | 5 | 8 | A7 | 1 | 4 | 6 | 4,17 |
| А8 | 2 | 3 | 5 | A8 | 2 | 4 | 6 | 3,67 |
| Среднее количество атретических фолликулов, оба яичника | 3,67 |
| Таблица 3 | ||||||||
| Гистологическая оценка яичников животных в группе В | ||||||||
| ИССЛЕДОВАНИЕ FCI/07/05FT-ГИСТОЛОГИЯ | ||||||||
| ГРУППА В | ||||||||
| Количество атретических фолликулов левый яичник | Количество атретических фолликулов, правый яичник | Среднее значение Атретические фолликулы. Оба яичника | ||||||
| ЖИВОТНОЕ | Срез 1 | Срез 2 | Срез 3 | ЖИВОТНОЕ | Срез 1 | Срез 2 | Срез 3 | |
| В1 | 5 | 4 | 4 | В1 | 2 | 4 | 6 | 4,17 |
| В2 | 3 | 6 | 6 | В2 | 2 | 4 | 2 | 3,83 |
| В3 | 4 | 5 | 3 | В3 | 5 | 5 | 5 | 4,50 |
| В4 | 5 | 4 | 0 | В4 | 2 | 3 | 4 | 3,00 |
| В5 | 3 | 4 | 5 | В5 | 3 | 3 | 2 | 3,33 |
| В6 | 3 | 3 | 4 | В6 | 1 | 2 | 4 | 2,83 |
| в7 | 1 | 3 | 1 | В7 | 2 | 6 | 4 | 2,83 |
| В8 | 1 | 1 | 4 | В8 | 3 | 3 | 4 | 2,67 |
| Среднее количество атретических фолликулов, оба яичника | 3,40 |
| Таблица 4 | ||||||||
| Гистологическая оценка яичников животных в группе В | ||||||||
| ИССЛЕДОВАНИЕ FCI/07/05FT - ГИСТОЛОГИЯ | ||||||||
| ГРУППА С | ||||||||
| Количество атретических фолликулов, левый яичник | Количество атретических фолликулов, правый яичник | среднее значение Атретические фолликулы. Оба яичника | ||||||
| ЖИВОТНОЕ | Срез 1 | Срез 2 | Срез 3 | ЖИВОТНОЕ | Срез 1 | Срез 2 | Срез 3 | |
| C1 | 2 | 2 | 2 | C1 | 4 | 4 | 3 | 2,83 |
| C2 | 2 | 4 | 5 | C2 | 3 | 2 | 2 | 3,00 |
| C3 | 2 | 2 | 2 | C3 | 2 | 4 | 4 | 2,67 |
| C4 | 3 | 3 | 3 | C4 | 2 | 4 | 1 | 2,67 |
| C5 | 2 | 2 | 4 | C5 | 1 | 5 | 4 | 3,00 |
| C6 | 2 | 2 | 5 | C6 | 2 | 3 | 2 | 2,67 |
| C7 | 3 | 3 | 2 | C7 | 1 | 2 | 2 | 2,17 |
| C8 | 2 | 5 | 3 | C8 | 3 | 3 | 4 | 3,33 |
| Среднее количество атретических фолликулов оба яичника | 2,79 |
| Таблица 5 | ||||||||
| Гистологическая оценка яичников животных в группе D | ||||||||
| ИССЛЕДОВАНИЕ FCI/07/05FT - ГИСТОЛОГИЯ | ||||||||
| ГРУППА D | ||||||||
| Количество атретических фолликулов, левый яичник | Количество атретических фолликулов, правый яичник | Среднее значение Атретические фолликулы. Оба яичника | ||||||
| ЖИВОТНОЕ | Срез 1 | Срез 2 | Срез 3 | ЖИВОТНОЕ | Срез 1 | Срез 2 | Срез 3 | |
| D1 | 2 | 2 | 3 | D1 | 2 | 5 | 5 | 3,17 |
| D2 | 2 | 2 | 3 | D2 | 4 | 5 | 4 | 3,33 |
| D3 | 4 | 4 | 4 | D3 | 3 | 3 | 4 | 3,67 |
| D4 | 2 | 3 | 3 | D4 | 4 | 5 | 3 | 3,33 |
| D5 | 2 | 2 | 4 | D5 | 2 | 1 | 4 | 2,50 |
| D6 | 2 | 4 | 3 | D6 | 1 | 2 | 3 | 2,50 |
| D7 | 3 | 3 | 4 | D7 | 2 | 3 | 3 | 3,00 |
| D8 | 2 | 3 | 3 | D8 | 1 | 4 | 5 | 3,00 |
| Среднее количество атретических фолликулов, оба яичника | 3,06 |
Выводы
Данные результаты демонстрируют очень значительное снижение уровней тестостерона в плазме крови у животных, которых лечили исследуемым веществом (метформином) в высокой дозе, по сравнению с группой, которую лечили контрольным веществом.
Также наблюдали значительное уменьшение количества атретических фолликулов у животных, которых лечили исследуемым веществом (метформином) в промежуточной дозе, по сравнению с группой, которую лечили контрольным веществом.
1. Применение по меньшей мере одного инсулин-сенсибилизирующего агента для изготовления вагинального лекарственного средства для лечения синдрома поликистозных яичников и/или связанных расстройств.
2. Применение по меньшей мере одного инсулин-сенсибилизирующего агента для изготовления вагинального лекарственного средства для лечения гиперандрогенных состояний яичникового происхождения и/или связанных расстройств.
3. Применение по п.1 или 2 для лечения гирсутизма, акне и/или выпадения волос, связанных с гиперандрогенными состояниями яичникового происхождения.
4. Применение по п.1 или 2, где инсулин-сенсибилизирующий агент представляет собой метформин или одну из его фармацевтически приемлемых солей, гидратов, полиморфных форм или пролекарств.
5. Применение по п.4, где доза метформина находится в диапазоне от 0,01 мг/сут до 1000 мг/сут.
6. Применение по п.5, где доза метформина находится в диапазоне от 0,1 мг/сут до 100 мг/сут.
7. Применение по п.6, где доза метформина находится в диапазоне от 0,5 мг/сут до 50 мг/сут.
8. Применение по п.7, где доза метформина находится в диапазоне от 1 мг/сут до 10 мг/сут.
9. Применение по п.1 или 2, где инсулин-сенсибилизирующий агент представляет собой тиазолидиндион или одну из его фармацевтически приемлемых солей, гидратов, полиморфных форм или пролекарств.
10. Способ лечения синдрома поликистозных яичников и/или связанных расстройств, включающий вагинальное введение по меньшей мере одного инсулин-сенсибилизирующего агента.
11. Способ лечения гиперандрогении яичникового происхождения и/или связанных расстройств, включающий вагинальное введение по меньшей мере одного инсулин-сенсибилизирующего агента.
12. Фармацевтический состав для вагинального введения, содержащий по меньшей мере один инсулин-сенсибилизирующий агент, для применения в лечении синдрома поликистозных яичников и/или связанных расстройств.
13. Фармацевтический состав для вагинального введения, содержащий по меньшей мере один инсулин-сенсибилизирующий агент, для применения в лечении гиперандрогении яичникового происхождения и/или связанных расстройств.