Неинвазивный способ диагностики степени фиброза печени
Иллюстрации
Показать всеИзобретение относится к медицине, в частности к терапии, и может быть использовано в гепатологии и гастроэнтерологии для диагностики фибротических процессов печени. Сущность неинвазивного способа диагностики степени фиброза печени: формируют группу условно здоровых обследуемых (F0), группу пациентов с установленной гистологически умеренной степенью фиброза (F1-F2) и группу пациентов с установленной гистологически выраженной степенью фиброза (F3-F4), измеряют средние скорости движения суспензии эритроцитов и минимальные, средние и максимальные диаметры эритроцитов в период воздействия переменного электрического поля у группы условно здоровых обследуемых (F0) и у групп пациентов с умеренной степенью фиброза (F1-F2) и с выраженной степенью фиброза (F3-F4). На основании полученных данных определяют электрические и вязкоупругие параметры эритроцитов, сравнивают электрические и вязкоупругие параметры эритроцитов группы условно здоровых обследуемых (F0) с группой пациентов с умеренной степенью фиброза (F1-F2) и группой пациентов с выраженной степенью фиброза (F3-F4). На основании полученных результатов формируют массив данных для диагностики степени фиброза печени. Затем проводят аналогичные измерения образцов проб эритроцитов пациента с неясной степенью фиброза с определением электрических и вязкоупругих параметров эритроцитов с последующим их сравнением с соответствующими значениями, определенными для группы условно здоровых обследуемых (F0), группы пациентов с умеренной степенью фиброза (F1-F2) и группы пациентов с выраженной степенью фиброза (F3-F4) и при наличии 60% и более отличающихся параметров от группы условно здоровых обследуемых (F0) и входящих в границы значений для групп пациентов с умеренной степенью фиброза (F1-F2) или с выраженной степенью фиброза (F3-F4) и выявляют степень фиброза печени для данного пациента. Использование способа позволяет более точно определить степень фиброза печени у пациента на ранних стадиях заболевания независимо от этиологии возникновения заболевания. 3 ил., 3 табл.
Реферат
Изобретение относится к медицине, в частности к терапии, и может быть использовано в гепатологии и гастроэнтерологии для ранней диагностики фибротических процессов печени.
Актуальной проблемой в гепатологии является повышение эффективности ранней диагностики фибротических изменений печени, так как раннюю степень фиброза трудно диагностировать в связи с бессимптомным течением. Прогрессирование фиброза в 60-80% случаев приводит к выявлению заболевания на стадии цирроза печени. Это приводит к высокой инвалидизации, росту заболеваемости, смертности и экономических затрат на лечение цирроза печени и его осложнений, в том числе трансплантацию печени. Степень фиброза и скорость его прогрессирования определяют прогноз болезни и выбор терапии. Характеристика стадии болезни в гепатологическом диагнозе является обязательным компонентом наряду с этиологией и активностью процесса. Отсюда следует важность раннего выявления, оценки динамики накопления фиброзной ткани.
Основным способом оценки степени фиброза печени на данный момент в клинической практике считается пункционная биопсия (Гастроэнтерология. Национальное руководство // Под ред. Ивашкина В.Т., Лапиной Т.Л., М.: изд. группа «ГЭОТАР-Медиа». 2008. 700 с. Ивашкин Н.Т. Болезни печени и желчевыводящих путей. Руководство для врачей. / Н.Т. Ивашкин, М.: Вести, 2002. - 451 с. Подымова С.Д. Болезни печени. // М.: Медицина. 1993. 544 с. ).
Недостатки данного способа заключаются в том, что биопсия печени подразумевает забор ткани (кусочков, образцов) печени для последующего морфологического анализа. Процедура носит инвазивный характер и может вызвать серьезные осложнения (например, кровотечения), которые напрямую зависят от умения и опыта врача, проводящего биопсию. Также сложно учесть индивидуальные анатомические особенности организма, которые могут привести к осложнению. Нередко отмечается неудовлетворительная физическая и психологическая переносимость процедуры пациентом. Кроме того, биопсия не дает полной картины заболевания. Учитывая тот факт, что фиброз зачастую поражает печень неоднородно, мозаично, можно просто «промахнуться» и взять на анализ здоровый участок, в то время как весь остальной орган окажется обширно пораженным. Оценка степени фиброза печени с помощью биопсии во многом зависит от квалификации и опыта специалиста, производящего биопсию и оценивающего биоптаты. Для того чтобы следить за развитием болезни рекомендуется повторять биопсию каждые 3-5 лет. При биопсии необходима госпитализация пациента. Данная процедура имеет противопоказания, также необходимо информированное согласие пациента. У данной процедуры высокая стоимость и трудоемкость.
Для морфологической оценки выраженности фиброзных изменений в ткани печени известны несколько систем полуколичественной оценки степени фиброза (METAVIR, Knodell, Ishak). Целью оценки является получение суммарного клинически значимого показателя, отражающего все морфологические признаки (локализацию, распространенность, выраженность) повреждения ткани печени. (Панфилов С.А. Диагностика заболеваний печени, билиарного тракта с курсом патологической анатомии / С.А. Панфилов, Е.В.Панфилова. М.: БИНОМ - Лаборатория знаний - 2003. - 342 с. Руководство по лабораторным методам диагностики. // Под ред. проф. Кишкуна А.А. М.: ГЭОТАР-Медиа. 2007. 800 с. )
Недостатки данных способов заключаются в том, что при работе с этими системами нет четкого разграничения критериев оценки фиброза печени, с одной стороны, и показателей, оценки выраженности некровоспалительной реакции (индекс гистологической активности, ИГА) - с другой, что приводит к неоднозначной трактовке полученных результатов. Во многом морфологическая оценка остается субъективной и зависит от опыта и квалификации патоморфолога. Возникает необходимость применения широкой дорогостоящей номенклатуры различных реактивов. Использование данных методик отличает высокая трудоемкость. Кроме того, исследование по METAVIR преимущественно ориентировано на диффузную патологию печени вирусной этиологии.
Применяются в практике и макроморфологические способы визуализации. Известны следующие способы: ультразвуковые (УЗИ, эластография), компьютерная томография (КТ), ядерно-магнитнорезонанасная томография (ЯМРТ).
Недостатки данных способов заключаются в отсутствии четких критериев оценки фиброза, особенно на ранних этапах его развития, что снижает ценность этой группы способов на доцирротической стадии заболевания. Высокая стоимость процедур и низкая доступность также снижают возможность их использования. Есть ограничения для применения данных способов, связанные с физическим состоянием (например, лишний вес, резко гиперстеническая или резко астеническая конституции) и психологическим состоянием (например, клаустрофобия) пациента (Ивашкин Н.Т. Болезни печени и желчевыводящих путей. Руководство для врачей. / Н.Т. Ивашкин, М.: Вести, 2002. - 451 с. Панфилов С.А. Диагностика заболеваний печени, билиарного тракта с курсом патологической анатомии / С.А. Панфилов, Е.В.Панфилова. М.: БИНОМ - Лаборатория знаний - 2003. - 342 с. Ивашкин В.Т. Фиброз печени / В.Т.Ивашкин, Ч.С.Павлов. М.: ГЭОТАР-Медиа. - 2011. - 168 с. ).
Для неинвазивной оценки степени фиброза печени в клинической практике также предлагаются так называемые «фибротесты», основанные на изучении комплексов биохимических показателей, имеющих прямое и косвенное отношение к образованию и деградации внематричного комплекса (в том числе, коллагена). Модель диагностики основывается на наличии баланса между процессами фиброгенеза и фибринолиза, а также сопутствующих биохимических нарушений, в частности, липидного обмена. (Ивашкин В.Т. Фиброз печени /В.Т. Ивашкин, Ч.С. Павлов. М.: ГЭОТАР-Медиа. 2011. - 168 с. ).
Недостатками данных способов являются невысокая чувствительность и специфичность на ранних стадиях фиброза печени, высокая трудоемкость и стоимость, малая доступность оборудования и реагентов, необходимость специального обучения персонала, осуществляющего способы, и необходимость применения широкой номенклатуры различных реагентов. Эти факторы определяют невозможность применения данных методов для массовой диагностики, в целях скрининга.
Раскрытие изобретения
Техническим результатом предлагаемого изобретения является создание способа определения стадии заболевания печени, т.е. фиброза печени, который определяет прогноз заболевания, независимо от этиологии (причины) процесса. Предотвращение серьезных осложнений в состоянии здоровья пациента при заборе материала для исследований и повышение физической и психологической переносимости пациентом. Увеличение объективности оценки показателей исследования вне зависимости от квалификации и опыта специалиста производящего исследования. Определение степени фиброза печени на ранних стадиях заболевания и повышение ценности заявленного способа на доцирротической стадии заболевания. Повышение доступности для массовой диагностики, в т.ч. в целях скрининга. Снижение стоимости и трудоемкости.
Указанный технический результат достигается тем, что проводят отбор проб эритроцитов пациентов с неясной степенью фиброза, помещают их в 3,65-3,85% цитратный буфер в соотношении 9-10:1-1,5, через интервал времени, равный 10-60 мин, пробы объемом 9,7-12 мкл вносят в 0,25-0,35 молярный раствор сахарозы, разводят с коэффициентом k 0,9-1,1:29-31 и переносят суспензию исследуемых эритроцитов с концентрацией клеток 1,6-1,8·105/мкл в измерительную кювету, в кювете формируют неоднородное переменное электрическое поле с частотой f от 5·104 Гц до 106 Гц и средней напряженностью Ео электрического поля в зазоре между электродами в пределах от 104 до 106 В/м и градиентом квадрата напряженности от 1011 до 1013 в2/м3, измеряют средние скорости v → к л движения каждой клетки в суспензии и их минимальный диаметр Dмин, средний диаметр D и максимальный диаметр Dмах через определенные интервалы времени в период воздействия электрического поля и после его отключения по истечении времени t от 2 до 4 сек, путем видеозаписи изображения движения клеток и изменения их размера, полученные данные в цифровом виде вводят и обрабатывают в компьютере, имеющем вычислительную программу накопления и обработки данных, в результате чего определяют интервалы значений поляризуемости при 5·104 Гц, при 105 Гц, при 5·105 Гц, при 106 Гц и интервалы значений относительной поляризуемости, средние значения характеристик xj эритроцитов для данного образца (где j - порядковый номер характеристики от 1 до 13):
x1=Dcp=(D1+D2+…+Dn)/n - средний диаметр клетки,
где D1 - диаметр первой клетки;
D2 - диаметр второй клетки;
Dn - диаметр n-ой клетки;
n - количество клеток;
- скорость поступательного движения клетки в электрическом поле,
где S - расстояние, пройденное клеткой за время t;
- дипольный момент,
где αкл - поляризуемость клетки;
εo - диэлектрическая постоянная 8,85·10-12;
Е - напряженность электрического поля;
х4=ωp1=(fp) - равновесная частота,
- емкость мембраны клетки,
где ωр - (fp) - равновесная частота;
Rм - сопротивление мембраны клетки;
Rcp - сопротивление среды;
Сср - емкость среды;
- электропроводность клетки,
где Rкл - сопротивление клетки;
Rcp - сопротивление среды;
- индекс деструкции клетки,
где N0 - количество клеток в измерительной камере до включения электрического поля;
N1 - количество клеток в измерительной камере после включения электрического поля;
- обобщенный показатель вязкости клетки,
где скл - обобщенный показатель жесткости клетки;
τи - длительность зондирующего радиоимпульса;
π - постоянная величина, равная 3,14;
rкл, - радиус клетки в электрическом поле;
хm - максимальная амплитуда деформации клетки;
- обобщенный показатель жесткости клетки,
где αкл - поляризуемость клетки;
εо - диэлектрическая постоянная, равная 8,85·10-12;
Е - напряженность электрического поля;
rкл, - радиус клетки в электрическом поле;
хm - максимальная амплитуда деформации клетки;
индекс агрегации клетки,
где С0 - концентрация клеток в измерительной камере до включения электрического поля;
С1 - концентрация клеток в измерительной камере после включения электрического поля;
- максимальная амплитуда деформации клетки, где
- начальный диаметр клетки, до включения НПЭП;
- максимальный диаметр клетки при включенном НПЭП;
- поляризуемость клетки на любой произвольной частоте,
где π - постоянная величина, равная 3, 1416;
ηcp, - вязкость среды, в которой находится клетка;
rкл, - радиус клетки в электрическом поле;
v → к л - скорость поступательного движения клетки в электрическом поле;
∇ → E 2 - градиент квадрата напряженности электрического поля;
εо - диэлектрическая постоянная, равная 8,85·10-12;
- относительная поляризуемость клетки (безразмерная величина),
где π - постоянная величина, равная 3, 1416;
ηср, - вязкость среды, в которой находится клетка;
v → к л - скорость поступательного движения клетки в электрическом поле;
rкл, - радиус клетки в электрическом поле;
∇ → E 2 - градиент квадрата напряженности электрического поля;
εо - диэлектрическая постоянная, равная 8,85·10-12;
αкл - поляризуемость клетки;
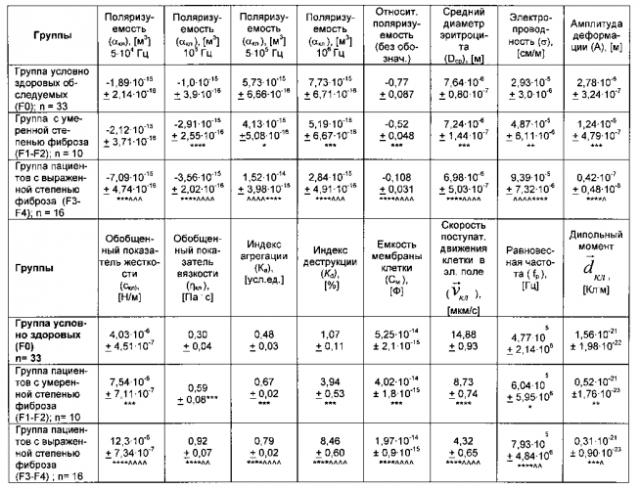
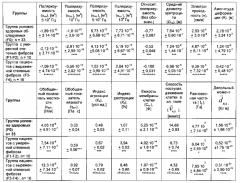
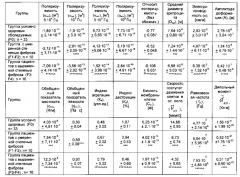
затем сравнивают полученные данные с соответствующими значениями, определенными для группы условно здоровых обследуемых (F0), и при наличии 60% и более отличающихся параметров от группы условно здоровых обследуемых (F0) и входящих в границы интервалов значений, указанных в таблице 1, у больных диагностируют умеренную (F1-F2) степень фиброза печени или выраженную (F3-F4) степень фиброза печени, причем таблица 1 «Электрические и вязкоупругие параметры эритроцитов у группы условно здоровых обследуемых и групп больных с разными степенями фиброза печени (M"+"m)» имеет следующий вид:
где: 1* - достоверность (Р) отличия от группы F0 (* - Р<0,05, ** - Р<0,02, *** - P<0,01, **** - Р<0,001), ∧ - достоверность (Р) отличия от 1-й группы (F1-F2) (∧ - Р<0,05, ∧ - Р<0,02, ∧∧∧ - Р<0,01, ∧∧∧∧ - Р<0,001), а параметры таблицы 1 имеют следующую размерность: поляризуемость (αкл), [м3] - 5·104 Гц; поляризуемость (αкл), [м3] - 105 Гц; поляризуемость (αкл), [м3] - 5·105 Гц; поляризуемость (αкл), [м3] - 106 Гц; относительная поляризуемость клетки (безразмерная величина); средний диаметр эритроцита, (Dcp), [м]; электропроводность (σ), [см/м]; амплитуда деформации (А), [м]; обобщенный показатель жесткости (скл), [Н/м]; обобщенный показатель вязкости (ηкл), [Па·с]; индекс агрегации (Ка), [усл. ед.]; индекс деструкции, [%]; емкость мембраны клетки (См), [Ф]; скорость поступательного движения клетки в эл. поле ( v → к л ) ,[мкм/с]; равновесная частота (fp), [Гц]; дипольный момент ( d → к л ) ,[Клм].
Способ реализуется с использованием устройства по патенту РФ на полезную модель №71439 (заявка №2007137837/22 от 15.10.2007, патентообладатель - ФБУН ГНЦ ВБ "Вектор") для измерения электрических и вязкоупругих параметров эритроцитов, включающее прозрачную измерительную кювету с электродами, соединенными с источником электропитания с зазором, достаточным для формирования в нем средней напряженности электрического поля в пределах от 104 до 106 Вольт/м.
Изобретение поясняется следующими графическими материалами. На фиг. 1 приведена блок-схема автоматизированной установки для реализации предлагаемого способа. На фиг. 2 приведена схема измерительной кюветы. На фиг. 3 представлена конструкция действующей автоматизированной установки для реализации предлагаемых способа измерения электрических и вязкоупругих параметров эритроцитов.
Вариант осуществления изобретения
Устройство для измерения электрических и вязкоупругих параметров эритроцитов включает разборную оптически прозрачную измерительную кювету 1 (фиг. 2), в которой расположены металлические электроды 2 и 3, соединенные с источником электропитания 4, а также измерительный блок. Источник электропитания 4 представляет собой генератор переменного электрического напряжения, а измерительный блок (фиг. 1) содержит микроскоп 5, оптически связанный с измерительной кюветой 1, и систему анализа изображения для измерения скорости движения эритроцитов, содержащую видеокамеру 6, оптически связанную с микроскопом 5, и компьютер 7, соединенный с видеокамерой 6. Компьютер 7 содержит специализированную программу обработки изображений. Измерительная кювета 1 размещена на подвижном столе микроскопа 5. Причем электроды 2 и 3 в измерительной кювете 1 установлены с зазором, достаточным для формирования в нем средней напряженности Eo электрического поля в пределах от 104 Вольт/м до 106 Вольт/м и градиента квадрата напряженности ∇ → E 2 с р от 1011 Вольт2/м3 до 1013 Вольт2/м3. Зазор между электродами 2 и 3 в экспериментальной конструкции кюветы 1 устанавливают в пределах от 45 до 105 мкм, а толщина указанных электродов составляет от 0,2 до 2 мкм. Конструкция экспериментальной действующей установки (фиг. 3) дополнительно предусматривает наличие осциллографа 8, подключенного к электродам 2 и 3 измерительной кюветы 1 для контроля электрических и вязкоупругих параметров, а также соединенный с цифровой видеокамерой 6 монитор 9.
Принцип работы устройства заключается в следующем. Измерительную кювету 1 устанавливают на подвижный стол микроскопа 5 и фиксируют на нем указанную кювету 1. В измерительную кювету 1 вносят пробу суспензии эритроцитов с известной степенью разведения. На электроды 2 и 3 измерительной кюветы 1 подают напряжение не более 10 Вольт от источника 4 (генератора) переменного напряжения, между которыми формируют среднюю напряженность Eo электрического поля в пределах от 104 до 106 Вольт/м. С помощью видеокамеры 6 регистрируют динамику движения отдельных эритроцитов в измерительной кювете 1. С видеокамеры 6 видеосигнал динамики движения клеток подают на компьютер 7 (со специализированной программой обработки изображений), где обрабатываются данные и вычисляются электрические и вязкоупругие характеристики эритроцитов.
Способ измерения электрических и вязкоупругих параметров эритроцитов реализуется следующим образом.
1-й этап формирования группы условно здоровых обследуемых и групп пациентов с различной степенью фиброза. В исследованиях принимали участие пациенты (мужчины) в возрасте от 35 до 60 лет, которые были изначально условно поделены на две группы. Первая группа пациенты с диффузными заболеваниями печени. Степень выраженности фиброза печени устанавливалась гистологически на основании данных биопсии. Вторая группа обследуемых - условно здоровые. В группе условно здоровых мужчин биопсия печени не проводилась по этическим соображениям.
Пациентам из обеих групп выполнены биохимические и инструментальные исследования, УЗИ печени, селезенки, а также портальных сосудов. Вирусная этиология заболевания устанавливалась на основании обнаружения серологических маркеров методом иммуноферментного анализа (ИФА) и (или) ДНК и РНК вирусов методом полимеразноцепной реакции (ПЦР), а алкогольная - при отрицательных результатах ИФА сывороточных маркеров вирусных гепатитов и достоверно подтвержденном систематическом потреблении алкоголя. У пациентов с диффузной патологией печени был выявлен вирусный (В, С, Д), алкогольный или смешанный (вирусно-алкогольный) генез заболевания. По результатам совокупного анализа сформированы три группы:
- первая группа включала десять пациентов с умеренной степенью фиброза (F1-F2);
- во вторую группу вошли шестнадцать пациентов с выраженной степенью фиброза (F3-F4);
- третья группа (F0) составила тридцать три условно здоровых обследуемых, у которых при клиническом и инструментальном обследовании патологий печени и сердца не выявлено.
2-й этап измерений и вычислений. Были произведены исследования средних скоростей движения эритроцитов суспензии и минимальные, средние и максимальные диаметры эритроцитов в период воздействия переменного электрического поля у группы условно здоровых обследуемых (F0) и групп пациентов с умеренной степенью фиброза (F1-F2) и с выраженной степенью фиброза (F3-F4), которые проводились следующим образом.
Был произведен отбор проб клеток биологических объектов, например проб крови объемом от 1,5 до 2,5 мл вакуумными пробирками в 3,65-3,85% цитратный буфер в соотношении 9-10:1-1,5. Через определенный интервал времени от 10 до 60 мин пробы объемом от 9,7 до 12 мкл вносят в 0,25-0,35 молярный раствор сахарозы (pH от 7,36 до 7,42) разводят с заданным коэффициентом k и переносят суспензию исследуемых эритроцитов с заданной концентрацией клеток в измерительную кювету 1. В кювете 1 формируют неоднородное переменное электрическое поле с частотой f, от 5·104 Гц до 106 Гц, средней напряженностью Ео электрического поля в зазоре между электродами в пределах от 104 Вольт/м до 106 Вольт/м и градиентом квадрата напряженности ∇ → E 2 от 1011 до 1013 в2/м3 путем подачи напряжения не более 10 Вольт на электроды 2 и 3 от источника 4 (генератора) электропитания. Далее измеряют средние скорости v → к л . движения эритроцитов в суспензии и их минимальный диаметр Dмин, средний диаметр D и максимальный диаметр Dмах через определенные интервалы времени в период воздействия электрического поля и после его отключения по истечении времени t путем видеозаписи изображения движения эритроцитов и изменения их размера, полученные данные в цифровом виде вводят и обрабатывают в компьютере, имеющем вычислительную программу накопления и обработки данных, в результате чего определяют средние значения характеристик xj эритроцитов, для данного образца (где j - порядковый номер характеристики от 1 до 13).
Первым диагностическим параметром является средний диаметр клетки, вычисляется как среднее арифметическое диаметров многих клеток по формуле:
где D1 - диаметр первой клетки;
напряжения, а измерительный блок (фиг.1) содержит микроскоп 5, оптически связанный с измерительной кюветой 1, и систему анализа изображения для измерения скорости движения эритроцитов, содержащую видеокамеру 6, оптически связанную с микроскопом 5, и компьютер 7, соединенный с видеокамерой 6. Компьютер 7 содержит специализированную программу обработки изображений. Измерительная кювета 1 размещена на подвижном столе микроскопа 5. Причем электроды 2 и 3 в измерительной кювете 1 установлены с зазором, достаточным для формирования в нем средней напряженности Eo электрического поля в пределах от 104 Вольт/м до 106 Вольт/м и градиенте напряженности ∇ → E c p от 1011 Вольт/м2 до 1013 Вольт/м2. Зазор между электродами 2 и 3 в экспериментальной конструкции кюветы 1 устанавливают в пределах от 45 до 105 мкм, а толщина указанных электродов составляет от 0,2 до 2 мкм. Конструкция экспериментальной действующей установки (фиг.3) дополнительно предусматривает наличие осциллографа 8, подключенного к электродам 2 и 3 измерительной кюветы 1 для контроля электрических и вязкоупругих параметров, а также соединенный с цифровой видеокамерой 6 монитор 9.
Принцип работы устройства заключается в следующем. Измерительную кювету 1 устанавливают на подвижный стол микроскопа 5 и фиксируют на нем указанную кювету 1. В измерительную кювету 1 вносят пробу суспензии эритроцитов с известной степенью разведения. На электроды 2 и 3 измерительной кюветы 1 подают напряжение не более 10 Вольт от источника 4 (генератора) переменного напряжения, между которыми формируют среднюю напряженность Eo электрического поля в пределах от 104 до 106 Вольт/м. С помощью видеокамеры 6 регистрируют динамику движения отдельных эритроцитов в измерительной кювете 1. С видеокамеры 6 видеосигнал динамики движения клеток подают на компьютер 7 (со специализированной программой обработки изображений), где обрабатываются данные и вычисляются электрические и вязкоупругие характеристики эритроцитов.
Способ измерения электрических и вязкоупругих параметров эритроцитов реализуется следующим образом.
1-й этап формирования группы условно здоровых обследуемых и групп пациентов с различной степенью фиброза. В исследованиях принимали участие пациенты (мужчины) в возрасте от 35 до 60 лет, которые были изначально условно поделены на две группы. Первая группа пациенты с диффузными заболеваниями печени. Степень выраженности фиброза печени устанавливалась гистологически на основании данных биопсии. Вторая группа обследуемых - условно здоровые. В группе условно здоровых мужчин биопсия печени не проводилась по этическим соображениям.
Пациентам из обеих групп выполнены биохимические и инструментальные исследования, УЗИ печени, селезенки, а также портальных сосудов. Вирусная этиология заболевания устанавливалась на основании обнаружения серологических маркеров методом иммуноферментного анализа (ИФА) и (или) ДНК и РНК вирусов методом полимеразноцепной реакции (ПНР), а алкогольная - при отрицательных результатах ИФА сывороточных маркеров вирусных гепатитов и достоверно подтвержденном систематическом потреблении алкоголя. У пациентов с диффузной патологией печени был выявлен вирусный (B, C, Д), алкогольный или смешанный (вирусно-алкогольный) генез заболевания. По результатам совокупного анализа сформированы три группы:
- первая группа включала десять пациентов с умеренной степенью фиброза (F1-F2);
- во вторую группу вошли шестнадцать пациентов с выраженной степенью фиброза(F3-F4);
- третья группа (F0) составила тридцать три условно здоровых обследуемых, у которых при клиническом и инструментальном обследовании патологий печени и сердца не выявлено.
2-й этап измерений и вычислений. Были произведены исследования средних скоростей движения эритроцитов суспензии и минимальные, средние и максимальные диаметры эритроцитов в период воздействия переменного электрического поля у группы условно здоровых обследуемых (F0) и групп пациентов с умеренной степенью фиброза (F1-F2) и с выраженной степенью фиброза (F3-F4), которые проводились следующим образом.
Был произведен отбор проб клеток биологических объектов, например проб крови объемом от 1,5 до 2,5 мл вакуумными пробирками в 3,65-3,85% цитратный буфер в соотношении 9-10:1-1,5. Через определенный интервал времени от 10 до 60 мин пробы объемом 0,097 до 0,12 мкл вносят в 0,25-0,35 молярный раствор сахарозы (pH от 7,36 до 7,42) разводят с заданным коэффициентом k и переносят суспензию исследуемых эритроцитов с заданной концентрацией клеток в измерительную кювету 1. В кювете 1 формируют неоднородное переменное электрическое поле с частотой f, от 5·104 Гц до 106 Гц, и средней напряженностью Eo электрического поля в зазоре между электродами в пределах от 104 Вольт/м до 106 Вольт/м и градиенте напряженности ∇ → E c p от 1011 Вольт/м2 до 1013 Вольт/м2 путем подачи напряжения не более 10 Вольт на электроды 2 и 3 от источника 4 (генератора) электропитания. Далее измеряют средние скорости ν → к л движения эритроцитов в суспензии и их минимальный диаметр Dмин, средний диаметр D и максимальный диаметр Dмах через определенные интервалы времени в период воздействия электрического поля и после его отключения по истечении времени t путем видеозаписи изображения движения эритроцитов и изменения их размера, полученные данные в цифровом виде вводят и обрабатывают в компьютере, имеющем вычислительную программу накопления и обработки данных, в результате чего определяют средние значения характеристик xj эритроцитов, для данного образца (где j - порядковый номер характеристики от 1 до 13).
Первым диагностическим параметром является средний диаметр клетки, вычисляется как среднее арифметическое диаметров многих клеток по формуле:
x 1 = D c p = ( D 1 + D 2 + … + D n ) / n . ( 1 )
где D1 - диаметр первой клетки;
D2 - диаметр второй клетки;
Dn - диаметр n-ой клетки;
n - количество клеток.
В условиях неоднородного электрического поля скорость поступательного движения клетки определяется по формуле:
x 2 = ν → к л . = S / t . ( 2 )
где S - расстояние, пройденное клеткой за время t.
Третьим диагностическим параметром является дипольный момент, который определяется по формуле:
x 3 = d → к л = α к л ε 0 E . ( 3 )
где αкл - поляризуемость клетки;
εо - диэлектрическая постоянная 8,85·10-12;
E - напряженность электрического поля.
Четвертым диагностическим параметром является равновесная частота x 4 = ω p 1 = ( f p ) . ( 4 )
измерения которой осуществляются в следующей последовательности. Измерительную ячейку устанавливают на подвижный стол микроскопа и соединяют с генератором переменного напряжения. В камеру измерительной ячейки вносится клеточная суспензия и накрывается покровным стеклом. Микроскоп фокусируется на клетки, которые расположены между электродами. С генератора на электроды измерительной ячейки подается переменное гармоническое напряжение U=(3÷10) В. В ходе изменения частоты генератора находится искомая величина ωp1 (равновесная частота), на которой отрицательный диэлектрофорез сменяется положительным. Строго на равновесной частоте клетки не имеют поступательного движения. Наблюдается лишь вращение некоторых из них вокруг собственной оси или друг относительно друга.
Емкость мембраны Cм находится на равновесной частоте ωp, которая разделяет частотные области положительного и отрицательного диэлектрофореза. Клетка на этой частоте не имеет поступательного движения. Ее электрическая емкость равна на этой частоте соответственно емкости среды (клеточной суспензии) Cм. Емкость мембраны клетки является пятым диагностическим параметром и вычисляется по формуле:
x 5 = C м = 1 ω p 1 ⋅ R м = C c p = 1 ω p 1 ⋅ R c p . ( 5 )
где ωp=(fp) - равновесная частота;
Rм - сопротивление мембраны клетки;
Rcp - сопротивление среды;
Ccp - емкость среды.
Шестым диагностическим параметром является электропроводность клетки 1/Rкл, которая находится на равновесной частоте ωp, которая разделяет частотные области положительного и отрицательного диэлектрофореза. Клетка на этой частоте не имеет поступательного движения. Ее проводимость равна на этой частоте соответственно проводимости среды (клеточной суспензии) 1/Rcp. и вычисляется по следующей формуле:
x 6 = σ = 1 R к л = 1 R c p . ( 6 )
где Rкл - сопротивление клетки;
Rcp - сопротивление среды.
Индекс деструкции клетки является седьмым диагностическим параметром K∂ - отношение количества клеток в измерительной камере до включения и после включения электрического поля. Клетки, имеющие патологию в НПЭП, подвергаются деструкции в области отрицательного диэлектрофореза. Вычисляется по формуле:
x 7 = K ∂ = N 0 N 1 . ( 7 )
где N0 - количество клеток в измерительной камере до включения электрического поля;
N1 - количество клеток в измерительной камере после включения электрического поля.
Измерением зависимости деформации клетки от времени определяется обобщенный показатель вязкости клетки, который является восьмым диагностическим параметром и определяется по формуле:
x 8 = η к л = − c к л ⋅ τ u 6 ⋅ π ⋅ r к л ⋅ ln | x m | . ( 8 )
где cкл - обобщенный показатель жесткости клетки;
τи - длительность зондирующего радиоимпульса;
π - постоянная величина, равная 3,14;
rкл, - радиус клетки в электрическом поле;
xm - максимальная амплитуда деформации клетки.
Девятым диагностическим параметром является обобщенный показатель жесткости клетки и вычисляется по формуле:
x 9 = c к л = α к л ε 0 E 2 2 r к л x m . ( 9 )
где αкл - поляризуемость клетки;
εо - диэлектрическая постоянная, равная 8,85·10-12;
E - напряженность электрического поля;
rкл, - радиус клетки в электрическом поле;
xm - максимальная амплитуда деформации клетки.
Десятым диагностическим параметром является индекс агрегации клетки. Измеряем отношение концентрации клеток в клеточной суспензии до процесса агрегации к концентрации оставшихся клеток в суспензии после процесса агрегации по формуле:
x 10 = K a = C 0 − C 1 C 0 ⋅ 100. ( 10 )
где C0