Таргетирование раковых опухолей за счет использования ингибиторов изоформ карбоангидразы ix
Иллюстрации
Показать всеИзобретение относится к области органической химии, а именно к новым производным нитроимидазола формулы (1) и к его фармацевтически приемлемым солям, где Z представляет собой Z1 с формулой (2а), или Z представляет собой Z2 с формулой (2b): (СН2)nCH2X, или Z представляет собой Z3 с формулой (2с), и R1 и R2 каждый независимо может представлять собой Н или СН3, R3, R4, R6 и R7 каждый независимо может представлять собой Н, сульфонамид, сульфамат или сульфамид, R5 может представлять собой Н, сульфонамид, сульфамат или сульфамид, Х=сульфонамид, сульфамат или сульфамид, Y=S, и n=0, 1 или 2, и где, если n=0, R2=2-CH3, Z=Z1, R3=R4=R6=R7=H и R5=SO2NH2, то NO2 находится не в положении 4, и где если R5 представляет собой Н, то по меньшей мере один из R3, R4, R6 и R7 не является Н. Также изобретение относится к применению соединения формулы (1) и способу лечения болезни, отличающейся сверхэкспрессией одной или нескольких карбоангидраз. Технический результат: получены новые производные нитроимидазола, полезные при лечении раковых заболеваний. 4 н. и 11 з.п. ф-лы, 18 ил., табл.1.
(1) (2а) (2с)
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к новым ингибиторам карбоангидразы IX, содержащим нитроимидазольный фрагмент, а также к их использованию при лечении рака, в частности при радиотерапии.
Уровень техники
Рак является ведущей причиной смерти и вызывает приблизительно 13% всех смертей в мире. В большинстве случаев злокачественные новообразования образуют в тканях солидные опухоли, как, например, в случае рака головы и шеи, толстой кишки, молочной железы, легких, печени и желудка, которые обычно характеризуются низкой концентрацией кислорода (гипоксией) и закислением микросреды вокруг опухолевых клеток. Гипоксия и закисление окружающей среды вне опухоли ассоциируются с агрессивным ростом опухоли, образованием метастазов и слабым откликом на радиотерапию, хирургическое лечение и/или на противоопухолевую химиотерапию. Наиболее важным сигнальным путем, оказывающим влияние на концентрацию кислорода, является 'путь индуцируемого гипоксией фактора-1' (путь HIF-1). В условиях гипоксии транскрипционный фактор HIF-1α стабилизируется и связывается с HIF-1β Образованный комплекс может перемещаться в ядро и связываться с реагирующими на гипоксию элементами (HRE) генов, вовлеченных в анаэробный обмен веществ, регуляцию pH, ангиогенез, пролиферацию и выживание клеток.
Карбоангидразы (CA) образуют большое семейство универсальных цинковых металлоферментов, имеющих большое физиологическое значение. В качестве катализаторов обратимой реакции гидратации диоксида углерода до бикарбоната и протонов эти ферменты участвуют в целом ряде биологических процессов, включая дыхание, кальцификацию, кислотно-щелочной баланс, костную резорбцию, образование внутриглазной жидкости. На сегодняшний день охарактеризовано 16 изоферментов, 15 из которых присутствуют у людей. У людей карбоангидразы присутствуют в нескольких тканях (например, в желудочно-кишечном тракте, половых путях, коже, почках, легких, глазах и т.д.) и локализуются в разных частях клетки. В целом, существует несколько цитоплазматических форм (CA I-III,CA VII), четыре мембраносвязанных изофермента (CA IV, CA IX, CA XII и CA XIV), одна митохондриальная форма (CA V), а также секретируемый CA изофермент, CA VI.
Было показано, что некоторые опухолевые клетки преимущественно экспрессируют только некоторые мембраносвязанные CA изоферменты, такие как CA IX и CA XII. CA демонстрируют широкое разнообразие в распределении в тканях, уровнях и предполагаемых или установленных биологических функциях. Некоторые из CA экспрессируются едва ли не во всех тканях (CA II), в то время как экспрессия других, по-видимому, является более ограниченной (например, CA VI и CA VII экспрессируются в слюнных железах).
Кроме того, можно допустить, что CA-активность также может использоваться в опухолях, поскольку опухоли зачастую демонстрируют обратный градиент pH в плазматической мембране по сравнению с нормальными тканями, что иллюстрирует вклад CA в предоставление протонов для подкисления внеклеточной окружающей среды и бикарбонатных ионов для поддержания нейтральной внутриклеточной среды. В дополнение к подкисляющему воздействию на внеклеточное значение pH карбоангидраза может влиять на поглощение противоопухолевых лекарственных средств и модулировать ответ опухолевых клеток на традиционную терапию, такую как лучевая терапия. Один из CA изоферментов, CA IX, ограниченно экспрессируется в нормальных тканях, но тесно связан с различными типами опухолей. CA IX, первоначально обнаруженный в клетках карциномы человека HeLa как антиген, регулируемый плотностью клеток (Pastorekova et al, 1992), сильно индуцируется при опухолевой гипоксии через транскрипционную активацию HIF-1-пути. Сильная связь между экспрессией карбоангидразы CA IX и внутриопухолевой гипоксией показана на карциномах. Распространение CA IX часто исследуют в связи со степенью некроза, как индикатора тяжелой гипоксии, и относительной плотности микрососудов, как показателя ангиогенеза. Кроме того, CA IX ассоциируется с худшими показателями безрецидивной выживаемости и общей выживаемости у пациентов с инвазивными опухолями. Кроме того, CA IX является важным прогностическим признаком общей выживаемости и выживаемости без метастазов после лучевой терапии и химиолучевой терапии.
Гипоксия связана с закислением внеклеточной окружающей среды, способствующим опухолевой инвазии, и CA IX, как полагают, играет некоторую роль в этом процессе посредством своей каталитической активности (Svastova et al, 2004). Было показано, что CA IX обладает очень высокой каталитической активностью с самой высокой скоростью переноса протонов среди всех известных CA, и что CA IX подкисляет внеклеточную окружающую среду и, как следствие, представляет собой интересную мишень для противоопухолевой терапии, предпочтительно в комбинации с обычными режимами лечения. Таргетирование CA DC может быть более предпочтительным, чем таргетирование HIF-1 - основного регулировщика транскрипционного ответа клеток млекопитающих на кислородную недостаточность, поскольку в уровне техники описывались противоречивые результаты, зависящие от использованного типа клеток, целевой субъединицы, местоположения опухоли и момента ингибирования HIF-1 (на ранней или поздней стадии развития опухоли). К тому же, так как большинство низкомолекулярных ингибиторов HIF-1 влияет на множество сигнальных путей и/или мишеней, косвенно связанных с HIF, оценка их активности как HIF-ингибиторов не может основываться на терапевтической эффективности, которая может быть не связана с ингибированием HIF (Melillo, 2006).
Недавно выяснилось, что ингибиторы карбоангидразы (CAI) могут иметь потенциал, в дополнение к доказанной роли диуретиков и лекарственных средств против глаукомы, для использования в качестве новых лекарственных средств против ожирения, противораковых и антибактериальных лекарственных средств. Существует 2 основных класса ингибиторов карбоангидраз: металл-комплексообразующие анионы и незамещенные сульфонамиды и их производные, которые связываются с ионом цинка фермента или путем замещения небелкового цинкового лиганда, или путем присоединения к металлической координационной сфере (Supuran, 2008). Однако существенной проблемой при разработке этих ингибиторов является большое число изоферментов, рассеянная локализация в тканях и отсутствие селективности к изоферментам у известных в настоящее время ингибиторов.
Все шесть классических CAI (ацетазоламид, метазоламид, этоксзоламид, дихлорфенамид, дорзоламид и дихлорфенамид), используемые в клинической медицине или в качестве средств диагностики, проявляют некоторые ингибирующие свойства в отношении роста опухолей. Большинство из упомянутых выше сульфонамидов, используемых в клинике, являются системно действующими ингибиторами, оказывающими некоторые нежелательные побочные действия вследствие ингибирования многих различных изоферментов CA, присутствующих в целевой ткани/органе (в настоящее время у человека известно 15 изоформ). Поэтому, в последнее время сообщалось о многих попытках разработки и синтеза новых сульфонамидов с целью избежать таких побочных эффектов. Изоферменты, связанные с клеточными мембранами (CA IV, CA IX, CA XII и CA XIV), в большинстве случаев с внеклеточно-ориентированным активным центром фермента, предоставляют рациональную основу для таргетирования. CA IX и CA XII располагаются внеклеточно на гипоксических опухолевых клетках, и поэтому являются наилучшими кандидатами.
Идеальные специфические CA IX ингибиторы должны демонстрировать относительно низкую константу ингибирования (Ki в наномолекулярном диапазоне) и должны быть относительно специфическими по отношению к цитозольным ферментам CA I и CA II. Был описан целый ряд ароматических сульфонамидов (смотри, например, WO 2004048544), которые специфически связываются с внеклеточными компонентами, в частности, фермента CAIX, обладающие более высокой специфичностью, чем известные ранее в данной области техники соединения. Терапевтические и диагностические сульфонамидные средства описаны в WO 2006137092. В WO 2008071421 было показано, что ингибирующий эффект гетероциклических сульфонамидов может быть дополнительно увеличен с помощью окислительных заместителей, в частности нитрозированных или нитрозилированных заместителей, поскольку такие группы могут повышать кислотность цинк-связывающих групп, и в связи с этим являются полезными для свойств ингибитора карбоангидразы. Металлические хелатные комплексы для визуализации на основе сульфонамида описаны в WO 2009089383. Однако, наблюдается большой разброс в константах ингибирования CA IX для указанных сульфонамидов, а также имеют место колебания в селективности ингибиторов. Сульфаматные и сульфамидные ингибиторы также предлагались в качестве кандидатов (Winum et al, 2009).
Традиционная противоопухолевая терапия, например хирургическое лечение, облучение и химиотерапия, используется для лечения раковых пациентов в виде комбинированного или отдельного лечения. Основным принципом облучения является повреждение раковых клеток до такой степени, чтобы они погибали. При этом образуются свободные радикалы, тут же повреждающие ДНК или реагирующие с кислородом, создавая активные формы кислорода, которые повреждают клетку и, более конкретно, ДНК в клетке. Однако в случае отсутствия кислорода или когда он присутствует в небольшом количестве, что часто наблюдается в гипоксических опухолях, образуется гораздо меньшее количество активных форм кислорода и облучение не является столь эффективным. Было показано, что для того, чтобы убить то же количество гипоксических клеток, что и клеток в условиях нормальных концентраций кислорода, необходима в три раза большая доза облучения. Представление о радиосенсибилизации гипоксических клеток появилось, когда были обнаружены определенные соединения, способные имитировать кислород и таким образом увеличивать повреждение при облучении. Первыми соединениями, которые продемонстрировали явление радиосенсибилизации, были нитробензолы, а затем нитрофураны и 2-нитроимидазолы, такие как мизонидазол (смотри, например, WO2006102759). Хотя на экспериментальных опухолевых моделях можно было наблюдать увеличение повреждения при облучении, большинство клинических исследований с применением мизонидазола оказалось неспособно продемонстрировать значительное улучшение ответа при облучении, хотя в некоторых подгруппах пациентов польза была видна (Overgaard, 1989). Наиболее вероятным объяснением этому факту является то, что дозы мизонидазола были слишком низкими ввиду их ограниченности риском появления нейротоксичности. В качестве альтернативы были синтезированы и протестированы более подходящие радиосенсибилизирующие лекарственные средства, такие как этанидазол и пимонидазол, однако их клинические результаты не показали значительного терапевтического эффекта. Менее токсичные лекарственные средства, такие как ниморазол, теоретически должны иметь более низкую сенсибилизирующую способность по сравнению с мизонидазолом, однако вследствие их значительно более низкой степени токсичности они могут быть использованы в значительно больших, клинически релевантных дозах. Только клинические исследования у пациентов с надъязычными и глоточными карциномами (DAHANCA 5) дали в результате значительное преимущество в плане улучшенного локорегионарного контроля опухоли и увеличенной выживаемости без признаков заболевания (Overgaard et al, 1998). Таким образом, более специфическое таргетирование гипоксических опухолевых клеток с использованием более низких доз является важным и необходимым свойством новых соединений.
В данной работе неожиданно было обнаружено, что соединения по изобретению, представленные формулой (1):
,
в которой Z представляет собой Z1, соответствующий формуле (2a):
,
или Z представляет собой Z2, соответствующий формуле (2b): (СН2)nCH2X,
или Z представляет собой Z3, соответствующий формуле (2c):
,
R1 и R2 каждый независимо может представлять собой H, алкил, алкенил, алкинил, циклоалкил, гетероциклическую группу, арил, цианогруппу или атом галогена,
R3, R4, R6 и R7 каждый независимо может представлять собой H, алкил, алкенил, алкинил, циклоалкил, гетероциклическую группу, арил, атом галогена, цианогруппу, алкоксигруппу, сульфонамид, сульфамат или сульфамид,
R5 может представлять собой сульфонамид, сульфамат или сульфамид,
X = сульфонамид, сульфамат или сульфамид,
Y=O или S,
и n=0, 1, 2, 3, 4 или 5, демонстрируют не только более высокую специфичность к CA IX, чем любое известное в данной области техники соединение, но также обладают значительно увеличенным радиосенсибилизирующим действием. Это является в значительной степени неожиданным, так как стереохимическая ориентация различных активных групп в соединениях по изобретению значительно отличается от ориентации соединений, известных в данной области техники, будь то сульфонамиды или нитроимидазолы. Другими словами, неожиданно оказалось, что радиосенсибилизирующая активность нитроимидазолов сохраняется несмотря на то, что эта группа здесь является частью большой молекулы, а соединения являются менее токсичными.
Таким образом, соединения по изобретению имеют значительно улучшенный общий профиль для лечения солидных опухолей, таких как опухоли молочной железы, мозга, почки, толстой кишки, легких, головы и шеи, мочевого пузыря и т.д., по сравнению с известными в данной области ингибиторами карбоангидразы. Кроме того, в рамки применения соединений по изобретению попадают и другие терапевтические области, такие как лечение глазных болезней, в частности глаукомы, повышенного внутриглазного давления, возрастной дегенерации желтого пятна, диабетического макулярного отека, диабетической ретинопатиии, гипертензивной ретинопатии и ретинальной васкулопатии, эпилепсии, высотной болезни и нервно-мышечных заболеваний.
Другой неожиданный факт заключается в том, что соединения по изобретению также оказывают неожиданное положительное действие на радиочувствительность. Полагают, что внеклеточный ацидоз является результатом избыточной выработки молочной кислоты. Однако, гликолитически-дефицитные клетки (клетки, в которых выработка молочной кислоты затруднена) дают в результате опухоли со сходной степенью внеклеточного ацидоза, что указывает на вовлечение других «игроков», кроме молочной кислоты. Некоторые исследования показывают, что внеклеточный ацидоз делает опухоли менее чувствительными к лечению облучением (Brizel et al, 2001; Quennet et al, 2006). Ингибирующие карбонангидразу сульфонамиды способны уменьшать внеклеточный ацидоз в опухолях и, следовательно, представляют собой возможный инструмент для улучшения чувствительности опухолей к облучению. В дополнение к этому, тот факт, что экспрессия CA IX в нормальной здоровой ткани ограничена, а в опухолях, напротив, чрезвычайно высока, делает изофермент карбонагидразы IX привлекательной мишенью в рамках данной концепции.
С другой стороны, гипоксические условия в опухолях делают их менее чувствительными к ионизирующему облучению, обычно используемому при радиотерапии (Thomlinson & Gray, 1955). Направляя CA-ингибирующие соединения к гипоксическим клеткам, можно было бы значительно увеличить возможный терапевтический эффект. Это может быть сделано с использованием нитроимидазолов, которые захватываются гипоксическими клетками после двукратного электронного восстановления в условиях низкого содержания кислорода.
Другими словами, с одной стороны существует необходимость увеличения антикислотных, антитуморогенных эффектов и специфичности CA IX-ингибирующих сульф(он)амидов, а с другой стороны существует необходимость специфического таргетирования гипоксических клеток с использованием замещенных нитроимидазолов, что делает эти соединения более подходящими для радиосенсибилизирующей терапии.
Эти потребности удовлетворяются настоящим изобретением, которое относится к многофункциональным двойственным нацеленным на CA IX лекарственным соединениям и препаратам для лечения рака у пациентов, нуждающихся в этом, содержащим соединения вышеуказанной формулы 1a-c.
Кроме того, дополнительными аспектами настоящего изобретения являются фармацевтические композиции, содержащие по меньшей мере одно соединение по настоящему изобретению формулы (1a-c) вместе с нетоксичными адьювантами и/или носителями, традиционно применяемыми в области фармацевтики.
Далее изобретение будет описано более подробно со ссылкой на фигуры, где:
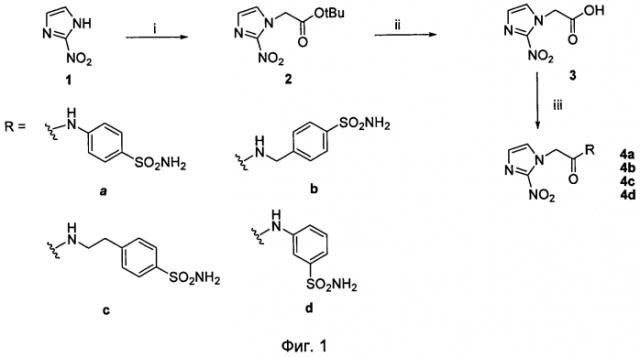
фиг.1 показывает синтез соединений 4a-d;
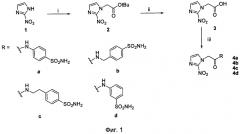
фиг.2 показывает синтез соединений 6a-d;
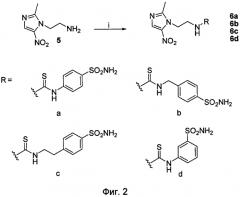
фиг.3 показывает предпочтительное соединение (7) по изобретению;
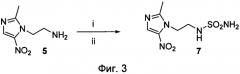
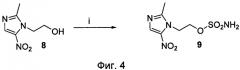
фиг.4 показывает другое предпочтительное соединение (9) по изобретению;
фиг.5a-b; показывает действие соединений (6a, 6c, 7 и 9) по изобретению на ацидоз на культуре опухолевых клеток in vitro;
фиг.6a-k показывает действие соединений по изобретению в комбинации с химиотерапевтическими средствами или облучением на опухолевой модели in vivo.
Фиг.1 представляет Схему 1.
Реактивы и условия: (i) 1 экв. 2-нитроимидазола, 1 экв. трет-бутил бромацетата, 4 экв. карбоната калия, MeCN, комнатная температура, 1 ночь; (ii) смесь трифторацетуксусная кислота/вода/тиоанизол 95/2,5/2,5 об./об., комнатная температура, 1 ночь; (iii) 1 экв. 4-диметиламинопиридина (DMAP), 1 экв. 1-(3-диметиламинопропил)-3-этилкарбодиимид гидрохлорида (EDC), N,N-диметилацетамид (DMA), комнатная температура, 2 дня.
Фиг.2 представляет Схему 2:
Реактивы и условия: (i) 1 экв. 1-(2-аминоэтил)-2-метил-5-нитроимидазол дигидрохлорид моногидрата, 1 экв. SCN-Ph-SO2NH2, 2 экв. триэтиламина, MeCN, комнатная температура, 1 час.
Фиг.3 представляет схему предпочтительного соединения по изобретению: Реактивы и условия: (i) 1 экв. 1-(2-аминоэтил)-2-метил-5-нитроимидазол дигидрохлорид моногидрата, 4 экв. триэтиламина, 1 экв. хлорсульфонилизоцианата, 1 экв. трет-бутанола, CH2Cl2, комнатная температура, 1 час; (iii) трифторуксусная кислота CH2Cl2 7/3, комнатная температура, 6 часов.
Фиг.4 представляет схему второго предпочтительного соединения по изобретению Реактивы и условия: (i) 1 экв. 2-метил-5-нитро-1-имидазолилэтанола, N,N-диметилацетамид, 3 экв. сульфамоилхлорида, комнатная температура, 1 ночь.
Соединения по настоящему изобретению могут быть синтезированы в соответствии со следующими методиками. Все реактивы и растворители были рыночного качества и использовались без дополнительной очистки, если специально не указано иное. Все реакции проводили в инертной атмосфере азота. TLC-анализы выполняли на силикагелевых пластинах 60 F254 (Merck Art. 1.05554). Пятна визуализировали при освещении УФ 254 нм или путем опрыскивания раствором нингидрина. Точку плавления (тр) определяли на Büchi Melting Point 510 и представлены без поправок. Спектры 1H и 13C ЯМР регистрировали на спектрометре Bruker DRX-400, используя DMSO-d6 в качестве растворителя и тетраметилсилан в качестве внутреннего стандарта. Для спектров 1H ЯМР химические сдвиги выражали в δ (ppm) в сторону слабого поля от тетраметилсилана, а константы взаимодействия (J) выражали в Герцах (Hz). Масс-спектры ионизации электронами регистрировали в положительном или отрицательном режиме на приборе Water MicroMass ZQ.
Речь идет о прилагаемых фиг.1 и 2.
трет-бутил-(2-нитро-имидазол-1-ил) ацетат (2): К смеси 2-нитроимидазола 1 (17,7 ммоль; 1 экв.) и безводного карбоната калия (70,74 ммоль; 4 экв.) в 20 мл ацетонитрила по каплям добавили раствор трет-бутилбромацетата (17,7 ммоль; 1 экв.) в 10 мл ацетонитрила. Смесь перемешивали одну ночь при комнатной температуре и концентрировали под вакуумом. Остаток очищали с помощью хроматографии на силикагеле, используя смесь CH2Cl2/MeOH 95/5 в качестве элюента, с получением ожидаемого соединения в виде белого порошка с выходом 71%. Тпл 95-97°С; 1H ЯМР (DMSO-d6, 400 MHz) δ 1.46 (s, 9H), 4.99 (s, 2H), 7.06 (d, 1H, J=1.01 Hz), 7.17 (d, 1H, J=1.01 Hz). MS(ESI+/ESI-) m/z 226.15 [M-H]-, 262.13 [M+Cl]-, 250.20 [M+H]+.
(2-нитро-имидазол-1-ил) уксусная кислота (3): Соединение 2 (2,5 г) растворили в 20 мл смеси из TFA, воды, тиоанизола 95-2.5-2.5 и перемешивали при комнатной температуре в течение одной ночи. Затем смесь концентрировали под вакуумом и несколько раз выпаривали совместно с диэтиловым эфиром до образования порошка. После фильтрования осадок промывали дихлорметаном и ацетонитрилом с получением ожидаемого продукта в количественном отношении. Тпл 143°C (разложение); 1H ЯМР (DMSO-d6, 400 MHz) δ 5.21 (s, 2H), 7.21 (d, 1H, J=1.01 Hz), 7.64 (d, 1H, J=1.01 Hz). 13C (DMSO-d6, 101 MHz) δ 50.65, 127.69, 128.44, 168.56, 168.57; MS (ESI+/ESI-) m/z 170.12 [M-H]- 341.05 [2M-H]- 194.14 [M+Na]+.
Общий метод получения соединений (4a-d)
К раствору соединения 3 (1,17 ммоль; 1 экв.) в 8 мл N,N-диметилацетамида добавили аминоалкилбензол сульфонамид (1,17 ммоль; 1 экв.), 4-диметиламинопиридин (1,17 ммоль; 1 экв.) и 1-этил-3-(3-диметиламинопропил) карбодиимид (1,17 ммоль; 1 экв.). Смесь перемешивали два дня при комнатной температуре, затем разбавили этилацетатом и три раза промыли водой. Органический слой высушили над безводным сульфатом магния, профильтровали и концентрировали под вакуумом. Затем остаток очистили с помощью хроматографии на силикагеле, используя смесь метиленхлорид - метанол 98-2 об. - об. как элюент.
2-(2-нитро-имидазол-1-ил)-]N-(4-сульфамоилфенил)ацетамид (4a, DH296): Выход: 68%; Тпл 163-165°C; 1H ЯМР (DMSO-d6 400 MHz) δ 5.36 (s, 2H), 7.24 (d, 1H, J=1.01 Hz), 7.28 (s, 2H), 7.67 (d, 1H, J=1.01 Hz), 7.70 (d, 2H, J=8.9Hz), 7.77 (d, 2H, J=8.9Hz), 10.7 (s, 1H); 13C (DMSO-d6, 101 MHz) δ 52.20, 118.70, 126.81, 127.57, 128.84, 138.76, 141.18, 144.79, 165.02; MS (ESI+/ESI-) m/z 324.09 [M-H]- 359.92 [M+Cl]-, 649.15 [2M-H]-, 685.01 [2M+Cl]-, 348.14 [M+Na]+.
2-(2-нитро-имидазол-1-ил)-N-(3-сульфамоилфенил)ацетамид (4b, DH304): Выход: 79%; Тпл 195-197°C; 1H ЯМР (DMSO-d6, 400 MHz) δ 5.35 (s, 2H), 7.24 (d, 1H, J=1.01Hz), 7.38 (s, 2H), 7.52 (m, 2H), 7.65 (m, 1H), 7.67 (d, 1H, J=1.01H), 8.14 (s, 1H), 10.81 (s, 1H); 13C (DMSO-d6 101 MHz) δ 52.16, 116.10, 120.72, 121.92, 127.59, 128.86, 129.67, 138.67, 144.72, 164.87, 167.75; MS (ESI+/ESI-) m/z 324.24 [M-H]-, 360.18 [M+Cl]-, 685.13 [2M+Cl]-, 326.24 [M+H]+, 348.07 [M+Na]+, 364.17 [M+K]+, 673.18 [2M+Na]+.
2-(2-нитро-имидазол-1-ил)-N-(4-сульфамоилбензил)ацетамид (4c, DH305): Выход: 83%; Тпл 181-183°C; 1H ЯМР (DMSO-d6, 400 MHz) δ 4.37 (d, 2H, J=5.7 Hz), 5.22 (s, 2H), 7.18 (d, 1H, J=1.01 Hz), 7.35 (s, 2H), 7.43 (d, 2H, J=8.4 Hz), 7.67 (d, 1H, J=1.01 Hz), 7.76 (d, 2H, J=8.4 Hz), 9.15 (t, 1H, J=6.06 Hz); 13C (DMSO-d6, 101 MHz) δ 41.81, 51.55, 106.87, 125.58, 127.39, 138.91, 142.66, 142.99, 156.82, 165.88; MS (ESI+/ESI-) m/z 338.15 [M-H]- 374.22 [M+Cl]- 713.16 [2M+Cl]- 340.15 [M+H]+, 362.17 [M+Na]+.
2-(2-нитро-имидазол-1-ил)-N-[2-(4-сульфамоилфенил)этил]ацетамид (4d, DH302): Выход: 89%; Тпл 139-141°C; 1H ЯМР (DMSO-d6, 400 MHz) δ 2.80 (t, 2H, J=6.9 Hz), 3.16 (m 2H), 5.07 (s, 2H), 7.18 (d, 1H, J=1.01 Hz), 7.30 (s, 2H), 7.40 (d, 2H, J=8.2 Hz), 7.61 (d, 1H, J=1.01 Hz), 7.74 (d, 2H, J=8.2 Hz), 8.46 (t, 1H, J=5.6 Hz); 13C (DMSO-d6 101 MHz) δ 34.59, 51.49, 125.64, 127.38, 128.74, 129.09, 142.05, 143.39, 144.87, 165.57; MS (ESI+/ESI-) m/z 352.19 [M-H]- 388.07 [M+Cl]-, 354.12 [M+H]+, 376.09 [M+Na]+, 729.21 [2M+Na]+.
Общий метод получения соединений (6a-d): К раствору коммерчески доступного соединения 5 (0,76 ммоль; 1 экв.) в 10 мл ацетонитрила добавили соответствующий изотиоцианат (0,76 ммоль; 1 экв.). Реакцию перемешивали в течение одного часа при комнатной температуре и затем смесь профильтровали. Фильтрат концентрировали под вакуумом, а полученный осадок очищали с помощью хроматографии на силикагеле с использованием метиленхлорида - метанола 95-5 в качестве элюента.
N-(4-сульфамоилфенил)-N-((2-аминоэтил)-2-метил-5-нитроимидазолил) тиомочевина (6a, DH307): Выход: 72%; Тпл 186-188°C; 1H ЯМР (DMSO-d6, 400 MHz) δ 2.42 (s, 3H), 3.91 (m, 2H), 4.5 (t, 2H, J=5.68 Hz), 7.3 (s, 2H), 7.46 (d, 2H, J=8.7 Hz), 7.71 (d, 2H, J=8.7Hz), 8.05 (s, 2H), 10.0 (s, 1H); 13C (DMSO-d6 101 MHz) δ 13.81, 42.87, 44.86, 122.46, 126.30, 133.19, 138.66, 139.14, 141.88, 151.35, 180.88; MS (ESI+/ESI-) m/z 385.17 [M+H]+, 407.07 [M+Na]+, 769.22 [2M+H]+, 383.21 [M-H]- 419.18 [M+Cl]-, 767.16. [2M-H]-
N-(3-сульфамоилфенил)-N-((2-аминоэтил)-2-метил-5-нитроимидазолил) тиомочевина (6b, DH309): Выход: 75%; Тпл 66-68°C; 1H ЯМР (DMSO-d6, 400 MHz) δ 2.43 (s, 3H), 3.91 (m, 2H), 4.49 (t, 2H, J=5.68Hz), 7.39 (s, 2H), 7.51 (m, 1H), 7.55 (s, 1H), 7.57 (m, 1H), 7.81 (s, 1H, 1H), 7.93 (m, 1H), 8.04 (s, 1H), 9.94 (s, 1H); 13C (DMSO-d6 101 MHz) δ 13.81, 42.82, 44.99, 120.29, 121.39, 126.62, 129.09, 133.18, 138.65, 139.51, 144.35, 151.37, 181.28; MS (ESI+/ESI-) m/z 385.23 [M+H]+, 406.94 [M+Na]+, 791.19 [2M+Na]+, 383.12 [M-H]-, 419.09 [M+Cl]-, 767.26 [2M-H]-.
N-(4-сульфамоилбензил)-N-((2-аминоэтил)-2-метил-5-нитроимидазолил) тиомочевина (6c, DH310): Выход: 82%; Тпл 67-69°C; 1H ЯМР (DMSO-d6 400 MHz) δ 2.37 (s, 3H), 2.87 (m, 2H), 4.43 (t, 2H, J=5.18 Hz), 4.70 (br s, 2H), 7.32 (s, 2H), 7.34 (d, 2H, J=8.4Hz), 7.68 (s, 1H), 7.75 (d, 2H, J=8.4 Hz), 8.03 (s, 1H), 8.15 (s, 1H); 13C (DMSO-d6, 101 MHz) δ 13.84, 30.64, 42.70, 45.44, 125.52, 127.23, 133.17, 138.61, 142.48, 151.41, 181.44; MS (ESI+/ESI-) m/z 399.23 [M+H]+, 421.16 [M+Na]+, 797.08 [2M+H]+, 819.26 [2M+Na]+, 397.10 [M-H]-, 433.09 [M+Cl]-, 795.33 [2M-H]-.
N-(4-сульфамоилфенилэтил)-N-((2-аминоэтил)-2-метил-5-нитроимидазолил) тиомочевина (6d; DH308): Выход: 86%; Тпл 75-77°C; 1H ЯМР (DMSO-d6 400 MHz) δ 2.35 (s, 3H), 2.83 (m, 2H), 3.62 (m, 2H), 3.82 (m, 2H), 4.41 (m, 2H), 7.31 (s, 2H), 7.37 (d, 2H, J=8.2 Hz), 7.52 (s, 1H), 7.63 (s, 1H), 7.74 (d, 2H, J=8.2 Hz), 8.03 (s, 1H).; 13C (DMSO-d6, 101 MHz) δ 13.78, 30.64, 45.4, 125.65, 129.05, 133.18, 138.54, 142.03, 143.45, 151.42, 180.83; MS (ESI+/ESI-) m/z 413.06 [M+H]+, 435.02 [M+Na]+, 825.09 [2M+H]+, 847.21 [2M+Na]+, 411.06 [M-H]-, 447.20 [M+Cl]-, 822.99 [2M-H]-, 859.26 [2M+Cl]-.
Предпочтительные соединения (7) и (9)
N-[2-(2-метил-5-нитро-имидазол-1-ил)этил]сульфамид (7; DH348): К раствору соединения 5 (3,83 ммоль; 1 экв.) и триэтиламина (30,63 ммоль; 4 экв.) в 10 мл метиленхлорида добавили раствор хлорсульфонилизоцианата (4,59 ммоль; 1.2 экв.), трет-бутанол (4,59 ммоль; 1.2 экв.) в 2 мл метиленхлорида (приготовленный с нуля). Смесь перемешивали при комнатной температуре в течение одного часа, затем разбавили этилацетатом и промыли водой. Органический слой высушили над безводным сульфатом натрия, профильтровали и концентрировали под вакуумом. Осадок очистили с помощью хроматографии на силикагеле с использованием метиленхлорида-метанола 98-2 в качестве элюента. Затем промежуточное соединение развели в растворе трифторуксусной кислоты в метиленхлориде (30% объем), и перемешивали при комнатной температуре в течение 6 часов. Затем смесь концентрировали под вакуумом и несколько раз выпаривали совместно с диэтиловым эфиром до получения искомого сульфамида в виде белого порошка. Общий выход: 70%; Тпл 122°C; 1H ЯМР (DMSO-d6 400 MHz) δ 2.52 (s, 3H), 3.26 (m, 2H), 4.37 (t, 2H, J=5.81 Hz), 6.65 (s, 2H), 6.86 (s, 1H), 8.1 (s, 1H); 13C (DMSO-d6, 101 MHz) δ 14.03, 41.8, 46.0, 132.68, 138.26, 151.65; MS (ESI+/ESI-) m/z 250.19 [M+H]+, 272.34 [M+Na]+, 499.32 [2M+H]+, 249.09 [M-H]-, 284.12 [M+Cl]-, 533.14 [2M+Cl]-.
N[2-(2-метил-5-нитро-имидазол-1-ил)этил]сульфамат (9; DH338): К раствору коммерчески доступного соединения 8 (1,75 ммоль; 1 экв.) в N,N-диметилцетамиде добавили сульфамоил хлорид (5,25 ммоль; 3 экв.). Смесь перемешивали при комнатной температуре в течение ночи, затем разбавили этилацетатом и промыли водой три раза. Органический слой высушили над безводным сульфатом магния, профильтровали и концентрировали под вакуумом. Вещество очистили с помощью хроматографии на силикагеле с использованием метиленхлорида-метанола 9-1 в качестве элюента. Выход: 81%; Тпл 166-168°C; 1H ЯМР (DMSO-d6 400 MHz) δ 2.45 (s, 3H), 4.35 (t, 2H, J=5.05 Hz), 4.61 (t, 2H, J=5.05 Hz), 7.57 (s, 2H), 8.06 (s, 1H); 13C (DMSO-d6, 101 MHz) δ 14.04, 44.98, 57.21, 133.10, 138.32, 151.82; MS (ESI+/ESI-) m/z 250.3 [M+H]+, 272.32 [M+Na]+, 521.30 [2M+Na]+, 770.16 [3M+Na]+.
Эксперименты in vitro
Эффект соединений по изобретению в отношении ингибирования CA и вытекающего из этого влияния на внеклеточный ацидоз были исследованы с помощью классических химических и биологических методов анализа.
CA-ингибирующая активность
В следующем эксперименте была исследована ингибирующая активность соединений по изобретению в отношении карбоангидразы.
Были определены константы ингибирования (Ki) соединений в отношении следующих изоферментов CA: CA I, II, IX и XII. Для оценки катализируемой CA гидратации CO2 использовался прибор Applied Photophysics (Оксфорд, Великобритания) для исследований в остановленном потоке (Khalifah, 1971). В качестве индикатора использовали феноловый красный (в концентрации 0,2 мМ), действующий при максимуме поглощения 557 нм, с использованием 10 мМ Hepes (pH 7,5) в качестве буфера, 0,1 M Na2SO4 (для поддержания постоянной ионной силы), с последующей CA-катализируемой реакцией гидратации CO2 в течение периода 10-100 сек. Для определения кинетических параметров и констант ингибирования использовали концентрации CO2 в пределах от 1,7 до 17 мМ. Для каждого ингибитора для определения начальной скорости использовали по меньшей мере шесть прогонов исходных 5-10% реакции. Некатализированные скорости определяли тем же способом и вычитали из общих наблюдаемых скоростей. Стоковые растворы ингибитора (1 мМ) были приготовлены в дистиллированной-деионизированной воде с 10-20% (об./об.) DMSO (который не является ингибирующим при этих концентрациях) и после этого были сделаны разведения дистиллированной-деионизированной водой вплоть до 0,1 нМ. Ингибитор и растворы ферментов предварительно до анализа инкубировали вместе в течение 15 мин при комнатной температуре, для того, чтобы образовался комплекс CA IX-ингибитор. Константы ингибирования, полученные с помощью нелинейного метода наименьших квадратов с использованием PRISM 3, представляют собой средние значения по меньшей мере из трех разных определений.
Результаты приводятся в таблице 1 ниже.
| Таблица 1 | ||||
| Соединения | K1 (нМ) | |||
| hCA I | hCA II | hCA IX | hCA XII | |
| 9 (DH 338) | 4435 | 33,8 | 8,3 | 8,9 |
| 7 (DH 348) | 9576 | 10,1 | 20,4 | 8,1 |
| 6a (DH 307) | 105 | 5,5 | 7,3 | 8,0 |
| 6d (DH 308) | 84 | 6,6 | 7,8 | 7,6 |
| 6b (DH 309) | 483 | 7,4 | 7,2 | 7,7 |
| 6c (DH 310) | 79 | 2,9 | 8,3 | 8,5 |
| 4a (DH 296) | 3203 | 330 | 70 | 64 |
| 4d (DH 302) | 101 | 3,8 | 7,3 | 8,0 |
| 4b (DH 304) | 107 | 37 | 7,9 | 8,1 |
| 4c (DH 305) | 79 | 4,8 | 8,0 | 6,7 |
Ацидоз
Действие соединений по изобретению на ацидоз в опухолевых клетках было измерено в следующем эксперименте.
Цель экспериментов in vitro заключалась в оценке эффективности 4 соединений (7, 9, 6a и 6c) в понижении внеклеточного закисления в результате гипоксии.
Эксперимент проводили, как описано в уровне техники (Dubois et al, 2007). Линии клеток колоректальной карциномы (НТ-29) (фиг.5а) и рака шейки матки (HeLa) (фиг.5b) исследовали при нормоксии (концентрация кислорода в среде с нормальным содержанием кислорода) и в условиях гипоксии (0,2% кислорода). Известно, что клетки HT-29 являются конститутивными гипоксия-индуцибельными клетками, экспрессирующими CA DC (CA IX экспрессия при нормоксии и повышенная CA IX экспрессия при гипоксии). Поэтому соединения добавляли после 1 часа воздействия гипоксии (чтобы обеспечить активную CA IX) и проводили инкубацию в течение дополнительных 23 часов (всего 24 часа гипоксии). Клетки HeLa являются гипоксия-индуцибельными (при более низкой плотности) клетками, экспрессирующими CA DC. Поэтому клетки HeLa сначала инкубировали при гипоксии 24 часа, чтобы сначала обеспечить экспрессию CA DC (момент времени, оцененный в серии экспериментов, связанных со временем). После этого добавляли соединения по изобретению и инкубировали клетки в течение последующих 24 часов.
Эксперименты проводили три раза для каждого условия. Описанные условия были выполнены и для НТ-29 и для HeLa при нормоксии и при гипоксии. Были оценены следующие условия:
- Холостой образец (пустой) 1 мМ или 0.1 мМ (без добавления соединения, только DMSO/PBS)
- DH307 1 мМ или 0.1 мМ
- DH310 1 мМ или 0.1 мМ
- DH338 1 мМ или 0.1 мМ
- DH 348 1 мМ или 0.1 мМ
- S=AEBS (4-(2-аминоэтилбензолсульфонамид); Sigma) 1 мМ или ОД мМ (известный как уменьшающий внеклеточное значение рН, как описано в Svastova et al, 2004).
Клетки высевали в чашки 6 см (HT-29: 10е6; HeLa: 4×105: чтобы компенсировать размер клеток) в 5 мл DMEM с добавлением 10% FCS. На следующий день среду заменяли на 3,6 мл свежеприготовленной DMEM/FCS 10%, в которой было измерено значение pH (pH при инкубации), после чего чашки помещали в гипоксическую камеру (чашки с нормоксией держали в атмосферном воздухе в инкубаторе: 37°c, влажность 95%, 5% CO2). Добавляли соединения (через 1 час для НТ-29 или 24 час для HeLa после начала действия гипоксии) так, чтобы получить окончательную концентрацию 1 мМ или 0,1 мМ путем добавления 400 мкл в чашки, начиная от 10 или 1 мМ стокового раствора (окончательная концентрация DMSO 0,1%). В холостые контроли добавляли DMSO/PBS без соединения.
Значение pH среды измеряли через 24 часа (НТ-29) или 48 часов (HeLa) внутри гипоксической камеры после калибровки электрода по пониженным концентрациям кислорода. Была вычислена разница значений pH (pH в конце воздействия гипоксии - pH замещающей среды до инкубации) и показана на графике Фиг.5a и 5b.
Далее описаны важные результаты:
- Гипоксия приводит к внеклеточному закислению. Среда является более кислой в условиях «холостого образца» после гипоксии по сравнению с нормоксией.
- Контрольное соединение (S) эффективно уменьшало внеклеточное подкисление после гипоксии при 1 мМ концентрации (меньше при 0,1 мМ) для обеих клеточных линий. Эффект не наблюдался при нормоксии.
- Все соединения были способны уменьшать внеклеточное закисление. В отношении клеток HT-29 DH348 (соединение 7) и DH338 (соединение 9) давали самые лучшие результаты (1 мМ). При 0,1 мМ DH348 дает дополнительное снижение по сравнению с другими соединениями. В отношении клеток HeLa - все соединения эффективно уменьшали внеклеточное закисление. Соединение DH310 даже делало среду щелочной (1 мМ) и, кроме того, при 0,1 мМ вызывало сильное восстановление. Так как этот эффект не наблюдался на НТ-29, интерпретировать эти данные следует с осторожностью. DH348 продемонстрировал самые лучшие результаты на HeLa, и подтвердил данные, полученные для HT-29.
Эксперименты in vivo.
Целью этих экспериментов являлась оценка in vivo терапевтического эффекта DH348 в комбинации с обычными методами лечения, такими как радиотерапия и химиотерапия. Авторы предположили, что блокирование CA IX может одновременно уменьшить внутриклеточный ацидоз и таким образом увеличить эффект облучения, а также увеличить поглощение слабощелочного доксорубицина и, следовательно, его терапевтический эффект. Кроме того, разрешенный для применения в клинике сульфонамид ацетазоламид (AZA) - известный общий ингибитор карбонангидразы (что означает отсутствие специфичности по отношению к какой-либо одной CA) - использовался для того, чтобы подтвердить CA IX специфичность исследуемых соединений.
Использовали две экспериментальные модели. Первые эксперименты были проведены на исходных HT-29-ксенотрансплантатах. Вторые эксперименты были выполнены на НТ-29-ксенотрансплантатах, нокаутных по CA IX. shPHK конструкт против CA IX был введен в клетки НТ-29 с использованием pRETRO-супервектора. После селекции и скрининга клетки с эффективностью 95% нокаутные по CA IX были отобраны и обозначены как KD-клетки. В качестве контроля использовали scrambled (кодированный) конструкт shPHK, и эти клетки были обозначены как EV-клетки. Эти клетки по-прежнему демонстрировали экспрессию мРНК и белка CA. Ксенотрансплантаты опухолей получали путем инъецирования клеток колоректальной карциномы (1,5 10е6) подкожно в бок мышей NMRI-nu (весом 28-32 г). Рост опухоли контролировали, измеряя три раза в неделю размеры опухолей в 3-х взаимоперпендикулярных направлениях. Делали поправку измерений с учетом толщины кожи (-0,5 мм), а объем опухолей вычисляли с использованием формулы A×B×C pi/6, где A, B и C представляют собой взаимоперпендикулярные диаметры. DH348 вводили внутривенно (5×5 мг/кг внутривенно) в боковую хвостовую вену при достижении среднего объема опухолей 250 мм3. На 3 день животным давали анестезию фенобарбиталом натрия (нембутал, 0,1 мл/100 г веса тела), помещали их в поле облучения, используя изготовленный на заказ шаблон, и облучали однократной дозой 10 Грэй (15 мэВ электронный пучок) с использованием линейного ускорителя (Siemens). В другой группе животных на 3 день начинали лечение доксорубицином (5 мг/кг внутривенно, 1x/неделю в течение 3 недель). Контролировали рост опухолей и возможную токсичность лечения (3 раза в неделю) путем ежедневной оценки веса тела. Когда опухоли достигали четырехкратного объема по сравнению с исходным объемом, животных умерщвляли, а опухоли извлекали для дополнительного гистопатологического исследования. В целом, были использованы следующие лечебные группы, а результаты представлены на фигурах:
6a: HT-29 исходные