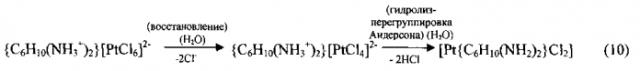Способ получения циклогексан-транс-1,2-d,l-диаминотетрахлорида платины (iv)
Иллюстрации
Показать всеИзобретение относится к области получения соединений платиновых металлов и фармацевтики, в частности к способу получения циклогексан-транс-1,2-d,l-диаминотетрахлорида платины(IV). Способ включает образование гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония из раствора платинохлористоводородной кислоты, причем выделение гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония проводят добавлением в солянокислый раствор платинохлористоводородной кислоты циклогексана-транс-1,2-d,l-диамина в ледяной уксусной кислоте, с последующим его отделением и гидролизом, который осуществляют при растворении гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония в водном растворе ацетата натрия с концентрацией 50-250 г CH3COONa·3H2O на 100 мл воды, взятого в количестве (300-800) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты, при 20-60°C в течение 0.5-5 часов. При этом процесс гидролиза проводят в реакторе, защищенном от прямого солнечного света и освещения, а выделение циклогексан-транс-1,2-d,l-диаминотетрахлорида платины(IV) из раствора гидролиза гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония проводят добавлением концентрированной соляной кислоты до pH раствора 1-3, высушиванием полученной суспензии при 60-90°C, растворением остатка в диэтиловом эфире, или ацетоне, или хлороформе, фильтрацией раствора от хлорида натрия и испарением диэтилового эфира, или ацетона, или хлороформа. Также предложены варианты способа. Изобретение позволяет усовершенствовать способ получения циклогексан-транс-1,2-d,l-диаминотетрахлорида платины(IV) в кристаллическом фазово-однородном состоянии [Pt{C6H10(транс-1,2-d,l-NH2)2}Cl4]·1/3H2O с высокой степенью чистоты, повысить стабильность синтеза, достичь высокого выхода целевого соединения. 3 н. и 15 з.п. ф-лы, 9 табл., 10 пр.
Реферат
Изобретение относится к области получения соединений платиновых металлов и фармацевтики, в частности синтезу соединений платины, а именно синтезу циклогексан-транс-1,2-d,l-диаминотетрахлорида платины(IV) (тетраплатин, ормаплатин), который является противоопухолевым препаратом.
Известен способ получения циклогексан-транс-1,2-d,l-диаминотетрахлорида платины(IV), включающий выделение циклогексан-транс-1,2-d,l-диаминодихлорида платины(II), при взаимодействии тетрахлороплатината(II) калия и циклогексан-транс-d,l-1,2-диамина, с последующим хлорированием продукта их взаимодействия (Eastland G.J. // Drugs Fut. 1987. V. 12.i.2. р. 139-141; Anderson W.K., Quagliato D.A., Haugwitz R.D., et al., // Cancer Treat. Rep. 1986. V. 70. Р. 997-1002). Процесс синтеза можно представить следующей схемой (циклогексан-транс-1,2-d,l-диамин - C6H10(NH2)2):
Недостатком способа является продолжительность и трудоемкость получения исходного тетрахлоридного комплекса Pt(II). При этом выход целевого продукта, с учетом выхода исходного K2[PtCl4] (при его синтезе из K2PtCl6 или H2PtCl6), составляет менее 65%.
Известен способ получения циклогексан-транс-1,2-d,l-диаминотетрахлорида платины(IV), основанный на взаимодействии гексахлороплатината(IV) калия с циклогексан-транс-1,2-d,l-диаммоний дихлоридом (Wyrig S.D., Chaney S.G. // J. Label. Compounds Radiopharm. 990. V. 28.i.7. Р. 753-756; Upjohn. Natl Canser Inst. // Drugs Fut. 1991. V. 16.i.2. р. 187). Синтез можно представить схемой:
Недостатком способа является также значительная продолжительность (более 10 часов) и низкий выход целевого продукта (менее 55%). При этом в процессе (2) используется малорастворимое соединение K2[PtCl6], что в значительной степени затрудняет проведение необходимых химических реакций.
Известен способ получения циклогексан-транс-1,2-d,l-диаминотетрахлорида платины(IV), в котором начальной стадией является взаимодействие платинохлористоводородной кислоты и циклогексан-транс-1,2-d,l-диаммоний дихлорида в растворе соляной кислоты с выделением ионного соединения циклогексан-транс-1,2-d,l-диаммоний гексахлороплатината(IV), который затем подвергается гидролизу в присутствии гидрооксида лития (Мулагалеев Р.Ф., Старков А.К, Кирик С.Д. // Патент РФ №2457838 от 10.08.2012. Бюл. №22). Общий процесс можно представить схемой:
Данный способ принят за прототип.
Недостатком способа является понижение выхода целевого соединения за счет частичного замещения хлоридных лигандов гидрооксидом и водой при добавлении гидрооксида лития. Присутствие ионов лития в растворе кристаллизации циклогексан-транс-1,2-d,l-диаминотетрахлорида платины(IV) делает необходимым дальнейшую очистку от них целевого продукта, и это приводит как к увеличению продолжительности синтеза, так и к уменьшению выхода продукта.
Задача изобретения состоит в разработке доступного и стабильного способа получения циклогексан-транс-1,2-d,l-диаминотетрахлорида платины(IV) (тетраплатина, ормаплатина) в кристаллическом монофазовом состоянии [Pt{C6H10(транс-1,2-d,l-NH2)2}Cl4]·1/3H2O с высокой степенью чистоты и высоким выходом.
Для решения поставленной задачи разработаны способ гидролиза гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония в водном растворе ацетата натрия до целевого циклогексан-транс-1,2-d,l-диаминотетрахлорида платины(IV) и способ восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония в водном растворе щавелевой кислоты, или оксалата натрия, или формиата натрия или гидразин гидрата с добавками ацетата натрия до циклогексан-тяранс-1,2-d,l-диаминодихлорида платины(II), который переводят в целевой продукт хлорированием или окислением перекисью водорода с последующей обработкой соляной кислотой.
Техническим результатом, на достижение которого направлено предлагаемое изобретение, является усовершенствование способа получения циклогексан-транс-1,2-d,l-диаминотетрахлорида платины(IV) в кристаллическом фазово-однородном состоянии [Pt{C6H10(транс-1,2-d,l-NH2)2}Cl4]·1/3H2O с высокой степенью чистоты, повышение стабильности синтеза, а также достижение высокого выхода целевого соединения.
Поставленная задача достигается тем, что образование циклогексан-транс-1,2-d,l-диаминотетрахлорида платины(IV) осуществлют гидролизом прекурсорного соединения - гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония или его восстановлением с последующим гидролизом до циклогексан-транс-1,2-d,l-диаминодихлорида платины(II), который окисляют хлором. Гидролиз прекурсорного соединения проводят при его растворении в водном растворе ацетата натрия с концентрацией (50-250) г CH3COONa·3H2O на 100 мл воды, взятого в количестве (300-800) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты, при (20-60)°C в течение (0.5-5) часов, при этом процесс гидролиза проводят в реакторе с перемешиванием и защищенном от прямого солнечного света и освещения. Выделение циклогексан-транс-1,2-d,l-диаминотетрахлорида платины(IV) из раствора гидролиза хлороплатината(IV) транс-1,2-d,l-диаммонийциклогексана ацетатом натрия проводят добавлением соляной кислоты до pH раствора (1-3), высушиванием полученной суспензии при (60-90)°C, растворением остатка в диэтиловом эфире, или ацетоне, или хлороформе, фильтрацией раствора от хлорида натрия и испарением диэтилового эфира, или ацетона, или хлороформа. Выделение прекурсорного соединения ведут из раствора платинохлористоводородной кислоты в концентрированной соляной кислоте с концентрацией платины (50-300) г/л, действием уксуснокислого или этанольного раствора циклогексан-транс-1,2-d,l-диамина, в котором на 1 г циклогексан-тэтраис-1,2-d,l-диамина приходится (5-20) мл ледяной уксусной кислоты или этанола, в количестве (100-120) % от мольного содержания платины в растворе, при температуре (20-60)°C.
Восстановление прекурсорного соединения до циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) проводят при его растворении в водном растворе щавелевой кислоты с концентрацией H2C2O4*2H2O (5-100) г на 100 мл воды в количестве (100-200) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты, при выдерживании образующегося раствора при (50-90)°C в течение (1-3) часов, с добавлением в образующийся раствор ацетата натрия с концентрацией в количестве (400-800) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты. Также восстановление прекурсорного соединения до циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) проводят в водном растворе оксалата натрия с концентрацией (3-6) г Na2C2O4 на 100 мл воды в количестве (100-400) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты, при выдерживании образующегося раствора при (50-90)°C в течение (1-3) часов с добавлением в образующийся раствор ацетата натрия в количестве (200-400) % CH3COONa·3H2O от мольного количества платины в исходном растворе платинохлористоводородной кислоты или в водном растворе формиата натрия с концентрацией HCOONa (10-150) г на 100 мл воды в количестве (95-100) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты, при выдерживании образующегося раствора при (30-50)°C в течение (1-3) часов, с добавлением в образующийся раствор ацетата натрия в количестве (300-400) % CH3COONa·3H2O от мольного количества платины в исходном растворе платинохлористоводородной кислоты или в водном растворе гидразин хлорида с концентрацией N2H4·2HCl (5-50) г на 100 мл воды в количестве (50-55) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты, при выдерживании образующегося раствора при (30-50)°C в течение (1-3) часов, с добавлением в образующийся раствор ацетата натрия в количестве (400-800) % CH3COONa·3H2O от мольного количества платины в исходном растворе платинохлористоводородной кислоты.
Окисление промежуточного циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) проводят через отделение его от раствора фильтрованием, суспендированием осадка в 10%-ном водном растворе соляной кислоты или хлороформе, взятом в количестве (10-25) мл на 1 г платины в исходном растворе платинохлористоводородной кислоты, и пропусканием хлора в полученную суспензию до растворения осадка, с последующим испарением раствора при (60-90)°C или при перемешивании суспензии циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) в (20-100) мл (5-30) %-ном по массе растворе перекиси водорода исходя из 1 г платины в исходном растворе платинохлористоводородной кислоты, в течение (2-4)-х часов при (40-80)°C, добавлении в полученную суспензию концентрированной соляной кислоты в количестве (2-5) мл на 1 г платины в исходном растворе платинохлористоводородной кислоты и перемешивании полученной суспензии до растворения осадка с дальнейшим испарением полученного раствора при (60-90)°C.
Процесс восстановления прекурсорного соединения до циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) можно также проводить и без выделения прекурсора, а восстановление с последующим гидролизом до циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) проводят в водном растворе щавелевой кислоты с концентрацией H2C2O4*2H2O (20-100) г на 100 мл воды в количестве (100-150) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты, при выдерживании образующегося раствора при (50-90)°C в течение (1-3) часов, с добавлением в образующийся раствор ацетата натрия в количестве (400-800) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты. Также восстановление прекурсорного соединения проводят в водном растворе оксалата натрия с концентрацией (3-6) г Na2C2O4 на 100 мл воды в количестве (100-400) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты, при выдерживании образующегося раствора при (50-90)°C в течение (1-3) часов с добавлением в образующийся раствор ацетата натрия в количестве (200-400) % CH3COONa·3H2O от мольного количества платины в исходном растворе платинохлористоводородной кислоты или в водном растворе формиата натрия с концентрацией HCOONa (10-150) г на 100 мл воды в количестве (95-100) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты, при выдерживании образующегося раствора при (30-60)°C в течение (1-3) часов, с добавлением в образующийся раствор ацетата натрия в количестве (300-400) % CH3COONa·3H2O от мольного количества платины в исходном растворе платинохлористоводородной кислоты или в водном гидразин хлорида с концентрацией N2H4·2HCl (5-50) г на 100 мл воды в количестве (50-55) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты, при выдерживании образующегося раствора при (30-60)°C в течение (1-3) часов, с добавлением в образующийся раствор ацетата натрия в количестве (400-800) % CH3COONa·3H2O от мольного количества платины в исходном растворе платинохлористоводородной кислоты. При этом образование прекурсорного соединения осуществляют из водного раствора платинохлористоводородной кислоты с концентрацией платины (50-150) г/л, действием водного раствора циклогексан-транс-1,2-d,l-диамина, в котором на 1 г циклогексан-транс-1,2-d,l-диамина приходится (5-20) мл воды, в количестве (99-101) % от мольного содержания платины в растворе при (15-60)°C.
Сущность способа состоит в том, что в системе циклогексан-транс-1,2-d,l-диаммоний - гексахлороплатинат(IV) образуется ряд катион-анионных соединений состава {C6H10(NH3)2}x[PtCl6]yzL (где L - сольватная молекула, x, y, z - стехиометрические коэффициенты), которые могут быть подвергнуты гидролизу, сопровождающемуся реакцией обмена внутрисферных хлоридных лигандов на группировки, играющие роль противоионов (перегруппировка Андерсона), или могут быть восстановлены до катион-анионных соединений Pt(II) {C6H10(NH3)2}x[PtCl4]y*zL, которые еще в большей степени подвержены гидролизу с параллельным замещением внутрисферных хлоридных лигандов (перегруппировке Андерсона).
Проведенные исследования фазообразования в системе циклогексан-транс-1,2-d,l-диаммоний - гексахлороплатинат(IV) показали, что варьированием температуры, кислотности раствора и изменением химических и физических свойств растворителя можно выделить целый ряд кристаллических фаз. В исследованных экспериментальных условиях были выделены в фазово-однородном состоянии и охарактеризованы химическим анализом, рентгено-фазовым анализом и методом дифференциальной сканирующей калориметрии с анализом выделяющихся газов следующие соединения: α- и β-{C6H10(NH3)2}[PtCl6]; {C6H10(NH3)2}[PtCl6]*H2O; α- и β-{C6H10(NH3)2}[PtCl6]*HCl; {C6H10(NH3)2}[PtCl6]*2HCl; {C6H10(NH3)2}2[PtCl6]*2Cl. В предлагаемом способе выделяемым прекурсором синтеза тетраплатина является смесь кристаллических фаз α-{CбH10(NH3)2}[PtCl6], {C6H10(NH3)2}[PtClб]*H2O и α- и β-{C6H10(NH3)2}[PtCl6]*HCl, где основным компонентом (с содержанием более 60% - в зависимости от условий кристаллизации) является первая фаза соответственно.
За счет своей ионной природы соединения {CбH10(NH3)2}x[PtCl6]y*zL имеют возможность взаимодействовать со многими полярными растворителями, что позволяет эффективно управлять их выделением из раствора. Поэтому такие катион-анионные соединения могут быть эффективными прекурсорами циклогексан-транс-1,2-d,l-диаминотетрахлорида платины(IV).
Гидролиз катион-анионного соединения, образующегося в системе циклогексан-транс-1,2-d,l-диаммоний - гексахлороплатинат(1У), приводит к депротонизации диамина, что сопровождается замещением хлоридных лигандов на аминный в координационном окружении платины (перегруппировка Андерсона):
В случае синтеза соединения с соотношением катионной и анионной части 1:1, состав исходного соединения {C6H10(NH3)2}[PtCl] регулирует соотношение между [PtCl6]2- и амином, что приводит к образованию только тетрахлоридного комплекса.
Так как вода менее склонна к протонизации, чем диаминциклогексан, для смещения равновесий (4)-(5) необходимо введение дополнительных акцепторов протона. В водных растворах такую роль, как правило, выполняют гидрооксиды. В связи с этим для реализации равновесий (4)-(5), протекающих в водном растворе, необходимо подавить возможное замещение хлоридных лигандов на воду и гидроксид (E. Blasius, W. Preetz, R. Schmitt // J. Inorg. Nucl. Chem. 1961. V. 19.i.1-2. Р. 115-132; С.И. Гинзбург, Н.А. Езерская, И.В. Прокофьев и др. // Аналитическая химия платиновых металлов. М. Наука. 1972. С. 70-73.):
Поэтому образование [Pt{C6H10(NH2)2}Cl4], через равновесия (4)-(5), обуславливается нейтрализацией протонов без смещения кислотности раствора в нейтральную или щелочную область и устойчивостью комплексообразования амина к Pt(IV). Так как устойчивость координационной связи Pt(IV)-NH2R выше чем Pt(IV)-Cl, то образование тетрахлоридного комплекса по реакциям (4)-(5) будет обусловлено кислотно-основным балансом в реакционной системе.
В данном случае подходящим реагентом для подавления избыточной кислотности может быть ацетат натрия. Его гидролиз:
позволяет реализовать взаимодействия (4)-(5) и поддерживать необходимый кислотно-основной баланс без побочных взаимодействий (6)-(7). Поэтому предлагаемый процесс, в общем виде, можно представить уравнением:
При гидролизе ацетата натрия (8) образуется уксусная кислота, замедляющая процесс (9), в связи с этим ацетат натрия используют в избытке, который нивелирует кислотность выделяющейся уксусной кислоты и позволяет провести взаимодействие (9) практически полностью. Раствор, в котором проводится реакция (9), является водным, что способствует частичному растворению целевого продукта. Для предотвращения таких потерь используется испарение раствора. Однако для этого необходимо выдерживание продукта при относительно повышенных температурах, при которых реализуются побочные процессы, приводящие к понижению его выхода. Поэтому перед испарением раствора добавляется соляная кислота, которая стабилизирует образовавшийся диаминтетрахлорид и переводит избыток ацетата натрия в хлорид натрия, который удаляется фильтрованием при растворении целевого соединения в органическом растворителе (ацетоне, или диэтиловом эфире, или хлороформе), в котором хлорид натрия не растворим.
За счет хорошей растворимости тетраплатина в водном растворе и других органических растворителях, а также сопутствующих трудностей, связанных с выделением этого соединения в чистом состоянии с высоким выходом, бывает удобнее использовать процесс восстановления {C6H10(NH3)2}[PtClб] до {C6H10(NH3)2}[PtCl4] с дальнейшим образованием [Pt{C6H10(NH2)2}Cl2], которое малорастворимо и за счет меньшей инертности Pt(II) по сравнению с Pt(IV) быстрее образуется:
Далее диаминдихлоридный комплекс подвергается окислению до целевого тетрахлорида:
Выделение [Pt{C6H10(NH2)2}Cl4] из системы (11) уже не представляет трудностей, так как из-за малой растворимости [Pt{C6H10(NH2)2}Cl2] можно добиться его высокой чистоты и выхода, а окисление из-за большей устойчивости рассматриваемых комплексов Pt(IV) по сравнению с Pt(II) протекает практически количественно.
В качестве восстановителя в процессе (10) используется щавелевая кислота, или оксалат натрия, или формиат натрия, или гидразин хлорид. Преимущества щавелевой кислоты и оксалата натрия в том, что они не восстанавливают платину до металла и их можно использовать в избытке, а формиат натрия и оксалат натрия, кроме восстановительных свойств, проявляют и свойства кислотно-основного буфера, что в дальнейшем можно использовать для гидролитического перевода ионного соединения Pt(II) в молекулярный комплекс Pt(II).
Конечная стадия синтеза целевого соединения по процессу (10)-(11) осуществляется хлорированием [Pt{C6H10(NH2)2}Cl2] в солянокислом водном растворе или в хлороформе в присутствии остаточной воды (после отделения [Pt{C6H10(NH2)2}Cl2] фильтрованием и суспендирования в хлороформе без высушивания от воды), так как это способствует лучшей растворимости диаминтетрахлоридного соединения и его конечной кристаллизации в устойчивой гидратной форме - [Pt{C6H10(NH2)2}Cl4]·1/3H2O. Более "мягкое" окисление [Pt{C6H10(NH2)2}Cl2] осуществляется перекисью водорода до промежуточного [Pt{C6H10(NH2)2}(ОН)2Cl2], которое прогреванием в соляной кислоте переходит в целевой тетрахлорид.
В ходе проведенных исследований установлено, что для проведения процесса получения циклогексан-транс-1,2-d,l-диаминотетрахлорида платины(IV) через образование хлороплатината(IV) транс-1,2-d,l-диаммонийциклогексана оптимальными параметрами являются:
- концентрация платины в исходном растворе платинохлористоводородной кислоты в концентрированной соляной кислоте (для выделения гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония) - (50-300) г/л;
- температура осаждения прекурсорного соединения - гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония - (20-60)°C;
- количество циклогексан-транс-1,2-d,l-диамина для проведения осаждения - (100-120) % от мольного содержания платины в растворе;
- объем ледяной уксусной кислоты или этанола для растворения циклогексан-транс-1,2-d,l-диамина и получения его раствора для осаждения прекурсорного соединения - (5-20) мл на 1 г циклогексан-транс-1,2-d,l-диамина;
- количество CH3COONa·3H2O от мольного количества платины в исходном растворе платинохлористоводородной кислоты для проведения гидролиза прекурсорного соединения - (300-800) %;
- содержание CH3COONa·3H2O в водном растворе для проведения гидролиза прекурсорного соединения - (50-250) г на 100 мл воды;
- температура гидролиза прекурсорного соединения - (20-70)°C;
- продолжительность гидролиза прекурсорного соединения - (0.5-5) часов;
- pH кислотности раствора при добавлении концентрированной соляной кислоты в суспензию, полученную после гидролиза для ее высушивания - (1-3);
- температура высушивания суспензии, полученной при гидролизе - (60-90)°C;
- количество H2C2O4·2H2O для восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония - (100-200) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты;
- концентрация H2C2O4·2H2O для восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония - (5-100) г на 100 мл воды;
- количество CH3COONa·3H2O для гидролиза восстановленного раствора гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония щавелевой кислотой или гидразин хлоридом до циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) - (400-800) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты;
- температура восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония щавелевой кислотой или оксалатом натрия - (50-90)°C;
- продолжительность выдерживания раствора для восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония щавелевой кислотой, или оксалатом натрия, или формиатом натрия, или гидразин хлоридом - (1-3) часа;
- объем жидкой фазы хлороформа или 10%-ного водного раствора соляной кислоты в суспензии для окисления циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) хлором - (10-25) мл на 1 г платины в исходном растворе платинохлористоводородной кислоты;
- температура испарения раствора после окисления циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) хлором - (60-90)°C;
- количество Na2C2O4 для восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония - (100-400) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты;
- концентрация Na2C2O4 для восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония - (3-6) г на 100 мл воды;
- количество CH3COONa·3H2O для гидролиза восстановленного раствора гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония (оксалатом натрия) до циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) - (200-400) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты;
- количество HCOONa для восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония - (95-100) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты;
- концентрация HCOONa для восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония - (10-150) г на 100 мл воды;
- количество CH3COONa·3H2O для гидролиза восстановленного раствора гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония формиатом натрия до циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) - (300-400) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты;
- температура раствора для восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония формиатом натрия или гидразин хлоридом - (30-60)°C;
- количество N2H4·2HCl для восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония - (50-55) % от мольного количества платины в исходном растворе платинохлористоводородной кислоты;
- концентрация N2H4·2HCl для восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония - (5-50) г на 100 мл воды;
- концентрация платины в исходном растворе платинохлористоводородной кислоты в воде (для образования, но не выделения гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония) - (50-150) г/л;
- количество циклогексан-транс-1,2-d,l-диамина (для образования, но не выделения гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония) - (99-101) % от мольного содержания платины в растворе;
- объем воды для растворения циклогексан-транс-1,2-d,l-диамина (для образования, но не выделения гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония) - (5-20) мл на 1 г циклогексан-транс-1,2-d,l-диамина;
- температура образования гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония (для образования, но не выделения) - (15-60)°C;
- объем водного раствора перекиси водорода для окисления циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) - (20-100) мл на 1 г платины в исходном растворе платинохлористоводородной кислоты;
- массовое содержание перекиси водорода в водном растворе для окисления циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) - (5-30) %;
- продолжительность перемешивания водного раствора перекиси водорода и циклогексан-транс-1,2-4 /-диаминодихлорида платины(II) - (2-4) ч;
- температура прогревания водного раствора перекиси водорода и циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) при перемешивании - (40-80)°C;
- объем концентрированной соляной кислоты, добавляемый в суспензию водного раствора перекиси водорода и циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) после перемешивания - (2-5) мл на 1 г платины в исходном растворе платинохлористоводородной кислоты;
- температура испарения раствора, полученного после добавления соляной кислоты в суспензию водного раствора перекиси водорода и циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) - (60-90)°C.
Увеличение концентрации платины в исходном растворе платинохлористоводородной кислоты в концентрированной соляной кислоте (случай выделения прекурсора - гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония) более 300 г/л приводит к образованию слишком плотной суспензии при кристаллизации прекурсора. Это вызывает трудности перемешивания и создает условия неполного взаимодействия, что приводит к понижению выхода прекурсора и его кристаллической неоднородности. Уменьшение концентрации платины в исходном растворе платинохлористоводородной кислоты в концентрированной соляной кислоте менее 50 г/л приводит к разбавлению раствора кристаллизации, что может приводить к уменьшению выхода прекурсора, вызывает излишний расход соляной кислоты и приводит (после отделения прекурсора фильтрацией) к увеличению фильтрационных (маточных) растворов.
Увеличение температуры осаждения прекурсорного соединения (гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония) выше 60°C может приводить к реализации побочных процессов взаимодействия органического амина и хлоридного комплекса платины, что ведет к загрязнению прекурсорного соединения, которое может перейти и на целевое соединение. Уменьшение температуры осаждения прекурсорного соединения (гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония) ниже 20°C приводит к относительно большому снижению дисперсности осадка, что приводит к более длительному процессу фильтрации и может сопровождаться частичным прохождением осадка через фильтр.
Увеличение количества циклогексан-транс-1,2-d,l-диамина для проведения осаждения прекурсора более 120% от мольного содержания платины в растворе приводит к его излишнему расходованию, что приводит к удорожанию процесса. При этом избыток органического диамина может вызывать образование катион-анионного соединения с соотношением в нем платины и органического диамина 1:2, что при дальнейшем гидролизе приводит к частичному образованию тетрааминного комплекса платины, который может как загрязнять целевой продукт, так и снижать его выход. Уменьшение количества циклогексан-транс-1,2-d,l-диамина для проведения осаждения прекурсора менее 100% от мольного содержания платины в растворе приводит к его недостатку, что снижает выход прекурсора.
Увеличение объема ледяной уксусной кислоты или этанола, для растворения циклогексан-транс-1,2-d,l-диамина и получения его раствора для осаждения прекурсорного соединения, более 20 мл на 1 г циклогексан-транс-1,2-d,l-диамина приводит к излишнему разбавлению образующейся суспензии прекурсора и излишнему расходованию растворителя, что увеличивает затраты на проведение процесса. Уменьшение объема ледяной уксусной кислоты или этанола, для растворения циклогексан-транс-1,2-d,l-диамина и получения его раствора для осаждения прекурсорного соединения, менее 5 мл на 1 г циклогексан-транс-1,2-d,l-диамина приводит к излишне плотному раствору диамина или даже его неполному растворению, что приводит к неравномерной кристаллизации гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония и может сопровождаться частичным захватом непрореагировавших реагентов в кристаллическую оболочку прекурсора, что приводит к неполному взаимодействию и понижает выход прекурсора.
Увеличение количества CH3COONa·3H2O более 500% от мольного количества платины в исходном растворе платинохлористоводородной кислоты для проведения гидролиза прекурсорного соединения приводит к излишнему расходованию реагента, что увеличивает затраты на проведение процесса. При этом большой избыток ацетата натрия может приводить к реализации побочных взаимодействий замещения хлоридных лигандов на воду и гидроксид (равновесия 6-7), что приводит к загрязнению целевого соединения и понижению его выхода. Уменьшение количества CH3COONa·3H2O менее 300% от мольного количества платины в исходном растворе платинохлористоводородной кислоты для проведения гидролиза прекурсорного соединения приводит к неполному гидролизу прекурсора, что уменьшает выход целевого продукта.
Увеличение содержания CH3COONa·3H2O в водном растворе для проведения гидролиза прекурсорного соединения более 250 г на 100 мл воды может приводить к неполному растворению ацетата натрия и, как следствие, к его неполному расходованию и недостатку в реакционной системе, что уменьшает выход целевого соединения. При этом проведение гидролиза в слишком концентрированном растворе может приводить к частичному захвату непрореагировавших реагентов в кристаллическую оболочку продукта, что также приводит к неполноте взаимодействия и уменьшению выхода целевого продукта. Уменьшение содержания CH3COONa·3H2O в водном растворе для проведения гидролиза прекурсорного соединения менее 50 г на 100 мл воды приводит к разбавлению раствора, что в дальнейшем требует более длительного упаривания, что увеличивает продолжительность процесса.
Увеличение температуры гидролиза прекурсорного соединения более 70°C может приводить к реализации побочных взаимодействий замещения хлоридных лигандов на воду и гидроксид (равновесия 6-7), что приводит к загрязнению целевого соединения и понижению его выхода. Уменьшение температуры гидролиза прекурсорного соединения менее 20°C приводит к увеличению продолжительности гидролиза и всего процесса и может приводить к неполноте взаимодействия, что понижает выход целевого соединения.
Увеличение продолжительности гидролиза прекурсорного соединения более 5 часов увеличивает продолжительность процесса без качественного улучшения свойств целевого соединения. Уменьшение продолжительности гидролиза прекурсорного соединения менее 0.5 часов может приводить к неполноте взаимодействия, что понижает выход продукта.
Увеличение кислотности раствора при добавлении концентрированной соляной кислоты в суспензию, полученную после гидролиза, для ее высушивания менее pH 1 приводит к избыточному содержанию соляной кислоты, что в дальнейшем увеличивает продолжительность упаривания. Уменьшение кислотности раствора при добавлении концентрированной соляной кислоты в суспензию, полученную после гидролиза, для ее высушивания более pH 3 может приводить к недостатку соляной кислоты для перевода всего ацетата натрия в хлорид натрия, что в дальнейшем может приводить к загрязнению целевого продукта ацетатом натрия (из-за его растворимости в органических растворителях). При этом недостаточная кислотность при упаривании суспензии после гидролиза может приводить к реализации побочных взаимодействий замещения хлоридных лигандов на воду и гидроксид (равновесия 6-7), что приводит к загрязению целевого соединения и понижению его выхода.
Увеличение температуры высушивания суспензии, полученной при гидролизе, более 90°C может приводить к реализации побочных процессов твердофазного востановления целевого продукта в циклогексан-транс-1,2-d,l-диаминодихлорид платины(II) и за счет частичного удаления хлоридных лигандов могут образовываться полиядерные соединения, что приводит к уменьшению выхода целевого соединения и его загрязнению. Уменьшение температуры высушивания суспензии, полученной при гидролизе, менее 60°C увеличивает продолжительность высушивания, что увеличивает продолжительность всего процесса.
Увеличение количества H2C2H4·2H2O для восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония более 200% от мольного количества платины в исходном растворе платинохлористоводородной кислоты может приводить к увеличению кислотности раствора, что приводит к неполному восстановлению прекурсора и вызывает снижение выхода промежуточного циклогексан-транс-1,2-d,l-диаминодихлорида платины(II). Уменьшение количества H2C2H4·2H2O для восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония менее 100% от мольного количества платины в исходном растворе платинохлористоводородной кислоты приводит к недостатку восстановителя, что является причиной неполного восстановления прекурсора, и снижает выход промежуточного (циклогексан-транс-1,2-d,l-диамин) дихлорида платины(II).
Увеличение концентрации H2C2H4·2H2O для восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония более 100 г на 100 мл воды может приводить к неполному растворению щавелевой кислоты при восстановлении прекурсора, что обуславливает неполноту взаимодействия и снижение выхода целевого соединения. Уменьшение концентрации H2C2H4·2H2O для восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония менее 5 г на 100 мл воды приводит к разбавлению раствора и уменьшению выхода промежуточного (циклогексан-транс-1,2-d,l-диамин)дихлорида платины(II).
Увеличение количества CH3COONa·3H2O для гидролиза восстановленного раствора гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония щавелевой кислотой или гидразин хлоридом до циклогексан-транс-1,2-4,/-диаминодихлорида платины(II) более 800% от мольного количества платины в исходном растворе платинохлористоводородной кислоты приводит к излишнему расходованию реагента, что увеличивает затраты на проведение процесса. Уменьшение количества CH3COONa·3H2O для гидролиза восстановленного раствора гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония щавелевой кислотой или гидразин хлоридом до циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) менее 400% от мольного количества платины в исходном растворе платинохлористоводородной кислоты приводит к неполному гидролизу прекурсора, что уменьшает выход целевого продукта.
Увеличение температуры восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония щавелевой кислотой или оксалатом натрия более 90°C может приводить к частичному удалению и замещению хлоридных лигандов гидроксо- и оксо-группами, что приводит к образовыванию малорастворимых полиядерных соединений, что ведет к загрязнению промежуточного циклогексан-транс-1,2-d,l-диаминодихлорида платины(II) и уменьшению выхода целевого соединения и его загрязнению. Уменьшение температуры восстановления гексахлороплатината(IV) циклогексан-транс-1,2-d,l-диаммония щавелевой кислотой или оксалатом натрия менее 50°C увеличивает продолжительность восстановления, что увеличивает продолжител