Иммунобиологическое средство на основе интерферона бета для терапии рака мочевого пузыря и способ его использования
Иллюстрации
Показать всеГруппа изобретений относится к медицине и касается иммунобиологического средства для лечения рака мочевого пузыря на основе аденовирусного вектора, содержащего ген интерферона бета под контролем промотора, где в качестве аденовирусного вектора используют аденовирус человека, а средство дополнительно включает фермент, который обеспечивает расщепление секрета слизистой оболочки мочевого пузыря. Также группа изобретений касается способа использования иммунобиологического средства для лечения рака мочевого пузыря, заключающегося во введении указанного иммунобиологического средства в мочевой пузырь. Группа изобретений обеспечивает пролонгированное действие иммунологического средства. 2 н. и 5 з.п. ф-лы, 5 пр., 5 ил., 1 табл.
Реферат
Область техники
Изобретение относится к иммунологии, а именно к иммунобиологическим композициям, и может быть использовано как иммуностимулирующее средство для лечения опухолей мочевого пузыря.
Предшествующий уровень техники
Интерфероны (ИФН) относятся к семейству цитокинов, обладающих мощным биологическим действием. Они секретируются клетками организма в ответ на вирусную инфекцию. В многочисленных исследованиях было показано, что интерфероны обладают не только противовирусной, но и противоопухолевой активностью, поскольку могут влиять на рост и дифференцировку клеток, модулировать реакции иммунной системы. Так, например, показана эффективность интерферонов при терапии опухолей молочной железы, легких, кишечника, мочевого пузыря и многих др.
Противоопухолевая терапия интерферонами является одним из перспективных направлений современной онкологии.
Изобретение согласно патенту US 8425896 B2 предусматривает решение, при котором интерферон альфа используют для лечения опухолей различной этиологии.
Известно также решение согласно патенту RU №2068709, которое предполагает использование интерферона альфа в комплексном лечении злокачественных новообразований почки и мочевого пузыря.
Изобретение согласно патенту US 5268169 A, подразумевает лечение рака яичников с использованием интерферона гамма для внутрибрюшинного введения в количествах, достаточных для эффективного лечения.
Известно также решение согласно патенту WO 2005123113 A2, в котором предлагаются композиции на основе интерферонов альфа и гамма и их использование для лечения различных заболеваний путем введения достаточного количества композиции.
В ряде работ было показано, что ИФН бета обладает более выраженным противоопухолевым эффектом, чем ИФН альфа или ИФН гамма. [Damdinsuren В, Nagano Н, Sakon М, et al. Interferon-β is more potent than interferon-α in inhibition of human hepatocellular carcinoma cell growth when used alone and in combination with anticancer drugs. Ann Surg Oncol. 2003; 10: 1184-1190. Vitale G, de Herder WW, van Koetsveld PM, et al. Interferon-beta is a highly potent inhibitor of gastroenteropancreatic neuroendocrine tumor cell growth in vitro. Cancer Res. 2006; 66: 554-562. The effect of α-, β- and λ-interferon on the growth of breast cancer cell lines. Anticancer Res. 1994; 14: 1779-1784.]
В патенте WO 2004020468 A2 представлено изобретение, которое предлагает использование интерферона бета в комплексном лечении солидных опухолей.
Известно также изобретение согласно патенту CA 2369427 A1, в котором интерферон бета используется для лечения опухолей Юинга.
Однако главным недостатком всех перечисленных технических решений является то, что интерфероны обладают краткосрочным действием, что приводит к необходимости многократных введений и использовании высоких доз, что в свою очередь приводит к высокой токсичности терапии. Поэтому актуальным является поиск новых лекарственных формуляций на основе интерферона.
Одним из подходов является применение различных ферментов, расщепляющих полисахариды, в комбинации с интерфероном. Расщепление полисахаридного слоя окружающего клетки (в том числе опухолевые) позволяет повысить доступность активного вещества в очаг опухолевой ткани, что напрямую влияет на возможность снижения используемой дозы и повышения эффективности проводимой терапии.
В заявке WO 2004103396 A1 представлено решение, которое предлагает использование интерферона альфа совместно с ферментами: фосфолипазой, гиалуронидазой, нейраминидазой и хондроитиназой в комплексном лечении опухолей различного генеза.
Известно также решение согласно заявке US 20070249043 A1, в котором использованы различные системы доставки интерферонов в опухолевую ткань. Здесь используют систему доставки интерферона на основе аденовирусных векторов. Преимуществом данного технического решения является то, что введение аденовирусного вектора, несущего ген интерферона, позволяет обеспечить стабильную экспрессию этого белка в течение нескольких недель. Указанное свойство позволяет вводить препарат со значительно меньшей кратностью, что в свою очередь снижает токсичность проводимой терапии.
Данное техническое решение как наиболее близкое к заявляемому по составу действующего вещества и способу его использования выбрано авторами заявляемого изобретения за прототип.
К недостаткам прототипа можно отнести следующее:
1. Низкая эффективность проникновения аденовирусного вектора в клетки эпителия мочевого пузыря, при внутрипузырном введении, что определяет низкий уровень продукции основного действующего вещества - интерферона бета.
2. Невозможность регуляции экспрессии интерферона, который может вызывать развитие побочных реакций в организме пациентов.
Таким образом, в уровне техники существует острая потребность в разработке эффективного препарата для терапии рака мочевого пузыря, которое было бы лишено указанных недостатков.
Раскрытие настоящего изобретения
Задачей настоящего изобретения является создание иммунобиологического средства пролонгированного действия для терапии рака мочевого пузыря, которое способно высокоэффективно проникать через слизистый слой в эпителий мочевого пузыря и являться безопасным.
Указанная выше задача настоящего изобретения решается за счет того, что создано иммунобиологическое средство для лечения рака мочевого пузыря на основе аденовирусного вектора, содержащего ген интерферона бета под контролем промотора, причем в качестве аденовирусного вектора используют аденовирус человека, а средство дополнительно включает фермент, с обеспечением расщепления секрета слизистой оболочки мочевого пузыря. В качестве промотора используют тетрациклин-зависимый промотор. В качестве фермента используют гиалуронидазу и/или нейраминидазу. Созданное иммунобиологическое средство содержит в дозе на одну инстилляцию в мочевой пузырь содержится:
Аденовирусный вектор - от 105 БОЕ/дозу до 1013 БОЕ/дозу
Фермент, расщепляющий секрет слизистой оболочки мочевого пузыря, а именно:
гиалуронидазы от 0,1 МЕ/дозу до 430 МЕ/дозу,
нейраминидазы от 0,1 МЕ/дозу до 430 МЕ/дозу
или их смесь
Буфер - остальное
Способ использования иммунобиологического средства заключается во введении созданного иммунобиологического средства в мочевой пузырь.
Заявленное иммунобиологическое средство используют в эффективном количестве для терапии рака мочевого пузыря.
Противоопухолевая активность интерферонов связана с их способностью замедлять или подавлять рост клеток, а также активировать противоопухолевые механизмы иммунной системы. Они могут оказывать непосредственное действие на опухолевый клетки, их рост и дифференцировку. К таким эффектам относятся: подавление синтеза РНК, подавление синтеза протеинов, стимуляция недифференцированных клеток к созреванию, увеличение экспрессии мембранных антигенов опухолевых клеток и рецепторов к гормонам, нарушение процессов сосудообразования. Опосредованное действие интерферонов связано с усилением способности иммунокомпетентных клеток обнаруживать и уничтожать атипичные клетки организма. К таким эффектам относятся: стимуляция активности клеток иммунной системы (макрофагов, NK-клеток, Т-цитотоксических лимфоцитов), усиление экспрессии на клетках молекул гистосовместимости I класса.
В данном изобретении заявляется использование интерферона бета для иммунотерапии опухолей, т.к. интерферон бета обладает большей терапевтической активностью по сравнению с другими типами интерферонов. Известна одна форма интерферона бета человека, ген, экспрессирующий соответствующий функциональный белок, нуклеотидная последовательность которой была использована в заявленном изобретении [GenBank: М25460.1]. Однако среднему специалисту в данной области будет очевидно, что искусственно измененные нуклеотидные последовательности гена интерферона бета человека, не приводящие к изменениям в соответствующих аминокислотных последовательностях или вносящие изменения, которые не снижают биологическую активность молекулы, будут так же эффективны, как и исходная молекула.
Аденовирусы человека широко используются в качестве векторов для генной терапии, а также при создании генно-инженерных вакцин. Их основными преимуществами перед другими способами доставки генов являются:
- способность к замещению относительно больших фрагментов вирусной ДНК фрагментами ДНК, содержащими ген(ы) интереса;
- способность проникать в различные типы клеток;
- структурная стабильность рекомбинантных аденовирусов;
- способность обеспечивать высокий уровень экспрессии генов в течении нескольких недель;
- безопасность для человека, которая определяется, в частности, невозможностью репликации аденовирусных векторов в клетках человека.
Дополнительно в данном решении для повышения безопасности противоопухолевого средства на основе аденовирусного вектора, содержащего ген интерферона бета, используют в качестве промотора - тетрациклин-зависимый (Tet-off) промотор, регулирующий экспрессию гена интерферона бета.
Использование данной генетической конструкции позволило увеличить безопасность разработанного иммунобиологического средства, поскольку при возникновении возможных острых побочных (например, аллергических) реакций, достаточно ввести терапевтическую дозу разрешенного к применению антибиотика тетрациклина, чтобы уменьшить экспрессию интерферона бета.
Для лечения опухолевых образований в мочевом пузыре необходимо повысить эффективность проникновения генно-инженерных векторных систем через секрет слизистой оболочки мочевого пузыря. Данная проблема решена в заявляемом иммунобиологическом средстве за счет включения в его состав композиции ферментов, а именно гиалуронидазы и нейраминидазы, которые специфически расщепляют секрет слизистой оболочки мочевого пузыря, тем самым способствуя увеличению эффективности проникновения аденовирусного вектора. Так, гиалуронидаза расщепляет кислые мукополисахариды, в т.ч. муцин, гиалуроновую кислоту, которые входят в состав секрета слизистой оболочки мочевого пузыря. Нейраминидаза гидролизует α-2→3-, α-2→6-, α-2→8-кетозидные связи концевых остатков сиаловой кислоты в олигосахаридах, гликопротеинах, гликолипидах, что также способствует проникновению аденовирусного вектора через слизистый слой мочевого пузыря, богатый сиаловой кислотой.
Краткое описание фигур
На фиг. 1
подтверждена эффективность использования аденовирусного вектора для доставки гена интерферона бета человека в ткань мочевого пузыря.
Представлены концентрационные кривые интерферона бета в ткани мочевого пузыря:
- после введения рекомбинантного интерферона бета 4 мкг/доза - сплошная кривая;
- после введения аденовирусного вектора, содержащего ген интерферона бета 109 БОЕ/дозу - пунктирная кривая.
Ось ординат - количество интерферона бета, нг/мл.
Ось абсцисс - время после внутрипузырного введения препаратов, часы.
Таким образом, показано, что использование аденовирусного вектора, содержащего ген интерферона бета, вызывает продукцию целевого белка значительно большей продолжительности (Т1/2=240 часов), по сравнению с использованием рекомбинантного интерферона бета человека (Т1/2=6 часов).
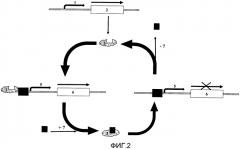
На фиг. 2
представлена схема работы тетрациклин-зависимого промотора:
1 - промотор гена, кодирующего трансактиваторный белок tTA
2 - ген, кодирующий трансактиваторный белок tTA
3 - трансактиваторный белок tTA
4 - тетрациклин-зависимый элемент (TRE)
5 - промотор гена интерферона бета
6 - ген интерферона бета
7 - тетрациклин.
Ключевым компонентом системы является ген (2), кодирующий трансактиваторный белок tTA (3). Он связывается с последовательностью тетрациклин-зависимого элемента TRE (4) и активирует процесс транскрипции интерферона бета (6). При введении тетрациклина (7) он связывается с белком tTA, чем блокирует взаимодействие трансактиваторного белка с TRE. Таким образом, в присутствии тетрациклина транскрипция гена интерферона останавливается.
На фиг. 3
показана способность используемого аденовирусного вектора, содержащего ген интерферона бета, проникать в опухолевые клетки мочевого пузыря in vitro.
Использован метод иммуноферментного анализа.
Представлена гистограмма, показывающая результаты определения концентрации интерферона бета в культуральной среде клеток RT-4.
Ось ординат - количество интерферона бета, нг/мл.
Ось абсцисс - время после добавления аденовирусного вектора, содержащего ген интерферона бета, часы.
На фиг. 4
результаты эксперимента по определению эффективной дозы ферментов. Использован метод иммуноферментного анализа.
Представлена гистограмма, показывающая количество интерферона в гомогенатах мочевого пузыря мышей через 24 часа после введения препарата.
Ось ординат - количество интерферона бета, нг/мл.
Ось абсцисс - экспериментальные группы.
1 - аденовирусный вектор, содержащий ген интерферона бета 109 БОЕ/мышь
2 - аденовирусный вектор, содержащий ген интерферона бета 1010 БОЕ/мышь
3 - нейраминидаза 0,1 МЕ/мышь, аденовирусный вектор, содержащий ген интерферона бета 109 БОЕ/мышь
4 - гиалуронидаза 0,1 МЕ/мышь, аденовирусный вектор, содержащий ген интерферона бета 109 БОЕ/мышь
5 - гиалуронидаза 0,1 МЕ/мышь, нейраминидаза 0,1 МЕ/мышь, аденовирусный вектор, содержащий ген интерферона бета 109 БОЕ/мышь
6 - нейраминидаза 32 МЕ/мышь, аденовирусный вектор, содержащий ген интерферона бета 109 БОЕ/мышь
7 - гиалуронидаза 32 МЕ/мышь, аденовирусный вектор, содержащий ген интерферона бета 109 БОЕ/мышь
8 - гиалуронидаза 32 МЕ/мышь, нейраминидаза 32 МЕ/мышь, аденовирусный вектор, содержащий ген интерферона бета 109 БОЕ/мышь.
На фиг. 5
показано, что в присутствии тетрациклина транскрипция гена интерферона в заявленном изобретении приостанавливается.
Представлена гистограмма, показывающая использование тетрациклин-зависимого промотора для увеличения безопасности иммунобиологического средства. Количество интерферона определяли в гомогенатах мочевого пузыря мышей через 24 часа после введения препарата. Тетрациклин добавляли в питьевую воду. Доступ к воде животных был ad libitum.
Ось ординат - количество интерферона бета, нг/мл.
Ось абсцисс - экспериментальные группы.
1 - гиалуронидаза 32 МЕ/мышь, нейраминидаза 32 МЕ/мышь аденовирусный вектор, содержащий ген интерферона бета 109 БОЕ/мышь
2 - гиалуронидаза 32 МЕ/мышь, нейраминидаза 32 МЕ/мышь аденовирусный вектор, содержащий ген интерферона бета 109 БОЕ/мышь + тетрациклин (3 мг/л воды)
Исследования, показывающие эффективность иммунобиологического средства, разработанного авторами, включают: определение дозы компонентов иммунобиологического средства; оценку эффективности проникновения аденовирусного вектора в клетки мочевого пузыря; оценку экспрессии интерферона бета, в культуре клеток после добавления иммунобиологического средства.
Примеры осуществления настоящего изобретения
Пример 1
Определение эффективной дозы аденовирусного вектора, содержащего ген интерферона бета, в составе разработанного иммунобиологического средства.
Аденовирусный вектор, содержащий ген интерферона бета является одним из основных компонентов иммунобиологического средства.
Эффективность использования аденовирусного вектора для доставки гена интерферона бета человека в ткань мочевого пузыря подтверждена экспериментом, результаты которого представлены на фиг. 1.
Показано, что использование аденовирусного вектора, содержащего ген интерферона бета вызывает продукцию целевого белка значительно большей продолжительности (Т1/2=240 часов), по сравнению с использованием рекомбинантного интерферона бета человека (T1/2=6 часов). Этим доказывается также пролонгированное действие данной векторной конструкции.
Определение эффективной дозы данного вектора было определено на примере вектора на основе аденовируса человека 5 серотипа с использованием коммерческой системы («AdEasy™ Adenoviral Vector System», Agilent Technologies). Для определения диапазона рабочих концентраций, была исследована способность вектора на основе аденовируса человека 5 серотипа, содержащего ген интерферона бета вызывать замедление роста опухолей аденокарциномы человека А431 у мышей линии D2&I при многократных внутриопухолевых инъекциях.
Среднему специалисту в данной области очевидно, что в качестве аденовирусного вектора может быть использован вектор на основе любого другого серотипа аденовируса человека, который обладает не меньшей безопасностью и эффективностью, например, серотипы 4,26,35 и др. С этой целью опухолевые клетки А431 прививались 8-недельным самкам мышей подкожно из расчета 106 клеток на инъекцию. Начиная с десятого дня, проводили внутриопухолевую терапию по схеме: 4 инъекции аденовирусного препарата с интервалом в три дня. Доза вектора на основе аденовируса человека 5 серотипа, содержащего ген интерферона бета на одну инъекцию составляла 104 БОЕ/мышь, 105 БОЕ/мышь, 107 БОЕ/мышь, 109 БОЕ/мышь, 1011 БОЕ/мышь или 1013 БОЕ/мышь. Максимальная доза для введения животным ограничена предельно возможным объемом введения препарата внутрь опухоли (100 мкл) и максимальной концентрацией препарата, которую можно получить всеми известными на сегодняшний день методиками получения высококонцентрированных препаратов аденовирусных векторов. Контрольным группам вводили фосфатный буфер. Объем опухолей измеряли на 20 день с помощью штангенциркуля. Результаты эксперимента представлены в таблице 1.
Как видно из представленных результатов во всех группах, где животные получали аденовирусный вектор, содержащий ген интерферона бета дозой от 105 до 1013 БОЕ/инъекцию, объем опухолей был достоверно меньше, чем в контрольной группе. Следовательно, можно заключить, что рабочий диапазон доз аденовирусного вектора, содержащего ген интерферона бета составляет от 105 до 1013 БОЕ/дозу.
Пример 2
Оценка способности вектора на основе аденовируса, содержащего ген интерферона бета проникать в клетки рака мочевого пузыря.
Целью данного эксперимента было определение способности используемого аденовирусного вектора, содержащего ген интерферона бета, проникать в опухолевые клетки мочевого пузыря in vitro. Для этого были использованы клетки рака мочевого пузыря человека RT-4. Клетки культивировали на минимальной среде Игла с 10% эмбриональной телячьей сывороткой, при температуре 37°C и содержании CO2 5%. Далее клетки помещали на 96-луночный планшет в концентрации 104 клеток/лунку и инкубировали 16 часов (до конфлюентности 70-80%). Затем к клеткам добавляли аденовирусный вектор, содержащий ген интерферона бета, в концентрации 106 БОЕ/лунку. Через 24 и 48 часов оценивали количество бета интерферона в культуральной среде клеток методом иммуноферментного анализа. Результаты эксперимента представлены на Фиг. 3.
Таким образом, представленные данные демонстрируют проникновение аденовирусного вектора в клетки рака мочевого пузыря человека RT-4 и последующую экспрессию интерферона бета в этих клетках (от 12,5 до 41,5 нг/мл, в зависимости от времени после добавления препарата).
Пример 3
Определение эффективной дозы ферментов, входящих в состав иммунобиологического средства.
Ферменты являются одним из важных компонентов разработанного иммунобиологического средства. Они обеспечивают проникновение аденовируса непосредственно в эпителий мочевого пузыря за счет специфического расщепления полисахаридов секрета слизистой оболочки мочевого пузыря.
Целью данного эксперимента было определение эффективной дозы ферментов нейраминидазы и гиалуронидазы, входящих в состав иммунобиологического средства. К аденовирусному вектору, содержащему ген интерферона бета (109 БОЕ/мышь), добавляли нейраминидазу 0,01 МЕ/мышь (препарат №3), 32 МЕ/мышь (препарат №6), гиалуронидазу 0,01 МЕ/мышь (препарат №4), 32 МЕ/мышь (препарат №7) или смесь ферментов гиалуронидазы и нейраминидазы по 0,01 МЕ/мышь каждого фермента (препарат №4) и по 32 МЕ/мышь (препарат №8). В качестве контрольных препаратов использовали аденовирусные вектора без ферментов в той же дозе (109 БОЕ/мышь) (препарат №1), а также в 10 раз большей (1010 БОЕ/мышь) (препарат №2). Максимальная доза фермента ограничена предельно возможным объемом введения препарата внутрь мочевого пузыря (50 мкл) и максимальной растворимостью препарата. Минимальная доза определяется минимальной эффективной дозой используемой в литературе. Препараты вводили через катетер в мочевой пузырь мышей Balb/c. Через 48 часов отбирали мочевой пузырь и в гомогенатах ткани определяли количество интерферона бета, экспрессируемого используемым аденовирусным вектором. Измерение интерферона бета проводили методом иммуноферментного анализа, согласно протоколу фирмы Abcam, США. Полученные данные представлены на фиг 4.
Результаты эксперимента показали, что использование комбинации какого-либо из ферментов с аденовирусным вектором значительно (до 1,3 раза) увеличивает продукцию интерферона бета в ткани мочевого пузыря по сравнению с индивидуальным препаратом аденовирусного вектора, взятым даже в большей дозе (в 10 раз больше, по сравнению с дозой аденовирусного вектора, используемой в комбинации с ферментами).
Наибольшую продукцию интерферона показала композиция, включающая оба фермента и аденовирусный вектор. Продукция интерферона в этой группе была значительно больше по сравнению аденовирусными векторами в той же дозе и в 10 раз большей, но без использования ферментов (в 2,4 и в 2 раза, соответственно).
Полученные данные отражают сверхсуммарный эффект в продукции основного активного компонента - интерферона бета при использовании аденовирусного вектора совместно с каким-либо ферментом или их сочетанием, т.к. использование даже 10-кратно превышающей дозы аденовирусного вектора содержащего ген интерферона бета, не может вызвать сравнимые уровни продукции данного белка.
Рабочий диапазон концентраций в среднем пересчете на дозу для человека составлял (гиалуронидаза от 0,1 до 430 МЕ/дозу, нейраминидаза от 0,1 до 430 МЕ/дозу).
Таким образом, эффективные композиции иммунобиологического средства включают помимо аденовирусного вектора, содержащего ген интерферона бета, либо один из ферментов (гиалуронидазу или нейраминидазу) в концентрациях от 0,1 до 430 МЕ/дозу, либо оба фермента, где концентрация каждого из ферментов может быть от 0,1 до 430 МЕ/дозу.
Пример 4
Оценка использования тетрациклин-зависимого промотора для повышения безопасности иммунобиологического средства.
Для обеспечения безопасности разработанного иммунобиологического средства ген интерферона бета был помещен под контроль тетрациклин-зависимого (Tet-off) промотора. Схема работы промотора представлена на Фиг. 2.
Ключевым компонентом системы является ген (2), кодирующий трансактиваторный белок tTA (3). Он связывается с последовательностью тетрациклин-зависимого элемента TRE (4) и активирует процесс транскрипции интерферона бета (6). При введении тетрациклина (7), он связывается с белком tTA, чем блокирует взаимодействие трансактиваторного белка с TRE.
Таким образом, в присутствии тетрациклина транскрипция гена интерферона останавливается.
Для того чтобы проверить возможность использования данного метода in vivo, был проведен эксперимент на мышах линии Balb/c. Животные были разделены на две группы по 5 мышей. Всем группам вводили в мочевой пузырь аденовирусный вектор, содержащий ген интерферона бета (109 БОЕ/мышь), нейраминидазу (32 МЕ/мышь), гиалуронидазу (32 МЕ/мышь) в 100 мкл фосфатного буфера. 1 группе животных в питьевую воду добавляли тетрациклин (3 мг/мл). Через 48 часов отбирали мочевой пузырь и в гомогенатах мочевого пузыря определяли количество интерферона бета (методом иммуноферментного анализа, согласно протоколу фирмы Abcam). Полученные данные представлены на фиг 5.
Результаты эксперимента показали, что в группе животных, которым давали тетрациклин, количество интерферона достоверно меньше, чем в контрольной группе. Следовательно, использование данной генетической конструкции увеличивает безопасность разработанного иммунобиологического средства, поскольку при возникновении возможных острых побочных реакций, достаточно ввести терапевтическую дозу разрешенного к применению антибиотика тетрациклина, чтобы уменьшить экспрессию интерферона бета.
Пример 5
Использование предполагаемых лекарственных форм иммунобиологического средства для лечения рака мочевого пузыря.
Любому специалисту среднего уровня в данной области понятно, что данное иммунобиологическое средство для лечения рака мочевого пузыря может быть изготовлено и расфасовано в любой удобной для хранения, транспортировки и непосредственного введения в мочевой пузырь пациента лекарственной форме, которая позволяет сохранить функциональную активность аденовирусного вектора и ферментов.
Иммунобиологическое средство может быть представлено в виде различных лекарственных форм.
- Например, лекарственная форма может быть представлена в форме суспензии аденовирусного вектора, содержащего ген интерферона бета и нейраминидазы и/или гиалуронидазы в буферном растворе. В качестве буферного раствора может выступать любой раствор, не токсичный для человека и содержащий все необходимые компоненты, обеспечивающие жизнеспособность аденовирусного вектора и активность ферментов, например нейтральный фосфатно-солевой буфер и др. Ввиду целесообразности сохранения удобства в хранении и транспортировке объем одной дозы препарата разумно ограничен, например, 1 мл. Введение же такого малого объема в мочевой пузырь пациента затруднено, в связи с чем непосредственно перед использованием специализированный медицинский персонал принимает решение, в каком объеме будет разведен препарат, или к какому объему второго раствора будет добавлен препарат. Для разведения используют любой стерильный раствор или какой-либо другой препарат, пригодный для медицинского применения, например изотонический раствор хлорида натрия. Производитель не может выпускать препарат в означенном финальном объеме, готовом для непосредственного применения, т.к. конечный объем для введения препарата может сильно варьировать и зависит от многих факторов (пол, возраст, вид патологии, степень выраженности патологии и др.), соответственно для его определения в каждом конкретном случае требуется решение квалифицированного специалиста. Следует подчеркнуть, что соотношение активных компонентов: аденовирусный вектор и ферменты присутствуют в дозе в фиксированных значениях, заявленных в данном изобретении и не изменяются при разведении препарата в различных итоговых объемах.
- Лекарственная форма может быть выпущена в виде лиофилизированной формы и представляет собой лиофильно высушенный препарат аденовирусного вектора, содержащего ген интерферона бета и нейраминидазы и/или гиалуронидазы в буферном растворе. Лиофилизированный осадок может быть растворен перед использованием стерильным раствором хлорида натрия, или другим пригодным для медицинского применения растворителем, или используемым в медицинской практике препаратом.
- Иммунобиологическое средство может быть также представлено в виде растворов, находящихся в двух отдельных флаконах и смешивающихся непосредственно перед использованием. При этом в одном флаконе содержится аденовирусный вектор, содержащий ген бета-интерферона человека в буферном растворе, а в другом флаконе содержится композиция ферментов, расщепляющих секрет слизистого слоя мочевого пузыря, также в буферном растворе. Допускается также, что содержимое одного или обоих флаконов лиофильно высушено.
- Специалисту среднего уровня также понятно, что разработанное иммунобиологическое средство может также использоваться в виде геля, мази, или в виде аэрозоля для более удобного введения в мочевой пузырь в случаях различных патологий и степени их выраженности.
Таким образом, векторные системы на основе аденовируса человека, содержащие ген интерферона бета, являются перспективными средствами для противоопухолевой терапии. Эффективность использования аденовирусного вектора для доставки гена интерферона бета человека в ткань мочевого пузыря доказана приведенными примерами.
Показано, что использование аденовирусного вектора, содержащего ген интерферона бета вызывает продукцию целевого белка значительно большей продолжительности (T1/2=240 часов), по сравнению с использованием рекомбинантного интерферона бета человека (Т1/2=6 часов), что доказывает пролонгированное действие иммунологического средства.
Доказано также, что использование предлагаемой генетической конструкции позволяет увеличить безопасность разработанного иммунобиологического средства, поскольку при возникновении возможных острых побочных, например, аллергических реакций, достаточно ввести терапевтическую дозу разрешенного к применению антибиотика тетрациклина, чтобы уменьшить экспрессию интерферона бета.
Доказана эффективность проникновения через секрет слизистой оболочки мочевого пузыря созданного иммунобиологического средства за счет включения в его состав композиции ферментов гиалуронидазы и/или нейраминидазы, которые специфически расщепляют секрет слизистой оболочки мочевого пузыря, тем самым способствуя увеличению эффективности проникновения аденовирусного вектора.
Таким образом, поставленная в данном изобретении задача решена.
Промышленная применимость также доказана приведенными примерами.
1. Иммунобиологическое средство для лечения рака мочевого пузыря на основе аденовирусного вектора, содержащего ген интерферона бета под контролем промотора,отличающееся тем, чтов качестве аденовирусного вектора используют аденовирус человека, а средство дополнительно включает фермент, который обеспечивает расщепление секрета слизистой оболочки мочевого пузыря.
2. Иммунобиологическое средство по п. 1, отличающееся тем, что в качестве промотора используют тетрациклин-зависимый промотор.
3. Иммунобиологическое средство по п. 1, отличающееся тем, что в качестве фермента используют гиалуронидазу.
4. Иммунобиологическое средство по п. 1, отличающееся тем, что в качестве фермента используют нейраминидазу.
5. Иммунобиологическое средство по п. 1, отличающееся тем, что в качестве фермента используют совместно гиалуронидазу и нейраминидазу.
6. Иммунобиологическое средство по п. 1, отличающееся тем, что в дозе на одну инстилляцию в мочевой пузырь содержится:Аденовирусный вектор - от 105 БОЕ/дозу до 1013 БОЕ/дозуФермент, расщепляющий секрет слизистой оболочки мочевого пузыря, а именно:гиалуронидазы от 0,1 МЕ/дозу до 430 МЕ/дозу,нейраминидазы от 0,1 МЕ/дозу до 430 МЕ/дозуили их смесь.Буфер - остальное
7. Способ использования иммунобиологического средства для лечения рака мочевого пузыря заключается во введении иммунобиологического средства по п. 1 в мочевой пузырь.