Компенсация невязки для биодатчика
Иллюстрации
Показать всеГруппа изобретений относится к анализу биологических жидкостей с помощью биосенсорных систем. Способ определения концентрации анализируемого вещества в образце включает: генерацию выходного сигнала, соответствующего концентрации анализируемого вещества в образце и входному сигналу; компенсацию выходного сигнала с помощью основной функции и первой функции невязки для определения скомпенсированного выходного сигнала, причем основная функция предназначена для компенсации основной ошибки в выходном сигнале, а первая функция невязки предназначена для компенсации оставшейся ошибки в выходном сигнале; и определение концентрации анализируемого вещества в образце по скомпенсированному выходному сигналу. Также описана биосенсорная система аналогичного назначения. Достигается повышение точности и надежности анализа. 2 н. и 28 з.п. ф-лы, 25 ил., 8 табл.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННУЮ ЗАЯВКУ
По данной заявке испрашивается приоритет предварительной заявки на патент США No. 61/316174, озаглавленной "Residual Compensation Including Underfill", поданной 22 марта 2010, содержимое которой полностью включено в данный документ посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
Биосенсорные системы обеспечивают анализ образца биологической жидкости, такой как цельная кровь, сыворотка, плазма, моча, слюна, внутритканевая или внутриклеточная жидкость. Обычно системы включают в себя измерительное устройство, которое анализирует образец, находящийся в тестирующем датчике (сенсоре). Образец обычно имеет жидкую форму и, в дополнение к биологической жидкости, может представлять собой производную биологической жидкости, такую как экстракт, раствор, фильтрат или восстановленный осадок. Анализ, выполняемый биосенсорной системой, позволяет определить наличие и/или концентрацию одного или нескольких анализируемых веществ (аналитов), таких как спирт, глюкоза, мочевая кислота, лактат, холестерин, билирубин, свободные жирные кислоты, триглицериды, белки, кетоны, фенилаланин или ферменты, в биологической жидкости. Анализ может быть полезным в диагностике или лечении физиологических патологий. Например, индивид, больной диабетом, может применять биосенсорную систему для определения уровня глюкозы в цельной крови с целью внесения изменений в диету и/или лекарственную терапию.
Могут быть спроектированы биосенсорные системы для анализа одного или более анализируемых веществ с использованием различных объемов биологических жидкостей. Некоторые системы могут анализировать одну каплю цельной крови, например, объемом 0,25-15 микролитров (мкл). Биосенсорные системы могут быть реализованы с использованием настольных, переносных и других измерительных устройств. Переносные измерительные устройства могут быть портативными и могут позволять идентифицировать и/или количественно определить одно или более анализируемых веществ в образце. Примеры переносных измерительных устройств включают в себя измерительные приборы Elite® компании Bayer HealthCare, Тарритаун, штат Нью-Йорк, тогда как примеры настольных измерительных систем включают в себя электрохимическую рабочую станцию, поставляемую фирмой CH Instruments, Остин, штат Техас.
Биосенсорные системы могут использовать оптические и/или электрохимические методы для анализа биологической жидкости. В некоторых оптических системах концентрация анализируемого вещества определяется путем измерения света, который взаимодействовал или был поглощен идентифицируемыми по свету объектами, такими как анализируемое вещество, или реакция, или продукт, сформированный из химического индикатора, реагирующего с анализируемым веществом. В других оптических системах химический индикатор флуоресцирует или излучает свет в ответ на анализируемое вещество при его освещении возбуждающим пучком. Свет может быть преобразован в электрический выходной сигнал, такой как ток или потенциал, который может быть аналогичным образом обработан с выдачей выходного сигнала из электрохимической системы. И в той, и в другой оптической системе система измеряет и сопоставляет свет с концентрацией анализируемого вещества в образце.
В оптических системах, основанных на поглощении света, химический индикатор производит продукт реакции, который поглощает свет. Может быть использован такой химический индикатор, как тетразолий, вместе с ферментом, таким как диафораза. Тетразолий обычно формирует формазан (хромоген) в ответ на окислительно-восстановительную реакцию анализируемого вещества. Падающий входной пучок от источника света направлен на образец. Источником света может быть лазер, светоизлучающий диод и т.п. Падающий пучок может иметь длину волны, выбранную для поглощения продуктом реакции. При прохождении падающего пучка через образец продукт реакции поглощает часть падающего пучка, таким образом, ослабляя или снижая интенсивность падающего пучка. Падающий пучок может быть отражен обратно от образца или может быть передан через образец на детектор. Детектор собирает и измеряет ослабленный падающий пучок (выходной сигнал). Объем света, ослабленный продуктом реакции, является указанием на концентрацию анализируемого вещества в образце.
В генерирующих свет оптических системах химический детектор флуоресцирует или излучает свет в ответ на окислительно-восстановительную реакцию анализируемого вещества. Детектор собирает и измеряет сгенерированный свет (выходной сигнал). Объем света, произведенный химическим индикатором, является указанием на концентрацию анализируемого вещества в образце.
В электрохимических биосенсорных системах концентрация анализируемого вещества определяется по электрическому сигналу, сгенерированному посредством окисления/восстановления, или окислительно-восстановительной реакции, анализируемого вещества или объектов, реагирующих на анализируемое вещество, когда к образцу прилагается входной сигнал. Входной сигнал может представлять собой потенциал или ток и может быть постоянным, переменным или их комбинацией, например, как в случае приложения сигнала переменного тока со смещением сигнала постоянного тока. Входной сигнал может быть приложен в форме одиночного импульса или множества импульсов, последовательностей или циклов. Фермент или аналогичный объект может быть добавлен к образцу с целью улучшения переноса электронов от первого объекта ко второму объекту в процессе окислительно-восстановительной реакции. Фермент или аналогичный объект может реагировать с одним анализируемым веществом, таким образом, обеспечивая специфичность для части сгенерированного выходного сигнала. Посредник может быть использован для поддержания степени окисления фермента и/или для помощи в переносе электронов от анализируемого вещества к электроду.
Электрохимические биосенсорные системы обычно включают в себя измерительное устройство, имеющее электрические контакты, которые соединены с электрическими проводниками тестирующего датчика. Проводники могут быть сделаны из проводящих материалов, таких как цельные металлы, металлические пасты, проводящий углерод, пасты из проводящего углерода, проводящие полимеры и т.п. Электрические проводники обычно соединяются с рабочим, интегрирующим, контрольным и/или другими электродами, которые протягиваются в резервуар с образцом. Один или более электрических проводников также могут протягиваться в резервуар с образцом для обеспечения функциональности, не обеспечиваемой электродами.
Измерительное устройство прилагает входной сигнал через электрические контакты к электрическим проводникам тестирующего датчика. Электрические проводники передают входной сигнал через электроды в образец, присутствующий в резервуаре с образцом. Окислительно-восстановительная реакция анализируемого вещества генерирует выходной электрический сигнал в ответ на входной сигнал. Выходной электрический сигнал от тестирующего датчика может представлять собой ток (например, сгенерированный посредством амперометрии или вольтаметрии), потенциал (например, сгенерированный посредством потенциометрии/гальванометрии) или накопленный заряд (например, сгенерированный посредством кулонометрии). Измерительное устройство может обладать способностью обработки для измерения и сопоставления выходного сигнала с наличием и/или концентрацией одного или более анализируемых веществ в образце.
В кулонометрии потенциал прилагается к образцу для полного окисления или восстановления анализируемого вещества. Биосенсорная система, использующая кулонометрию, описана в патенте США No. 6120676. В амперометрии электрический сигнал с постоянным потенциалом (напряжением) прилагается к электрическим проводникам тестирующего датчика, тогда как измеряемым выходным сигналом является ток. Биосенсорные системы, использующие амперометрию, описаны в патентах США № 5620579; 5653863; 6153069; и 6413411. В вольтаметрии электрический сигнал с переменным потенциалом прилагается к образцу биологической жидкости, тогда как измеряемым выходом является ток. В стробированной амперометрии и стробированной вольтаметрии используются импульсные входные сигналы, в соответствии с описанным в WO 2007/013915 и WO 2007/040913, соответственно.
Во многих биосенсорных системах тестирующий датчик (сенсор) может быть приспособлен для использования вне, внутри или частично внутри живого организма. При использовании вне живого организма образец биологической жидкости может быть помещен в резервуар для образца в тестирующем датчике (сенсоре). Тестирующий сенсор может быть помещен в измерительное устройство до, после или во время помещения образца для анализа. При использовании внутри или частично внутри живого организма тестирующий сенсор может быть непрерывно погружен в образец, или образец может периодически помещаться в тестирующий сенсор. Тестирующий сенсор может включать в себя резервуар, который частично изолирует объем образца или может быть открыт для образца. При открытии для образца тестирующий сенсор может принимать форму волокна или другой структуры, помещенной в соприкосновение с биологической жидкостью. Аналогично, образец может непрерывно протекать через тестирующий сенсор, например, в случае непрерывного контроля, или может прерываться, например, в случае периодического контроля, в целях выполнения анализа.
Эксплуатационные характеристики измерения биосенсорной системы определяются в отношении точности, которая отражает объединенные эффекты случайной и систематической компонент ошибки. Систематическая ошибка, или верность, это разность между средним значением, определенным в биосенсорной системе, и одним или более принятыми контрольными значениями для концентрации анализируемого вещества биологической жидкости. Верность может быть выражена в терминах разности средних значений, при этом большие разности средних значений представляют меньшую верность и, следовательно, относятся к меньшей точности. Достоверность представляет собой близость соответствия множества показаний для анализируемого вещества относительно среднего значения. Одна или более ошибок в анализе вносят вклад в погрешность и/или расхождение концентрации анализируемого вещества, определяемой биосенсорной системой. Следовательно, снижение ошибки анализа биосенсорной системы приводит к повышению точности и, таким образом, к улучшению характеристик измерений.
Погрешность может быть выражена в терминах «абсолютной погрешности» или «процентной погрешности». Абсолютная погрешность может быть выражена в единицах измерения, таких как мг/дл, тогда как процентная погрешность может быть выражена как процентная доля значения абсолютной погрешности свыше 100 мг/дл или доля контрольной концентрации анализируемого вещества в образце. Для концентраций глюкозы, меньших чем 100 мг/дл, процентная погрешность определяется как (абсолютная погрешность свыше 100 мг/дл)*100. Для концентраций глюкозы 100 мг/дл и выше процентная погрешность определяется как абсолютная погрешность, превышающая контрольную концентрацию анализируемого вещества, *100. Принятые контрольные значения для анализируемого вещества глюкозы в образцах цельной крови могут быть получены с помощью контрольного прибора, такого как YSI 2300 STAT PLUS™, поставляемого YSI Inc., Yellow Springs, штат Огайо. Другие контрольные инструменты и способы определения процентной погрешности могут быть использованы для других анализируемых веществ.
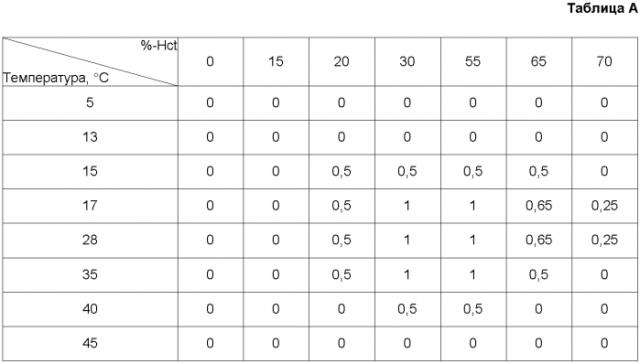
Погрешность гематокритного числа относится к средней разности (систематической ошибке) между контрольной концентрацией глюкозы, полученной с помощью контрольного инструмента, и экспериментальными измерениями глюкозы, полученными биосенсорной системой для образцов, имеющих различные гематокритные числа. Разность между контролем и значениями, полученными системой, появляется по причине различающихся гематокритных чисел между конкретными образцами цельной крови, и может быть выражена в общем виде в форме процента с помощью следующей формулы: %Hct-Bias=100%×(Gm-Gref)/Gref, где Gm - определенная концентрация глюкозы при конкретном гематокритном числе и Gref - контрольная концентрация глюкозы при контрольном гематокритном числе. Чем больше абсолютное значение %Hct-bias, тем больше гематокритное число образца (выраженное как %Hct, процентное отношение объема красных клеток крови к объему образца) понижает точность определения концентрации глюкозы.
Например, если анализируются образцы цельной крови, содержащие идентичные концентрации глюкозы, но имеющие гематокритные числа 20, 40 и 60%, то три различных концентрации глюкозы будут выданы системой на основании одного множества калибровочных констант (например, наклон и пересечение для образца цельной крови, имеющего 40% гематокритное число). Таким образом, даже хотя концентрации глюкозы в цельной крови одинаковы, система сообщит, что образец с гематокритным числом 20% содержит больше глюкозы, чем образец с гематокритным числом 40%, и что образец с гематокритным числом 60% содержит меньше глюкозы, чем образец с гематокритным числом 40%. "Чувствительность к гематокритному числу" представляет собой выражение степени, до которой изменения в гематокритном числе образца влияют на значения погрешности в анализе. Чувствительность к гематокритному числу может быть определена как численные значения процентной погрешности на процент гематокритного числа, то есть погрешность/%-погрешность на %Hct.
Биосенсорные системы могут выдавать в процессе анализа биологической жидкости выходной сигнал, который включает в себя ошибки из множества источников ошибок. Данные источники ошибок вносят вклад в общую погрешность, которая может быть отражена в аномальном выходном сигнале, например, таком, что одна или более частей всего выходного сигнала не соответствуют или неверно соответствуют концентрации анализируемого вещества в образце.
Данные погрешности могут происходить из одного или более источников, таких как физические характеристики образца, аспекты окружающей среды образца, условия эксплуатации системы, производственные различия между партиями тестирующих датчиков и т.п. Физические характеристики образца включают в себя гематокритное число (концентрацию красных клеток крови), вносящие помехи вещества, такие как липиды и белки, и т.п. Вносящие помехи вещества включают в себя аскорбиновую кислоту, мочевую кислоту, ацетаминофен и т.п. Аспекты окружающей среды образцы включают в себя температуру и т.п. Условия эксплуатации системы включают в себя условия недостаточного заполнения, когда размер образца недостаточно большой, медленное заполнение образца, прерывающийся электрический контакт между образцом и одним или более электродов в тестирующем датчике, предшествующее разложение реагентов, которые взаимодействуют с анализируемым веществом, и т.п. Производственные различия между партиями тестирующих датчиков включают в себя изменения в объеме и/или активности реагентов, изменения в площади электродов и/или расстоянии между ними, изменения в электрической проводимости проводников и электродов и т.п. Партия тестирующих датчиков предпочтительно производится в одном производственном цикле, при котором производственные различия между партиями значительно снижаются или устраняются. Производственные различия также могут появиться при изменении или снижении активности реагентов между моментом времени, когда тестирующий датчик был произведен, и моментом времени, когда он был использован для анализа. Также могут существовать другие источники или комбинации источников, вызывающие погрешность анализа.
Предел процентной погрешности, стандартное отклонение процентной погрешности, среднее стандартное отклонение процентной погрешности, средний разброс процентной погрешности и чувствительность к гематокритному числу представляют собой независимые способы выражения эксплуатационных характеристик измерений биосенсорной системы. Могут быть использованы дополнительные способы для выражения эксплуатационных характеристик измерений биосенсорной системы.
Пределы процентной погрешности представляют точность биосенсорной системы относительно контрольной концентрации анализируемого вещества, тогда как стандартное отклонение процентной погрешности и среднее стандартное отклонение процентной погрешности отражают достоверность, достигаемую для множества тестирующих датчиков из одной или нескольких производственных партий, соответственно, в отношении погрешностей, возникающих вследствие физических характеристик образца, аспектов окружающей среды образца и условий эксплуатации системы. Средний разброс процентной погрешности (расстояние от средней процентной погрешности одной партии до средней процентной погрешности двух или более партий тестирующих датчиков) отражает близость концентрации анализируемых веществ, определяемой тестирующими датчиками из двух или более партий тестирующих датчиков для одной и той же концентрации анализируемого вещества, связанную с производственными различиями между партиями.
Доля анализов, которая попадает в «пределы процентной погрешности» для выбранной границы процентной погрешности, указывает долю определенных концентраций анализируемых веществ, которые близки к контрольной концентрации. Таким образом, предел определяет, насколько близко определенные концентрации анализируемых веществ находятся к контрольной концентрации. Например, 95 из 100 выполненных анализов (95%), попадающих в пределы процентной погрешности ±10%, представляют собой более точный результат, чем 80 из 100 выполненных анализов (80%), попадающих в пределы процентной погрешности ±10%. Таким образом, увеличение доли анализов, попадающих в выбранные пределы процентной погрешности, показывает улучшение характеристик измерений биосенсорной системы.
Среднее значение может быть определено для процентных погрешностей, определенных по множеству анализов с применением тестирующих датчиков из одной партии, с целью получения "средней процентной погрешности" для множества анализов. Средняя процентная погрешность может быть определена для одной партии датчиков путем использования подмножества из партии, например, 100-140 тестирующих датчиков, для анализа множества образцов крови. Поскольку средняя процентная погрешность может быть определена для одной партии тестирующих датчиков, то "стандартное отклонение процентной погрешности" также может быть определено с целью описания того, насколько далеко процентная погрешность для отдельного анализа находится от средней процентной погрешности партии тестирующих датчиков. Стандартное отклонение процентной погрешности может рассматриваться как показатель достоверности единичного анализа относительно среднего значения для множества анализов из той же партии тестирующих датчиков. Такие значения стандартного отклонения процентной погрешности могут быть усреднены, например, арифметически, с использованием среднеквадратичных значений, или другими средствами, в целях предоставления показателя достоверности единичного анализа относительно среднего значения для множества анализов для множества партий тестирующих датчиков. Таким образом, уменьшение стандартного отклонения процентной погрешности или среднего стандартного отклонения процентной погрешности представляет улучшение характеристик измерений биосенсорной системы в отношении единичной партии тестирующих датчиков или множества партий тестирующих датчиков, соответственно.
Среднее значение может быть определено для средних процентных погрешностей, определенных для множества анализов с применением тестирующих датчиков из множества партий, с целью получения "общей средней процентной погрешности" для множества партий. Общая средняя процентная погрешность может быть определена для двух или более партий тестирующих датчиков. Поскольку общая средняя процентная погрешность может быть определена для множества партий тестирующих датчиков, то "разброс средней процентной погрешности" также может быть определен с целью описания того, насколько далеко средняя процентная погрешность для отдельной партии тестирующих датчиков находится от общей средней процентной погрешности множества партий тестирующих датчиков. Разброс средней процентной погрешности может рассматриваться в качестве показателя достоверности единичной партии тестирующих датчиков относительно среднего значения среднего для множества анализов множества партий тестирующих датчиков. Таким образом, уменьшение разброса средней процентной погрешности представляет улучшение характеристик измерений биосенсорной системы относительно производственных различий для множества партий тестирующих датчиков и повышение достоверности, достигаемой для множества тестирующих датчиков из множества производственных партий в отношении погрешностей, возникающих вследствие производственных различий между партиями.
Улучшение характеристик измерений биосенсорной системы посредством снижения ошибок из этих или других источников означает, что большее количество концентраций анализируемых веществ, определенных биосенсорной системой, может быть использовано для правильной терапии пациентом, например, в случае, когда контролируется уровень глюкозы в крови. Кроме того, также может быть снижена необходимость отбраковки тестирующих датчиков и повторения анализа пациентом.
Набор тестовых данных представляет собой совокупность множества анализов (выборка данных), проводившихся, по существу, в одинаковых тестовых условиях с использованием тестирующих датчиков из одной партии. Например, определенные значения концентрации анализируемого вещества обычно демонстрировали худшие характеристики измерений при самотестировании пользователем, чем при тестировании медицинским работником ("HCP"), и худшие характеристики измерений для HCP-тестирования, чем для тестирования в регулируемой окружающей среде. Такая разница в характеристиках измерений может быть отражена в больших стандартных отклонениях процентной погрешности для концентрации анализируемых веществ, определенной посредством самотестирования пользователем, чем для концентрации анализируемых веществ, определенной посредством HCP-тестирования или посредством тестирования в регулируемой окружающей среде. Регулируемая окружающая среда представляет собой среду, в которой физические характеристики и аспекты окружающей среды образца могут регулироваться, и, предпочтительно, имеют лабораторные настройки. Таким образом, в регулируемой окружающей среде гематокритные концентрации могут быть фиксированными, и действительные температуры образцов могут быть известны и скомпенсированы. В случае тестирования HCP могут быть снижены или устранены ошибки условий эксплуатации. В случае самотестирования пользователем, например, при клиническом обследовании, определенные концентрации анализируемых веществ, вероятно, будут включать в себя ошибки из источников ошибок всех типов.
Биосенсорные системы могут иметь единственный источник некорректированных выходных значений, отвечающих на окислительно-восстановительную или основанную на свете реакцию анализируемого вещества, такой как интегрирующий и рабочий электроды в электрохимической системе. Биосенсорные системы также могут иметь необязательную способность определять или оценивать температуру, например, с помощью одной или более термопар или других средств. В дополнение к данным системам, биосенсорные системы также могут иметь способность генерации дополнительных выходных значений, не относящихся к значениям для анализируемого вещества или посредника, чувствительного к анализируемому веществу. Например, в электрохимическом тестирующем датчике один или более электрических проводников также могут протягиваться в резервуар для образца с целью обеспечения функциональности, не обеспечиваемой рабочим и интегрирующим электродами. Такие проводники могут не иметь одного из реагентов рабочего электрода, такого как посредник, таким образом, позволяя вычитать сигнал фоновых помех из сигнала рабочего электрода.
Многие биосенсорные системы включают в себя один или более способов компенсации ошибок, связанных с анализом, посредством чего предпринимается попытка улучшения характеристик измерений биосенсорной системы. Способы компенсации могут улучшить характеристики измерений биосенсорной системы посредством обеспечения для биосенсорной системы возможности компенсировать неточные анализы, в результате чего повышается точность и/или достоверность значений концентрации, получаемых системой. Обычные способы компенсации ошибок для ошибок, связанных с физическими факторами и факторами окружающей среды, обычно разрабатываются в лаборатории, поскольку ошибки данных типов могут быть воспроизведены регулируемой окружающей среде. Однако ошибки, связанные с условиями функционирования, сложнее воспроизвести в лаборатории, поскольку многие из этих ошибок появляются вследствие способа, которым пользователь использует биосенсорную систему. Таким образом, ошибки, возникающие вследствие ошибок функционирования, может быть сложно воспроизвести в лабораторных условиях, и, следовательно, их сложно скомпенсировать с помощью обычного способа компенсации.
Соответственно, имеется текущая потребность в улучшенных биосенсорных системах, особенно в тех, которые могут обеспечить повышенную точность определения концентрации анализируемых веществ в образце при внесении в анализ ошибок эксплуатации вследствие самотестирования пользователем. Системы, устройства и способы по настоящему изобретению преодолевают, по меньшей мере, один из недостатков, ассоциированных с обычными биосенсорными системами.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
В одном из аспектов изобретение предоставляет способ определения концентрации анализируемого вещества в образце, который включает в себя: генерацию выходного сигнала, соответствующего концентрации анализируемого вещества в образце, и выходного сигнала; компенсацию выходного сигнала с помощью основной функции и первой функции невязки для определения скомпенсированного выходного сигнала; и определение концентрации анализируемого вещества в образце по скомпенсированному выходному сигналу. Функция преобразования может быть использована для преобразования выходного сигнала в некомпенсированный выходной сигнал до компенсации выходного сигнала. Некомпенсированный выходной сигнал может представлять собой некомпенсированное значение концентрации анализируемого вещества.
В другом аспекте изобретения представлен способ определения концентрации анализируемого вещества в образце, который включает в себя: генерацию выходного сигнала, соответствующего концентрации анализируемого вещества в образце, и выходного сигнала, определение скомпенсированного выходного сигнала по выходному сигналу с помощью основной функции и первой функции невязки и определение концентрации анализируемого вещества в образце по скомпенсированному выходному сигналу. Основная функция может включать в себя индексную функцию или комплексную индексную функцию и, предпочтительно, исправляет ошибки, возникающие вследствие гематокритных чисел в образцах цельной крови и вследствие температуры.
В другом аспекте изобретения представлен способ определения функции невязки, который включает в себя: выбор множества параметров ошибок в качестве потенциальных элементов первой функции невязки, определение первого значения исключения для потенциальных элементов с целью идентификации одного или более потенциальных элементов для исключения из первой функции невязки и исключение одного или более идентифицированных потенциальных элементов из первой функции невязки.
В другом аспекте изобретения представлена биосенсорная система для определения концентрации анализируемого вещества в образце, которая включает в себя: тестирующий датчик (сенсор), имеющий интерфейс образца в электрическом соединении с резервуаром, сформированным датчиком, и измерительное устройство, имеющее процессор, соединенный с интерфейсом датчика через генератор сигналов, при этом интерфейс датчика имеет электрическое соединение с интерфейсом образца, и процессор, имеющий электрическое соединение с носителем информации. Процессор выдает генератору сигналов команды на приложение входного электрического сигнала к интерфейсу образца, определяет значение выходного сигнала с интерфейса датчика в соответствии с концентрацией анализируемого вещества в образце и компенсирует, по меньшей мере, 50% суммарной ошибки в значении выходного сигнала с помощью основной функции. Процессор также компенсирует, по меньшей мере, 5% оставшейся ошибки в значении выходного сигнала с помощью первой функции невязки, при этом первая функция невязки предварительно сохранена на носителе информации, с целью определения скомпенсированного значения, и определяет концентрацию анализируемого вещества в образце по скомпенсированному значению. Измерительное устройство биосенсорной системы предпочтительно является переносным.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Изобретение может быть лучше понято со ссылкой на прилагаемые чертежи и описание. Компоненты на фигурах не обязательно показаны в масштабе, напротив, акцент сделан на иллюстрации принципов изобретения.
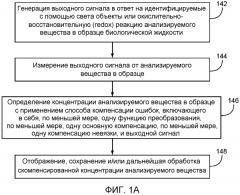
На Фиг.1A представлен способ определения концентрации анализируемого вещества в образце биологической жидкости.
На Фиг.1B представлен способ компенсации ошибок, включающий в себя функцию преобразования, основную компенсацию и, по меньшей мере, одну компенсацию невязки.
На Фиг.1C представлен общий способ определения функции невязки или функций, соответствующих случаю тестирования в нерегулируемой окружающей среде, такому как самотестирование пользователем.
На Фиг.1D представлен способ выбора элементов для включения в функцию невязки.
Фиг.2A представляет собой график корреляции между суммарными ошибками при самотестировании для двух партий датчиков в клиническом исследовании и основной функцией.
Фиг.2B представляет собой график корреляции между наблюдаемыми остаточными ошибками при самотестировании и значениями функции невязки после выделения функции невязки.
Фиг.2C представляет собой график корреляции между суммарными ошибками при самотестировании для двух партий датчиков в клиническом исследовании и суммой значений основной функции и функции невязки.
Фиг.3A представляет собой график корреляции эффекта дозы между токами выходных сигналов для образца цельной крови и контрольной концентрацией глюкозы для каждого образца в соответствии с определенным посредством контрольного инструмента YSI.
На Фиг.3B показан график корреляции после компенсации данных с Фиг.3A с применением компенсации ошибок, включающей в себя основную функцию и функцию невязки.
На Фиг.3C показан график процентных погрешностей до и после компенсации на Фиг.3A и Фиг.3B для образцов крови, собранных при тестировании HCP, при этом 99,3% совокупности скомпенсированных данных находится в пределах ±10%.
На Фиг.3D показана чувствительность к гематокритному числу до и после компенсации данных с Фиг.3A, при этом зависимость процентных погрешностей от гематокритного числа, по существу, исключена после компенсации.
Фиг.4A представляет собой график корреляции соответствия между токами выходных сигналов из капиллярных и венозных образцов и контрольной концентрацией глюкозы для каждого образца в соответствии с определенным посредством контрольного прибора YSI.
На Фиг.4B показан график корреляции после компенсации данных с Фиг.4A с применением одной и той же компенсации ошибок, включающей в себя основную функцию и функцию невязки и для капиллярных, и для венозных образцов.
На Фиг.4C показан график процентных погрешностей до и после компенсации для образцов венозной крови с Фиг.4A.
На Фиг.4D показана чувствительность к гематокритному числу до и после компенсации пиковых венозных образцов, в которых зависимость процентных погрешностей от гематокритного числа, по существу, устранена с целью выдачи, по существу, прямой линии после компенсации.
На Фиг.5A показано стандартное отклонение значений для каждой партии тестирующих датчиков до и после компенсации суммарно для 87 тестовых случаев.
На Фиг.5B показана корреляция средней процентной погрешности множества отдельных партий тестирующих датчиков и наклона линии регрессии для выходных токов в зависимости от контрольной концентрации глюкозы для каждой партии в тестировании HCP.
На Фиг.5C показана корреляция средней процентной погрешности множества партий тестирующих датчиков для случаев тестирования HCP и самотестирования пользователем после компенсации с применением основной функции и после компенсации с применением основной функции и функции невязки.
На Фиг.5D показан процент определений анализируемого вещества, имеющих пределы процентного отклонения в интервале ±10% от предела процентного отклонения для каждой партии тестирующих датчиков в случаях тестирования HCP и самотестирования.
Фиг.6A представляет последовательность стробированных импульсов, в которой входной сигнал, прилагаемый к рабочему и интегрирующему электродам, включает в себя множество импульсов и в которой второй сигнал прилагается к дополнительному электроду с целью генерации вторичного выходного сигнала.
Фиг.6B представляет собой график корреляции между суммарными ошибками данных множества внутренних клинических исследований и значениями основной функции.
На Фиг.6C показан график корреляции между суммарными ошибками тех же самых данных в зависимости от объединенных значений основной функции и функции невязки.
Фиг.6D изображает процентные отклонения как функцию времени с использованием невязки BC.
Фиг.6E изображает процентные отклонения как функцию времени с использованием невязки CD.
Фиг.7A изображает схематическое представление биосенсорной системы, которая определяет концентрацию анализируемого вещества в образце биологической жидкости.
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
Ошибки в анализе и получающаяся в результате погрешность в определенных концентрациях анализируемых веществ может быть снижена посредством компенсации ошибок невязки. Путем сосредоточения внимания на ошибках невязки и нахождения функций невязки, ассоциированных с ошибками невязки, суммарная ошибка в анализах может быть снижена. Ошибки в биосенсорной системе могут происходить из множества источников ошибок и факторов, вносящих вклад в ошибки, происходящих из различных процессов/режимов работы, которые являются частично или полностью независимыми. Путем компенсации основных ошибок, таких как температура и гематокритное число, с помощью основной функции компенсации с целью удаления, по меньшей мере, 50% от суммарной ошибки могут быть определены оставшиеся ошибки невязки и функция невязки, ассоциированная с данными ошибками невязки.
Компенсация ошибок невязки может, по существу, компенсировать суммарные ошибки анализа до тех пор, пока ошибки не станут случайными. Случайные ошибки - это такие ошибки, которые не относятся к какому-либо вносящему ошибки фактору и не описываются функцией невязки на уровне, считающемся статистически значимым. Компенсация с помощью основной функции и функции невязки, используемых совместно, может улучшить характеристики измерений биосенсорной системы более чем одним способом. Например, объединенная основная компенсация и компенсация невязки может улучшить характеристики измерений биосенсорной системы в отношении одного или более пределов процентной погрешности стандартного отклонения процентной погрешности, среднего стандартного отклонения процентной погрешности, разброса средней процентной погрешности и/или другими способами.
Компенсация ошибки невязки может обеспечить наилучший эффект для образц