Способ и состав для получения реагента для радионуклидной диагностики на основе меченной технецием-99m 5-тио-d-глюкозы
Иллюстрации
Показать всеИзобретение относится к медицине, радиологии, к составам и способам получения радиоактивных препаратов медицинского назначения, которые могут быть использованы для радионуклидной диагностики в онкологии. Способ получения реагента для радионуклидной диагностики на основе меченной технецием-99m 5-тио-D-глюкозы включает приготовление реакционной смеси, состоящей из производной глюкозы, олова (II) хлорида дигидрата, соляной кислоты и аскорбиновой кислоты в 1 мл раствора, фильтрование и стерилизацию полученного раствора с последующей лиофилизацией реагента и его герметизацией во флаконе, причем лиофилизацию смеси проводят без предварительного замораживания в жидком азоте. Реакционная смесь содержит 5-тио-D-глюкозу и воду для инъекций при следующем соотношении компонентов: 5-тио-D-глюкозы 15 мг, олова (II) хлорида дигидрата 0,150-0,175 мг, 0,05 М соляной кислоты 200 мкл (0,36 мг), аскорбиновой кислоты 0,5 мг и 1 мл воды для инъекций. Технический результат: создание стандартного состава устойчивого при хранении для изготовления радиофармацевтического препарата на основе 99mTc-5-тио-D-глюкозы с целью получения изображений опухоли с помощью гамма-камеры методом ОФЭКТ и визуализации биохимических изменений метаболизма, что будет способствовать точной диагностике и эффективному лечению опухолей. 2 н.п. ф-лы, 2 пр., 3 фиг., 1 табл.
Реферат
Изобретение относится к медицине, радиологии, к составам и способам получения радиоактивных препаратов медицинского назначения, которые могут быть использованы для радионуклидной диагностики в онкологии.
В существующей мировой практике наиболее перспективными радиофармпрепаратами (РФП) для ранней диагностики злокачественных новообразований являются меченные радиоактивными изотопами производные глюкозы. Это связано с тем, что в клетках опухоли отмечается повышенный уровень метаболизма глюкозы по сравнению с нормальными клетками. Поэтому при введении в организм меченой глюкозы в этих клетках наблюдается увеличенное количество радиоактивного маркера, что позволяет получать информацию о местоположении и размерах опухоли за счет высокого соотношения концентраций РФП «опухоль/фон».
В настоящее время в России и за рубежом для диагностики опухолей и оценки эффективности противоопухолевой терапии применяется, главным образом, метод позитрон-эмиссионной томографии (ПЭТ) с РФП 2-фтор-2-дезокси-D-глюкоза (18F-ФДГ), содержащий позитрон-излучающий радионуклид фтор-18 [Baum R.P., Schmuecking M., Bonnet R. et all. F-18 FDG PET for metabolic 3D-radiation treatment planning of non-small cell lung cancer // Eur. J. Nucl. Med. and Mol. Imag. - 2002. Vol.43. - P.96-99]. Несмотря на высокую диагностическую информативность метода ПЭТ, его широкое применение в России ограничено из-за высокой стоимости, а также отсутствия ПЭТ-центров. Так стоимость одного обследования с 18F-ФДГ (в зависимости от исследуемой области) колеблется от 7-20 тыс. рублей и более, а ориентировочная стоимость строительства ПЭТ-центра составляет около 700 млн. рублей. В данное время в России реально функционируют только 10 центров позитронно-эмиссионной томографии. Из них 6 расположены в Москве и Санкт-Петербурге.
Вместе с тем, в стране существует более 200 центров, оснащенных гамма-камерами для проведения однофотонной эмиссионной компьютерной томографии (ОФЭКТ), где диагностика чаще всего осуществляется с использованием РФП на основе короткоживущего (T1/2=6 ч) технеция-99м (99mTc). Как правило, технециевые РФП изготавливаются в виде стандартных наборов реагентов (лиофилизатов) к генератору технеция-99м, которые представляют собой смеси, приготовленные методом сублимационной сушки [Лыков А.В. Сублимационная сушка // В кн.: Теория сушки. - M.: Энергия. - 1968. - С.334-362]. При их смешивании с элюатом технеция-99м (раствор натрия пертехнетата, 99mTc), выделенного из генератора, получается готовый РФП с заданными свойствами. Срок годности лиофилизатов обычно составляет 1 год.
Разработка для ОФЭКТ в качестве диагностического средства лиофилизатов для приготовления меченых 99mTc тех или иных производных глюкозы позволила бы во много раз увеличить количество исследований в онкологии и значительно снизить демографические потери населения от социально значимых заболеваний. Однако до настоящего времени такие препараты до практического применения в России и в мире не доведены.
Основные проблемы, с которыми сталкиваются исследователи при получении меченных 99mTc производных глюкозы, связаны с химическими свойствами этого радионуклида. В отличие от РФП на основе таких изотопов, как 123I и 18F, которые могут быть получены в результате окислительно-восстановительных реакций или реакций нуклеофильного замещения с лигандом, РФП с 99mTc обычно получают только через координационную связь с определенным лигандом, что является гораздо более трудным. Тем более, что глюкоза имеет в молекуле только кислород и атомы углерода, и здесь сложно сформировать устойчивую координационную связь с 99mTc. Решением указанной проблемы является введение в молекулы производных глюкозы азота или серы. При этом 99mTc в степени окисления +5 выступает в качестве донора электронов и может образовывать координационные связи с этими атомами. Как известно, 99mTc, выделяемый из генератора, имеет степень окисления +7. Поэтому для образования координационных связей с производными глюкозы, содержащими в молекуле атом азота или серы, необходимо снизить валентность 99mTc, например, с помощью восстанавливающего агента - олова (II) хлорида дигидрата (SnCl2·2H2O).
В настоящее время имеется достаточно много способов получения меченных технецием-99м различных производных глюкозы. Например, в работе [Zhu Lin Liu. Glucose Derivative complex marked with 99mTc, 188Re or 186Re and its prepn process // CN Заявка №101020697 МПК A61K 51/04; C07F 13/00; A61K 103/10 - 22.08.2008] рассматриваются способы приготовления меченных радионуклидами комплексов производных глюкозы. Отмечается, что комплексы глюкозы с 99mTc, 188Re и 186Re имеют низкую стоимость в сочетании с удобным периодом полураспада и энергией излучения для проведения ОФЭКТ исследований.
Известен относительно простой способ получения 5-тио-D-глюкозы с технецием-99м [Suleyman Kutlan Ozker, Bert David Collier. Imaging methods and compositions // United States Patent No.: 60998222003 A61K 51/00 - 08.08.2000], в соответствии с которым препарат 99mTc-5-тио-D-глюкозу готовят путем смешивания 10 мг 5-тио-D-глюкозы с 74 мкг хлорида олова (II) дигидрата с последующим введением в полученную смесь 2-4 мл раствора пертехнетата, 99mTc с активностью 50-100 мКи (1,85-3,7 ГБк) и инкубацией в течение 30 мин. При этом эффективность мечения составляет 98,5±0,8% и остается стабильной 24 ч. Авторы предполагают, что реакция мечения будет хорошо проходить в присутствии 0,01-2 мг ионов олова (II) в виде хлорида дигидрата или фторида. Недостатком предложенного способа является то, что в отличие от лиофилизатов, исходная смесь реагентов для получения препарата не может храниться более 1-2 часов вследствие окисления олова (II) до 4-х валентного состояния.
Такой же недостаток имеет методика мечения 5-тио-D-глюкозы, предложенная в [Hee-Kyung Lee, Dae-Hybk Moon, Jin-Sook Ryu et al. Radioisotope-labeled complexes of glucose derivatives and kits for the preparation thereof // Patent United States Pub. No.: 2003/0120046 A1 - 26.06.2003]. Здесь во флакон, содержащий смесь 5-тио-D-глюкозы (5 мг, 0,51 ммоль) и SnCl2·H2O (80 мкг), добавляют 20 мКи/мл 99mTcO4-. После перемешивают в течение 10 мин. Затем проводят исследования.
Наиболее близким к заявляемому является состав и способ получения реагента для приготовления меченной технецием-99м производной 1-тио-D-глюкозы, приведенный в этой же работе и выбранный в качестве прототипа. Согласно этому способу смесь 1 мг 1-тио-β-D-глюкозы, 80 мкг хлорида олова (II), 100 мкл 0,02 М HCl и 0,5 мг аскорбиновой кислоты, используемой в качестве добавки, препятствующей восстановлению олова (II), растворяют в 1 мл физиологического раствора. Затем полученный раствор пропускают через стерильный фильтр (размер пор 0,22 мкм) и вносят во флакон вместимостью 10 мл. После содержимое флакона замораживают в жидком азоте и лиофилизируют. По окончании обезвоживания флакон запечатывают алюминиевой крышкой под вакуумом и выдерживают при комнатной температуре. Перед использованием во флакон с реагентом вносят 50 мКи 99mTc, содержащегося в 1,5 мл физиологического раствора, и перемешивают при комнатной температуре в течение 10 минут.
В приведенном способе-прототипе не рассматриваются условия и возможность создания реагента в виде лиофилизата для приготовления меченой 99mTc производной 5-тио-D-глюкозы.
Таким образом, эта задача до настоящего времени остается нерешенной. Технический результат от предлагаемого изобретения состоит в создании стандартного состава (лиофилизата), устойчивого при хранении для изготовления радиофармацевтического препарата на основе 99mTc-5-тио-D-глюкозы, с целью получения изображений опухоли с помощью гамма-камеры методом ОФЭКТ и визуализации биохимических изменений метаболизма, что будет способствовать точной диагностике и эффективному лечению опухолей.
Для достижения нового технического результата в способе получения реагента для радионуклидной диагностики на основе меченной технецием-99m 5-тио-D-глюкозы, включающем приготовление реакционной смеси, состоящей из производной глюкозы, олова (II) хлорида дигидрата, соляной кислоты и аскорбиновой кислоты в 1 мл раствора, фильтрование и стерилизацию полученного раствора с последующей лиофилизацией реагента и его герметизацией во флаконе, причем лиофилизацию смеси проводят без предварительного замораживания в жидком азоте.
Реакционная смесь содержит 5-тио-D-глюкозу и воду для инъекций при следующем соотношении компонентов: 5-тио-D-глюкозы 15 мг, олова (II) хлорида дигидрата 0,150-0,175 мг, 0,05 М соляной кислоты 200 мкл (0,36 мг), аскорбиновой кислоты 0,5 мг и 1 мл воды для инъекций.
Изобретение поясняется Фиг. 1-3, на которых представлено:
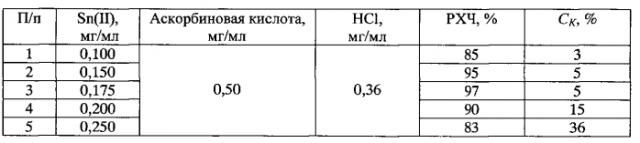
Фиг. 1. Радиохроматограмма препарата 99mTc-3-тио-D-глюкоза. Подвижная фаза: ацетон.
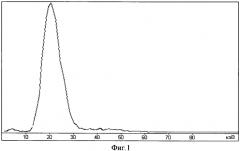
Фиг. 2. Радиохроматограмма препарата 99mTc-тио-D-глюкоза. Подвижная фаза - смесь C2H5OH: 25% NH4OH:H2O÷2:5:5 (по объему).
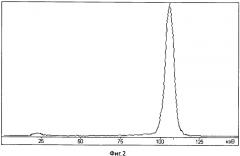
Фиг. 3. Сцинтиграмма мыши линии C57BL/6 с привитой в область бедра карциномой Льюиса (LLC) через 30 мин после инъекции препарата 99mTc-6-тио-D-глюкоза.
Сущность изобретения поясняется примером конкретного выполнения.
Пример 1. Во флакон вместимостью 10 мл вносят навеску 5-тио-D-глюкозы массой 15 мг и разводят ее в 1 мл воды для инъекций. Затем последовательно добавляют 25 мкл свежеприготовленного раствора Sn (II) (концентрация 7 мг/мл по SnCl2·2H2O), 50 мкл водного раствора аскорбиновой кислоты с концентрацией 10 мг/мл и 200 мкл 0,05М HCl. Полученный раствор пропускают через стерилизующий фильтр (размер пор 0,22 мкм) во флакон вместимостью 10 мл. После флакон без предварительного замораживания смеси помещают в холодильную камеру лиофилизатора и проводят процесс лиофилизации в автоматическом режиме при заданных параметрах: P=0,2 Па, t=-50°C в течение 24 часов.
Для приготовления препарата во флакон с реагентом вводят 4 мл элюата 99mTc с активностью 1,5-2 ГБк (40-50 мКи) и инкубируют в ультразвуковой ванне в течение 30 мин.
Радиохимическую чистоту (РХЧ) полученного продукта оценивают путем снятия хроматограмм в двух подвижных фазах: в ацетоне с использованием пластин силикагеля ПТСХ-АФ-А-УФ (Sorbfil) и в смеси C2H5OH: 25% NH4OH:H2O÷2:5:5 на полосках ватмана Filtrak-17 (Германия) с последующим изучением распределения активности 99mTc по длине радиохроматограмм.
В среде ацетона комплекс 99mTc-тио-D-глюкоза остается на линии старта, а непрореагировавшие ионы 99mTc(VII) поднимаются с фронтом растворителя, что позволяет сделать количественную оценку этой примеси. Напротив, в среде этанола с фронтом элюента вместе с ионами 99mTc(VII) поднимается и комплекс 99mTc-5-тио-D-глюкоза, а на линии старта остается примесь несвязанного с субстанцией гидролизированного оксида технеция (99mTcO2), что также позволяет сделать ее количественную оценку. Хроматограммы меченной 99mTc-5-тио-D-глюкозы, полученные в ацетоне и в смеси этанола с аммиаком, представлены на фиг. 1 и 2, соответственно. Расчеты, сделанные по этим хроматограммам, показывают, что общее содержание примесей 99mTc(VII) и гидролизованного оксида (99mTcO2) в препарате не превышает 3%, а его радиохимическая чистота составляет 97% и остается на этом уровне в течение 24 ч.
Пример 2. Реакционную смесь готовят так же, как и в примере 1, с тем отличием, что после ее фильтрации через стерилизующий фильтр во флакон, проводят предварительное замораживание флакона в жидком азоте с последующим его помещением в холодильную камеру лиофилизатора и проведением лиофилизации смеси в том же режиме. Для приготовления препарата во флакон с реагентом также вводят элюат 99mTc с активностью 1,5-2 ГБк (40-50 мКи) и инкубируют в ультразвуковой ванне в течение 30 мин.
Последующее изучение радиохроматограмм препарата в ацетоне и смеси этанола с аммиаком показало, что его радиохимическая чистота составляет 87%, что хуже, чем в примере 1, где предварительное замораживание смеси не проводилось.
В состав смеси, приведенной в Примере 1, в качестве вспомогательных веществ, обеспечивающих восстановление 99mTc(VII) и его стабилизацию в этом состоянии при последующем взаимодействии с 5-тио-D-глюкозой, входят 0,175 мг Sn(II), 0,5 мг аскорбиновой кислоты и 0,36 мг HCl. Здесь количество аскорбиновой кислоты совпадает с прототипом. Приведенное количество HCl обеспечивает значение pH=5 готового препарата после смешивания лиофилизата с 4 мл элюата технеция-99м.
К числу факторов, осложняющих получение целевого меченного 99mTc продукта, относится то, что при взаимодействии 99mTc(VII) с Sn(II) возможно дополнительное образование коллоида типа (-O-TcO-O-SnCl2-O-TcO-)n, где n=2, 3 … - число, зависящее от pH раствора. Образование коллоида олова возможно также вследствие гидролиза избытка SnCl2, протекающего по уравнению: SnCl2+N2O→Sn(OH)Cl+HCl [Зайцева Л.Л., Величко А.В., Виноградов И.В. Соединения технеция и области их применения // Итоги науки и техники. - М.: ВИНИТИ, 1984. - Т.9. - С.180].
В этой связи были проведены предварительные исследования для установления необходимого и достаточного количества Sn(II) в составе лиофилизата, которое бы обеспечивало практически полное восстановление 99mTc(VII) при минимальном образовании коллоида. Активность 99mTc, связанного на коллоиде, определяли путем фильтрации препарата через фильтрующие насадки типа Minisart с диаметром пор 50 нм с последующим измерением активности фильтрата. Расчет вклада активности коллоидной формы (СК) в общую активность препарата проводили по разности активностей исходного раствора препарата (АИсх) и фильтрата (АФ) [%].
Радиохимическую чистоту препаратов, полученных из лиофилизатов с различным содержанием Sn(II), определяли так же, как и в Примере 1. Результаты этих исследований приведены в Таблице.
Из представленных результатов следует, что с увеличением в составе смеси содержания Sn(II) в препарате существенно возрастает количество радиоактивного коллоида с одновременным снижением его РХЧ. Снижение радиохимической чистоты наблюдается также при концентрации Sn(II) в смеси ниже 150 мг/мл. Лучшие показатели РХЧ достигаются в области значений 0,150-0,175 мг/мл, что и определило содержание Sn(II) в лиофилизате.
В целом предлагаемый способ позволяет получать реагент для приготовления меченного технецием-99м препарата на основе 5-тио-D-глюкозы, пригодный для проведения гамма-сцинтиграфических исследований в онкологии, о чем свидетельствует сцинтиграмма на фиг. 3, полученная через 30 мин после введения радиофармпрепарата экспериментальному животному (мыши).
1. Состав реагента для радионуклидной диагностики на основе меченной технецием-99m 5-тио-D-глюкозы, содержащий производную глюкозы, олова (II) хлорида дигидрат, соляную кислоту и аскорбиновую кислоту в 1 мл раствора, отличающийся тем, что в качестве производной глюкозы содержит 5-тио-D-глюкозу, а в качестве раствора воду для инъекций при следующем соотношении компонентов в 1 мл раствора:
| 5-тио-D-глюкозы | 15 мг |
| олова (II) хлорида дигидрата | 0,150-0,175 мг |
| 0,05 М соляной кислоты | 0,36 мг |
| аскорбиновой кислоты | 0,5 мг |
2. Способ получения реагента для радионуклидной диагностики на основе меченной технецием-99m 5-тио-D-глюкозы, включающий приготовление реакционной смеси, состоящей из производной глюкозы, олова (II) хлорида дигидрата, соляной кислоты и аскорбиновой кислоты в 1 мл раствора, фильтрующую стерилизацию полученного раствора, последующую лиофилизацию и герметизацию реагента во флаконе, отличающийся тем, что в для приготовления реакционной смеси используют состав по п. 1, а лиофилизацию смеси проводят без предварительного замораживания в жидком азоте.