Лечение и предупреждение вич-инфекции
Иллюстрации
Показать всеГруппа изобретений относится к долговременному применению парентерального состава для производства лекарственного препарата для лечения субъекта, инфицированного ВИЧ, причем данный препарат предназначен для подкожной или внутримышечной инъекции и состоит из бреканавира, или его соли в форме водной суспензии микро- или наночастиц, содержащей полисорбат-20, и вводится периодически с интервалами от 6 до 12 месяцев и к указанной фармацевтической композиции. Технический результат состоит в снижении числа инъекции композиции (препарата) в отсутствие дополнительного агента ритонавира. 2 н. и 5 з.п. ф-лы, 4 ил., 4 табл.
Реферат
Область техники, к которой относится изобретение
Данное изобретение относится к области долговременного лечения ВИЧ-инфекции путем периодического введения парентерального состава, содержащего бреканавир, в течение относительно длительных интервалов времени. Данное изобретение дополнительно относится к фармацевтическим композициям для парентерального введения, содержащим микро- или наночастицы бреканавира, суспендированные в водном фармацевтически приемлемом носителе, для лечения и профилактики ВИЧ-инфекции.
Предпосылки создания изобретения
Лечение инфекции, вызываемой вирусом иммунодефицита человека (ВИЧ), известного как причина синдрома приобретенного иммунодефицита (СПИД), остается глобальной медицинской проблемой. ВИЧ способен уклонятся от иммунологического давления, способен адаптироваться к различным типам клеток и условиям роста и способен вырабатывать резистентность к существующим на сегодняшний день лекарственным средствам. Последние включают нуклеозидные ингибиторы обратной транскриптазы (NRTI), ненуклеозидные ингибиторы обратной транскриптазы (NNRTI), нуклеотидные ингибиторы обратной транскриптазы (NtRTI), ингибиторы ВИЧ-протеазы (PI) и более современные ингибиторы слияния (также известные как ингибиторы проникновения).
Несмотря на то что каждое из этих лекарственных средств эффективно подавляет ВИЧ, их действие при индивидуальном применении препятствует возникновению резистентных мутантов. Это привело к введению комбинированной терапии несколькими анти-ВИЧ агентами, обычно имеющими различные профили действия. В частности, введение «HAART» (высокоактивная противовирусная терапия) привело к значительному улучшению анти-ВИЧ лечения, сильно снизившейся ВИЧ-ассоциированной заболеваемости и смертности. В существующих руководствах по противовирусной терапии такая схема тройной комбинированной терапии рекомендуется даже для начальной терапии. Однако ни одна из существующих на сегодняшний день лекарственных терапий не способна полностью устранить ВИЧ. Даже в случае HAART возможно возникновение резистентности, часто вследствие несоблюдения и непостоянного выполнения схемы противовирусной терапии. В этих случаях, эффективность HAART можно восстановить заменой одного из ее компонентов другим компонентом, относящимся к другому классу. При правильном применении лечение комбинациями HAART может подавлять вирус в течение многих лет (до десятилетий) до уровня, на котором он не может вызывать появление СПИД.
Одним классом анти-ВИЧ лекарственных средств, используемых в HAART, являются PI, ряд которых доступен в продаже на сегодняшний день, а несколько других находятся на различных стадиях разработки. Одним из PI, находящихся в разработке, является соединение [(3R,3aS,6aR)-2,3,3a,4,5,6a-гексагидрофуро[5,4-b]фуран-3-ил]-N-[(2S,3R)-4-(1,3-бензодиоксол-5-илсульфонил(2-метилпропил)амино)-3-гидрокси-1-[4-[(2-метил-1,3-тиазол-4-ил)метокси]фенил]бутан-2-ил]карбамат, также называемый N-(3R,3aS,6aR)-гексагидрофуро[2,3-b]фуран-3-илоксикарбонил-(4S,5R)-4-[4-(2-метилтиазоло-4-метилокси)бензил]-5-изобутил[(3,4-метилендиоксифенил)сульфонил]аминометил-2,2-диметилоксазолидином (CAS 313682-08-5), обычно называемый бреканавиром. Хотя данное соединение проявляло выраженную активность против ВИЧ дикого типа, а также против мутированных вариантов, его разработка была прекращена вследствие непреодолимых проблем, связанных с фармацевтическим составом.
Вследствие их фармакокинетических свойств и необходимости поддерживать концентрацию в плазме выше минимального уровня, для большинства анти-ВИЧ лекарственных средств требуется частое введение в относительно высоких дозах. Число и/или объем дозированных форм, которые необходимо вводить, обычно называют «лекарственной нагрузкой». Высокая лекарственная нагрузка нежелательна по многим причинам, например, из-за частоты введения, часто в сочетании с необходимостью проглатывать дозированные формы крупного размера, а также необходимостью хранить и транспортировать большое число или объем лекарственных препаратов. Высокая лекарственная нагрузка повышает риск того, что пациенты не принимают полную дозу препарата, таким образом, не выполняя предписанную схему дозирования. Кроме снижения эффективности лечения это также приводит к возникновению вирусной резистентности. Проблемы, ассоциированные с высокой лекарственной нагрузкой, умножаются, когда пациент должен принимать комбинацию различных анти-ВИЧ агентов.
Поэтому желательна ВИЧ-ингибирующая терапия, снижающая лекарственную нагрузку благодаря тому, что терапия включает введение дозированных форм относительно небольшого размера и, кроме того, не требует их частого введения. Представляет интерес анти-ВИЧ терапия, включающая введение дозированных форм с большими интервалами, например, с двухнедельными интервалами или более длительными интервалами, или даже с интервалами в один месяц или более длительными интервалами.
Согласно данным, полученным in vitro, пероральное введение бреканавира без агента, положительно влияющего на метаболизм и/или фармакокинетику лекарственного средства, улучшая биодоступность, как, например, ритонавира, давало концентрацию бреканавира, теоретически недостаточную для ингибирования PI-резистентного вируса. Однако совместное введение бреканавира с ритонавиром значительно увеличивало для бреканавира площадь под кривой зависимости концентрации от времени и максимальную концентрацию, позволяя достичь концентраций бреканавира, теоретически способных ингибировать PI-резистентный ВИЧ (Antimicrob. Agents Chemother. 50: 2201-2206). Соединение бреканавира, его фармакологическое действие, а также ряд методик его получения были описаны в WO 2000/076961. Совместное введение с ритонавиром не только увеличивает лекарственную нагрузку, но ритонавир сам по себе влияет также на эффективность множества других лекарственных препаратов, затрудняя их совместное введение. Кроме того, он сам по себе может вызывать большое число побочных эффектов.
Поэтому обеспечение терапии на основе бреканавира без необходимости в совместном введении ритонавира должно быть желаемой задачей в отношении упрощения схемы лечения и устранения побочных эффектов при введении ритонавира.
ВИЧ никогда нельзя полностью устранить, поэтому индивидуум, инфицированный ВИЧ, подвергает постоянному риску заражения других людей. После первоначального заражения проходит длительное время перед возникновением первых симптомов СПИД. Люди могут жить годами с инфекцией, не испытывая каких-либо ее признаков, тем самым не беспокоясь о риске дальнейшей передачи вируса другим людям. Поэтому критичным является предупреждение передачи ВИЧ. Профилактика в настоящий момент сфокусирована на предупреждении передачи в результате половых контактов, в частности, на использовании презервативов в популяциях, имеющих риск инфицирования, на тщательной проверке образцов крови на присутствие ВИЧ и на устранении контактов с кровью, потенциально зараженной ВИЧ.
Несмотря на все эти меры, всегда существует неизбежный риск заражения для индивидуумов, находящихся в контакте с ВИЧ-инфицированными людьми. Это особенно актуально для медицинского персонала, обеспечивающего уход за инфицированными пациентами или пациентами с риском заражения, например, для терапевтов, медсестер или дантистов. В другую группу риска входят дети на грудном вскармливании, чьи матери являются инфицированными или имеют риск инфицирования, особенно в развивающихся странах, где альтернатив грудному вскармливанию существует гораздо меньше.
Поэтому существует необходимость в дополнительных средствах, предупреждающих передачу ВИЧ. Особенно необходимы эффективные средства предупреждения, легкие в применении. Такие профилактические средства являются еще одной задачей настоящего изобретения.
Было обнаружено, что периодическое введение парентеральных составов бреканавира с интервалами в две недели или с более длительными интервалами, например до одного года, приводило к его содержанию в плазме, достаточному для эффективного предупреждения ВИЧ-инфекции или для эффективного подавления ВИЧ-инфекции. Это позволяет снизить число введений, снижая, таким образом, лекарственную нагрузку, и способствует соблюдению пациентом схемы приема лекарственного средства. Дополнительным преимуществом является отсутствие необходимости в совместном введении дополнительного агента, имеющего положительный эффект на метаболизм и/или фармакокинетику лекарственного средства в отношении улучшения биодоступности, например, ритонавира, в результате чего дополнительно снижается лекарственная нагрузка, а также исключаются побочные эффекты, ассоциированные с введением ритонавира.
Сущность изобретения
В одном аспекте настоящее изобретение относится к применению парентерального состава, содержащего эффективное в отношении вируса количество бреканавира или его фармацевтически приемлемой аддитивной соли кислоты и носитель, для изготовления лекарственного препарата для предупреждения передачи ВИЧ-инфекции или для лечения субъекта, инфицированного ВИЧ, где состав вводят или должны вводить периодически с помощью подкожной или внутримышечной инъекции с временными интервалами в диапазоне от двух недель до одного года.
Другой аспект изобретения относится к способу предупреждения передачи ВИЧ-инфекции или лечения субъекта, инфицированного ВИЧ, включающему введение парентерального состава, содержащего эффективное в отношении вируса количество бреканавира или его фармацевтически приемлемой аддитивной соли кислоты и носитель, где состав вводят периодически с помощью подкожной или внутримышечной инъекции с временными интервалами в диапазоне от двух недель до одного года.
В одном варианте осуществления изобретение относится к применению или способу, как определено в данном описании, где парентеральный состав вводят или должны вводить с временными интервалами, которые составляют интервал от двух недель до одного месяца, или интервал от одного месяца до трех месяцев, или интервал от трех месяцев до шести месяцев, или интервал от шести месяцев до двенадцати месяцев.
В другом варианте осуществления изобретение относится к применению или способу, как определено в данном описании, где парентеральный состав вводят или должны вводить один раз в две недели, или один раз в месяц, или один раз в три месяца.
Один аспект настоящего изобретения касается того факта, что парентеральные составы могут быть введены без агента, положительно влияющего на метаболизм и/или фармакокинетику лекарственного средства в отношении улучшения биодоступности, например, ритонавира.
В дополнительном варианте осуществления настоящее изобретение относится к фармацевтической композиции для введения с помощью внутримышечной или подкожной инъекции, содержащей терапевтически эффективное количество бреканавира или его соли в форме суспензии микро- или наночастиц, содержащей:
(а) бреканавир или его соль в форме микро- или наночастиц, имеющих адсорбированный на своей поверхности модификатор поверхности; и
(b) фармацевтически приемлемый водный носитель, в котором суспендирован активный ингредиент бреканавира.
Изобретение дополнительно относится к способу лечения субъекта, инфицированного ВИЧ, включающему введение с помощью внутримышечной или подкожной инъекции эффективного в отношении ВИЧ количества фармацевтической композиции, как определено в данном описании выше или ниже. Или, альтернативно, изобретение относится к применению фармацевтической композиции, как определено в данном описании выше или ниже, для изготовления лекарственного препарата для лечения ВИЧ-инфекции. В одном варианте осуществления композиция предназначена для долговременного лечения ВИЧ-инфекции.
Другой аспект изобретения обеспечивает способ долговременного лечения субъекта, инфицированного ВИЧ, включающий введение эффективного количества фармацевтической композиции, как определено в данном описании выше или ниже, с помощью внутримышечной или подкожной инъекции; где композицию вводят или должны вводить периодически с временными интервалами, которые составляют интервал от двух недель до одного года или от двух недель до двух лет. Или, альтернативно, изобретение относится к применению фармацевтической композиции, как определено в данном описании выше или ниже, для изготовления лекарственного препарата для долговременного лечения субъекта, инфицированного ВИЧ, для введения с помощью внутримышечной или подкожной инъекции, где композицию вводят или должны вводить периодически с временными интервалами, которые составляют интервал от двух недель до одного года или от двух недель до двух лет.
Изобретение дополнительно относится к способу предупреждения ВИЧ-инфекции у субъекта с риском инфицирования ВИЧ, включающему введение эффективного для предупреждения ВИЧ-инфекции количества фармацевтической композиции, как определено в данном описании выше или дополнительно ниже, указанному субъекту. Или, альтернативно, изобретение относится к применению фармацевтической композиции, как определено в данном описании выше или дополнительно ниже, для изготовления лекарственного препарата для предупреждения ВИЧ-инфекции у субъекта с риском инфицирования ВИЧ.
В другом аспекте изобретение относится к способу долговременного предупреждения ВИЧ-инфекции у субъекта с риском инфицирования ВИЧ, включающему введение указанному субъекту эффективного количества фармацевтической композиции, как определено в данном описании выше или дополнительно ниже, где композицию вводят или должны вводить периодически с временными интервалами, которые составляют интервал от двух недель до одного года или от двух недель до двух лет.
Настоящее изобретение, кроме того, относится к применению фармацевтической композиции, как определено в данном описании выше или дополнительно ниже, для изготовления лекарственного препарата для долговременного предупреждения ВИЧ-инфекции у субъекта с риском инфицирования ВИЧ, где композицию вводят или должны вводить периодически с временными интервалами, которые составляют интервал от двух недель до одного года или от двух недель до двух лет.
В одном варианте осуществления изобретение относится к применению или способу, как определено в данном описании, где фармацевтическую композицию вводят или должны вводить с временными интервалами, которые составляют интервал от двух недель до одного месяца, или интервал от одного месяца до трех месяцев, или интервал от трех месяцев до шести месяцев, или интервал от шести месяцев до двенадцати месяцев.
В другом варианте осуществления изобретение относится к применению или способу, как определено в данном описании, где фармацевтическую композицию вводят или должны вводить один раз в две недели, или один раз в месяц, или один раз в два месяца, или один раз в три месяца.
Дополнительные фармацевтические композиции, способы лечения или предупреждения, а также применение для изобретения лекарственных препаратов на основе указанных композиций будут описаны в настоящем описании ниже, и подразумевается, что они являются частью настоящего изобретения.
Описание фигур
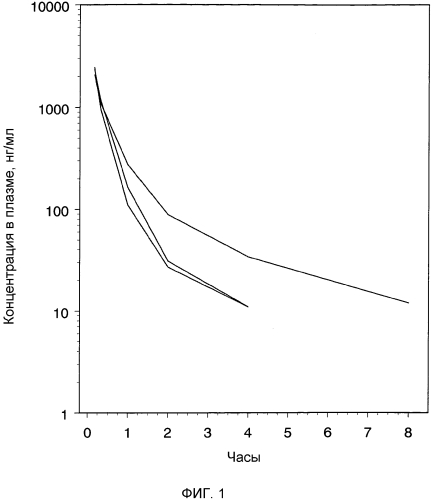
Фиг.1: индивидуальные профили плазматических концентраций (нг/мл) относительно времени после внутривенного введения крысам раствора бреканавира в количестве 2 мг/кг.
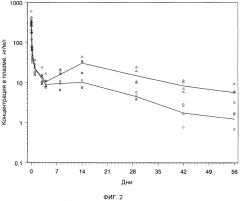
Фиг.2: индивидуальные и средние концентрации бреканавира в плазме после однократной подкожной инъекции крысам раствора бреканавира в количестве 16 (Δ) и 56 мг/кг (o).
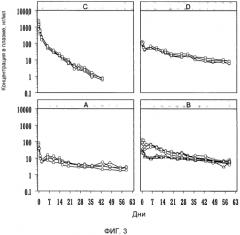
Фиг.3: индивидуальные профили плазматических концентраций бреканавира (нг/мл) относительно времени после однократной внутримышечной (o) и подкожной (Δ) инъекции крысам:
А. микросуспензии бреканавир-Tween 20 (62,5 мг/мл) в количестве 50 мг/кг;
B. наносуспензии бреканавир-Tween 20 (100 мг/мл) в количестве 50 мг/кг;
С. наносуспензии бреканавир-F108 (100 мг/мл) в количестве 50 мг/кг;
D. наносуспензии бреканавир-Tween 20 (200 мг/мл) в количестве 50 мг/кг;
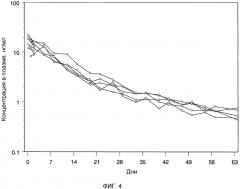
Фиг.4: индивидуальные профили плазматических концентраций бреканавира (нг/мл) относительно времени после однократной внутримышечной дозы (50 мг/животное) наносуспензии в Tween 20 (100 мг/мл).
Подробное описание изобретения
Бреканавир можно использовать в основной форме или в виде фармацевтически приемлемой соли, например, в виде аддитивной соли кислоты. Фраза «фармацевтически приемлемые аддитивные соли кислот» означает, что они содержат терапевтически активные нетоксичные соли. Везде в настоящем описании термин «бреканавир» относится как к свободной форме, так и к любой его фармацевтически приемлемой соли.
Термин «профилактика ВИЧ-инфекции» относится к предупреждению или предотвращению заражения субъекта ВИЧ. Источник инфекции может быть различным: материал, содержащий ВИЧ, в частности, жидкость тела, содержащая ВИЧ, например, кровь или сперма, или другой субъект, инфицированный ВИЧ. Предупреждение ВИЧ-инфекции относится к предупреждению передачи вируса из материала, содержащего ВИЧ, или от ВИЧ-инфицированного индивидуума к неинфицированному человеку, или оно связано с предупреждением проникновения вируса в организм неинфицированного человека. Передачей ВИЧ может являться любой известный случай ВИЧ-передачи, например, в результате передачи половым путем или в результате контакта с кровью инфицированного субъекта, например, медицинского персонала, обеспечивающего уход за инфицированными субъектами. Передача ВИЧ может произойти в результате контакта с ВИЧ-зараженной кровью, например, при работе с образцами крови или при переливании крови. Она также может произойти в результате контакта с инфицированными клетками, например, при проведении лабораторных экспериментов с ВИЧ-инфицированными клетками.
Термины «лечение ВИЧ-инфекции», «анти-ВИЧ терапия», а также аналогичные термины относятся к лечению, в результате которого снижается вирусная нагрузка ВИЧ (представляемая в виде числа копий вирусной РНК в определенном объеме сыворотки). Чем более эффективно лечение, тем меньше вирусная нагрузка. Предпочтительно снижать вирусную нагрузку до минимально возможного уровня, например, ниже примерно 200 копий/мл, в частности, ниже примерно 100 копий/мл, более предпочтительно, ниже 50 копий/мл, при возможности - ниже предела обнаружения вируса. Снижение вирусной нагрузки на один, два или даже три порядка (например, снижение примерно в 10-100 раз или в большей степени, например, снижение примерно в 1000 раз) указывает на эффективность лечения. Другим параметром эффективности анти-ВИЧ лечения является число CD4-положительных клеток, которое у здоровых взрослых людей находится в интервале примерно от 500 до примерно 1500 клеток на мкл. Снижение числа CD4-положительных клеток указывает на ВИЧ-инфекцию, и при его падении ниже примерно 200 клеток на мкл может развиться СПИД. Увеличение числа CD4-положительных клеток, например, примерно на 50, 100, 200 или больше клеток на мкл, также указывает на эффективность анти-ВИЧ лечения. Число CD4-положительных клеток, в частности, должно увеличиваться до уровня выше примерно 200 клеток на мкл или выше примерно 350 клеток на мкл. Вирусную нагрузку или количество CD4-положительных клеток (или оба эти параметра) можно использовать для диагностики степени выраженности ВИЧ-инфекции.
Термины «эффективное лечение ВИЧ» и аналогичные термины относятся к такому лечению, которое снижает вирусную нагрузку или повышает число CD4-положительных клеток (или оказывает оба эти действия), как описано выше.
Термин «лечение ВИЧ-инфекции» также относится к лечению заболеваний, ассоциированных с ВИЧ-инфекцией, например, СПИД, или других состояний, ассоциированных с ВИЧ-инфекцией, включая тромбоцитопению, саркому Капоши и инфекцию центральной нервной системы, отличающуюся прогрессирующей демиелинизацией, приводящую к деменции и симптомам, таким как прогрессирующая дизартрия, атаксия и дезориентация, и другие состояния, с которыми также ассоциирована ВИЧ-инфекция, например, периферическая невропатия, прогрессирующая генерализованная лимфоаденопатия (PGL) и СПИД-связанный комплекс (ARC).
Термин «эффективное предупреждение ВИЧ» и аналогичные термины относятся к ситуации, при которой наблюдается снижение относительного числа ново инфицированных субъектов в популяции, контактирующей с источником ВИЧ-инфекции, например, материалом, содержащим ВИЧ, или ВИЧ-инфицированным субъектом. Эффективность предупреждения можно измерить, например, изучая в смешанной популяции ВИЧ-инфицированных и неинфицированных индивидуумов, наблюдается ли снижение относительного числа новоинфицированных индивидуумов при сравнении неинфицированных индивидуумов, получавших лечение фармацевтической композицией по изобретению, и неинфицированных индивидуумов, не получавших лечение. Это снижение можно измерить, используя статистический анализ числа инфицированных и неинфицированных индивидуумов в данной популяции в динамике.
Термин «эффективное количество» относится к такому количеству бреканавира, которое при введении обеспечивает эффективное лечение ВИЧ. Термин «эффективный уровень в плазме» относится к такому уровню бреканавира в плазме, который приводит к снижению вирусной нагрузки, в частности, ниже числа копий, указанных выше. Термин «эффективное количество» аналогично относится к количеству бреканавира, которое при введении эффективно предупреждает ВИЧ.
Термины «терапевтически эффективное количество», «количество, эффективное для предупреждения ВИЧ-инфекции», и аналогичные термины относятся к количеству активного ингредиента бреканавира, которое обеспечивает действующий уровень в плазме крови. Под «действующим уровнем в плазме крови» понимается такой уровень ВИЧ-ингибитора бреканавира в плазме крови, который обеспечивает эффективное лечение или эффективное предупреждение ВИЧ-инфекции.
Термин «субъект», в частности, относится к человеку.
Применение или способы применения парентеральных композиций бреканавира по настоящему изобретению могут предназначаться для лечения ВИЧ-инфекции или для предупреждения передачи ВИЧ-инфекции в течение длительного периода времени. В случае предупреждения ВИЧ-инфекции, композиции следует применять, пока существует риск инфицирования. Или когда риск инфицирования присутствует в течение ограниченного периода времени, композиции следует применять в тот период, когда существует риск инфицирования, например, от двух до трех недель, или от трех до четырех недель, или от одного до двух месяцев, или от двух до трех месяцев, или от трех до шести месяцев, или от шести месяцев до 12 месяцев, или от 12 месяцев до 24 месяцев. Для лечения ВИЧ-инфекции парентеральные композиции бреканавира следует применять в течение длительного периода времени, например, в течение одного года или нескольких лет.
Под выражением «эффективно в течение по меньшей мере двух недель или более длительного периода» понимается, что минимальное значение концентрации активного ингредиента бреканавира в плазме в конце интервала дозирования или между двумя интервалами дозирования должно быть выше порогового значения. В случае терапевтического применения, указанное пороговое значение представляет собой минимальный уровень в плазме, при котором бреканавир обеспечивает эффективное лечение ВИЧ-инфекции. В случае применения для предупреждения ВИЧ-инфекции, указанное пороговое значение представляет собой минимальный уровень в плазме, при котором бреканавир эффективно предупреждает передачу ВИЧ-инфекции.
Фармацевтические композиции по настоящему изобретению можно вводить с различными временными интервалами. При использовании для предупреждения ВИЧ-инфекции фармацевтические композиции по настоящему изобретению можно вводить однократно или ограниченное число раз, например, дважды, три, четыре, пять или шесть раз, или большее число раз. Этот вариант можно рекомендовать, когда предупреждение необходимо на ограниченный период времени, например, период, в течение которого существует риск инфицирования.
Фармацевтические композиции по настоящему изобретению можно вводить с временными интервалами, указанными выше, такими как временные интервалы, которые составляют интервал от двух недель до одного месяца или интервал от одного месяца до трех месяцев, или интервал от трех месяцев до шести месяцев, или интервал от шести месяцев до двенадцати месяцев. В одном варианте осуществления изобретения фармацевтическую композицию можно вводить каждые две недели, или один раз в месяц, или один раз в три месяца. В другом варианте осуществления изобретения временной интервал составляет интервал от одной до двух недель, или от двух до трех недель, или от трех до четырех недель, или временной интервал составляет от одного до двух месяцев, или от двух до трех месяцев, или от трех до четырех месяцев, или от трех до шести месяцев, или от шести месяцев до двенадцати месяцев, или от двенадцати месяцев до двадцати четырех месяцев. Временной интервал может составлять по меньшей мере две недели, но также может составлять несколько недель, например, две, три, четыре, пять или шесть недель, или временной интервал может составлять один месяц или несколько месяцев, например, два, три, четыре, пять или шесть месяцев, или даже более длительный период времени, например, семь, восемь, девять или двенадцать месяцев. В одном варианте осуществления изобретения фармацевтическую композицию по настоящему изобретению вводят с временным интервалом один, два или три месяца. Эти более длительные периоды между каждым введением фармацевтических композиций по изобретению обеспечивают дополнительные преимущества в отношении лекарственной нагрузки и соблюдения пациентом схемы лечения. Для дополнительного улучшения соблюдения пациентом схемы лечения пациента можно проинструктировать принимать свой лекарственный препарат в определенный день недели, если композицию вводят еженедельно, или в определенный день месяца, если препарат вводят ежемесячно.
Длительность временных интервалов между каждым введением композиции по настоящему изобретению может меняться. Например, указанные временные интервалы могут быть выбраны в зависимости от уровня соединения в плазме. Интервалы могут быть сокращены, если уровень бреканавира в плазме крови считается слишком низким, например, когда он приближается к минимальному уровню в плазме крови, указанному в настоящем описании ниже. Интервалы могут быть увеличены, если уровень бреканавира в плазме крови считается слишком высоким. В одном варианте осуществления композиции по изобретению вводят с одинаковыми временными интервалами. Предпочтительно вводить композиции без любых промежуточных дополнительных введений, или другими словами, композиции можно вводить в определенные моменты времени, отделенные друг от друга варьирующим или одинаковым интервалом, например, составляющим по меньшей мере две недели, или любой другой период времени, указанный в настоящем описании, в течение которого не вводят дополнительное количество бреканавира. Временные интервалы одинаковой продолжительности обладают преимуществом простоты схемы введения, то есть введение происходит в один и тот же день недели или один и тот же день месяца. Поэтому такая схема введения включает ограниченную лекарственную нагрузку, тем самым положительно влияя на соблюдение пациентом предписанной схемы дозирования.
Дозу (или количество) вводимого бреканавира, которая представляет собой количество бреканавира в парентеральном составе для использования в изобретении, выбирают таким образом, чтобы концентрация бреканавира в плазме крови поддерживалась при лечении продолжительного периода времени выше минимального уровня в плазме крови. Термин «минимальный уровень в плазме крови» (Cmin) в контексте лечения ВИЧ относится к наименьшему действующему уровню в плазме крови, причем последний представляет собой такой уровень бреканавира в плазме крови, который обеспечивает эффективное лечение ВИЧ, или другими словами, такой уровень бреканавира в плазме крови, который эффективно подавляет ВИЧ. Уровень бреканавира в плазме следует поддерживать выше этого порогового уровня, поскольку низкое содержание лекарственного средства не будет эффективным, тем самым увеличивая риск возникновения мутаций. В случае предупреждения ВИЧ термин «минимальный уровень в плазме крови (или Cmin) относится к наименьшему уровню бреканавира в плазме крови, который обеспечивает эффективное предупреждение передачи ВИЧ-инфекции, то есть представляет собой наименьший уровень в плазме крови, который эффективно ингибирует указанную передачу.
Доза вводимого бреканавира также зависит от временного интервала, в котором его вводят. При менее частом введении доза будет более высокой.
Доза вводимого бреканавира зависит от количества бреканавира в фармацевтических композициях по изобретению или от количества данной композиции, которую вводят. Если желателен более высокий уровень в плазме, то можно ввести любую из двух или обе композиции с более высокой концентрацией бреканавира, или большее количество данной композиции. Если желателен более низкий уровень бреканавира в плазме, то действуют наоборот. Кроме того, можно подобрать комбинацию различных временных интервалов и различных дозировок для того, чтобы получить определенный желаемый уровень в плазме крови.
Доза (или количество) вводимого бреканавира зависит также от частоты введения (то есть временного интервала между каждым введением). Обычно доза будет выше при менее частом введении. Все эти параметры можно использовать для получения желаемого значения уровня в плазме крови.
Схема дозирования также зависит от того, предполагается ли лечение или предупреждение ВИЧ-инфекции. В случае лечения, дозу вводимого бреканавира или частоту введения (или оба параметра) выбирают таким образом, чтобы поддерживать концентрацию бреканавира в плазме крови выше минимального уровня в плазме крови. В частности, уровень бреканавира в плазме крови поддерживают выше минимального уровня в плазме крови примерно 24 нг/мл или выше примерно 40 нг/мл, или выше примерно 50 нг/мл, или выше примерно 75 нг/мл. Уровень бреканавира в плазме крови можно поддерживать выше минимального уровня в плазме крови, то есть выше, например, примерно 100 нг/мл или выше примерно 150 нг/мл, или выше примерно 200 нг/мл. Минимальный уровень в плазме крови можно определить, умножая значение ЕС50 на фактор, выражающий связывание белка и резерв безопасности, который можно установить примерно как 10. Значение ЕС50 можно получить в тесте с использованием ВИЧ дикого типа. О нем также можно узнать из Antimicrobial Agents and Chemotherapy, Apr. 2007, pp. 1202-1208.
В одном варианте осуществления изобретения уровень бреканавира в плазме крови поддерживается в определенном диапазоне, в частности, в диапазоне от минимального уровня в плазме крови, выбранного из указанных выше, и до более высокого уровня в плазме крови, такого как примерно 100 нг/мл, или примерно 200 нг/мл, или примерно 500 нг/мл, или примерно 1000 нг/мл. В одном варианте осуществления уровень бреканавира в плазме крови поддерживают в диапазоне примерно от 5 до примерно 500 нг/мл, или примерно от 10 нг/мл до примерно 200 нг/мл, или примерно от 10 нг/мл до примерно 100 нг/мл, или примерно от 10 нг/мл до примерно 50 нг/мл.
Уровень бреканавира в плазме следует поддерживать выше указанного выше минимального уровня в плазме крови, поскольку более низкая концентрация не будет достаточно подавлять вирус, так что он сможет размножаться с дополнительным риском возникновения мутаций.
В частности, в случае предупреждения ВИЧ, уровень бреканавира в плазме крови можно поддерживать выше минимального уровня в плазме крови, указанного выше для терапевтического применения. Однако при предупреждении ВИЧ концентрацию бреканавира в плазме крови можно поддерживать на более низком уровне, например, на уровне выше примерно 1 нг/мл или примерно 5 нг/мл, или примерно 10 нг/мл. Предпочтительно следует поддерживать уровень бреканавира в плазме крови выше этих указанных минимальных значений уровня в плазме крови, поскольку более низкое содержание лекарственного средства может оказаться неэффективными, тем самым, увеличивая риск передачи ВИЧ. Концентрацию бреканавира в плазме можно поддерживать на несколько большем уровне для создания резерва безопасности. Такие более высокие уровни начинаются примерно с 24 нг/мл или выше. Концентрацию бреканавира в плазме можно поддерживать на уровне, находящемся в диапазоне, указанном выше для терапевтического применения, но в котором нижняя граница включает уровни в плазме крови примерно 4 нг/мл или примерно 5 нг/мл, или примерно 8 нг/мл.
В некоторых обстоятельствах может быть желательно поддерживать концентрацию бреканавира в плазме на относительно низком уровне, например, как можно ближе к минимальным уровням в плазме крови, указанным в настоящем описании. Это позволит снизить частоту введений и/или количество бреканавира, вводимого каждый раз. Это также позволит избежать нежелательных побочных эффектов, что тоже повлияет на одобрение дозированных форм в большинстве групп целевой популяции, которые состоят из здоровых людей с риском инфицирования и, поэтому, менее склонных переносить побочные эффекты. Концентрацию бреканавира в плазме можно поддерживать на относительно низком уровне в случае предупреждения ВИЧ. В других случаях, может быть желательно поддерживать концентрацию бреканавира в плазме на относительно более высоком уровне, например, когда существует высокий риск инфицирования, и более частое введение и/или более высокие дозы не представляют проблему. В этих случаях, минимальный уровень в плазме крови может равняться наименьшему уровню бреканавира в плазме крови, обеспечивающему эффективное лечение ВИЧ, например, такому как конкретные уровни, указанные в настоящем описании.
В случае предупреждения ВИЧ, вводимую парентерально дозу следует вычислять исходя из дозировки примерно от 0,2 мг/день до примерно 50 мг/день или от 0,5 мг/день до примерно 50 мг/день, или примерно от 1 мг/день до примерно 10 мг/день, или примерно от 2 мг/день до примерно 5 мг/день, например, исходя примерно из 3 мг/день. Это соответствует недельной дозе примерно от 1,5 мг до примерно 350 мг, в частности, примерно от 3,5 мг до примерно 350 мг, в частности, примерно от 7 мг до примерно 70 мг, или примерно от 14 мг до примерно 35 мг, например, примерно 35 мг, или это соответствует месячной дозе от 6 мг до примерно 3000 мг, в частности, примерно от 15 мг до примерно 1500 мг, более конкретно, примерно от 30 мг до примерно 300 мг, или примерно от 60 мг до примерно 150 мг, например, примерно 150 мг. Дозировки для других схем лечения можно легко вычислить, умножая дневную дозу на число дней между каждым введением.
В случае лечения, доза, вводимая парентерально, должна быть несколько выше, и ее следует вычислять, исходя из количества примерно от 1 мг/день до примерно 150 мг/день или примерно от 2 мг/день до примерно 100 мг/день, или примерно от 5 мг/день до примерно 50 мг/день, или примерно от 10 мг/день до примерно 25 мг/день, например, примерно 15 мг/день. Соответствующие недельные или месячные дозировки можно вычислить, как указано выше. Для предупреждения ВИЧ дозировки могут быть ниже, хотя можно использовать такие же дозировки, как для лечения.
Было обнаружено, что после введения уровень бреканавира в плазме крови остается более или менее стабильным, то есть меняется в ограниченных пределах. Было обнаружено, что уровень в плазме крови остается более или менее стабильным, или скорость выведения приблизительно остается нулевой в течение продолжительного периода времени. Под «стабильным» понимается состояние, в котором количество лекарственного средства, присутствующего в плазме крови субъекта, остается более или менее на том же уровне в течение продолжительного периода времени. Уровень бреканавира в плазме не падает ниже минимального уровня, при котором лекарственное средство является эффективным. Термин «остаетс