Неподвижная фаза для газовой хроматографии
Иллюстрации
Показать всеИзобретение относится к аналитической химии, конкретно к неподвижным фазам для разделения веществ методом капиллярной газовой хроматографии, и может быть использовано в анализе различных классов химических веществ. Описана неподвижная фаза для газовой хроматографии, представляющая собой функционализированный полимер, полученный путем окислительной обработки поли(1-триметилсилил-1-пропина) закисью азота. Техническим результатом является возможность разделять с высокой степенью селективности различные классы химических соединений, а температура и размер колонки оказывают сильное влияние на удерживание компонентов. 9 ил, 1 табл., 7 пр.
Реферат
Изобретение относится к аналитической химии, конкретно к неподвижным фазам для разделения веществ методом капиллярной газовой хроматографии, и может быть использовано в анализе различных классов химических веществ.
Для разделения смесей соединений неорганической и органической природы методом газовой хроматографии обычно используют органические неподвижные жидкие фазы различной полярности, например оксидипропионитрил, полиэтиленгликоль, полиэтиленгликольсукцинат и др. [SU 544913, G01N 31/08, 30.01.1977].
Однако такие фазы обладают недостаточно высокой селективностью к углеводородам с близкими температурами кипения, в частности к изомерам, либо, имея хорошую селективность, характеризуются большим временем удерживания. Для этих фаз селективность в гомологическом ряду полярных соединений практически отсутствует.
Известен способ и неподвижная фаза для анализа летучих органических соединений методом парофазной хроматографии. Неподвижная фаза в своем составе содержит водный раствор N-метилморфолин-N-оксида [SU 771543, G01N 31/08, 15.10.1980].
Недостатком известного способа является то, что он не позволяет достичь разделения смеси легких углеводородов, фреонов, серосодержащих соединений.
Известна неподвижная фаза и способ хроматографического анализа с ее применением [RU 2018822, G01N 30/50, 30.08.1994; SUPELCO Хроматография. Продукты для анализа и очистки. С. 214-215], которые позволяют во многих случаях реализовать высокую селективность при анализе полярных соединений различных классов.
Однако на этой фазе хроматографический анализ происходит в условиях программированного режима, характеризуется большими временами удерживания для большинства классов анализируемых соединений.
Наиболее близким техническим решением к предлагаемому изобретению являются неподвижная фаза на основе дивинилбензола и способ хроматографического анализа с ее применением [Другов Ю.С., Конопелько Л.А. Газохроматографический анализ газов. Москва: МОИМПЕКС, 1995 С. 278-283], которые также позволяют селективно разделять смеси полярных соединений.
Однако в некоторых случаях при анализе сложных смесей веществ, содержащих, например, углеводороды и серосодержащие соединения, структурные изомеры ароматических углеводородов, смеси фреонов проявляли недостаточную селективность и наблюдаемые пики разделяемых веществ имели асимметричный характер.
Задачей изобретения является создание неподвижной жидкой фазы, применение которой обеспечит высокую селективность разделения неорганических и органических соединений, включая полярные соединения.
Для решения этой задачи предложена неподвижная фаза для газовой хроматографии, основу которой, согласно изобретению, составляет функционализированный полимер, полученный путем окислительной обработки поли(1-триметилсилил-1-пропина) (ПТМСП) закисью азота.
Используемый образец ПТМСП представляет собой стеклообразный полимер из класса ненасыщенных полиацетиленов, подвергнутый окислительной обработке закисью азота. При такой обработке [RU 2230754, C08F 8/06, 20.06.2004] двойные C=C связи ненасыщенных полимеров вступают в реакцию с закисью азота с образованием карбонильных (альдегидных и кетонных) групп, которые существенно изменяют полярность ПТМСП, полученного в процессе обработки закисью азота. Изменение полярности полимера приводит к селективному разделению, в том числе полярных кислородсодержащих соединений.
Модифицирование ПТМСП осуществляют следующим образом.
В реактор из нержавеющей стали объемом 100 см3 загружают 0,15 г указанного полимера и 60 см3 толуола в качестве растворителя. Из реактора удаляют воздух путем откачки вакуумом и затем напускают закись азота до начального давления 15 атм. Реакцию ведут при 220°C в течение 96 ч.
Навеску функционализированного ПТМСП в количестве 0,1000 г помещают в стеклянную колбу, объемом 50 мл, добавляют 20 мл толуола и перемешивают на магнитной мешалке в течение 4 ч. Приготовленным раствором заполняют кварцевый капилляр, диаметром 0,32 мм и длиной от 15 до 30 м, толщина пленки полимера 0,5 мкм подсоединяют колонку к источнику инертного газа (аргон) и продувают инертным газом в течение часа при температуре 200°C. Затем температуру термостата повышают до 220°С. В этих условиях колонку кондиционируют аргоном в течение 4 ч.
Хроматографическую капиллярную колонку, на внутреннюю поверхность которой равномерно нанесена пленка окисленного ПТМСП, используют при анализе различных классов химических веществ. Температуру хроматографической колонки при анализе изменяют в интервале от 25 до 220°C.
Анализ реакционных смесей проводят с использованием трех типов детектирующих устройств: микро-детектор по теплопроводности (микро-ДТП), пламенно-ионизационный детектор (ПИД), квадрупольный масс-спектрометр (кв. МС).
Сущность изобретения иллюстрируется следующими примерами и фиг. 1-9.
Пример 1
Анализируют смесь газов предельных и непредельных углеводородов (C1-C4). Условия анализа: хроматографическая колонка 30 м × 0,32 мм × 0,5 мкм, заполненная неподвижной фазой описанным выше способом. Температура колонки 50°C, давление 0,45 атм, температура испарителя 200°C, температура детектора 220°C, объем пробы 10 мкл, газ-носитель - гелий, ПИД. Время анализа 10 мин.
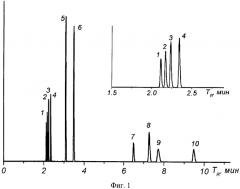
На фиг. 1 представлена полученная при указанных условиях хроматограмма разделения смеси газов предельных и непредельных углеводородов (C1-C4). На хроматограмме отчетливо видно разделение всех компонентов смеси: 1 - метан; 2 - ацетилен; 3 - этилен; 4 - этан; 5 - пропилен; 6 - пропан; 7 - 1,3-бутадиен; 8 - 1-бутен; 9 - изобутан; 10 - н-бутан. Следует отметить, что на этой неподвижной фазе наблюдается уникальный порядок выхода компонентов, когда ацетилен элюирует перед этиленом.
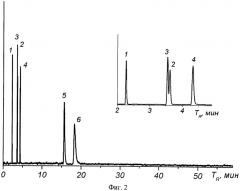
На фиг. 2 представлена полученная при указанных условиях хроматограмма разделения смеси газов предельных и непредельных углеводородов (C1-C2). Порядок выхода компонентов этого же состава и в аналогичных условиях, за исключением давления 0,62 атм, на капиллярной колонке с дивинилбензолом Rt-Q-BOND (прототипа) отличается, а именно, ацетилен элюирует после этилена, и время анализа только углеводородов C1-C2 составляет 20 мин, время выхода углеводородов C3-C4 значительно превышает 50 мин.
1 - метан; 2 - ацетилен; 3 - этилен; 4 - этан; 5 - пропилен; 6 - пропан.
Пример 2
Анализируют смесь ароматических углеводородов. Условия хроматографирования аналогичны условиям в примере 1, за исключением температуры хроматографической колонки, которая в данном примере составляет 160°C, объем пробы 0,2 мкл.
На фиг. 3 представлена полученная в этих условиях хроматограмма разделения, на которой: 11 - бензол; 12 - толуол; 13 - этилбензол; 14 - м-ксилол; 15 - п-ксилол; 16 - о-ксилол.
Пример 3
Анализируют смесь воздуха, диоксида углерода, серосодержащих компонентов и углеводородов C1-C2. Условия анализа: температура колонки 25°C, температура испарителя 150°C, температура детектора 200°C, объем пробы 10 мкл, газ-носитель - гелий, микро-ДТП.
На фиг. 4 представлена полученная при этих условиях хроматограмма разделения, на которой идентифицированы основные компоненты: 17 - воздух + метан; 18 - диоксид углерода; 2 - ацетилен; 3 - этилен; 19 - сероводород; 4 - этан; 20 - диоксид серы.
Пример 4
Анализу подвергают смесь тиофена и ароматических углеводородов. Начальная температура колонки составляет 120°C, выдержка 5 мин, затем программированный нагрев со скоростью 12°C/мин до 170°C, выдержка 2,5 мин; температура испарителя 240°C, температура детектора 240°C, объем пробы 0,5 мкл, газ-носитель - гелий, ПИД.
Следует отметить, что на этой неподвижной фазе наблюдается уникальный порядок выхода компонентов, когда тиофен элюирует перед бензолом. Время анализа составляет 10 мин, все пики на хроматограмме имеют гауссову форму.
На фиг. 5 представлена полученная при этих условиях хроматограмма разделения, на которой: 21 - тиофен; 11 - бензол; 12 - толуол; 22 - метилциклогексан; 23 - н-гептан.
На фиг. 6 представлена хроматограмма разделения смеси этого же состава и при следующих условиях хроматографирования: начальная температура колонки составляет 120°C, выдержка 3 мин, затем программированный нагрев со скоростью 12°C/мин до 200°C, выдержка 2,5 мин; температура испарителя 240°C, температура детектора 240°C, объем пробы 0,5 мкл, газ-носитель - гелий, ПИД, на капиллярной колонке с дивинилбензолом Rt-Q-BOND (прототип): 21+11 - тиофен + бензол; 12 - толуол; 22 - метилциклогексан; 23 - н-гептан. Порядок выхода компонентов отличается, а именно, тиофен и бензол выходят одним пиком, время анализа составило 23 мин, пики метилциклогексана, толуола широкие и несколько асимметричны.
Пример 5
Анализируют смесь хлорсодержащих соединений. Температура колонки 160°C, температура испарителя 200°C, температура детектора 220°C, объем пробы 0,2 мкл, газ-носитель - гелий, ПИД.
На фиг. 7 представлена хроматограмма смеси хлорсодержащих соединений:
24 - хлористый метилен, 25 - хлороформ, 26 - дихлорэтан, 27 - углерод четыреххлористый.
Пример 6
Анализу подвергают сложную смесь фреонов. Начальная температура колонки составляет 50°C, выдержка 5 мин, затем программированный нагрев со скоростью 12°C/мин до 200°C, выдержка 5 мин; температура испарителя 200°C, температура детектора 200°C, объем пробы 10 мкл, газ-носитель - гелий, квадрупольный МС.
На фиг. 8 представлена хроматограмма анализируемой смеси веществ, полученная при указанных условиях. Идентифицированные компоненты смеси: 17 - воздух + метан, 28 - фреон 125 (пентафторэтан), 29 - фреон 115 (пентафторхлорэтан), 30 - фреон 124+24а (тетрафторхлорэтан), 31 - фреон 133а (трифторхлорэтан), 32 - фреон 114а (тетрафтордихлорэтан), 33 - фреон 1112 (дифтордихлорэтилен), 34 - фреон 123+123а (трифтордихлорэтан), 35 - фреон 113 (трифтортрихлорэтан), 36 - фреон 1111 (фтортрихлорэтилен), 37 - фреон 122 (дифтортрихлорэтан), 38 - перхлорэтилен.
Пример 7
Анализу подвергают смесь спиртов. Температура колонки 130°C, температура испарителя 220°C, температура детектора 200°C, ПИД. Отмечена высокая селективность разделения и форма пиков симметрична (фиг. 9):
39 - этанол, 40 - 1-пропанол, 41 - изобутанол, 42 - 1-бутанол, 43 - изоамиловый, 44 - амиловый.
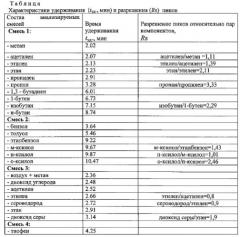
В таблице приведены полученные с применением предлагаемой неподвижной фазы данные по удерживанию величины разрешения пиков (Rs) соединений различной химической природы при различных температурах (25 -220°C) и разной длины хроматографической капиллярной колонки (15-30 м).
Величина разрешения капиллярной колонки (Rs) рассчитывается по формуле:
Rs=2×(tR2-tR1)/(w1+w2),
где tR2, tR1 - неисправленное время удерживания; w1, w2 - ширина пиков этих двух соединений при основании, измеренная между точками пересечения касательных к их сторонам с нулевой линией и выраженная в тех же единицах, что и числитель.
Как видно из представленной таблицы, предлагаемая неподвижная фаза позволяет разделять с высокой степенью селективности самые разные классы химических соединений. При этом температура и размер колонки оказывают сильное влияние на удерживание компонентов.
Неподвижная фаза для газовой хроматографии, характеризующаяся тем, что она представляет собой функционализированный полимер, полученный путем окислительной обработки поли(1-триметилсилил-1-пропина) закисью азота.