Пестицидная композиция
Иллюстрации
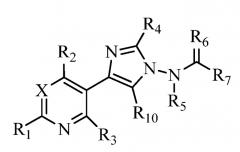
Показать всеИзобретение относится к сельскому хозяйству. Пестицидная композиция содержит соединение, соответствующее формуле один:
где X представляет собой CR8; R1 представляет собой Н; R2 представляет собой Н; R3 представляет собой Н; R4 представляет собой Н, F, Cl, Br, I или незамещенный C1-С6 алкил; R5 представляет собой Н, замещенный или незамещенный С1-С6 алкил, где указанный C1-C6 алкил замещен С3-С10 циклоалкилом; R6 представляет собой О; R7 представляет собой замещенный или незамещенный С1-С6 алкил, OR9, OR9S(O)nR9, где каждый указанный R7, который является замещенным, содержит один или несколько заместителей, выбранных из F, Cl, Br или I; R8 представляет собой Н, F, Cl, Br или I, R9 (каждый независимо) представляет собой незамещенный C1-С6 алкил; R10 представляет собой Н или незамещенный C1-С6 алкил; и n равен 0. Изобретение позволяет повысить эффективность композиции. 35 з.п. ф-лы, 4 табл.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Данное изобретение относится к области техники, связанной со способами получения соединений, которые могут применяться в качестве пестицидов (например, акарицидов, инсектицидов, моллюскоцидов и нематоцидов), таким соединениям и способам применения таких соединений для контроля сельскохозяйственных вредителей.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Каждый год сельскохозяйственные вредители вызывают миллионы человеческих смертей по всему миру. Кроме того, существует более десяти тысяч видов вредителей, которые причиняют значительный ущерб сельскому хозяйству. Ежегодные потери в сельском хозяйстве во всем мире составляют миллиарды долларов США.
Термиты вызывают повреждение всех видов частных и государственных строений. Во всем мире ущерб от термитов составляет миллиарды долларов США в год.
Сельскохозяйственные вредители поедают и делают непригодными для употребления находящиеся на хранении продукты питания. Ежегодные потери пищевых запасов во всем мире составляют миллиарды долларов США, но, что более важно, лишают людейнеобходимых продуктов питания.
Существует острая потребность в новых пестицидах. У некоторых сельскохозяйственных вредителей развивается резистентность к пестицидам, используемым в настоящее время. Сотни видов сельскохозяйственных вредителей резистентны к одному или нескольким пестицидам. Развитие резистентности к некоторым ранее разработанным пестицидам, таким как ДДТ, карбаматы и фосфаты, хорошо известно. Но резистентность развивается даже к некоторым более новым пестицидам.
Таким образом, вследствие множества причин, включая указанные выше, существует потребность в новых пестицидах.
ОПРЕДЕЛЕНИЯ
Примеры, приведенные в определениях, обычно не являются исчерпывающими и не должны рассматриваться как ограничивающие изобретение, описанное в данном документе. Следует представлять, что заместитель должен соответствовать правилам образования химической связи и пространственной совместимости относительно конкретного соединения, к которому он присоединен.
Термин «алкенил» означает ациклический, ненасыщенный (содержащий по меньшей мере одну углерод-углеродную двойную связь), разветвленный или неразветвленный заместитель, состоящий из атомов углерода и водорода, например винил, аллил, бутенил, пентенил и гексенил.
Термин «алкенилокси» означает алкенил, дополнительно включающий углерод-кислородную одинарную связь, например аллилокси, бутенилокси, пентенилокси, гексенилокси.
Термин «алкокси» означает алкил, дополнительно включающий углерод-кислородную одинарную связь, например метокси, этокси, пропокси, изопропокси, бутокси, изобутокси и трет-бутокси.
Термин «алкил» означает ациклический, насыщенный, разветвленный или неразветвленный заместитель, состоящий из атомов углерода и водорода, например метил, этил, (С3)алкил, который представляет собой н-пропил и изопропил, (C4)алкил, который представляет собой н-бутил, втор-бутил, изобутил и трет-бутил.
Термин «алкинил» означает ациклический, ненасыщенный (содержащий по меньшей мере одну углерод-углеродную тройную связь), разветвленный или неразветвленный заместитель, состоящий из атомов углерода и водорода, например этинил, пропаргил, бутинил и пентинил.
Термин «алкинилокси» означает алкинил, дополнительно включающий углерод-кислородную одинарную связь, например пентинилокси, гексинилокси, гептинилокси и октинилокси.
Термин «арил» означает циклический ароматический заместитель, состоящий из атомов водорода и углерода, например фенил, нафтил и бифенил.
Термин «(Сх-Cy)», где индексы «х» и «у» представляют собой целые числа, такие как 1, 2 или 3, означает интервал количества атомов углерода для заместителя - например (C1-C4) алкил означает метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, и трет-бутил, каждый в отдельности.
Термин «циклоалкенил» означает моноциклический или полициклический, ненасыщенный (содержащий по меньшей мере одну углерод-углеродную двойную связь) заместитель, состоящий из атомов углерода и водорода, например циклобутенил, циклопентенил, циклогексенил, норборненил, бицикло[2.2.2]октенил, тетрагидронафтил, гексагидронафтил и октагидронафтил.
Термин «циклоалкенилокси» означает циклоалкенил, дополнительно включающий углерод-кислородную одинарной связь, например циклобутенилокси, циклопентенилокси, норборненилокси и бицикло[2.2.2]октенилокси.
Термин «циклоалкил» означает моноциклический или полициклический насыщенный заместитель, состоящий из атомов углерода и водорода, например циклопропил, циклобутил, циклопентил, норборнил, бицикло[2.2.2]октил и декагидронфатил.
Термин «циклоалкокси» означает циклоалкил, дополнительно включающий углерод-кислородную одинарную связь, например циклопропилокси, цикдлобутилокси, циклопентилокси, норборнилокси и бицикло[2.2.2]октилокси.
Термин «галоген» означает атом фтора, хлора, брома и йода.
Термин «галогеналкокси» означает алкокси, дополнительно включающий от одного до максимально возможного числа одинаковых или разных атомов галогенов, например фторметокси, трифторметокси, 2,2-дифторпропокси, хлорметокси, трихлорметокси, 1,1,2,2-тетрафторэтокси и пентафторэтокси.
Термин «галогеналкил» означает алкил, дополнительно включающий от одного до максимально возможного числа одинаковых или разные атомов галогенов, например фторметил, трифторметил, 2,2-дифторпропил, хлорметил, трихлорметил, 1,1,2,2-тетрафторэтил.
Термин «гетероциклил» означает циклический заместитель, который может быть полностью насыщенным, частично ненасыщенным или полностью ненасыщенным, где циклическая структура содержит по меньшей мере один атом углерода и по меньшей мере один гетероатом, причем указанный гетероатом представляет собой атом азота, серы или кислорода. В случае, когда гетероатом представляет собой атом серы, данный атом может быть и в других состояниях окисления, таких как сульфоксид и сульфон. Примеры ароматических гетероциклов включают, но без ограничения указанным перечнем, бензофуранил, бензоизотиазолил, бензизоксазолил, бензоксазолил, бензотиенил, бензотиазолил, циннолинил, фуранил, имидазолил, индазолил, индолил, изоиндолил, изохинолинил, изотиазолил, изоксазолил, оксадиазолил, оксазолинил, оксазолил, фталазинил, пиразинил, пиразолинил, пиразолил, пиридазинил, пиридил, пиримидинил, пирролил, хиназолинил, хинолинил, хиноксалинил, тетразолил, тиазолинил, тиазолил, тиенил, триазинил и триазолил. Примерами полностью насыщенных гетероциклилов включают, но не без ограничения указанным перечнем, пиперазинил, пиперидинил, морфолинил, пирролидинил, оксетанил, тетрагидрофуранил, тетрагидротиенил и тетрагидропиранил. Примеры частично ненасыщенных гетероциклилов включают, но без ограничения представленным перечнем, 1,2,3,4-тетрагидрохинолинил, 4,5-дигидрооксазолил, 4,5-дигидро-1H-пиразолил, 4,5-дигидро-изоксазолил и 2,3-дигидро-[1,3,4]-оксадиазолил. Дополнительные примеры включают следующие
.
ПОДРОБНОЕ ОПИСАНИЕ
Данное изобретение раскрывает соединения представленной ниже формулы («формулы один»):
Формула один
где
(a) X представляет собой N или CR8;
(b) R1 представляет собой H, F, Cl, Br, I, CN, NO2, замещенный или незамещенный C1-C6 алкил, замещенный или незамещенный C2-C6 алкенил, замещенный или незамещенный C1-C6 алкокси, замещенный или незамещенный C2-C6 алкенилокси, замещенный или незамещенный C3-C10 циклоалкил, замещенный или незамещенный C3-C10 циклоалкенил, замещенный или незамещенный C6-C20 арил, замещенный или незамещенный C1-C20 гетероциклил, OR9, C(=X1)R9, C(=X1)OR9, C(=X1)N(R9)2, N(R9)2, N(R9)C(=X1)R9, SR9, S(О)nOR9 или R9S(О)nR9,
где каждый указанный R1, который является замещенным, содержит один или несколько заместителей, выбранных из F, Cl, Br, I, CN, NO2, C1-C6 алкила, C2-C6 алкенила, C1-C6 галогеналкила, C2-C6 галогеналкенила, C1-C6 галогеналкилокси, C2-C6 галогеналкенилокси, C3-C10 циклоалкила, C3-C10 циклоалкенила, C3-C10 галогенциклоалкила, C3-C10 галогенциклоалкенила, OR9, S(О)nOR9, C6-C20 арила или C1-C20 гетероциклила (каждый из которых может быть замещенным, может быть необязательно замещенным R9);
(c) R2 представляет собой H, F, Cl, Br, I, CN, NO2, замещенный или незамещенный C1-C6 алкил, замещенный или незамещенный C2-C6 алкенил, замещенный или незамещенный C1-C6 алкокси, замещенный или незамещенный C2-C6 алкенилокси, замещенный или незамещенный C3-C10 циклоалкил, замещенный или незамещенный C3-C10 циклоалкенил, замещенный или незамещенный C6-C20 арил, замещенный или незамещенный C1-C20 гетероциклил, OR9, C(=X1)R9, C(=X1)OR9, C(=X1)N(R9)2, N(R9)2, N(R9)C(=X1)R9, SR9, S(О)nOR9 или R9S(О)nR9,
где каждый указанный R2, который является замещенным, содержит один или несколько заместителей, выбранных из F, Cl, Br, I, CN, NO2, C1-C6 алкила, C2-C6 алкенила, C1-C6 галогеналкила, C2-C6 галогеналкенила, C1-C6 галогеналкилокси, C2-C6 галогеналкенилокси, C3-C10 циклоалкила, C3-C10 циклоалкенила, C3-C10 галогенциклоалкила, C3-C10 галогенциклоалкенила, OR9, S(О)nOR9, C6-C20 арила или C1-C20 гетероциклила (каждый из которых может быть замещенным, может быть необязательно замещенным R9);
(d) R3 представляет собой H, F, Cl, Br, I, CN, NO2, замещенный или незамещенный C1-C6 алкил, замещенный или незамещенный C2-C6 алкенил, замещенный или незамещенный C1-C6 алкокси, замещенный или незамещенный C2-C6 алкенилокси, замещенный или незамещенный C3-C10 циклоалкил, замещенный или незамещенный C3-C10 циклоалкенил, замещенный или незамещенный C6-C20 арил, замещенный или незамещенный C6-C20 гетероциклил, OR9, C(=X1)R9, C(=X1)OR9, C(=X1)N(R9)2, N(R9)2, N(R9)C(=X1)R9, SR9, S(О)nOR9 или R9S(О)nR9,
где каждый указанный R3, который является замещенным, содержит один или несколько заместителей, выбранных из F, Cl, Br, I, CN, NO2, C1-C6 алкила, C2-C6 алкенила, C1-C6 галогеналкила, C2-C6 галогеналкенила, C1-C6 галогеналкилокси, C2-C6 галогеналкенилокси, C3-C10 циклоалкила, C3-C10 циклоалкенила, C3-C10 галогенциклоалкила, C3-C10 галогенциклоалкенила, OR9, S(О)nOR9, C6-C20 арила или C1-C20 гетероциклила (каждый из которых может быть замещенным, может быть необязательно замещенным R9);
(e) R4 представляет собой H, F, Cl, Br, I, CN, NO2, замещенный или незамещенный C1-C6 алкил, замещенный или незамещенный C2-C6 алкенил, замещенный или незамещенный C1-C6 алкокси, замещенный или незамещенный C2-C6 алкенилокси, замещенный или незамещенный C3-C10 циклоалкил, замещенный или незамещенный C3-C10 циклоалкенил, замещенный или незамещенный C6-C20 арил, замещенный или незамещенный C1-C20 гетероциклил, OR9, C(=X1)R9, C(=X1)OR9, C(=X1)N(R9)2, N(R9)2, N(R9)C(=X1)R9, SR9, S(O)nOR9 или R9S(O)nR9,
где каждый указанный R4, который является замещенным, содержит один или несколько заместителей, выбранных из F, Cl, Br, I, CN, NO2, C1-C6 алкила, C2-C6 алкенила, C1-C6 галогеналкила, C2-C6 галогеналкенила, C1-C6 галогеналкилокси, C2-C6 галогеналкенилокси, C3-C10 циклоалкила, C3-C10 циклоалкенила, C3-C10 галогенциклоалкила, C3-C10 галогенциклоалкенила, OR9, S(О)nOR9, C6-C20 арила или C1-C20 гетероциклила (каждый из которых может быть замещенным, может быть необязательно замещенным R9);
(f) R5 представляет собой H, замещенный или незамещенный C1-C6 алкил, замещенный или незамещенный C2-C6 алкенил, замещенный или незамещенный C1-C6 алкокси, замещенный или незамещенный C2-C6 алкенилокси, замещенный или незамещенный C3-C10 циклоалкил, замещенный или незамещенный C3-C10 циклоалкенил, замещенный или незамещенный C6-C20 арил, замещенный или незамещенный C1-C20 гетероциклил, OR9, C(=X1)R9, C(=X1)OR9, C(=X1)N(R9)2, N(R9)2, N(R9)C(=X1)R9, SR9, S(O)nOR9, R9S(O)nR9, C1-C6 алкил-C6-C20 арил (где алкил и арил независимо могут быть замещенными или незамещенными), C(=X2)R9, C(=X1)X2R9, R9X2C(=X1)R9, R9X2R9, C(=О)(C1-C6 алкил)S(О)n(C1-C6 алкил), C(=О)(C1-C6 алкил)C(=О)О(C1-C6алкил), (C1-C6 алкил)OC(=О)(C6-C20 арил), (C1-C6 алкил)OC(=О)(C1-C6 алкил), C1-C6 алкил-(C3-C10 циклогалогеналкил) или (C1-C6 алкенил)C(=О)О(C1-C6 алкил) или R9X2C(=X1)X2R9;
где каждый указанный R5, который является замещенным, содержит один или несколько заместителей, выбранных из F, Cl, Br, I, CN, NO2, C1-C6 алкила, C2-C6 алкенила, C1-C6 галогеналкила, C2-C6 галогеналкенила, C1-C6 галогеналкилокси, C2-C6 галогеналкенилокси, C3-C10 циклоалкила, C3-C10 циклоалкенила, C3-C10 галогенциклоалкила, C3-C10 галогенциклоалкенила, OR9, S(О)nOR9, C6-C20 арила или C1-C20 гетероциклила, R9 арила (каждый из которых может быть замещенным, может быть необязательно замещенным R9),
необязательно R5 и R7 могут объединяться в циклическую структуру, где необязательно такая структура, полученная из соединенных R5 и R7, может содержать один или несколько гетероатомов, выбранных из атомов O, S или N;
(g) R6 представляет собой O, S, NR9 или NOR9;
(h) R7 представляет собой замещенный или незамещенный C1-C6 алкил, замещенный или незамещенный C2-C6 алкенил, замещенный или незамещенный C1-C6 алкокси, замещенный или незамещенный C2-C6 алкенилокси, замещенный или незамещенный C3-C10 циклоалкил, замещенный или незамещенный C3-C10 циклоалкенил, замещенный или незамещенный C6-C20 арил, замещенный или незамещенный C1-C20 гетероциклил, OR9, OR9S(О)nR9, C(=X1)R9, C(=X1)OR9, R9C(=X1)OR9, R9X2C(=X1)R9X2R9, C(=X1)N(R9)2, N(R9)2, N(R9)(R9S(О)nR9), N(R9)C(=X1)R9, SR9, S(О)nOR9, R9S(О)nR9, C1-C6 алкил-ОС(=О)-C1-C6 алкил, OC1-C6 алкил-C1-C20 гетероциклил, C1-C6алкил-C1-C20 гетероциклил, C1-C6 алкилS(=N-CN)(C1-C6алкил), C1-C6алкилS(О)(=N-CN)(C1-C6алкил), C1-C6алкилS(О)n(C1-C6 алкил-C1-C20 гетероциклил), C1-C6 алкил-S(O)(=N-CN)(C1-C6 алкил-C1-C20 гетероциклил), C1-C6 алкил-NH(C(=O)OC1-C6 алкил), C1-C6 алкил-С(=О)OC1-C6 алкил, C1-C6 алкил(C6-C20арил)NH(C(=О)OC1-C6алкил), C1-C6 алкил(S-C1-C6 алкил)NH(C(=О)OC1-C6алкил), C1-C6алкил(S-C1-C6алкил-C6-C20арил)NH(C(=О)OC1-C6алкил), C1-C6 алкил(NHC(=О)OC1-C6алкил-C6-C20 арил)NH(C(=О)OC1-C6 алкил), C1-C6 алкил(OC1-C6 алкил-C6-C20 арил)NH(C(=О)OC1-C6алкил), C1-C6 алкил-N(C1-C6алкил)(C(=О)OC1-C6 алкил), C1-C6 алкилNH(C1-C6 алкил), C6-C20 арилSC1-C6 галогеналкил, C1-C6алкил-N(C1-C6 алкил)(C(=О)C1-C6 алкилC6-C20 арил), C1-C6 алкил-N(C1-C6 алкил)(C1-C6алкил), C1-C6 алкил-N(C1-C6 алкил)(S(О)nC1-C6 алкил), C1-C6 алкилN(C1-C6 алкил)(S(О)nC1-C6 алкенил-C6-C20 арил), C1-C6 алкил-N(C1-C6 алкил)(C(=О)-C1-C20 гетероциклил), C1-C6 алкил-N(C1-C6 алкил)(C(=О)OC1-C6 алкил-C6-C20арил), NH(C1-C6 алкилS(О)nC1-C6 алкил), NH(C1-C6 алкилS(О)nC6-C20 арил), C1-C6 алкил(S(О)nC1-C6 алкил)(C(=О)C1-C6 алкилS(О)n(C1-C6 алкил) или R9S(О)n(NZ)R9,
где каждый указанный R7, который является замещенным, содержит один или несколько заместителей, выбранных из F, Cl, Br, I, CN, NO2, C1-C6 алкила, C2-C6 алкенила, C1-C6 галогеналкила, C2-C6 галогеналкенила, C1-C6 галогеналкилокси, C2-C6 галогеналкенилокси, C3-C10 циклоалкила, C3-C10 циклоалкенила, C3-C10 галогенциклоалкила, C3-C10 галогенциклоалкенила, OR9, S(О)nOR9, C6-C20 арила или C1-C20 гетероциклила (каждый из которых может быть замещенным, может быть необязательно замещенным R9), C(=X1)R9, C(=X1)OR9, C(=X1)N(R9)2, =X2, N(R9)2, S(=X2)nR9, R9S(О)nR9, S(О)nN(R9)2;
(i) R8 представляет собой H, F, Cl, Br, I, CN, NO2, замещенный или незамещенный C1-C6 алкил, замещенный или незамещенный C2-C6 алкенил, замещенный или незамещенный C1-C6 алкокси, замещенный или незамещенный C2-C6 алкенилокси, замещенный или незамещенный C3-C10 циклоалкил, замещенный или незамещенный C3-C10 циклоалкенил, замещенный или незамещенный C6-C20 арил, замещенный или незамещенный C1-C20 гетероциклил, OR9, C(=X1)R9, C(=X1)OR9, C(=X1)N(R9)2, N(R9)2, N(R9)C(=X1)R9, SR9, S(О)nR9, S(О)nOR9 или R9S(О)nR9,
где каждый указанный R8, который является замещенным, содержит один или несколько заместителей, выбранных из F, Cl, Br, I, CN, NO2, C1-C6 алкила, C2-C6 алкенила, C1-C6 галогеналкила, C2-C6 галогеналкенила, C1-C6 галогеналкилокси, C2-C6 галогеналкенилокси, C3-C10 циклоалкила, C3-C10 циклоалкенила, C3-C10 галогенциклоалкила, C3-C10 галогенциклоалкенила, OR9, S(О)nOR9, C6-C20 арила или C1-C20 гетероциклила (каждый из которых может быть замещенным, может быть необязательно замещенным R9);
(j) R9 (каждый независимо) представляет собой H, CN, замещенный или незамещенный C1-C6 алкил, замещенный или незамещенный C2-C6 алкенил, замещенный или незамещенный C1-C6 алкокси, замещенный или незамещенный C2-C6 алкенилокси, замещенный или незамещенный C3-C10 циклоалкил, замещенный или незамещенный C3-C10 циклоалкенил, замещенный или незамещенный C6-C20 арил, замещенный или незамещенный C1-C20 гетероциклил, S(О)nC1-C6 алкил, N(C1-C6алкил)2,
где каждый указанный R9, который является замещенным, содержит один или несколько заместителей, выбранных из F, Cl, Br, I, CN, NO2, C1-C6 алкила, C2-C6 алкенила, C1-C6 галогеналкила, C2-C6 галогеналкенила, C1-C6 галогеналкилокси, C2-C6 галогеналкенилокси, C3-C10 циклоалкила, C3-C10 циклоалкенила, C3-C10 галогенциклоалкила, C3-C10 галогенциклоалкенила, OC1-C6 алкила, OC1-C6 галогеналкила, S(О)n-C1-C6 алкила, S(О)nOC1-C6 алкила, C6-C20 арила или C1-C20 гетероциклила;
(k) R10 представляет собой H, F, Cl, Br, I, CN, NO2, замещенный или незамещенный C1-C6 алкил, замещенный или незамещенный C2-C6 алкенил, замещенный или незамещенный C1-C6 алкокси, замещенный или незамещенный C2-C6 алкенилокси, замещенный или незамещенный C3-C10 циклоалкил, замещенный или незамещенный C3-C10 циклоалкенил, замещенный или незамещенный C6-C20 арил, OR9, C(=X1)R9, C(=X1)OR9, C(=X1)N(R9)2, N(R9)2, N(R9)C(=X1)R9, SR9, S(О)nOR9 или R9S(О)nR9,
где каждый указанный R10, который является замещенным, содержит один или несколько заместителей, выбранных из F, Cl, Br, I, CN, NO2, C1-C6 алкила, C2-C6 алкенила, C1-C6 галогеналкила, C2-C6 галогеналкенила, C1-C6 галогеналкилокси, C2-C6 галогеналкенилокси, C3-C10 циклоалкила, C3-C10 циклоалкенила, C3-C10 галогенциклоалкила, C3-C10 галогенциклоалкенила, OR9, S(О)nOR9 или C6-C20 арила (каждый из которых может быть замещенным, может быть необязательно замещенным R9);
(l) n (каждый независимо) равен 0, 1, или 2;
(m) X1 (каждый независимо) представляет собой O или S;
(n) X2 (каждый независимо) представляет собой O, S, =NR9 или =NOR9; и
(о) Z представляет собой CN, NO2, C1-C6 алкил(R9), C(=X1)N(R9)2.
Формула один и ее подразделы от (а) до (о) далее в описании определены как «Вариант осуществления А1».
В другом варианте осуществления данного соединения X представляет собой CR8.
В еще одном варианте осуществления данного соединения R1 представляет собой H.
В еще одном варианте осуществления данного соединения R2 представляет собой H.
В еще одном варианте осуществления данного соединения R3 представляет собой H.
В еще одном варианте осуществления данного соединения R4 представляет собой атом галогена или незамещенный C1-C6 алкил.
В еще одном варианте осуществления данного соединения R4 представляет собой атом F, Cl или незамещенный C1-C2 алкил.
В еще одном варианте осуществления данного соединения R4 представляет собой атом Cl или CH3.
В еще одном варианте осуществления данного соединения R5 представляет собой H, замещенный или незамещенный C1-C6 алкил.
В еще одном варианте осуществления данного соединения R5 представляет собой замещенный C1-C6 алкил, который замещен C3-C10 циклоалкилом.
В еще одном варианте осуществления данного соединения R5 представляет собой H, CH3, CH2-циклопропил или CH2CH3.
В еще одном варианте осуществления данного соединения R6 представляет собой O.
В еще одном варианте осуществления данного соединения R7 представляет собой замещенный или незамещенный C1-C6 алкил, OR9 или R9S(О)nR9.
В еще одном варианте осуществления данного соединения R7 представляет собой замещенный C1-C6 алкил, где указанный заместитель представляет собой один или несколько атомов галогенов.
В еще одном варианте осуществления данного соединения R7 представляет собой замещенный C1-C6 алкил, где указанный заместитель представляет собой один или несколько атомов F или Cl или их сочетание.
В еще одном варианте осуществления данного соединения R7 представляет собой замещенный C1-C6 алкил, где указанный заместитель представляет собой один или несколько атомов F.
В еще одном варианте осуществления данного соединения R7 представляет собой CH2CF3.
В еще одном варианте осуществления данного соединения R7 представляет собой незамещенный C1-C6 алкил.
В еще одном варианте осуществления данного соединения R7 представляет собой CH(CH3)2, CH3, C(CH3)3 или CH2CH2CH2CH3.
В еще одном варианте осуществления данного соединения R7 представляет собой OR9.
В еще одном варианте осуществления данного соединения R7 представляет собой О(незамещенный C1-C6 алкил).
В еще одном варианте осуществления данного соединения R7 представляет собой OC(CH3)3.
В еще одном варианте осуществления данного соединения R7 представляет собой R9S(О)nR9.
В еще одном варианте осуществления данного соединения R7 представляет собой (незамещенный C1-C6 алкил)S(незамещенный C1-C6 алкил).
В еще одном варианте осуществления данного соединения R7 представляет собой CH2CH(CH3)SCH3, CH2CH2SCH3, CH(CH3)2SCH3 или CH(CH3)CH2SCH3.
В еще одном варианте осуществления данного соединения R8 представляет собой H или атом галогена.
В другом варианте осуществления данного соединения R8 представляет собой H, атом F или Cl.
В еще одном варианте осуществления данного соединения R8 представляет собой H или атом F.
В еще одном варианте осуществления данного соединения R9 представляет собой незамещенный C1-C6 алкил.
В еще одном варианте осуществления данного соединения R10 представляет собой H или незамещенный C1-C6 алкил.
В еще одном варианте осуществления данного соединения R10 представляет собой H или CH3.
В еще одном варианте осуществления данного соединения n равно 0.
Подразумеваются также комбинации этих вариантов осуществления.
Молекулярная масса соединений формулы один будет обычно составлять от примерно 100 дальтон до примерно 1200 дальтон. Однако обычно предпочтительна молекулярная масса от примерно 120 дальтон до примерно 900 дальтон, еще более предпочтительна молекулярная масса от примерно 140 дальтон до примерно 600 дальтон.
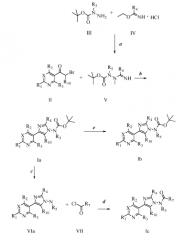
Представленная далее схема иллюстрирует подход к получению 2-метилимидазолиламинов. На стадии а схемы I обработка соединений формулы III гидрохлоридами этилацетамидата формулы IV, где R5 принимает значения, определенные в варианте осуществления А1, и R4 представляет собой метил, приводит к получению соответствующих ацетамидинов формулы V. На стадии b схемы I α-бромкетоны формулы II, где R1, R2, R3, R10 и X принимают значения, определенные в варианте осуществления A1, могут подвергаться обработке ацетамидинами формулы V в присутствии органического основания, такого как триэтиламин, в полярном протонном растворителе, таком как этиловый спирт, с получением N-Вос-аминоимидазолов формулы Ia. Когда R5=H, карбаматы формулы Ia, где R1, R2, R3, R4, R10 и X принимают значения, определенные в варианте осуществления A1, могут подвергаться алкилированию в присутствии основания, такого как гидрид натрия, и алкилгалогенида, такого как йодметан, в апротонном полярном растворителе, таком как N,N-диметилформамид, с получением соединений формулы Ib, как показано на стадии е схемы I. Снятие защиты, представленной в форме сложных трет-бутиловых эфиров карбаминовой кислоты формулы Ia может выполняться как показано на стадии с схемы I с помощью трифторуксусной кислоты (ТФУК) в полярном апротонном растворителе, таком как дихлорметан (ДХМ), с получением аминоимидазолов формулы VIa, где R1, R2, R3, R4, R10, R5 и X принимают значения, определенные в варианте осуществления A1. На стадии d схемы I соединения формулы VIa могут подвергаться обработке хлорангидридом формулы VII, где R7 принимает значения, определенные в варианте осуществления А1, в присутствии как органического основания, такого как N,N-диметиламинопиридин (DMAP), так и неорганического основания, такого как карбонат калия, в полярном апротонном растворителе, таком как 1,2-дихлорэтан (ДХЭ), с получением соединения формулы Ic.
Схема I
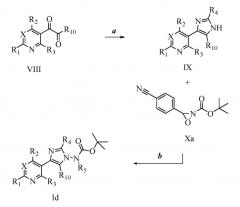
Другой подход к получению имидазолиламинов представлен на схеме II. Дионы формулы VIII, где R1, R2, R3, R10 и X принимают значения, определенные в варианте осуществления А1, могут подвергаться обработке альдегидом, таким как ацетальдегид, источником аммиака, каким как ацетат аммония, в присутствии катализатора, такого как хлорид индия(III), в протонном растворителе, таком как метанол, с получением соединений формулы IX. Соединения формулы IX, где R1, R2, R3, R4, R10 и X принимают значения, определенные в варианте осуществления А1, могут подвергаться обработке основанием, таким как гидрид натрия, в растворителе, таком как ТГФ, с добавлением оксазиридинов формулы Xa для получения соединений формулы Id, где R5 представляет собой H.
Схема II
Еще один подход к получению имидазолиламинов представлен на схеме III. Замещенные 2-аминоимидазолины формулы XI были получены в соответствии с общей методикой, описанной в публикации Li et al. J. Med. Chem., 2010, 53, 2409. Обработка соединений формулы XI, где R1, R2, R3, R10 и X принимают значения, определенные в варианте осуществления А1, в условиях Сандмейера (Sandmeyer) приводит к получению соединений формулы XII, где R4 представляет собой атом галогена, как показано в стадии a схемы III. Гидразоны формулы XII могут подвергаться превращению в соответствующие амины формулы VIb, где R5 представляет собой Н, при обработке гидразином в полярном протонной растворителе, таком как 2-метоксиэтанол, как показано на стадии b.
Схема III
Еще один подход к получению имидазолиламинов представлен на схеме IV. Имидазолы формулы XIII, где R4 и R10 принимают значения, определенные в варианте осуществления А1 и Q представляет собой атом галогена (например, брома), могут подвергаться обработке основанием, таким как гидрид натрия, в полярном апротонном растворителе, таком как тетрагидрофуран, и агентом аминирования, таким как оксазиридин формулы Xb, с получением соединений формулы XIVa, как показано в стадии а схемы IV. Карбаматы формулы XIVa могут подвергаться алкилированию в присутствии основания, такого как гидрид натрия, и алкилгалогенида, такого как йодэтан, в полярном апротонном растворителе, таком как N,N-диметилформамид, с получением соединений формулы XIVb, где R4, R5 и R10 принимают значения, определенные в варианте осуществления А1, могут подвергаться взаимодействию посредством реакции связывания с бороновой кислотой формулы XV в условиях Сузуки, где R1, R2 и R3 принимают значения, определенные в варианте осуществления А1, с получением гетероцикл-связанного имидазола формулы Ie, как показано в стадии с. Когда R4=Н, соединения формулы Ie могут подвергаться галогенированию в присутствии основания, такого как н-бутиллитий, в полярном апротонном растворителе, таком как тетрагидрофуран, с электрофильным источником галогена, таким как гексахлорэтан, для получения 2-галогенимидазолов формулы If, где R4 представляет собой атом галогена и R1, R2, R3, R5, R10 и Х принимают значения, определенные в варианте осуществления А1, как показано в стадии d.
Схема IV
ПРИМЕРЫ
Представленные далее примеры предназначены для иллюстративных целей и не должны рассматриваться как ограничение раскрытого в данном документе изобретения вариантами осуществления изобретения, описанными в данных примерах.
Исходные материалы, реагенты и растворители, которые были получены из коммерческих источников, использовались без дополнительной очистки. Безводные растворители приобретены как Sure/Seal™ от Aldrich и использовались без дополнительной обработки. Температуры плавления получены на капиллярном аппарате определения температуры плавления Thomas Hoover Unimelt или с помощью системы OptiMelt Automated Melting Point System от Stanford Research Systems и не корректировались. Соединениям даны их известные названия, полученные в соответствии с программами в ISIS Draw, ChemDraw или ACD Name Pro. Если программа не способна назвать соединение, название соединения было составлено с использованием стандартных правил номенклатуры. Все ЯМР представлены в м.д. (δ) и записаны при 300, 400 или 600 МГц, если не заявлено другого.
Пример 1, стадия 1: Получение трет-бутилового эфира N'-(1-иминоэтил)-N-метил-гидразинкарбоновой кислоты
Раствор трет-бутил-1-метилгидразинкарбоксилата (10,0 г, 68,4 ммоль), гидрохлорида этилацетимидата (42,1 г, 342 ммоль) и карбоната калия (94,4 г, 684 ммоль) в ДМФА (150 мл) нагревают до 105°C и выдерживают при указанной температуре в течение 5 часов. Реакционную смесь охлаждают до 0°C, образовавшийся осадок собирают вакуумной фильтрацией и снова суспендируют в H2O (100 мл). Смесь энергично перемешивают в течение 30 минут, образовавшийся осадок собирают и сушат в вакуумной печи при 45°C в течение ночи, получая указанное в заголовке соединение в виде твердого белого вещества (7,56 г, 59,0%): т.пл. 187-189°C; 1H ЯМР (400 МГц, ДМСО-d6) δ 6,28 (ушир. с, 1H), 2,77 (с, 3H), 1,64 (с, 3H), 1,36 (с, 9H).
Пример 1, стадия 2: Получение трет-бутилового эфира метил-(2-метил-4-пиридин-3-илимидазол-1-ил)карбаминовой кислоты (соединение 3)
К раствору трет-бутилового эфира N'-(1-иминоэтил)-N-метил-гидразинкарбоновой кислоты (5,00 г, 26,7 ммоль) и триэтиламина (9,30 мл, 66,8 ммоль) в EtOH (100 мл) небольшими порциями добавляют гидробромид 2-бром-1-пиридин-3-илэтанона (8,99 г, 32,0 ммоль). Смесь нагревают до 80°C и выдерживают при указанной температуре в течение 3 часов, после чего растворитель удаляют при пониженном давлении и остаток очищают хроматографией (силикагель, ДХМ:MeOH 10:1), получая указанное в заголовке соединение в виде масла оранжевого цвета (1,55 г, 20,1 %): 1H ЯМР (400 МГц, CDCl3) δ 8,92 (д, J=2,4 Гц, 1H), 8,43 (дд, J=4,9, 1,4 Гц, 1H), 8,03 (дт, J=8,3, 1,6 Гц, 1H), 7,28 (дд, J=7,7, 4,8 Гц, 1H), 7,21 (с, 1H), 3,38 (с, 3H), 2,36 (с, 3H), 1,43 (с, 9H); МС(ESI) m/z 289 [(M+H)]+.
Пример 1, стадия 3: Получение метил-(2-метил-4-пиридин-3-илимидазол-1-ил)амина
Способ A:
Раствор трет-бутилового эфира метил-(2-метил-4-пиридин-3-илимидазол-1-ил)карбаминовой кислоты (1,50 г, 5,20 ммоль) и трифторуксусной кислоты (0,40 мл, 5,20 ммоль) в ДХМ (5 мл) перемешивают при температуре окружающей среды в течение 3 часов. Растворитель удаляют при пониженном давлении, остаток снова суспендируют в ДХМ (10 мл) и добавляют триэтиламин (1,45 мл, 10,4 ммоль). Смесь перемешивают в течение 10 минут, затем растворитель удаляют и остаток очищают хроматографией (силикагель, ДХМ:MeOH, 10:1), получая неразделимую смесь указанного в заголовке соединения и его триэтиламмониевых солей (822 мг). Смесь используют в последующих реакциях без дополнительной очистки.
Способ B:
Раствор трет-бутилметил-(2-метил-4-(пиридин-3-ил)-1H-имидазол-1-ил)карбамата (2,7 г, 9,4 ммоль) в дихлорметане (50 мл) обрабатывают HCl в диоксане (4M, 20 мл). Смесь перемешивают в течение ночи при комнатной температуре. Осадок удаляют фильтрацией, получая указанное в заголовке соединение в виде твердого вещества коричневого цвета (1,15 г, 54,5%): 1H ЯМР (300 МГц, ДМСО-d6) δ 9,41-9,32 (м, 1H), 8,82-8,56 (м, 3H), 7,97-7,89 (м, 1H), 2,85 (с, 3H), 2,67 (д, J=3,0 Гц, 3H); МС(ESI) m/z 189 [(M+H)]+.
N-Этил-2-метил-4-(пиридин-3-ил)-1H-имидазол-1-амин получают в соотвествии с методикой, описанной в примере 1 (стадия 3, способ B): 1H ЯМР (300 МГц, ДМСО-d6) δ 9,32 (с, 1H), 8,76-8,69 (м, 2H), 8,57-8,46 (м, 1H), 7,81 (с, 1H), 3,12-3,03 (м, 2H), 2,63 (с, 3H), 1,06 (т, 3H, J=7,2 Гц); МС(ESI) m/z 203 [(M+H)]+.
N-(Циклопропилметил)-2-метил-4-(пиридин-3-ил)-1H-имидазол-1-амин получают в соотвествии с методикой, описанной в примере 1 (стадия 3, способ B): 1H ЯМР (300 МГц, ДМСО-d6) δ 9,26 (с, 1H), 8,74-8,72 (м, 1H), 8,67-8,59 (м, 1H), 8,51-8,46 (м, 1H), 7,81 (с, 1H), 2,95 (д, 2H, J=7,2 Гц), 2,66 (с, 3H), 0,93-0,86 (м, 1H), 0,46-0,43 (м, 2H), 0,07-0,06 (м, 2H); МС(ESI) m/z 229 [(M+H)]+.
4-(5-Фторпиридин-3-ил)-N,2-диметил-1H-имидазол-1-амин получают в соотвествии с методикой, описанной в примере 1 (стадия 3, способ B): 1H ЯМР (300 МГц, CD3OD) δ 9,05 (с, 1H), 8,84 (с, 1H), 8,47-8,44 (м, 2H), 2,97 (с, 3H), 2,74 (с, 3H); МС(ESI) m/z 207 [(M+H)]+.
N-Этил-4-(5-фторпиридин-3-ил)-2-метил-1H-имидазол-1-амин получают в соотвествии с методикой, описанной в примере 1 (стадия 3, способ B): 1H ЯМР (300 МГц, CD3OD) δ 8,99 (с, 1H), 8,80 (с, 1H), 8,41-8,35 (м, 2H), 3,26 (кв., J=7,2 Гц, 2H), 2,74 (с, 3H), 1,19 (т, 3H, J=7,2 Гц); МС(ESI) m/z 221 [(M+H)]+.
N-(Циклопропилметил)-4-(5-фторпиридин-3-ил)-2-метил-1H-имидазол-1-амин получают в соотвествии с методикой, описанной в примере 1 (стадия 3, способ B): 1H ЯМР (300 МГц, CD3OD) δ 8,965 (с, 1H), 8,746 (с, 1H), 8,39-8,30 (м, 2H), 3,08-3,05 (м, 2H), 2,77 (с, 3H), 1,08-0,95 (м, 1H), 0,56-0,56 (м, 2H), 0,19-0,15 (м, 2H); МС(ESI) m/z 247 [(M+H)]+.
Пример 1, стадия 4: Получение N-метил-N-(2-метил-4-пиридин-3-илимидазол-1-ил)-3-метилсульфанилбутрамида (соединение 2)
Раствор метил-(2-метил-4-пиридин-3-илимидазол-1-ил)амина (400 мг, 2,13 ммоль), 3-метилсульфанилбутирилхлорида (649 мг, 4,25 ммоль), DMAP (260 мг, 2,13 ммоль) и карбоната калия (881 мг, 6,38 ммоль) в ДХЭ (5 мл) нагревают до 80°C и выдерживают при данной температуре в течение 6 часов. Растворитель удаляют при пониженном давлении и остаток очищают хроматографией с обращенной фазой (ацетонитрил/вода от 0 до 100%), получая указанное в заголовке соединение в виде масла коричневого цвета (290 мг, 44,8%): 1H ЯМР (400 МГц, CDCl3) δ 8,94 (ушир.с, 1H), 8,47 (дд, J=5,0, 1,4 Гц, 1H), 8,04 (дт, J=8,2, 1,5 Гц, 1H), 7,36-7,27 (м, 2H), 3,39 (с, 3H), 3,25-3,18 (м, 1H), 2,38 (с, 3H), 2,27-2,19 (м, 2H), 2,02 (с, 3