Новые гетероциклы
Иллюстрации
Показать всеИзобретение относится к новым и известным производным пиримидина, обладающим свойствами ингибитора PDE4, и их применению для лечения заболеваний, опосредованных активностью указанного рецептора. Эти соединения пригодны для лечения иммунологических заболеваний, воспаления, болевого нарушения, ревматоидного артрита; остеопороза; множественной миеломы; увеита; острого и хронического миелогенного лейкоза; атеросклероза; рака; кахексии и других заболеваний. В частности, изобретение относится к применению соединения формулы (I), для изготовления лекарственного средства, используемого для лечения хронического обструктивного заболевания легких COPD. В соединении (I)
А представляет собой арильную группу, выбранную из фенила; В представляет собой арильную группу, выбранную из фенила или пиридила; X представляет собой атом углерода или атом азота; R представляет собой замещенные или незамещенные группы, выбранные из гетероарильных групп, включающих пиридил, тиенил, фурил, пирролил, пиразолил, оксазолил, тиазолил, имидазолил, тиадиазолил, триазолил, тетразолил, пиримидинил и пиразинил, и гетероциклических групп, включающих морфолин, тиоморфолин, пиперазин, пиперидин, пиперидин-4-он, пирролидин, пиррол-2,5-дион, тиазолидин, 1-оксидотиазолидин и 1,1-диоксидо-1,3-тиазолидин; где гетероциклическая группа необязательно замещена заместителями, независимо выбранными из замещенного или незамещенного (С6)арила, -СН2-С6арила, -СН2-гетероарила, СО-С6арила, -СО-гетероарила, -CS-гетероарила, -СО-С3-6циклоалкила, циано(C1-4)алкила, -О-метилоксима, -SO2Cl, формила, или другой замещенной или незамещенной гетероциклической группы, выбранной из пиридила, пиримидинила и пиперидинила; где присоединение гетероциклической группы к пиримидиновому кольцу происходит через атом углерода или азота; и где группа R или заместитель гетероциклической группы R необязательно замещены. Другие заместители указаны в формуле изобретения. 12 н. и 3 з.п. ф-лы, 15 табл., 158 пр.
Реферат
Область техники, к которой относится изобретение
Описаны новые гетероциклические соединения общей формулы (I), их производные, аналоги, таутомерные формы, стереоизомеры, полиморфы, гидраты, сольваты, фармацевтически приемлемые соли и композиции, их метаболиты и пролекарства.
Настоящее изобретение также относится к способу получения указанных выше новых гетероциклических соединений общей формулы (I).
Новые гетероциклические соединения по настоящему изобретению пригодны для лечения воспаления и иммунологических заболеваний. В частности, соединения по настоящему изобретению пригодны для лечения рака, воспаления и иммунологических заболеваний, опосредуемых цитокинами, такими как TNF-α, IL-1, IL-6, IL-1β, IL-8, IL-12, и циклооксигеназами, такими как COX-1, COX-2 и COX-3. Более конкретно, соединения по настоящему изобретению пригодны в качестве ингибиторов PDE4 и пригодны для лечения опосредуемых PDE4 заболеваний, таких как астма, COPD, IBD, артрит, псориаз и т.п. Они также пригодны для лечения ревматоидного артрита; остеопороза; множественной миеломы; увеита; острого и хронического миелогенного лейкоза; ишемической болезни сердца, атеросклероза, рака, индуцированного ишемией повреждения клеток, разрушения β-клеток поджелудочной железы; остеоартрита; ревматоидного спондилита; подагрического артрита; IBD; респираторного дистресс-синдрома взрослых (ARDS); псориаза; болезни Крона; аллергического ринита; язвенного колита; анафилаксии; контактного дерматита; астмы; мышечной дегенерации; кахексии; диабета I типа и II типа; заболеваний резорбции кости; ишемического реперфузионного повреждения; травмы головного мозга; рассеянного склероза; церебральной малярии; сепсиса; септического шока; синдрома токсического шока; лихорадки; миалгий вследствие инфекции и заболеваний, опосредованных вирусами HIV-1; HIV-2; HIV-3; цитомегаловирусом (CMV); вирусом гриппа; аденовирусом; вирусами герпеса (включая HSV-1, HSV-2) и опоясывающего лишая.
Предпосылки создания изобретения
Настоящее изобретение относится к лечению иммунологических заболеваний или воспаления, в особенности таких заболеваний, которые опосредованы цитокинами или циклооксигеназами. Периферические элементы иммунной системы представляют собой макрофаги или антигенпрезентирующие клетки, T-клетки и B-клетки. Роль других клеток иммунной системы, таких как NK-клетки, базофилы, тучные клетки и дендритные клетки, известна, но их роль в первичных иммунологических нарушениях не определена. Макрофаги являются важными медиаторами обоих видов воспаления и обеспечивают необходимую "помощь" для стимуляции и пролиферации T-клеток. Самое главное, что макрофаги вырабатывают IL-1, IL-12 и TNF-α, которые все являются мощными провоспалительными молекулами, а также обеспечивают помощь T-клетками. Кроме того, активация макрофагов приводит к индукции таких ферментов, как циклооксигеназа-2 (COX-2) и циклооксигеназа-3 (COX-3), индуцибельной синтазы оксида азота (iNOS), и продукции свободных радикалов, способных повреждать нормальные клетки. Макрофаги активируют многие факторы, включая бактериальные продукты, суперантигены и интерферон гамма (IFN-γ). Полагают, что в процесс активации вовлечены фосфотирозинкиназы (PTK) и другие не определенные клеточные киназы.
Цитокины представляют собой молекулы, секретируемые иммунными клетками, признано, что большое количество хронических и острых состояний ассоциировано с нарушением воспалительного ответа. В этом ответе принимают участие большое количество цитокинов, включая IL-1, IL-6, IL-8 и TNF. Полагают, что активность этих цитокинов в регуляции воспаления зависит, по меньшей мере, частично от активации фермента на пути клеточной сигнализации, представителя MAP, известного как CSBP и RK. Эта киназа активируется при двойном фосфорилировании после стимуляции посредством физикохимического стресса, воздействием липополисахаридов или провоспалительными цитокинами, такими как IL-1 и TNF. Таким образом, ингибиторы киназной активности p38 являются пригодными противовоспалительными средствами.
Цитокины представляют собой молекулы, секретируемые иммунными клетками, которые важны в опосредовании иммунного ответа. Продукция цитокинов может приводить к секреции других цитокинов, измененному функционированию клеток, делению или дифференцировке клеток. Воспаление представляет собой нормальный ответ организма на повреждение или инфекцию. Однако при воспалительных заболеваниях, таких как ревматоидный артрит, патологические воспалительные процессы могут приводить к заболеваемости и смертности. Цитокин фактор некроза опухоли-альфа (TNF-α) играет центральную роль в воспалительном ответе и намечен в качестве точки вмешательства при воспалительных заболеваниях. TNF-α представляет собой полипептидный гормон, высвобождаемый активированными макрофагами и другими клетками. В низких концентрациях TNF-α принимает участие в защитном воспалительном ответе, активируя лейкоциты и стимулируя их миграцию в внесосудистые участки воспаления (Moser et al., J. Clin. Invest., 83, 444-55, 1989). При более высоких концентрациях TNF-α может действовать как мощный пироген и индуцировать продукцию других провоспалительных цитокинов (Haworth et al., Eur. J. Immunol., 21, 2575-79, 1991; Brennan et al., Lancet, 2, 244-7, 1989). TNF-α также стимулирует синтез белков острой фазы. При ревматоидном артрите, хроническом и прогрессирующем воспалительном заболевании, поражающем приблизительно 1% взрослого населения США, TNF-α опосредует каскад цитокинов, приводящий к повреждению и разрушению суставов (Arend et al, Arthritis Rheum, 38, 151-60, 1995). Ингибиторы TNF-α, включая растворимые рецепторы TNF, этанерцепт (Goldenberg, Clin Ther, 21, 75-87, 1999 и anti-TNF-α антитело) и инфликсимаб (Luong et al., Ann Pharmacother, 34, 743-60, 2000), недавно одобрены FDA США для лечения ревматоидного артрита.
Повышенные уровни TNF-α также вовлечены во многие другие нарушения и болезненные состояния, включая кахексию, синдром септического шока, остеоартрит, воспалительное заболевание кишечника (IBD), такие как болезнь Крона и язвенный колит и т.д.
Повышенные, относительно базовых уровней, уровни TNF-α и/или IL-1 вовлечены в опосредование и обострение ряда болезненных состояний, включая ревматоидный артрит; остеопороз; множественную миелому; увеит; острый и хронический миелогенный лейкоз; разрушение β-клеток поджелудочной железы; остеоартрит; ревматоидный спондилит; подагрический артрит; воспалительное заболевание кишечника; респираторный дистресс-синдром взрослых (ARDS); псориаз; болезнь Крона; аллергический ринит; язвенный колит; анафилаксию; контактный дерматит; астму; мышечную дегенерацию; кахексию; диабет I типа и II типа; заболевания резорбции костей; ишемическое реперфузионное повреждение; атеросклероз; травму головного мозга; рассеянный склероз; церебральную малярию; сепсис; септический шок; синдром токсического шока; лихорадку и миалгии вследствие инфекции. Также вследствие действия TNF-α обостряются HIV-1, HIV-2, HIV-3, цитомегаловирус (CMV), вирус гриппа, аденовирус, вирусы герпеса (включая HSV-1, HSV-2) и опоясывающий лишай.
Можно видеть, что ингибиторы TNF-α потенциально пригодны для лечения широкого множества заболеваний. Соединения, ингибирующие TNF-α описаны в нескольких патентах.
Цитокины играют важную роль в коммуникации клеток многоклеточных организмов. Ранние исследования показали, что линия B-клеток имеет тенденцию к секреции IL-6 в ответ на механизмы иммунной защиты хозяина, но исследования в последнем десятилетии показали повышенные уровни IL-6 у различных фенотипов рака.
Выявлено, что IL-6 является фактором роста для клеток множественной миеломы; показано, что антитела к IL-6 блокируют пролиферацию клеток миеломы у пациентов с лейкозом Lkein et al., Blood, 78, 5, 1198-1204, 1991 и Lu et al., Eur. J. Immunol., 22. 2819-24, 1992.
Повышение уровней воспалительных цитокинов, в частности IL-6 и TNF-α, по-видимому, также ассоциировано со связанной с раком кахексией, синдромом, включающим потерю жировой ткани и ткани скелетной мускулатуры, и синдромом, который не отвечает на повышенное потребление калорий. Кахексия также может быть связана с ролью белков острой фазы. Ответ острой фазы и продукция белков острой фазы, например, C-реактивного белка (CRP) опосредованы IL-6. Исследования демонстрируют корреляцию повышенных уровней IL-6 с повышением белков острой фазы, что, примечательно, также ассоциировано с увеличением потери массы и сниженной выживаемостью. Таким образом, при повышении уровней IL-6 метаболизм аминокислот направляется из периферических тканей к печени для продукции белков острой фазы, что в свою очередь приводит к атрофии мускулатуры, что является компонентом кахексии. Таким образом, индуцированный цитокинами ответ острой фазы может являться первичным компонентом, связанной со злокачественными заболеваниями кахексии. Кроме того, снижение или блокировка активности IL-6 в моделях на животных уменьшает кахексию, дополнительно демонстрируя существенную роль, которую IL-6 играет в развитии этого синдрома.
Таким образом, наличие соединения с ингибирующей IL-6 активностью может быть полезным для различных воспалительных заболеваний, сепсиса, множественной миеломы, плазмацитарного лейкоза, остеопороза, кахексии, псориаза, нефрита, саркомы Капоши, аутоиммунного ревматоидного артрита, эндометриоза и солидного рака (WO02/074298 Al). Соединения, ингибирующие IL-6, описаны в US 6004813; US 5527546 и US 5166137.
Также в воспалительном ответе принимает участие цитокин IL-1β. Он стимулирует пролиферацию тимоцитов, активность фактора роста фибробластов и высвобождение простагландинов из синовиальных клеток. Повышенные или нерегулируемые уровни цитокина IL-1β ассоциированы с рядом воспалительных заболеваний и других болезненных состояний, включая в качестве неограничивающих примеров респираторный дистресс-синдром взрослых, аллергию, болезнь Альцгеймера и т.д. Так как сверхпродукция IL-1β ассоциирована с множеством болезненных состояний, желательно разработать соединения, ингибирующие продукцию или активность IL-1β.
В моделях ревматоидного артрита на животных множественные внутрисуставные инфекции IL-1 приводили к острой и деструктивной форме артрита (Chandrasekhar et al., Clinical Immunol Immunopathol. 55, 382, 1990). В исследованиях с применением культивируемых ревматоидных синовиальных клеток IL-1 является более мощным индуктором стромелизина, чем TNF-α (Firestein, Am. J. Pathol. 140, 1309, 1992). В участках локальной инфекции наблюдали эмиграцию нейтрофилов, лимфоцитов и моноцитов. Эмиграцию связывают с индукцией хемокинов (например, IL-8) и положительной регуляцией молекул адгезии (Dinarello, Eur. Cytokine Netw. 5, 517-531, 1994).
При ревматоидном артрите IL-1 и TNF-α индуцируют синовиоциты и хондроциты с продукцией коллагеназы и нейтральных протеаз, что приводит к разрушению ткани в суставах. В модели артрита (индуцированный коллагеном артрит, CIA у крыс и мышей) внутрисуставное введение TNF-α до или после индукции CIA приводило к ускоренному началу артрита и более тяжелому течению заболевания (Brahn et al., Lymphokine Cytokine Res. 11, 253, 1992; и Cooper, Clin. Exp. Immunol. 898, 244, 1992).
IL-8 вовлечен в обострение и/или вызов многих болезненных состояний при которых хемотаксическим характером IL-8 опосредована массивная инфильтрация нейтрофилов в участки воспаления или повреждения (например, ишемия), включая в качестве неограничивающих примеров, следующее: астму, воспалительное заболевание кишечника, псориаз, респираторный дистресс-синдром взрослых, сердечное или почечное реперфузионное повреждение, тромбоз и гломерулонефрит. В дополнение к хемотаксическому действию на нейтрофилы, IL-8 также способен активировать нейтрофилы. Таким образом, уменьшение уровней IL-8 может приводить к снижению нейтрофильной инфильтрации.
IL-12 представляет собой гетеродимерный цитокин, состоящий из субъединиц p40 и p35, с мощными иммунорегуляторными свойствами, первично высвобождаемый антигенпрезентирующими клетками, дендритными клетками и моноцитами/макрофагами в ответ на бактериальные продукты и иммунные сигналы. Он усиливает опосредованную природными киллерами (NK) цитотоксичность и индуцирует продукцию интерферона-гамма (IFN-γ) NK-клетками и T-лимфоцитами. IL-12 играет ключевую роль в стимуляции иммунного ответа Th1, что показано и in vitro, и in vivo. Таким образом, антитела к IL-12 применяют для положительного воздействия в экспериментальных моделях аутоиммунных заболеваний, контролируемых Th1, таких как экспериментальный аллергический энцефаломиелит (EAE) и индуцированное 2,4,6-тринитробензолсульфоновой кислотой (TNBS) хроническое воспаление кишечника у мышей, модели воспалительного заболевания кишечника человека. У обработанных TNBS мышей, введение антител к IL-12 после индукции колита приводит к стойкому улучшению развернутого заболевания, клиническому и гистопатологическому, ассоциированному со снижением продукции IFN-g стимулированными ex vivo CD4+-клетками собственной пластинки. Подобным образом лечение антителами к IL-12 мышей C3H, инфицированных Borrelia burgorferi, значительно снижает тяжесть артрита Лайма, сопровождаемого снижением уровней IFN-g в сыворотке. Ряд данных свидетельствует о критической роли IL-12 в патогенезе CD, включая то, что экспрессия IL-12 мононуклеарными клетками также увеличена у пациентов с CD относительно контроля (Kakazu T et al. Am. J. Gastroenterol. 1999, 94, 2149-2155).
Продукция IL-12 в хирургических образцах пациентов с CD по сравнению с образцами контрольных пациентов с раком слепой кишки увеличена (Colpaert S et al. Eur. Cytokine Netw. 2002, 13, 431-437). В образцах подвздошной кишки и слизистой желудка детской CD, по сравнению с малым количеством или отсутствием кластеров в образцах с гастритом вследствие H. pylori и нормальной слизистой желудка, найдено множество кластеров положительных по IL-12 клеток (Berrebi D et al. Am. J. Pathol. 1998, 152, 667-672). Значительные количества содержащих IL-12 макрофагов присутствуют в собственной пластинке и мышечной оболочке кишечника при активной CD, тогда как в контрольных образцах с невоспалительными нарушениями кишечника эти клетки обнаруживают редко или не обнаруживают (Parronchi P et al. Am. J. Pathol. 1997, 150, 823-832). мРНК p40 IL-12 в мононуклеарных клетках собственной пластинки, выделенных у пациентов с CD, выявили у 11/13 пациентов по сравнению с 1/13 у здоровых контролей (P<0,001) (Monteleone G et al. Gastroenterology. 1997, 112, 1169-1178). Экспрессия мРНК IL-12 существенно увеличена в образцах биопсии толстого кишечника пациентов с активной CD по сравнению со здоровыми контролями (P<0,04) (Nielsen OH et al. Scand. J. Gastroenterol. 2003, 38, 180-185).
Опубликовано, что фермент циклооксигеназа существует в трех изоформах, а именно, COX-1, COX-2 и COX-3. Фермент COX-1 является жизненно необходимым и в основном отвечает за регуляцию жидкостей желудка, тогда как фермент COX-2 присутствует на фоновых уровнях и, как опубликовано, играет большую роль в синтезе простагландинов для воспалительного ответа. Известно, что эти простагландины вызывают в организме воспаление; таким образом, если посредством ингибирования фермента COX-2 синтез этих простагландинов остановить, можно лечить воспаление и связанные с ним нарушения. COX-3 обладает зависимой от гликозилирования циклооксигеназной активностью. Сравнение активности COX-3 собаки с COX-1 и COX-2 мыши показало, что этот фермент селективно ингибируют обезболивающие/жаропонижающие лекарственные средства, такие как ацетаминофен, фенацетин, антипирин и дипирон, и его потенциально ингибируют некоторые нестероидные противовоспалительные лекарственные средства. Таким образом, ингибирование COX-3 может представлять собой первичный центральный механизм, посредством которого эти лекарственные средства снижают боль и, возможно, лихорадку. В ранних публикациях до разработки коксибов показано, что ингибиторы фермента COX-1 вызывают язвы желудка, тогда как селективные ингибиторы ферментов COX-2 и COX-3 не обладают таким действием и, таким образом, выявлено, что они являются безопасными. Но в некоторых публикациях показано, что селективные ингибиторы COX-2 (коксибы) ассоциированы с риском возникновения сердечно-сосудистых нарушений. Таким образом, показано, что ингибирование COX-2 без увеличения рисков сердечно-сосудистых нарушений и язв желудка вследствие ингибирования COX-1, является безопасным.
Фосфодиэстеразы ("PDE") представляют собой семейство ферментов, метаболизирующих 3'5' циклические нуклеотиды до 5' нуклеозидмонофосфатов, терминируя, таким образом, активность вторичного мессенджера цАМФ. Интерес в качестве потенциальной мишени для разработки новых противоастматических и противовоспалительных соединений вызывала конкретная фосфодиэстераза, фосфодиэстераза-4 ("PDE4", также известная как "PDE IV"), которая представляет собой высокоаффинный, специфичный к цАМФ тип IV PDE. Известно, что PDE4 существует, по меньшей мере, в виде четырех изоферментов, каждый из которых кодируется отдельным геном. Полагают, что каждый из этих известных генных продуктов PDE4 играет различные роли в аллергическом и/или воспалительном видах ответа. Таким образом, полагают, что ингибирование PDE4, в частности конкретной изоформы PDE4, дающей неблагоприятный ответ, может благоприятно подействовать на симптомы аллергии и воспаления. Предоставление способа лечения ревматоидного артрита посредством введение соединений и композиций, ингибирующих активность PDE4 может быть желательным.
Основной проблемой применения ингибиторов PDE4 является побочный эффект в виде тошноты, который наблюдали для некоторых соединений-кандидатов, как описано в патентах US 5622977, WO 99/50262, US 6410563 и US 5712298. Также описана большая вариация тяжести нежелательных побочных эффектов, вызываемых различными соединениями. Существует большой интерес к терапевтическим ингибиторам PDE4, и проводятся их масштабные исследования, как описано в указанных выше патентах и цитируемых в них ссылках.
Предшествующий уровень техники
I) В US 6420385 описаны новые соединения формулы (IIa),
где представляет собой X представляет собой O, S или NR5; каждый из R1 и R2 независимо представляет собой -Y или -Z-Y и R3 и R4 каждый независимо представляет собой -Z-Y или R3 представляет собой водородный радикал; при условии, что R4 отличается от радикала в виде замещенного арила, (замещенный арил)метила или (замещенный арил)этила, где каждый Z независимо необязательно замещен алкилом, алкенилом, алкинилом, гетероциклилилом, арилом или гетероарилом; Y независимо представляет собой водород; галоген, циано, нитро и т.д., R5 независимо представляет собой водород, необязательно замещенный алкил, алкенил, алкинил и т.д., каждый из R11 и R12 независимо представляет собой необязательно замещенный арил или гетероарил. Пример этих соединений представлен в формуле (IIb),
II) В US 5728704 описаны новые пиримидины формулы (I),
где R1 представляет собой водород, CF3, (C1-C6)-алкил, (C1-C6)-алкил-S-(C1-C6)-алкил, (C1-C6)-алкил-SO-(C1-C6)-алкил, (C1-C6)-алкил-SO2-(C1-C6)-алкил, гидрокси-(C1-C6)-алкил, дигидрокси-(C1-C6)-алкил, (C1-C6)-алкокси, (C1-C6)-алкоксикарбонил-(C1-C6)-алкил, арил, выбранный из фенила и нафтила, арил-(C1-C6)-алкил; R2 и R3 независимо выбраны из водорода, (C1-C6)-алкила, фенила и фенил-(C1-C4)-алкила, или R2 и R3 совместно с азотом, к которому они присоединены, образуют циклическую группу, выбранную из азетидино, пирролидино, пиперидино, пиперазино и морфолино, где указанная циклическая группа необязательно может быть замещена; R4 представляет собой водород, хлор, бром, циано, нитро, трифторметил, амино, (C1-C6)-алкил, (C1-C6)-гидроксиалкил, (C1-C6)-алкокси, фенил, нафтил или фурил, где указанные фенил, нафтил и фурил необязательно могут быть замещены; R5 представляет собой водород, (C1-C6)-алкил, (C1-C6)-алкокси, трифторметил, (C1-C6)-гидроксиалкил, -S-(C1-C6)-алкил, -SO-(C1-C6)-алкил, -SO2-(C1-C6)-алкил, фенил или фурил.
III) В US 6420385 и 6410729 описаны новые соединения формулы (IIe),
где каждый из R1 и R2 независимо представляют собой -Z-Y, где предпочтительно R2 представляет собой радикал водорода, (C1-C4)-алкила, галогена, гидрокси, амино и т.д., Z независимо представляет собой связь, алкил, алкенил и т.д., Y независимо представляет собой водородный радикал, галоген, нитрорадикал; R20 независимо представляет собой (1) алкил, алкенил, гетероциклический радикал, арил, гетероарил; R21 независимо представляет собой водородный радикал, R20; R22 независимо представляет собой водород, гетероциклил, арил или гетероарил.
IV) В US 7317014 описаны новые соединения формулы (I),
где R1, R2, R3 и R4 могут быть одинаковыми или различными и независимо представляет собой водород, гидрокси, нитро, нитрозо, формил, азидо, галоген или замещенные или незамещенные группы, выбранные из алкила, галогеналкила, алкокси, арила, арилокси, аралкила, аралкокси, гетероарила, гетероциклила, ацила, ацилокси, циклоалкила, амино, гидразина, моноалкиламино, диалкиламино, ациламино, алкилсульфонила, арилсульфонила, алкилсульфинила, арилсульфинила, алкилтио, арилтио, алкоксикарбонила, арилоксикарбонила, алкоксиалкила, сульфамоила, карбоновой кислоты и ее производных; A представляет собой производное пиримидина формулы
где R5, R6, R7 могут быть одинаковыми или различными и представляют собой, водород, нитро, нитрозо, формил, азидо, галоген или замещенные или незамещенные группы, выбранные из алкила, алкокси, ацила, циклоалкила, галогеналкила, амино, гидразина, моноалкиламино, диалкиламино, ациламино, алкилсульфонила, алкилсульфинила, арилсульфонила, арилсульфинила, алкилтио, арилтио, алкоксикарбонила, арилоксикарбонила, алкоксиалкила, сульфамоила, карбоновой кислоты и ее производных; пиримидиновую группу может быть присоединена к фенильному кольцу посредством атома углерода или азота.
V) В US 5622977 описаны ингибиторы PDE IV на основе тризамещенных арильных производных с приведенной ниже общей структурой.
где Y представляет собой галоген или OR1, где R1 представляет собой замещенный или незамещенный алкил; X представляет собой -O-, -S- или -N(R8)-, где R8 представляет собой водород или алкил; R2 представляет собой замещенный или незамещенный алкил, алкенил, циклоалкил или циклоалкенил; R3 представляет собой водород, галоген или OR9, где R9 представляет собой водород или замещенный или незамещенный алкил, алкенил, алкоксиалкил, или алканоил, формилкарбоксамид или тиокарбоксамидо; каждый из R4 и R5, которые могут быть одинаковыми или различными, представляют собой -(CH3)nAr, где Ar представляет собой моноциклическую или бициклическую арильную группу или моноциклический или бициклический гетероарил и n представляет собой целое число от 0 до 3; R6 представляет собой водород или замещенный или незамещенный алкил; R7 представляет собой водород или замещенный или незамещенный алкил.
VI) В WO 99/50262 описаны ингибиторы PDE IV, триарильные этановые производные с приведенной ниже общей структурой
где L представляет собой водород или замещенный или незамещенный алкил или арил; A и B независимо представляют собой замещенные или незамещенные атомы углерода, соединенные вместе одинарной или двойной связью; D представляет собой кислород или замещенный или незамещенный азот; Q представляет собой замещенный или незамещенный арил; каждый из R1, R2, R3 независимо представляет собой водород, галоген, гидрокси, замещенный или незамещенный алкил, алкокси и т.п.
VII) В US 6410563 описаны 8-арилхинолиновые соединения, представляющие собой ингибиторы PDE4
где каждый из S1, S2 и S3 независимо представляет собой водород, галоген, гидрокси, замещенный или незамещенный алкил, алкокси, и т.п.; каждый из R1, R2, R3 независимо представляет собой водород, галоген, замещенный или незамещенный алкил, алкокси, арил, гетероарил, замещенный или незамещенный сульфонамид и т.п.; A представляет собой замещенный или незамещенный атом углерода.
VIII) В US 5712298 описаны другие ингибиторы PDE4 как указано ниже.
где, каждый из R1, R2 независимо представляет собой замещенный или незамещенный гидрокси, алкокси и т.п., R3 представляет собой замещенный или незамещенный фенил или арил и т.п.
IX) В WO2007/083182 описаны новые гетероциклические соединения формулы (I), используемые для лечения нарушений, связанных с болью, воспаления и иммунологических заболеваний, опосредуемых такими цитокинами, как TNF-α, IL-1β и IL-6.
где, A представляет собой замещенные или незамещенные группы, выбранные из арилов; где B представляет собой замещенные или незамещенные группы, выбранные из арила или пиридила. Когда B представляет собой арил или пиридил, тогда R представляет собой замещенные или незамещенные группы, выбранные из арила, гетероарильных групп, где гетероарильные группы можно выбирать из пиридила, тиенила, фурила, пирролила, оксазолила, тиазолила, имидазолила, тиадиазолила, тетразолила, пиримидинила, пиразина, бензофуранила, бензимидазолила, бензотиазолила и т.п., арилокси и гетероциклических групп, таких как морфолин, пиперазин, пиперидин, пирролидин, тиазолидин и т.п.; R1, R2, R3 и R4 представляют собой водород, гидрокси, нитро, азидо, галогены, замещенные или незамещенные группы, выбранные из алкила, галогеналкила, алкокси, арила, арилокси, ацилокси, амино, гидразина, алкилтио, алкоксикарбонила, алкоксиалкила, сульфамоила, -SO2NHNH2, -SO2Cl, карбоновой кислоты и ее производных.
Цели изобретения
Заявители сфокусировали исследования на идентификации ингибиторов цитокинов, преимущественно действующих посредством ингибирования TNF-α, которые лишены любых побочных эффектов, обычно ассоциированных с ингибиторами TNF-α, и на идентификации новых низкомолекулярных противораковых средств. Длительные усилия заявителей в результате привели к новым гетероциклическим соединениям формулы (I). Эти производные могут быть полезными для лечения воспаления, рака и иммунологических заболеваний. Конкретные соединения по настоящему изобретению пригодны для лечения иммунологических заболеваний, опосредуемых цитокинами, такими как TNF-α, IL-1, IL-6, IL-1β, IL-8; IL-12 и воспаления. Более конкретно, соединения по настоящему изобретению пригодны в качестве ингибиторов PDE4 и пригодны для лечения опосредуемых PDE4 заболеваний. Соединения по настоящему изобретению также пригодны для лечения ревматоидного артрита; остеопороза; множественной миеломы; увеита; острого и хронического миелогенного лейкоза; ишемической болезни сердца; атеросклероза; индуцированного ишемией повреждения клеток; разрушения β-клеток поджелудочной железы; остеоартрита; ревматоидного спондилита; подагрического артрита; воспалительного заболевания кишечника; респираторного дистресс-синдрома взрослых (ARDS); астмы, хронического обструктивного заболевания легких (COPD), псориаза; болезни Крона; аллергического ринита; язвенного колита; анафилаксии; контактного дерматита; астмы; мышечной дегенерации; кахексии; заболеваний резорбции кости; ишемического реперфузионного повреждения; травмы головного мозга; рассеянного склероза; сепсиса; септического шока; синдрома токсического шока; лихорадки и миалгий вследствие инфекции.
Сущность изобретения
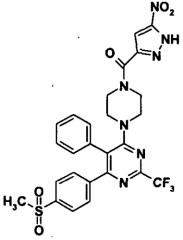
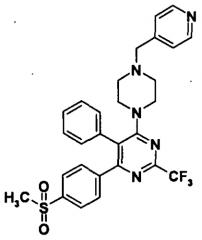
Описаны новые гетероциклические соединения формулы (I),
их производные, аналоги, таутомерные формы, стереоизомеры, полиморфы, сольваты, фармацевтически приемлемые соли и фармацевтические композиции, метаболиты и их пролекарства, где A представляет собой замещенные или незамещенные арильные группы; B представляет собой замещенные или незамещенные группы, выбранные из арила или пиридила; X представляет собой атом углерода или азот; R представляет собой замещенные или незамещенные группы, выбранные из азидо, галогенов, алкила, алкокси, ацила, циклоалкила, галогеналкила, амино, гидразина, моноалкиламино, диалкиламино, ациламино, алкилсульфонила, алкилсульфинила, арилсульфонила, арилсульфинила, алкоксикарбонила, арилоксикарбонила, алкоксиалкила, сульфамоила, арила, гетероарила, арилокси, -OSO2R' и гетероциклических групп; где R' представляет собой замещенные или незамещенные группы, выбранные из алкила, арила, алкилдиалкиламино, галогеналкила, гетероциклических и гетероарильных групп; R1 представляет собой водород, гидрокси, нитро, формил, азидо, галогены, замещенные или незамещенные группы, выбранные из алкила, галогеналкила, алкокси, арила, арилокси, ацилокси, амино, гидразина, моноалкиламино, диалкиламино, ациламино, алкилсульфонила, алкилсульфинила, гетероциклилсульфонила, алкилтио, алкоксикарбонила, алкоксиалкила, сульфамоила, -SO2NHNH2, -SO2Cl, карбоновой кислоты и ее производных; R2 представляет собой водород, гидрокси, нитро, формил, азидо, галогены, замещенные или незамещенные группы, выбранные из алкила, галогеналкила, алкокси, арила, арилокси, ацилокси, амино, гидразина, моноалкиламино, диалкиламино, ациламино, алкилсульфонила, алкилсульфинила, алкилтио, алкоксикарбонила, алкоксиалкила, сульфамоила, -SO2NHNH2, -SO2Cl, карбоновой кислоты и ее производных; R3 представляет собой водород, гидрокси, нитро, формил, азидо, галогены, замещенные или незамещенные группы, выбранные из алкила, галогеналкила, алкокси, арила, арилокси, ацилокси, амино, гидразина, моноалкиламино, диалкиламино, ациламино, алкилсульфонила, алкилсульфинила, алкилтио, алкоксикарбонила, алкоксиалкила, сульфамоила, -SO2NHNH2, -SO2Cl, карбоновой кислоты и ее производных; R4 представляет собой водород, гидрокси, нитро, формил, азидо, галогены, замещенные или незамещенные группы, выбранные из алкила, галогеналкила, алкокси, арила, арилокси, ацилокси, амино, гидразина, моноалкиламино, диалкиламино, ациламино, алкилсульфонила, алкилсульфинила, алкилтио, алкоксикарбонила, алкоксиалкила, сульфамоила, -SO2NHNH2, -SO2Cl, карбоновой кислоты и ее производных.
Подробное описание изобретения
Описаны новые гетероциклические соединения формулы (I),
их производные, аналоги, таутомерные формы, стереоизомеры, полиморфы, сольваты, фармацевтически приемлемые соли, композиции, метаболиты и их пролекарства, где A представляет собой замещенную или незамещенную арильную группу;
B представляет собой замещенные или незамещенные группы, выбранные из арила или пиридила;
X представляет собой атом углерода или атом азота;
R представляет собой замещенные или незамещенные группы, выбранные из азидо; галогенов; линейных или разветвленных алкильных групп, таких как метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, н-пентил, изопентил, гексил и т.п.; алкокси группы, такие как метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, трет-бутокси и т.п.; галогеналкильные группы, такие как дихлорметил, дифторметил, трифторметил, трихлорметил и т.п.; ацильные группы, такие как ацетил, пропаноил и т.п.; циклоалкильные группы, такие как циклопропил, циклобутил, циклопентил и т.п.; амино; гидразин; моноалкиламино; диалкиламино; ациламиногруппы, такие как ацетиламино, пропаноиламино и т.п.; алкилсульфонильные группы, такие как метилсульфонил, этилсульфонил, пропилсульфонил и т.п.; алкилсульфинил; арилсульфонил; арилсульфинил; алкоксикарбонил, такой как метоксикарбонил, этоксикарбонил и т.п.; арилоксикарбонил; алкоксиалкил; сульфамоил; арильные группы, такие как фенил, нафтил и т.п.; гетероарильные группы, такие как пиридил, тиенил, фурил, пирролил, пиразолил, оксазолил, тиазолил, имидазолил, тиадиазолил, триазолил, тетразолил, пиримидинил, пиразинил, бензофуранил, бензимидазолил и бензотиазолил; арилокси; -OSO2R' и гетероциклические группы, такие как морфолин, тиоморфолин, пиперазин, пиперидин, пиперидин-4-он, пирролидин, пиррол-2,5-дион, тиазолидин, 1-оксидотиазолидин и 1,1-диоксидо-1,3-тиазолидин; гетероциклическая группа, необязательно замещена заместителями, независимо выбранными из замещенного или незамещенного алкила, арила, гетероарила, аралкила (-CH2-арила), алкилгетероарила (-CH2-гетероарила), замещенного арилкарбонила (-CO-Ar), гетероарилкарбонила (-CO-гетероарила), гетероарилтиокарбонила (-CS-гетероарила), циклоалкилкарбонила (-CO-циклоалкила), цианоалкила, -O-метилоксима, алкилсульфонила, галогеналкиласульфонила, галогенацила, -SO2Cl, формила, гидроксамовой кислоты и другой замещенной или незамещенной гетероциклической группы; присоединение гетероциклической группы к пиримидиновому кольцу осуществляется через атом углерода или азота; где R' представляет собой замещенные или незамещенные группы, выбранные из алкила, арила, алкилдиалкиламино, галогеналкила, гетероциклических и гетероарильных групп;
R1 представляет собой водород; гидрокси; нитро; формил; азидо; галогены; замещенные или незамещенные группы, выбранные из алкилов; галогеналкил; алкокси; арил; арилоксигруппы, выбранные из фенокси и нафтокси; ацилоксигруппы, такие как MeCOO-, EtCOO- и PhCOO-; амино; гидразин; моноалкиламино; диалкиламино; ациламино; алкилсульфонил; алкилсульфинил; алкилтио; алкоксикарбонил; алкоксиалкил; сульфамоил; -SO2NHNH2; -SO2Cl; карбоновую кислоту и ее производные;
R2 представляет собой водород; гидрокси; нитро; формил; азидо; галогены; замещенные или незамещенные группы, выбранные из алкилов; галогеналкил; алкокси; арил; арилокси; ацилокси; амино; гидразин; моноалкиламино; диалкиламино; ациламино; алкилсульфонил; алкилсульфинил; алкилтио; алкоксикарбонил; алкоксиалкил; сульфамоил; -SO2NHNH2; -SO2Cl; карбоновую кислоту и ее производные;
R3 представляет собой водород; гидрокси; нитро; формил; азидо; галогены; замещенные или незамещенные группы, выбранные из алкилов; галогеналкил; алкокси; арил; арилокси; ацилокси; амино; гидразин; моноалкиламино; диалкиламино; ациламино; алкилсульфонил; алкилсульфинил; алкилтио; алкоксикарбонил; алкоксиалкил; сульфамоил; -SO2NHNH2; -SO2Cl; карбоновую кислоту и ее производные;
R4 представляет собой водород; гидрокси; нитро; формил; азидо; галогены; замещенные или незамещенные группы, выбранные из алкилов; галогеналкил; алкокси; арил; арилокси; ацилокси; амино; гидразин; моноалкиламино; диалкиламино; ациламино; алкилсульфонил; алкилсульфинил; алкилтио; алкоксикарбонил; алкоксиалкил; сульфамоил; -SO2NHNH2; -SO2Cl; карбоновую кислоту и ее производные;
группы R, R1, R2, R3, R4 и R' необязательно замещены одним или несколькими заместителями, выбранными из галогенов; гидрокси; нитро; циано; мочевин; азидо; амино; имино-1-фенилбутанона; амидных групп, таких как ацетамид, бензамид и т.п.; тиоамида; гидразина; линейных или разветвленных алкильных групп, таких как метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, н-пентил, изопентил, гексил и т.п.; алкоксигрупп, таких как метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, трет-бутокси и т.п.; галогеналкильных групп, таких как дихлорметил, дифторметил, трифторметил, трихлорметил и т.п.; ацильных групп, таких как ацетил, пропаноил, бензоил и т.п.; галогеналкоксигрупп, таких как трифторметокси, трифторэтокси, трихлорметокси и т.п.; циклоалкильных групп, таких как циклопропил, циклобутил и т.п.; галогенацильных групп, таких как трифторацетил, трихлорацетил и т.п.; ацилоксиацила; гетероциклила; арила; гетероарила; моноалкиламино; диалкиламино; ациламино; арилоксигрупп, таких как фенокси, нафтокси и т.п.; алкоксикарбонильных групп, таких как метоксикарбони