Соединение нибентана с аминокислотой, обладающее противоаритмической активностью, и способ его получения
Иллюстрации
Показать всеИзобретение относится к медицине и может найти применение в медицинской практике для коррекции нарушений ритма сердечной деятельности и касается способа получения нибентана с аминокислотой формулы (1) путем растворения 4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида в этиловом спирте, к полученному раствору при 50°C приливают раствор глутаминовой кислоты в воде, с последующей фильтрацией и выделением 4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида глутамината. Изобретение позволяет снизить токсичность, устранить нежелательные побочные эффекты и увеличить широту терапевтического действия. 4 табл., 3 пр.
Реферат
Изобретение относится к медицине и может найти применение в медицинской практике для коррекции нарушений ритма сердечной деятельности.
Известно соединение нитрофенилдиэтиламинопентилбензамид под названием нибентан, проявляющее противоаритмическое действие при жизнеугрожающих нарушениях ритма сердца (Создание оригинальных отечественных антиаритмических препаратов III класса. Вестн. РАМН, 2003; 12, с. 61-65).
Недостатком известного решения является его высокая токсичность, высокая вероятность развития нежелательных эффектов, незначительная широта терапевтического действия и узкий терапевтический спектр - эффективен в основном при предсердных нарушениях ритма.
Наиболее близким по технической сущности к предлагаемому техническому решению является способ получения соединения нибентана с аминокислотой, по которому в колбу загружают 3,84 (0,01 М) 1-фенил-1-(п-нитробензоиламино)-5-(N-диэтиламино)пентана, 120 мл этилового спирта 80% и 0,74 г (0,005 М) L-глутаминовой кислоты. Реакционную массу перемешивают при 35-40°C до получения раствора. Растворитель отгоняют в вакууме, остаток промывают эфиром, сушат до постоянного веса. Получают 4,05 г (89,3%).
Недостатком известного способа является недостаточно высокий выход продукта (89,3%), полученное соединение проявляет только антиаритмическую активность, также способ является экономически затратным.
Технический результат заключается в получении целевого продукта стабильной полиморфной модификации, повышении выхода продукта, снижении экономических затрат, увеличении широты терапевтического действия, обладании противоишемической активностью, кроме того, не обладает ДНК-повреждающим действием и мутагенностью, а также является более безопасным и эффективным соединением для терапии нарушений сердечного ритма различного генеза.
Сущность изобретения достигается тем, что способ получения соединения нибентана с аминокислотой, обладающего противоаритмической активностью, отличается тем, что 0,01 М 4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида растворяют в 20 мл этилового спирта, приливают при 50°C 0,01 М раствора L-глутаминовой кислоты в воде. Полученный раствор фильтруют, отгоняют растворитель. К осадку приливают 30 мл ацетона, тщательно перемешивают, кристаллизуют. Осадок отделяют и сушат с выделением 4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида глутамината.
Способ иллюстрируется следующим примером.
Пример. 3,83 г (0,01 М) 4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида растворяют в 20 мл этилового спирта. К раствору при 50°C приливают 1,47 г (0,01 М) L-глутаминовой кислоты в воде. К осадку приливают 30 мл ацетона, тщательно перемешивают, кристаллизуют. Осадок отделяют, сушат до постоянного веса. Получают 4,92 г 4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида глутамината, белый с кремоватым оттенком кристаллический порошок.
Выход 4,92 г (93%).
Вычислено, %: С 61,11; Н 7,03; N 10,56; O 21,11.
Найдено, %: С 60,85; Н 7,41; N 10,03.
Были проведены исследования фармакологической активности (RS)-4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида L-глутамината.
Исследование 1. Исследование генотоксичности соединения (RS)-4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида L-глутамината. Использованы стандартные тест-системы in-vitro и in-vivro: ДНК повреждающее действие (Rec-тест) на бактериях Е. coli, тест Эймса (в качестве индикаторных микроорганизмов использованы тестерные штаммы S-typhimurium ТА 1537, ТА 98, ТА 100. Набор этих штаммов позволяет регистрировать действие мутагенов. Наличие мутагенного действия или его отсутствия регистрировали на основе индукции у них реверсий от ауксотрофности к протогрофности по гистидину. В качестве контроля использовали нитрозометилмочевину. Статистический анализ проводили методом множественных сравнений Даннета. Полученные результаты свидетельствуют, что заявляемое соединение нибентана с аминокислотой не обладает ДНК повреждающим действием и мутагенностью.
Исследование 2. Исследование фармакологической активности (RS)-4-нитро-N-[1-фегтил-5-(диэтиламино)пентил]бензамида L-глутамината:
Пример 1. Острая токсичность (RS)-4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида L-глутамината, структурного аналога нибентана.
Острая токсичность противоаритмических средств является одним из основных параметров, характеризующих безопасность препаратов. Острую токсичность исследовали при внутрибрюшинном введении водных растворов (RS)-4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида L-глутамината и структурного аналога нелинейным белым лабораторным мышам. Каждую дозу испытуемых соединений вводили группе из 6-10 животных в растворе, объем которого не превышал 0,5 мл внутрибрюшинно. LD50 (дозу, вызывающую летальный исход в половине наблюдений) рассчитывали с помощью графического метода Миллера и Тейнтера (Беленький М.Л. Элементы количественной оценки фармакологического эффекта. - Рига: Изд. АН ЛССР, 1963. - С. 60-64.)
Результаты исследования заявляемого соединения и структурного аналога приведены в табл. 1.
Острая токсичность (RS)-4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида L-глутамината оказалась ниже структурного предшественника нибентана.
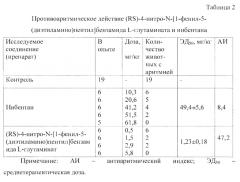
Пример 2. Активность (RS)-4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида L-глутамината и нибентана на модели аконитиновой аритмии у крыс.
Аритмию воспроизводили по методу Ю.И. Вихляева и Н.В. Кавериной (1958) (кн. Каверина Н.В., Бердяев С.Ю., Кущук Е.П., Пасхина О.Е. Методические указания по изучению антиаритмической активности новых фармакологических веществ // Руководство по экспериментальному (доклиническому) исследованию новых фармакологических веществ / Под ред. В.П. Фисенко. М., 2000. С. 210). Нитрат аконитина вводили животным в дозе 50 мкг/кг. Результаты исследований представлены в табл. 2. Данная модель позволяет судить о широте терапевтического действия представляемого соединения и его ближайшего аналога по величине противоаритмического индекса, определяемого как отношение LD50 при внутрибрюшинном способе введения к ЭД50 на аконитиновой модели аритмий.
Проведенный эксперимент показывает, что (RS)-4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида L-глутаминат эффективно купирует предсердную аритмию, вызванную внутривенным введением нитрата аконитина. При этом значение антиаритмического индекса, рассчитанного для 1, превосходит таковой нибентана, следовательно, (RS)-4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида L-глутаминат обладает большей широтой терапевтического действия, чем сравниваемый аналог, что свидетельствует о большей его безопасности при эквивалентной активности.
Представленные данные свидетельствуют, что (RS)-4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида L-глутаминат проявляет выраженные противоаритмические свойства на моделях желудочковых и предсердно-желудочковых аконитиновых аритмий, превосходящие противоаритмические свойства структурного аналога нибентана.
Длительность противоаритмического эффекта (RS)-4-нитро-N-[1-фенил-5-(диэтиламино)нентил]бензамида L-глутаминат незначительно превышает длительность эффекта нибентана. Важным достоинством заявляемого соединения является его большая широта терапевтического действия на аконитиновой модели аритмий по сравнению с аналогом.
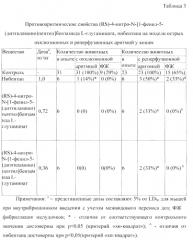
Пример 3. Противоаритмическая активность RS)-4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида L-глутамината и структурного аналога при желудочковой аритмии у кошек, вызванных высокой перевязкой коронарной артерии и ее последующей реперфузией.
Для оценки эффективности (RS)-4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида L-глутамината в условиях транзиторного ишемического и реперфузионного аритмогенеза использовали метод, описанный Сторожук Б.Г. Противофибрилляторная активность некоторых антиаритмических средств при максимально высокой перевязке коронарной артерии и ее реперфузии у кошек // Фармакол. и токсикол. 1985. №3. С. 47-49 и Manning G.A.S., Grome R., Istcol K. et al. Reperfusion induced ventricular fibrillation. Modification by pharmacological agents // Adv. Myocardiol. Vol. 6. New York, London, 1985. P. 515-522.
Введение (RS)-4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида L-глутамината в дозе 0,72 мг/кг (5% от LD50) и 0,36 мг/кг (2,5% от LD50) позволило подавить ишемическую и реперфузионную фибрилляцию желудочков в 100% опытов (достоверно при сравнении с контролем при p<0,05) и достоверно снизить риск возникновения желудочковой аритмии: ишемической до 14%, реперфузионной - до 50% (табл. 3).
Таким образом, по силе и длительности противоаритмического эффекта (RS)-4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида L-глутамината сопоставим со своим структурным предшественника - нибентаном.
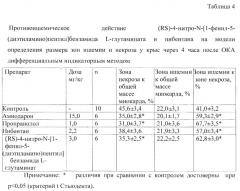
Пример 4. Изучение противоишемической активности (RS)-4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида L-глутамината и структурного аналога нибентана у крыс после перевязки левой коронарной артерии.
В опытах на крысах-самцах линии Vistar мы изучили влияние (RS)-4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида L-глутамината и нибентана на размеры зон некроза и ишемии после перевязки левой коронарной артерии дифференциальным индикаторным методом (Сернов Л.Н., Гацура В.В. // Бюлл. эксп. биол. мед. - 1989. - Т. 108. - №5. - С. 534-53). Результаты представлены в табл. 4.
Проведенное исследование показывает, что (RS)-4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида L-глутамината ограничивает альтеративные процессы в миокарде крыс с окклюзией левой коронарной артерии за счет преимущественного уменьшения размера зоны некроза и отношения размеров зоны ишемии к зоне некроза. Это может быть связано со способностью входящих в состав вещества естественных метаболитов, во-первых, возбуждать NMDA-рецепторы (глутаматные) в миокарде и ограничивать его симпатическую активацию, а во-вторых, напрямую вмешиваться в метаболические процессы кардиомиоцитов. Кроме того, не исключается возможность ассоциировать антиишемическую активность основания, так как для нибентана показана тенденция к ограничению зон повреждения. Подобный фармакологических эффект может быть обусловлен противоаритмической активностью последнего.
Таким образом, представленные данные свидетельствуют, что (RS)-4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида L-глутаминат обладает противоишемическим действием, превосходящим своего структурного аналога нибентана.
По сравнению с известным решением предлагаемое позволяет получить целевой продукт стабильной полиморфной модификации, обладающий противоаритмической и противоишемической активностью, повысить выход продукта, не обладающего ДНК-повреждающим действием и мутагенностью, снизить экономические затраты, увеличить широту терапевтического действия, кроме того, соединение является более безопасным и эффективным для терапии нарушений сердечного ритма различного генеза.
Способ получения соединения нибентана с аминокислотой, обладающего противоаритмической активностью, включающий перемешивание нибентана с этиловым спиртом и L-глутаминовой кислотой, отгон растворителя, получение остатка, отличающийся тем, что 0,01 М 4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида растворяют в 20 мл этилового спирта, к полученному раствору при 50°C приливают 0,01 М раствора L-глутаминовой кислоты в воде, с последующей фильтрацией и приливанием к осадку 30 мл ацетона с выделением 4-нитро-N-[1-фенил-5-(диэтиламино)пентил]бензамида глутамината.