Хинолил-содержащее соединение гидроксамовой кислоты, способ его получения, а также применение при лечении заболеваний, вызванных аномальной активностью протеинкиназы и/или гистондеацетилазы
Иллюстрации
Показать всеНастоящее изобретение относится к области органической химии, а именно к новым хинолил-содержащим соединениям гидроксамовой кислоты общей формулы (I), где каждый из V1 и V2 независимо представляет собой галоген; один из R и R′ представляет собой группу Q, содержащую гидроксамовую кислоту, а другой представляет собой метокси, где группа Q, содержащая гидроксамовую кислоту, представлена формулой ; А представляет собой О; L представляет собой С1-6алкил; J представляет собой NH, пиперидинил, или J отсутствует; X отсутствует; Y представляет собой С1-6алкил, или Y отсутствует. Также изобретение относится к способу получения соединения формулы (I), фармацевтической композиции на основе соединения формулы (I) и ее применению для лечения заболеваний, вызванных активностью протеинкиназы и/или гистондеацетилазы. Технический результат: получены новые соединения, которые могут быть применимы при лечении рака. 6 н. и 19 з.п. ф-лы, 7 ил., 7 табл., 45 пр.
Реферат
Область изобретения
Настоящее изобретение относится к областям органической химии и медицинской химии, в частности к хинолил-содержащему соединению гидроксамовой кислоты, способу его получения, фармацевтической композиции, содержащей это соединение, и его применению.
Предшествующий уровень техники
Протеинкиназы представляют один из видов фосфотрансфераз и осуществляют функцию переноса гамма-фосфатной группы АТФ на специфический аминокислотный остаток субстрата для фосфорилирования белка, тем самым проявляя свои физиологические и биохимические функции. Протеинкиназы представляют важный класс киназ. При передаче сигнала их главные функции лежат в двух аспектах: один состоит в том, чтобы регулировать активность белка посредством фосфорилирования; другой состоит в том, чтобы постепенно усиливать сигнал путем последовательного фосфорилирования белка, тем самым вызывая клеточный ответ.
Аномальная активность протеинкиназ не только тесно связана с аномальным состоянием на определенных этапах в последовательности внутриклеточных путей передачи сигнала, таких как пролиферация опухолевых клеток, апоптоз и метастазирование, но также является основной причиной возникновения ряда других заболеваний человека, связанных с воспалительным или пролиферативным ответом, например ревматоидного артрита, заболеваний сердечно-сосудистой и нервной системы, астмы, псориаза. На данный момент известно о существовании свыше 400 видов заболеваний человека, непосредственно или опосредованно связанных с протеинкиназой, что делает протеинкиназу еще одной важной мишенью для лекарственных средств после сопряженных с G-белком рецепторов.
Большое семейство протеинкиназ состоит из более чем 500 членов, которое обычно подразделяют на два класса, а именно протеинтирозинкиназы (РТК) и серин-треонинкиназы. По расположению киназ в клетках их классифицируют на рецепторные киназы и нерецепторные киназы, также называемые внутриклеточными киназами. Рецепторные киназы главным образом принадлежат к тирозинкиназам, также называемым рецепторными тирозинкиназами (RTK). Такие рецепторные киназы состоят из внеклеточной части, трансмембранной области и внутриклеточной части. Часть киназы, обладающая каталитической активностью, находится в цитоплазме. Подавляющее большинство серин-треонинкиназ находится внутри клетки и принадлежит к нерецепторным киназам, также называемым цитоплазматическими киназами.
Типичными представителями семейства RTK являются рецепторы факторов роста, которые могут быть разделены на по меньшей мере 19 подсемейств. Главными подсемействами являются следующие:
(а) рецепторные тирозинкиназы семейства HER, включая EGFR (рецептор эпителиального фактора роста), HER2, HER3 и HER4. EGFR является мишенью синтетических низкомолекулярных лекарственных средств Tarceva®, Tykerb® и моноклонального антитела Erbitux® для лечения немелкоклеточного рака легких;
(б) подсемейство, состоящее из рецептора инсулина (IR), рецептора инсулиноподобного фактора роста 1 (IGF-1R) и рецептора, родственного инсулиновому рецептору (IRR), где IGF-1R является хорошо известной мишенью противораковой терапии, однако поскольку он чрезвычайно похож на IR, особенно во внутриклеточной части киназы, в которой аминокислотная последовательность на 100% идентична соответствующей аминокислотной последовательности IR, также может ингибироваться активность IGF-1R, в то время как обычно ингибируется активность IR. Доказано, что IR также является эффективной мишенью противораковой терапии. Однако необходимо найти баланс между эффективностью и допускаемым риском при использовании ингибиторов IR против рака из-за того, что ингибирование IR ведет к появлению риска повышения уровня сахара в крови;
(в) семейство рецепторов фактора роста тромбоцитов (PDGFR), включая PDGFR-α, PDGFR-β, CSF1R, c-KIT и c-fms, где с-Kit также служит молекулярной мишенью лекарственного средства Gleevec® для лечения лейкоза, а также для лечения стромальных опухолей желудочно-кишечного тракта;
(г) семейство рецепторов фактора роста эндотелия сосудов (VEGFR), включая FLT1 (Fms-подобная тирозинкиназа 1 или VEGFR1), KDR (или VEGFR-2) и FLT4 (или VEGFR3), члены этого семейства являются молекулярными мишенями для Sutent® и Naxavar®;
(д) семейство рецепторов фактора роста фибробластов (FGFR), включая FGFR1, FGFR2, FGFR3 и FGFR4, а также 7 лигандов FGF1, FGF2, FGF3, FGF4, FGF5, FGF6 и FGF7, члены этого семейства являются молекулярными мишенями для лекарственных средств, в настоящее время проходящих клинические испытания;
(е) семейство МЕТ, включая c-Met, также называемый рецептором фактора роста гепатоцитов человека (hHGFR), и RON, где c-Met играет важную роль в росте и метастазировании первичной опухоли. Лекарственные средства, нацеленные на членов семейства МЕТ, в настоящее время все еще проходят клинические испытания;
(ж) семейство RET. RET представляет собой рецептор членов семейства GDNF, имеющих изоформы RET51, RET43 и RET9. Лекарственные средства, нацеленные на членов семейства RET, в настоящее время все еще проходят клинические испытания;
(з) семейство Eph, которое является самым большим семейством рецепторных тирозинкиназ и состоит из 16 рецепторов (ЕРНА1, ЕРНА2, ЕРНА3, ЕРНА4, ЕРНА5, ЕРНА6, ЕРНА7, ЕРНА8, ЕРНА9, ЕРНА10, ЕРНВ1, ЕРНВ2, ЕРНВ3, ЕРНВ4, ЕРНВ5, ЕРНВ6) и 9 лигандов (EFNA1, EFNA2, EFNA3, EFNA4, EFNA5, EFNB1, EFNB2, EFNB3). Члены этого семейства играют важную роль в развитии животных, и некоторые из них играют роль в опухолевых процессах.
AXL представляет собой еще одну важную рецепторную тирозинкиназу. AXL также известна как UFO/ARK/Tyro, а ее лиганд представляет собой витамин K-зависимый ростовой стимулирующий фактор GAS6. AXL впервые обнаружена как трансформирующий ген при хроническом миелогенном лейкозе (CML). AXL сверхэкспрессируется при метастатическом раке толстой кишки, раке щитовидной железы, раке молочной железы, раке предстательной железы и меланоме. Ингибирование активности AXL может играть роль в ингибировании клеточного роста, пролиферации и метастазах.
Нерецепторные киназы не имеют внеклеточной части и трансмембранной области, а вся киназа находится в цитоплазме. На настоящий момент известно, что существует по меньшей мере 24 вида нерецепторных киназ, которые подразделяют на 11 подсемейств, а именно подсемейства Src, Frk, Btk, CsK, Abl, Zap70, Fes, Fps, Fak, Jak и AcK. Подсемейство Src является самым большим и включает киназы Src, Yes, Fyn, Lyn, Lck, Blk, Hck, Fgr, AUR1, AUR2 и Yrk. Для более подробной информации см. Neet, К.; Hunter, Т. Genes to Cells 1996, 1, 147-169, и документы, упомянутые там. Хотя некоторые нерецепторные киназы принадлежат тирозинкиназам, большинство нерецепторных киназ являются серин-треонинкиназами. Некоторые их члены являются молекулярными мишенями лекарственных средств Gleevec® и Sprycel® для лечения лейкоза.
Как указано выше, при клиническом и практическом применении было доказано, что рецепторные киназы и нерецепторные киназы являются мишенями противоопухолевой терапии, и некоторые противоопухолевые лекарственные средства разрешены к продаже на рынке для лечения пациентов. Кроме лечения опухолей ингибирование аномальной активности рецепторных киназ и нерецепторных киназ также может быть использовано для лечения следующих заболеваний, которые включают: псориаз, или serpedo, цирроз, диабет, заболевания, связанные с ангиогенезом, заболевания, связанные с рестенозом, заболевания глаз, возрастную дегенерацию желтого пятна, ревматоидный артрит и другие воспалительные заболевания, заболевания иммунной системы, такие как аутоиммунные заболевания, сердечно-сосудистые заболевания, такие как атеросклероз, или заболевание почек, но не ограничиваются ими. Таким образом, необходимо продолжать разработки ингибиторов этих киназ.
Гистондеацетилаза (HDAC) представляет класс ферментов, повсеместно обнаруживаемых в бактериях, грибах, растениях и животных, роль которой заключается в удалении ацетила из аминогрупп N-концевых лизиновых остатков гистонового ядра, что усиливает объединение N-концевого положительно заряженного гистонового ядра с отрицательно заряженной ДНК и тем самым предотвращает транскрипционный алгоритм от контактирования с ДНК-матрицей. Согласно их гомологии с белками грибов гистондеацетилазы (HDAC) подразделяют на четыре класса: класс I включает HDAC1, HDAC2, HDAC3 и HDAC8, которые гомологичны белку грибов RPD3; класс II включает HDAC4, HDAC5, HDAC7 и HDAC9, которые гомологичны белку грибов HDA1; класс IIа включает HDAC6 и HDAC10, содержащие две каталитические точки; класс IV включает HDAC11, каталитический центр которого содержит аминокислотные остатки, относящиеся к классу I и II HDAC. Каталитические сайты 11HDAC изоформ имеют ионы цинка и могут ингибироваться соединениями гидроксамовых кислот, такими как SAHA (Vorinostat), трихостатин A (TSA). Ингибиторы HDAC в качестве стабилизаторов настроения и противоэпилептических лекарственных средств имеют длинную историю применения в психиатрии и неврологии. Ингибиторы HDAC изучаются для применения в лечении нейродегенеративных заболеваний, таких как болезнь Альцгеймера, болезнь Гентингтона, болезнь Паркинсона. Еще один большой класс применений ингибиторов HDAC используется в качестве противораковых лекарственных средств, репрезентативный пример которого представляет собой Vorinostat, разработанный фирмой Merck, который одобрен FDA для лечения метастатической кожной T-клеточной лимфомы (CTCL) в 2006 году. Лечение других опухолей, включающих солидные опухоли и лейкоз, ингибиторами HDAC находится в стадии клинических испытаний.
Краткое изложение сущности изобретения
Задача настоящего изобретения состоит в том, чтобы предложить хинолил-содержащее соединение гидроксамовой кислоты, обладающее ингибирующей активностью в отношении протеинкиназы и/или гистондеацетилазы, и также способ его получения.
Также в задачу настоящего изобретения входит применение вышеуказанного хинолил-содержащего соединения гидроксамовой кислоты для изготовления фармацевтической композиции для лечения заболеваний, связанных с аномальной активностью протеинкиназы и/или гистондеацетилазы.
Также в задачу настоящего изобретения входит предложение фармацевтической композиции, включающей указанную хинолил-содержащую гидроксамовую кислоту, способную лечить заболевания, связанные с аномальной активностью протеинкиназы и/или гистондеацетилазы.
Подробное описание изобретения
Предложено хинолил-содержащее соединение гидроксамовой кислоты, имеющее молекулярную структуру, представленную следующей ниже формулой (I):
где
каждый из V1 и V2 независимо представляет собой водород, галоген, группу -OCF3, -CF3, -NO2, -CN, -ОН, -NH2, -NMe2, С1-6алкил, С2-6алкенил, С2-6алкинил, С3-6циклоалкил, С3-12гетероалициклил, С1-6алкокси, С3-6циклоалкилокси или С3-12гетероалициклилокси;
один из R и R′ представляет собой группу Q, содержащую гидроксамовую кислоту, а другой представляет собой водород, метокси, метоксиэтокси или группу Q, содержащую гидроксамовую кислоту,
где группа Q, содержащая гидроксамовую кислоту, представлена формулой
А представляет собой О, NH, S(=O)m, С1-6алкил, или А отсутствует, и водород в А может быть замещен G1;
L представляет собой С1-6алкил, С2-6алкенил, С2-6алкинил, С3-6циклоалкил, С6арил, С5-6гетероарил, С3-12гетероалициклил, или L отсутствует, и водород в L может быть замещен G2;
J представляет собой О, NH, S(=O)m, С1-6алкил, С2-6алкенил, С2-6алкинил, С3-6циклоалкил, С6арил, С5-6гетероарил, С3-12гетероалициклил, или J отсутствует, и водород в J может быть замещен G3;
X представляет собой -С(=O)-, -S(O)m, С1-6алкил, С2-6алкенил, С2-6алкинил, С3-6циклоалкил, С6арил, С5-6гетероарил, С3-12гетероалициклил, или X отсутствует, и водород в X может быть замещен G4;
Y представляет собой С1-6алкил, С2-6алкенил, С2-6алкинил, С3-6циклоалкил, С6арил, С5-6гетероарил, С3-12гетероалициклил, или Y отсутствует, и водород в Y может быть замещен G5;
где
каждый из G1, G2, G3, G4 и G5 независимо представляет собой Н, -CN, - CF3, -СО2Н, галоген, С1-6алкил, С3-6циклоалкил, С2-6алкенил, С2-6алкинил, С6арил, С5-6гетероарил, С3-12гетероалициклил, R1O-, R1R2N-, R1S(=O)m-, R1R2NS(=O)m-, R3C(=O)-, R1R2NC(=O)-, R1OC(=O)-, R3C(=O)O-, R1R2NC(=O)O-, R3C(=O)NR1-, R1R2NC(=O)NR4-, R1OC(=O)NR4-, R1S(=O)mNR4-, R1R2NS(=O)mNR4-, R1R2NC(=NR5)NR4-, R1R2NC(=CHNO2)NR4-, R1R2NC(=N-CN)NR4-, R1R2NC(=NR5)-, R1S(=O)(=NR5)NR4- или R1R2NS(=O)(=NR5)-;
каждый из R1, R2, R3, R4 и R5 независимо представляет собой Н, С1-6алкил, С2-6алкенил, С2-6алкинил, С3-6циклоалкил, С6арил, С5-6гетероарил или С3-12гетероалициклил; когда R1 и R2 связаны с одним и тем же атомом азота, они могут образовывать С3-12гетероалициклильное кольцо вместе с атомом азота, к которому они присоединены, и это С3-12гетероалициклильное кольцо может дополнительно содержать один или более гетероатомов, выбранных из О, N, или S(=O)m; водород в R1, R2, R3, R4 и R5 может быть замещен галогеном, CN, С1-6алкилом или С3-6циклоалкилом;
m равен от 0 до 2.
Структура хинолил-содержащего соединения гидроксамовой кислоты представлена формулой (Ia) ниже:
где
каждый из V1 и V2 независимо представляет собой водород, галоген, группу -OCF3, -CF3, -CN, -NMe2, С1-6алкил, С3-6циклоалкил, С3-12гетероалициклил, С1-6алкокси, С3-6циклоалкилокси или С3-12гетероалициклилокси;
А представляет собой О, NH или S(=O)m, и водород в А может быть замещен G1;
L представляет собой С1-6алкил или С3-6циклоалкил, и водород в L может быть замещен G2;
J представляет собой О, NH или S(=O)m, и водород в J может быть замещен G3;
Y представляет собой С1-6алкил или С3-6циклоалкил, и водород в Y может быть замещен G5;
m равен от 0 до 2.
Структура хинолил-содержащего соединения гидроксамовой кислоты представлена формулой (Ib) ниже:
где
каждый из V1 и V2 независимо представляет собой водород, галоген, группу -OCF3, -CF3, -CN, -NMe2, С1-6алкил, С3-6циклоалкил, С3-12гетероалициклил, С1-6алкокси, С3-6циклоалкилокси или С3-12гетероалициклилокси;
А представляет собой О, NH или S(=O)m, и водород в А может быть замещен G1;
L представляет собой С1-6алкил, и водород в L может быть замещен G2;
J представляет собой С3-6циклоалкил или С3-12гетероалициклил, и водород в J может быть замещен G3;
X представляет собой -С(=O)-, S(=O)m, или X отсутствует;
Y представляет собой С1-6алкил или С3-6циклоалкил, и водород в Y может быть замещен G5;
m равен от 0 до 2.
Структура хинолил-содержащего соединения гидроксамовой кислоты представлена формулой (Ic) ниже:
где
каждый из V1 и V2 независимо представляет собой водород, галоген, группу -OCF3, -CF3, -CN, -NMe2, С1-6алкил, С3-6циклоалкил, С3-12гетероалициклил, С1-6алкокси, С3-6циклоалкилокси или С3-12гетероалициклилокси;
А представляет собой О, NH или S(=O)m, и водород в А может быть замещен G1;
L представляет собой С1-6алкил или С3-6циклоалкил, и водород в L может быть замещен G2;
J представляет собой О, NH или S(=O)m, и водород в J может быть замещен G3;
Y представляет собой С1-6алкил или С3-6циклоалкил, и водород в Y может быть замещен G5;
m равен от 0 до 2.
Структура хинолил-содержащего соединения гидроксамовой кислоты представлена формулой (Id) ниже:
где
каждый из V1 и V2 независимо представляет собой водород, галоген, группу -OCF3, -CF3, -CN, -NMe2, С1-6алкил, С3-6циклоалкил, С3-12гетероалициклил, С1-6алкокси, С3-6циклоалкилокси или С3-12гетероалициклилокси;
А представляет собой О, NH или S(=O)m, и водород в А может быть замещен G1;
L представляет собой С1-6алкил, и водород в L может быть замещен G2;
J представляет собой С3-6циклоалкил или С3-12гетероалициклил, и водород в J может быть замещен G3;
X представляет собой -С(=O)-, S(=O)m, или X отсутствует;
Y представляет собой С1-6алкил или С3-6циклоалкил, и водород в Y может быть замещен G5;
m равен от 0 до 2.
Структура хинолил-содержащего соединения гидроксамовой кислоты представлена формулой (Ie) ниже:
где
каждый из V1 и V2 независимо представляет собой водород, галоген, группу -OCF3, -CF3, -CN, -NMe2, С1-6алкил, С3-6циклоалкил, С3-12гетероалициклил, С1-6алкокси, С3-6циклоалкилокси или С3-12гетероалициклилокси;
L представляет собой С1-6алкил или С3-6циклоалкил, и водород в L может быть замещен G2;
Y представляет собой С1-6алкил или С3-6циклоалкил, и водород в Y может быть замещен G5.
Структура хинолил-содержащего соединения гидроксамовой кислоты представлена формулой (If) ниже:
где
каждый из V1 и V2 независимо представляет собой водород, галоген, группу -OCF3, -CF3, -CN, -NMe2, С1-6алкил, С3-6циклоалкил, G3-12гетероалициклил, С1-6алкокси, С3-6циклоалкилокси или С3-12гетероалициклилокси;
Y представляет собой С1-6алкил или С3-6циклоалкил, и водород в Y может быть замещен G5.
Структура хинолил-содержащего соединения гидроксамовой кислоты представлена формулой (Ig) ниже:
где
каждый из V1 и V2 независимо представляет собой водород, галоген, группу -OCF3, -CF3, -CN, -NMe2, С1-6алкил, С3-6циклоалкил, С3-12гетероалициклил, С1-6алкокси, С3-6циклоалкилокси или С3-12гетероалициклилокси;
L представляет собой С1-6алкил или С3-6циклоалкил, и водород в L может быть замещен G2.
Структура хинолил-содержащего соединения гидроксамовой кислоты представлена формулой (Ih) ниже:
где
каждый из V1 и V2 независимо представляет собой водород, галоген, группу -OCF3, -CF3, -CN, -NMe2, С1-6алкил, С3-6циклоалкил, С3-12гетероалициклил, С1-6алкокси, С3-6циклоалкилокси или С3-12гетероалициклилокси;
L представляет собой С1-6алкил или С3-6циклоалкил, и водород в L может быть замещен G2.
Структура хинолил-содержащего соединения гидроксамовой кислоты представлена формулой (Ii) ниже:
где
каждый из V1 и V2 независимо представляет собой водород, галоген, группу -OCF3, -CF3, -CN, -NMe2, С1-6алкил, С3-6циклоалкил, С3-12гетероалициклил, С1-6алкокси, С3-6циклоалкилокси или С3-12гетероалициклилокси;
Y представляет собой С1-6алкил или С3-6циклоалкил, и водород в Y может быть замещен G5.
Хинолил-содержащее соединение гидроксамовой кислоты представляет собой любое из следующих соединений:
N1′-[3-фтор-4-[[7-[[1-[2-(гидроксиамино)-2-оксоэтил]-4-пиперидинил]-метокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[3-[[2-(гидроксиамино)-2-оксоэтил]амино]пропокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[3-[[3-(гидроксиамино)-3-оксопропил]амино]пропокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[2-(гидроксиамино)-2-оксоэтокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[3-(гидроксиамино)-3-оксопропокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[4-(гидроксиамино)-4-оксобутокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[5-(гидроксиамино)-5-оксопентилокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[6-(гидроксиамино)-6-оксогексилокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[7-(гидроксиамино)-7-оксогептилокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[6-[[1-[2-(гидроксиамино)-2-оксоэтил]-4-пиперидинил]-метокси]-7-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[6-[3-[[2-(гидроксиамино)-2-оксоэтил]амино]пропокси]-7-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[6-[3-[[3-(гидроксиамино)-3-оксопропил]амино]пропокси]-7-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[6-[2-(гидроксиамино)-2-оксоэтокси]-7-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[6-[3-(гидроксиамино)-3-оксопропокси]-7-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[6-[4-(гидроксиамино)-4-оксобутокси]-7-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[6-[5-(гидроксиамино)-5-оксопентилокси]-7-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[6-[6-(гидроксиамино)-6-оксогексилокси]-7-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[6-[7-(гидроксиамино)-7-оксогептилокси]-7-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[[1-[2-(гидроксиамино)-2-оксоэтил]-4-пиперидинил]метокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[3-[[2-(гидроксиамино)-2-оксоэтил]амино]-пропокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[3-[[3-(гидроксиамино)-3-оксопропил]амино]-пропокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[2-(гидроксиамино)-2-оксоэтокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[3-(гидроксиамино)-3-оксопропокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[4-(гидроксиамино)-4-оксобутокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[5-(гидроксиамино)-5-оксопентилокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[6-(гидроксиамино)-6-оксогексилокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[7-(гидроксиамино)-7-оксогептилокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[6-[[1-[2-(гидроксиамино)-2-оксоэтил]-4-пиперидинил]метокси]-7-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[6-[3-[[2-(гидроксиамино)-2-оксоэтил]амино]-пропокси]-7-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[6-[3-[[3-(гидроксиамино)-3-оксопропил]амино]-пропокси]-7-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[6-[2-(гидроксиамино)-2-оксоэтокси]-7-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[6-[3-(гидроксиамино)-3-оксопропокси]-7-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[6-[4-(гидроксиамино)-4-оксобутокси]-7-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[6-[5-(гидроксиамино)-5-оксопентилокси]-7-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[6-[6-(гидроксиамино)-6-оксогексилокси]-7-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[6-[7-(гидроксиамино)-7-оксогептилокси]-7-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид.
Хинолил-содержащее соединение гидроксамовой кислоты предпочтительно представляет собой любое из следующих соединений:
N1′-[3-фтор-4-[[7-[[1-[2-(гидроксиамино)-2-оксоэтил]-4-пиперидинил]-метокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[3-[[2-(гидроксиамино)-2-оксоэтил]амино]пропокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[3-[[3-(гидроксиамино)-3-оксопропил]амино]пропокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[2-(гидроксиамино)-2-оксоэтокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[3-(гидроксиамино)-3-оксопропокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[4-(гидроксиамино)-4-оксобутокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[5-(гидроксиамино)-5-оксопентилокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[6-(гидроксиамино)-6-оксогексилокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[7-(гидроксиамино)-7-оксогептилокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[[1-[2-(гидроксиамино)-2-оксоэтил]-4-пиперидинил]метокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[3-[[2-(гидроксиамино)-2-оксоэтил]амино]-пропокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[3-[[3-(гидроксиамино)-3-оксопропил]амино]-пропокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[2-(гидроксиамино)-2-оксоэтокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[3-(гидроксиамино)-3-оксопропокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[4-(гидроксиамино)-4-оксобутокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[5-(гидроксиамино)-5-оксопентилокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[6-(гидроксиамино)-6-оксогексилокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[7-(гидроксиамино)-7-оксогептилокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид.
Хинолил-содержащее соединение гидроксамовой кислоты более предпочтительно представляет собой любое из следующих соединений:
N1′-[3-фтор-4-[[7-[[1-[2-(гидроксиамино)-2-оксоэтил]-4-пиперидинил]-метокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[4-(гидроксиамино)-4-оксобутокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[5-(гидроксиамино)-5-оксопентилокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-[3-фтор-4-[[7-[6-(гидроксиамино)-6-оксогексилокси]-6-метокси-4-хинолил]окси]фенил]-N1-(4-фторфенил)циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[[1-[2-(гидроксиамино)-2-оксоэтил]-4-пиперидинил]метокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[4-(гидроксиамино)-4-оксобутокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[5-(гидроксиамино)-5-оксопентилокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид;
N1′-(4-фторфенил)-N1-[4-[[7-[6-(гидроксиамино)-6-оксогексилокси]-6-метокси-4-хинолил]окси]фенил]циклопропан-1,1-дикарбоксамид.
Рацематы или энантиомеры любого из вышеупомянутых хинолил-содержащих соединений гидроксамовой кислоты охватываются настоящим изобретением.
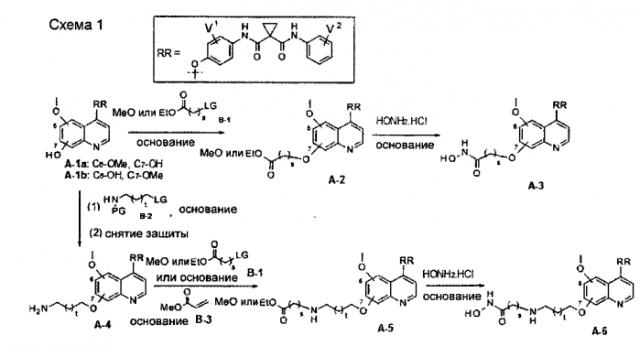
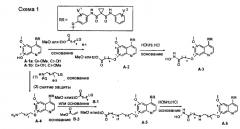
Один из способов получения хинолил-содержащего соединения гидроксамовой кислоты заключается в осуществлении стадий, показанных на Схеме 1:
где
t равен от 0 до 6;
s равен от 1 до 10;
каждый из V1 и V2 независимо представляет собой водород, галоген, группу -OCF3, -CF3, -CN, -NMe2, С1-6алкил, С3-6циклоалкил, С3-12гетероалициклил, С1-6алкокси, С3-6циклоалкилокси или С3-12гетероалициклилокси;
LG представляет собой общепринятую в области органической химии уходящую группу и представляет собой любую из F, Cl, Br, I, MsO, TsO или TfO;
PG представляет собой общепринятую в области органической химии защитную группу и представляет собой Boc или CBZ.
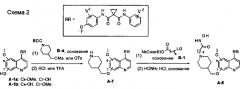
Один из способов получения хинолил-содержащего соединения гидроксамовой кислоты заключается в осуществлении стадий, показанных на Схеме 2:
каждый из V1 и V2 независимо представляет собой водород, галоген, группу -OCF3, -CF3, -CN, -NMe2, С1-6алкил, С3-6циклоалкил, С3-12гетероалициклил, С1-6алкокси, С3-6циклоалкилокси или С3-12гетероалициклилокси;
s равен от 1 до 10.
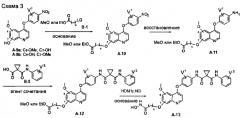
Один из способов получения хинолил-содержащего соединения гидроксамовой кислоты заключается в осуществлении стадий, показанных на Схеме 3:
каждый из V1 и V2 независимо представляет собой водород, галоген, группу -OCF3, -CF3, -CN, -NMe2, С1-6алкил, С3-6циклоалкил, С3-12гетероалициклил, С1-6алкокси, С3-6циклоалкилокси или С3-12гетероалициклилокси;
s равен от 1 до 10.
В данной заявке предложено применение фармацевтической композиции, включающей хинолил-содержащее соединение гидроксамовой кислоты, для лечения заболеваний, вызванных аномальной активностью протеинкиназы и/или гистондеацетилазы.
В применении фармацевтической композиции, содержащей соединение по настоящему изобретению, протеинкиназа представляет собой ALK, AXL, ВТК, CDK11, c-Met, KDR, VEGFR2, RET, PDGFR-α, PDGFR-β, c-KIT, Flt3, MEK1, MEK2, CSF1R, EPHA2, MKNK2, TIE2, TRKA, SRC, PLK4, RON, EGF1R, HER2, HER3, HER4, PDGFR-α, c-fms, FLT1, Src, Frk, Btk, CsK, Abl, Fes, Fps, Fak, AcK, Yes, Fyn, Lyn, Lck, Hck, Fgr, Yrk, PDK1, TAK1, Tie-1, YSK4, TRK B, TRK C, SLK, PKN2, MST1R, MAP4K или DDR2.
Предпочтительно в применении фармацевтической композиции, содержащей соединение по настоящему изобретению, протеинкиназа представляет собой ALK, AXL, ВТК, CDK11, c-Met, KDR, VEGFR2, RET, PDGFR-α, PDGFR-β, c-KIT, Flt3, MEK1, MEK2, CSF1R, EPHA2, MKNK2, TIE2, TRKA, SRC или PLK4.
В применении фармацевтической композиции, содержащей соединение по настоящему изобретению, гистондеацетилаза представляет собой HDAC2, HDAC6, HDAC1, HDAC3, HDAC4, HDAC5, HDAC7, HDAC8, HDAC9, HDAC10 или HDAC11.
Предпочтительно в применении фармацевтической композиции, содержащей соединение по настоящему изобретению, гистондеацетилаза представляет собой HDAC2 и/или HDAC6.
В применении фармацевтической композиции, содержащей соединение по настоящему изобретению, заболевание представляет собой псориаз, цирроз, диабет, опосредованное ангиогенезом заболевание, заболевания глаза, заболевание иммунной системы, сердечно-сосудистое заболевание, эпилепсию, нейродегенеративное заболевание, болезнь Альцгеймера, болезнь Гентингтона или болезнь Паркинсона.
В применении фармацевтической композиции, содержащей соединение по настоящему изобретению, заболевание представляет собой опухоль, включая солидные опухоли и жидкие опухоли.
В применении фармацевтической композиции, содержащей соединение по настоящему изобретению, опухоль, в частности, включает одну из следующих опухолей или любую их комбинацию: рак легкого, рак кости, рак поджелудочной железы, рак кожи, рак головы и шеи, меланому кожи или внутриглазную меланому, рак матки, рак яичника, рак прямой кишки, рак анальной области, рак желудка, рак ободочной кишки, рак молочной железы, рак фаллопиевой трубы, рак эндометрия, рак шейки матки, рак влагалища, рак вульвы, болезнь Ходжкина, рак пищевода, рак тонкой кишки, рак эндокринной системы, рак щитовидной железы, рак паращитовидной железы, саркому мягкой ткани, рак уретры, рак полового члена, рак предстательной железы, хронический или острый лейкоз, рак мочевого пузыря, рак почки или мочеточника, почечный рак, опухоли центральной нервной системы (ЦНС), опухоли спинного мозга, аденомы гипофиза, желудочно-кишечные стромальные опухоли, колоректальный рак, немелкоклеточный рак легкого, мелкоклеточный рак легкого, мастоцитоз, глиому, саркому и лимфому.
В настоящей заявке предложена фармацевтическая композиция для лечения заболеваний, вызванных аномальной активностью протеинкиназы и/или гистондеацетилазы, содержащая любое одно или комбинацию из указанных выше соединений по настоящему изобретению или их фармацевтически приемлемые соли, сольваты или пролекарства, либо рацематы или энантиомеры любого одного или комбинации из указанных выше соединений или их фармацевтически приемлемых солей, сольватов или пролекарств.
Фармацевтическая композиция по настоящему изобретению может дополнительно содержать один или более фармацевтически приемлемых носителей.
Лекарственная форма любой из фармацевтических композиций по настоящему изобретению является следующей:
(1) пероральная форма; (2) инъекционная форма; (3) форма ректального суппозитория; (4) форма для назальной ингаляции; (5) форма глазных капель и (6) форма кожного пластыря.
Ряд экспериментов подтверждает, что хинолил-содержащее соединение гидроксамовой кислоты по настоящему изобретению обладает следующими преимуществами: (1) скрининговые тесты ингибирования активности киназы и/или гистондеацетилазы показывают, что соединения по настоящему изобретению оказывают сильное ингибирующее действие на ряд протеинкиназ и их мутантов и гистондеацетилазу; (2) тесты по ингибированию опухоли на животных моделях показывают, что такое хинолил-содержащее соединение гидроксамовой кислоты значительно ингибирует рост опухолей без видимой токсичности; (3) соединения по настоящему изобретению могут быть использованы в комбинации с другими противоопухолевыми лекарственными средствами таким образом, чтобы оказывать синергетический или аддитивный эффект; (4) соединения по настоящему изобретению могут быть использованы совместно с другими видами терапии опухолей, например радиотерапией, интервенционной терапией. Таким образом, хинолил-содержащее соединение гидроксамовой кислоты по изобретению может быть использовано в качестве эффективного лекарственного средства для лечения заболеваний, вызванных аномальной активностью протеинкиназы и/или гистондеацетилазы.
В применении соединений по изобретению для лечения заболеваний, вызванных аномальной активностью протеинкиназы и/или гистондеацетилазы, почечный рак представляет собой рак надпочечника, почечно-клеточную карциному или карциному почечной лоханки; и глиома представляет собой нейроглиому ствола головного мозга, нейроэндокринную глиому и нейроспонгиобластому.
В применении соединений по изобретению для лечения заболеваний, вызванных аномальной активностью протеинкиназы и/или гистондеацетилазы, помимо опухолей заболевания могут представлять собой псориаз, цирроз, диабет, связанные с ангиогенезом заболевания, связанные с рестенозом заболевания, заболевания глаза, такие как AMD (возрастная макулярная дегенерация), ревматоидный артрит и другие воспалительные заболевания, заболевания иммунной системы, такие как аутоиммунное заболевание (например СПИД и тому подобное), сердечно-сосудистые заболевания, такие как атеросклероз, почечные заболевания, эпилепсию, нейродегенеративные заболевания, такие как болезнь Альцгеймера, болезнь Гентингтона, болезнь Паркинсона и тому подобное.
Фармацевтическая композиция, содержащая соединение по настоящему изобретению, может быть использована для лечения заболеваний, вызванных аномальной активностью протеинкиназ и/или гистондеацетилазы у млекопитающего, такого как человек.
Посредством спо