Сконструированные клетки, экспрессирующие множественные иммуномодуляторы, и их применения
Иллюстрации
Показать всеНастоящее изобретение относится к области биотехнологии и может быть использовано для рекомбинантной экспрессии иммуномодуляторных белков. Конструируют вектор, содержащий полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, которая функционально связана с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, и (2) полинуклеотид, кодирующий полипептид IL-12 и один или более иммуномодуляторных полипептидов, выбранных из IL-2, IL-7, IL-15, IL-18, IL-21, GM-CSF, CCL3 (MIP-1a), CCL5 (RANTES), CCL7 (MCP3), XCL1 (лимфотактин), CCL19 (MIP-3b), CXCL9 (MIG), CXCL10 (IP-10), CXCL12 (SDF-1), CCL21 (6Ckine) или TNF-альфа. Изобретение позволяет использовать вектор для управляемой экспрессии иммуномодуляторных белков. 4 н. и 8 з.п. ф-лы, 9 ил., 4 табл., 2 пр.
Реферат
ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка испрашивает приоритет предварительной заявки США, номер 61/103,810, поданной 8 октября 2008 г., которая настоящим полностью включена в данную заявку посредством ссылки.
ССЫЛКА НА ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ, ПРИЛОЖЕННЫЙ В ЭЛЕКТРОННОМ ВИДЕ ПОСРЕДСТВОМ СИСТЕМЫ EFS-WEB
[0002] Содержание приложенного в электронном виде перечня последовательностей (название: sequence listing.ST25.txt; размер: 213102 байта; дата создания: 8 октября 2009 г.), поданного вместе с настоящей заявкой, полностью включено в данную заявку посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
Область техники
[0003] Настоящее изобретение относится к области генной терапии, направленной на лечение заболеваний и расстройств, таких как рак. В одном варианте реализации настоящее изобретение обеспечивает конструирование иммунных клеток или вспомогательных клеток для терапии (TSC) таким образом, чтобы они экспрессировали один или более иммуномодуляторов, и применение указанных клеток в качестве лекарственного средства.
Уровень техники
[0004] Интерлейкин-12 (IL-12) представляет собой член семейства цитокинов I типа, который участвует во множестве биологических процессов, включая защитный иммунный ответ и подавление онкогенеза, но не ограничивается ими (Abdi и др., 2006; Adorini, 1999; Adorini, 2001; Adorini и др., 2002; Adorini и др., 1996; Akhtar и др., 2004; Akiyama и др., 2000; Al-Mohanna и др., 2002; Aliberti и др., 1996; Allavena и др., 1994; Alii и Khar, 2004; Alzona и др., 1996; Amemiya и др., 2006; Araujo и др., 2001; Arulanandam и др., 1999; Athie и др., 2000; Athie-Morales и др., 2004; Bertagnolli и др., 1992; Bhardwaj и др., 1996; Biedermann и др., 2006; Brunda и Gately, 1994; Buchanan и др., 1995; Romani и др., 1997; Rothe и др., 1996; Satoskar и др., 2000; Schopfn др., 1999; Thomas и др., 2000; Tsung и др., 1997; Wolf и др., 1994; Yuminamochi и др., 2007). Все большее число полученных данных позволяет предположить, что IL-12 может представлять собой перспективную мишень для борьбы с заболеваниями человека (например, раком).
[0005] Несмотря на тот факт, что IL-12 остается перспективным агентом для терапии рака, благодаря наличию сильного вспомогательного действия на противоопухолевые клетки NK 1 типа, CD4+ Т-клетки и CD8+ Т-клетки (Trinchieri, 2003), описанная токсичность рекомбинантного IL-12 человека (rhIL-12) у пациентов (Atkins и др., 1997), а также ограниченное количество источников, из которых можно получить rhIL-12 со степенью чистоты, удовлетворяющей требованиям GMP для клинического применения, создают препятствия для успешного применения терапевтических подходов, основанных на IL-12. Таким образом, возможно геннотерапевтические подходы могут представлять собой более безопасные, более надежные варианты лечения. Действительно, в I фазе клинических испытаний введение рекомбинантной кДНК IL-12 на основе вируса внутрь опухоли или рядом с ней (Sangro и др., 2004; Triozzi и др., 2005) или плазмиды (Heinzeriing и др., 2005), или аутологических фибробластов, модифицированных геном IL-12 (Kang и др., 2001), оказалась безопасной и хорошо переносимой.
[0006] Тем не менее, объективные клинические ответы пациентов, страдающих меланомой или разнообразными формами карцином, которые получали данные геннотерапевтические средства, были редкими, переменными, временными и преимущественно сосредоточенными в месте введения лекарственного средства (Heinzeriing и др., 2005; Kang и др., 2001; Sangro и др., 2004; Triozzi и др., 2005). В случаях, когда наблюдалось частичное или полное излечение от заболевания, отмечали повышенную встречаемость инфильтрирующих опухоль лимфоцитов (Heinzeriing и др., 2005; Sangro и др., 2004) и повышенные уровни опухолеспецифических CD8+ Т-клеток в кровотоке (Heinzeriing и др., 2005), что согласуется с улучшенным примированием перекрестнореагирующим антигеном антигенспецифических Т-клеток у таких пациентов.
[0007] Поскольку примирование перекрестнореагирующим антигеном специфических Т-клеток лучше всего осуществляют дендритные клетки (DC), которые служат природным, хотя и регулируемым, источником IL-12 (Berard и др., 2000), недавние сообщения о превосходной доклинической эффективности основанной на дендритных клетках генной терапии IL-12 представляли огромный интерес (Satoh и др., 2002; Tatsumi и др., 2003; Yamanaka и др., 2002). Например, было показано, что внутриопухолевая (i.t.) инъекция DC, сконструированных таким образом, что они продуцировали IL-12p70 (путем инфекции рекомбинантным аденовирусом), приводит к значительному улучшению примирования перекрестнореагирующим антигеном набора опухолеспецифических CD8+ Т-клеток широкого спектра действия и к отторжению опухоли в моделях на мышах (Tatsumi и др., 2003). С учетом предыдущего применения рекомбинантного аденовируса, кодирующего mIL-12 под контролем промотора CMV (rAd.cIL12, (Tatsumi и др., 2003)), продуцирование IL-12 сконструированными DC было конститутивным, следовательно, иммунологическое действие данного цитокина, направленное сначала на повреждение опухоли, а затем на дренирующие опухоль лимфатические узлы, невозможно предугадать по отношению к результату терапии. Таким образом, существует потребность в DC, сконструированных для экспрессии IL-12 при определенных условиях, с целью регуляции как уровня экспрессии трансгена, так и момента активации трансгена. Настоящее изобретение обеспечивает многообещающий результат терапии при применении таких клеток.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0008] Настоящее изобретение обеспечивает рекомбинантный вектор, кодирующий белок (белки), обладающий (обладающие) функцией (функциями) одного или нескольких иммуномодуляторов, под контролем одного или нескольких промоторов. В одном варианте реализации настоящего изобретения, один или более промоторов являются промоторами, функционирующими при определенных условиях. В другом варианте реализации настоящего изобретения, один или более промоторов являются конститутивными. В другом варианте реализации настоящего изобретения, вектор представляет собой аденовирусный вектор, кодирующий белок (белки), экспрессия которого (которых) запускается промотором, который может быть активирован при определенных условиях путем обеспечения растворимого низкомолекулярного лиганда, такого как диацилгидразины (например, RG-115819, RG-115830 или RG-115932). Такой вектор позволяет контролировать экспрессию указанного белка (белков) иммунными клетками и TSC.
[0009] В одном варианте реализации, настоящее изобретение обеспечивает вектор для определяемой условиями экспрессии белка(белков), обладающего функцией (функциями) одного или нескольких иммуномодуляторов, содержащий полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид, кодирующий генный переключатель, содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, и (2) полинуклеотид, кодирующий один или более белков, обладающих функцией иммуномодулятора, связанный с промотором, который активируется указанным лиганд-зависимым фактором транскрипции. В одном варианте реализации настоящего изобретения, иммуномодулятор выбирают из IL-1, IL-2, IL-3, IL-4, IL-5, IL-7, IL-8, IL-9, IL-10R DN или его субъединицы, IL-15, IL-18, IL-21, IL-23, IL-24, IL-27, GM-CSF, IFN-альфа, IFN-гамма, CCL3 (MIP-1a), CCL5 (RANTES), CCL7 (МСР3), ХСL1 (лимфотактина), CXCL1 (MGSA-альфа), CCR7, CCL19 (MIP-3b), CXCL9 (MIG), CXCL10 (IP-10), CXCL12 (SDF-1), CCL21 (6Ckine), OX40L, 4-1BBL, CD40, CD70, GITRL, LIGHT, b-дефензина, HMGB1, Flt3L, IFN-бета, TNF-альфа, dnFADD, TGF-альфа, РНКи PD-L1, антисмыслового олигонуклеотида PD-L1, TGFbRII DN, ICOS-L и S100.
[00010] В другом варианте реализации, настоящее изобретение обеспечивает вектор для экспрессии белка (белков), обладающего функцией (функциями) одного или нескольких иммуномодуляторов, и белка, обладающего функцией IL-12, содержащий полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, (2) полинуклеотид, кодирующий указанный белок(белки), обладающий функцией (функциями) одного или нескольких иммуномодуляторов, и (3) полинуклеотид, кодирующий белок, обладающий функцией IL-12; при этом по меньшей мере один полинуклеотид из (2) и (3) связан с промотором, который активируется лиганд-зависимым фактором транскрипции.
[00011] Настоящее изобретение дополнительно обеспечивает способ получения популяции клеток, например, иммунных клеток или TSC, экспрессирующих белок (белки), обладающие функцией (функциями) одного или нескольких иммуномодуляторов, путем модификации (например, трансфекции, электропорации и т.д.) указанных клеток рекомбинантным вектором, при определенных условиях экспрессирующим белок (белки), обладающий функцией (функциями) одного или нескольких иммуномодуляторов, при этом указанный вектор содержит полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, и (2) полинуклеотид, кодирующий один или более белков, обладающих функцией иммуномодулятора, связанный с промотором, который активируется указанным лиганд-зависимым фактором транскрипции.
[00012] В другом варианте реализации, настоящее изобретение обеспечивает способ получения популяции клеток, например, иммунных клеток или TSC, экспрессирующих белки, обладающие функцией (функциями) одного или нескольких иммуномодуляторов, и белок, обладающий функцией IL-12, путем модификации клеток рекомбинантным вектором, содержащим полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, (2) полинуклеотид, кодирующий указанный белок (белки), обладающий функцией (функциями) одного или нескольких иммуномодуляторов, и (3) полинуклеотид, кодирующий белок, обладающий функцией IL-12; при этом по меньшей мере один полинуклеотид из (2) и (3) связан с промотором, который активируется указанным лиганд-зависимым фактором транскрипции.
[00013] Настоящее изобретение дополнительно обеспечивает популяцию клеток, например, иммунных клеток или TSC, экспрессирующих белок (белки), обладающий функцией (функциями) одного или нескольких иммуномодуляторов, которая была модифицирована (например, путем трансфекции, электропорации и т.д.) рекомбинантным вектором, при определенных условиях экспрессирующим белок (белки), обладающий функцией (функциями) одного или нескольких иммуномодуляторов, при этом указанный вектор содержит полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, и (2) полинуклеотид, кодирующий один или более белков, обладающих функцией иммуномодулятора, связанный с промотором, который активируется указанным лиганд-зависимым фактором транскрипции.
[00014] В другом варианте реализации, настоящее изобретение обеспечивает популяцию клеток, например, иммунных клеток или TSC, экспрессирующих белки, обладающие функцией(ями) одного или нескольких иммуномодуляторов, и белок, обладающий функцией IL-12, которая была модифицирована рекомбинантным вектором, включающим полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность . фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, (2) полинуклеотид, кодирующий указанный белок (белки), обладающий функцией (функциями) одного или нескольких иммуномодуляторов, и (3) полинуклеотид, кодирующий белок, обладающий функцией IL-12; при этом по меньшей мере один полинуклеотид из (2) и (3) связан с промотором, который активируется указанным лиганд-зависимым фактором транскрипции.
[00015] В другом варианте реализации, настоящее изобретение обеспечивает композицию, содержащую две или более популяций клеток согласно настоящему изобретению, например, иммунных клеток или TSC, при этом каждая популяция клеток в указанной композиции экспрессирует один или более иммуномодуляторов, которые отличаются от одного или нескольких иммуномодуляторов, экспрессируемых другой популяцией (популяциями) клеток в указанной композиции. В одном варианте реализации, указанная композиция содержит две популяции клеток. В другом варианте реализации, композиция содержит более двух популяций клеток. В другом варианте реализации, композиция содержит три популяции клеток. В другом варианте реализации, композиция содержит четыре популяции клеток.
[00016] В другом варианте реализации, настоящее изобретение обеспечивает сконструированную in vitro клетку, например, иммунную клетку или TSC, содержащую вектор, включающий полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, и (2) полинуклеотид, кодирующий белок, обладающий функцией иммуномодулятора, связанный с промотором, который активируется указанным лиганд-зависимым фактором транскрипции. В другом варианте реализации, настоящее изобретение обеспечивает сконструированную in vitro клетку, например, иммунную клетку или TSC, содержащую вектор, включающий полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, (2) полинуклеотид, кодирующий белок, обладающий функцией иммуномодулятора, и (3) полинуклеотид, кодирующий белок, обладающий функцией IL-12; при этом по меньшей мере один полинуклеотид из (2) и (3) связан с промотором, который активируется указанным лиганд-зависимым фактором транскрипции.
[00017] В другом варианте реализации, настоящее изобретение обеспечивает композицию, содержащую две или более популяций сконструированных in vitro клеток, например, иммунных клеток или TSC, согласно настоящему изобретению, при этом каждая из популяций сконструированных in vitro клеток в композиции содержит вектор, содержащий полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, и (2) полинуклеотид, кодирующий белок, обладающий функцией иммуномодулятора, связанный с промотором, который активируется указанным лиганд-зависимьм фактором транскрипции, и при этом каждая популяция сконструированных in vitro клеток в композиции экспрессирует один или более иммуномодуляторов, которые отличаются от одного или нескольких иммуномодуляторов, экспрессируемых другой популяцией(ями) сконструированных in vitro клеток в указанной композиции. В одном варианте реализации, настоящее изобретение обеспечивает композицию, содержащую две или более популяций сконструированных т vitro клеток, например, иммунных клеток или TSC, при этом каждая из указанных популяций клеток содержит вектор, включающий полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, (2) полинуклеотид, кодирующий белок, обладающий функцией иммуномодулятора, и (3) полинуклеотид, кодирующий белок, обладающий функцией IL-12; при этом по меньшей мере один полинуклеотид из (2) и (3) связан с промотором, который активируется указанным лиганд-зависимым фактором транскрипции. В одном варианте реализации, указанная композиция содержит две популяции сконструированных in vitro клеток. В другом варианте реализации, композиция содержит более двух популяций сконструированных in vitro клеток. В другом варианте реализации, композиция содержит три популяции сконструированных in vitro клеток. В другом варианте реализации, композиция содержит четыре популяции сконструированных in vitro клеток.
[00018] Настоящее изобретение также обеспечивает фармацевтическую композицию, содержащую популяцию клеток, например, иммунных клеток или TSC, описанных в данной заявке.
[00019] В одном варианте реализации настоящего изобретения, полинуклеотид, кодирующий один или более белков, обладающих функциями иммуномодуляторов, находится под контролем промотора генного переключателя и полинуклеотид, кодирующий белок, обладающий функцией IL-12, находится под контролем конститутивного промотора. В другом варианте реализации настоящего изобретения, как полинуклеотид, кодирующий белок (белки), обладающий функцией иммуномодулятора(ов), так и полинуклеотид, кодирующий белок, обладающий функцией IL-12, находятся под контролем мультицистронного промотора генного переключателя. В другом варианте реализации настоящего изобретения, полинуклеотид, кодирующий белок (белки), обладающий функцией(ями) иммуномодулятора(ов), находится под контролем промотора генного переключателя и полинуклеотид, кодирующий белок, обладающий функцией IL-12, находится под контролем промотора, функционирующего в определенных условиях, который отличается от промотора генного переключателя. В дополнительном варианте реализации настоящего изобретения, система регуляции генов для полинуклеотида, кодирующего белок (белки), обладающий функцией(ями) иммуномодулятора(ов), и система регуляции генов для полинуклеотида, обладающего функцией IL-12, являются независимыми. В дополнительном варианте реализации настоящего изобретения, система регуляции генов для каждого полинуклеотида, кодирующего каждый белок, является независимой.
[00020] В одном варианте реализации, настоящее изобретение также обеспечивает лечение рака, такого как, меланомные опухоли, глиомные опухоли, рак почки и раки предстательной железы, а также раков, перечисленных в данной заявке в Таблице 1, но не ограничивается ими. Генотерапия IL-12 продемонстрировала противоопухолевую эффективность в исследованиях моделей на животных в виде вектора рекомбинантной кДНК (Faure и др., 1998; Sangro и др., 2005), но даже более того, в контексте генномодифицированных дендритных клеток (Satoh и др., 2002; Svane и др., 1999; Tatsumi и др., 2003; Yamanaka и др., 2002). На сегодняшний день, тем не менее, I фаза клинических испытаний на человеке генотерапии IL-12 с внедрением плазмид или вирусных векторов не позволила достигнуть длительных, объективных клинических ответов для лечения рака (Heinzerling и др., 2005; Kang и др., 2001; Sangro и др., 2004; Triozzi и др., 2005). Генотерапия, описанная в данной заявке, обеспечивает многообещающее терапевтическое воздействие.
[00021] В одном варианте реализации, настоящее изобретение обеспечивает способ лечения опухоли у млекопитающего, включающий следующие этапы:
(a) введение в микроокружение опухоли популяции иммунных клеток или TSC, которые сконструированы in vitro таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора; и
(b) введение указанному млекопитающему терапевтически эффективного количества активирующего лиганда;
вызывая тем самым экспрессию белка, обладающего функцией иммуномодулятора, и лечение указанной опухоли.
[00022] В другом варианте реализации, настоящее изобретение обеспечивает способ лечения опухоли у млекопитающего, включающий следующие этапы:
(a) введение в микроокружение опухоли двух или более популяций иммунных клеток или TSC, которые сконструированы in vitro таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора, при этом каждая популяция иммунных клеток или TSC экспрессирует различный набор одного или нескольких иммуномодуляторов; и
(b) введение указанному млекопитающему терапевтически эффективного количества одного или нескольких активирующих лигандов;
вызывая тем самым экспрессию белков, обладающих функциями иммуномодуляторов, и лечение указанной опухоли.
[00023] В другом варианте реализации, настоящее изобретение обеспечивает способ лечения опухоли у млекопитающего, включающий следующие этапы:
(a) введение в микроокружение опухоли популяции иммунных клеток или TSC, которые сконструированы in vitro таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора, и белок, обладающий функцией IL-12, при этом по меньшей мере один из белков, обладающих функцией иммуномодулятора или IL-12, находится под контролем функционирующего при определенных условиях промотора, который активируется лигандом; и
(b) введение указанному млекопитающему терапевтически эффективного количества активирующего лиганда;
вызывая тем самым экспрессию белка, обладающего функцией иммуномодулятора, и/или белка, обладающего функцией IL-12, и лечение указанной опухоли.
[00024] В другом варианте реализации, настоящее изобретение обеспечивает способ лечения опухоли у млекопитающего, включающий следующие этапы:
(a) введение в микроокружение опухоли двух или более популяций иммунных клеток или TSC, которые сконструированы in vitro таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора, и белок, обладающий функцией IL-12, при этом каждая популяция иммунных клеток или TSC экспрессирует различный набор одного или нескольких белков, обладающих функцией иммуномодулятора, при этом по меньшей мере один из белков, обладающих функцией иммуномодулятора или IL-12, находится под контролем функционирующего при определенных условиях промотора, который активируется лигандом; и
(b) введение указанному млекопитающему терапевтически эффективного количества одного или нескольких активирующих лигандов;
вызывая тем самым экспрессию белка, обладающего функциями иммуномодуляторов, и/или белка, обладающего функцией IL-12, и лечение указанной опухоли.
[00025] В другом варианте реализации, настоящее изобретение обеспечивает способ лечения заболевания или расстройства у млекопитающего, включающий следующие этапы:
(a) введение указанному млекопитающему популяции модифицированных клеток, которые модифицированы таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора; и
(b) введение указанному млекопитающему терапевтически эффективного количества активирующего лиганда;
вызывая тем самым экспрессию белка, обладающего функцией иммуномодулятора, и лечение указанного заболевания или расстройства.
[00026] В другом варианте реализации, настоящее изобретение обеспечивает способ лечения заболевания или расстройства у млекопитающего, включающий следующие этапы:
(a) введение указанному млекопитающему двух или более популяций модифицированных клеток, которые модифицированы таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора, при этом каждая популяция модифицированных клеток экспрессирует различный набор одного или нескольких иммуномодуляторов; и
(b) введение указанному млекопитающему терапевтически эффективного количества одного или нескольких активирующих лигандов;
вызывая тем самым экспрессию белков, обладающих функциями иммуномодуляторов, и лечение указанного заболевания или расстройства.
[00027] В другом варианте реализации, настоящее изобретение обеспечивает способ лечения заболевания или расстройства у млекопитающего, включающий следующие этапы:
(a) введение указанному млекопитающему популяции модифицированных клеток, которые модифицированы таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора, и белок, обладающий функцией IL-12, при этом по меньшей мере один из белков, обладающих функцией иммуномодулятора или IL-12, находится под контролем функционирующего при определенных условиях промотора, который активируется лигандом; и
(b) введение указанному млекопитающему терапевтически эффективного количества активирующего лиганда;
вызывая тем самым экспрессию белка, обладающего функцией иммуномодулятора, и/или белка, обладающего функцией IL-12, и лечение указанного заболевания или расстройства.
[00028] В другом варианте реализации, настоящее изобретение обеспечивает способ лечения заболевания или расстройства у млекопитающего, включающий следующие этапы:
(а) введение указанному млекопитающему двух или более популяций модифицированных клеток, которые модифицированы таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора, и белок, обладающий функцией IL-12, при этом каждая популяция модифицированных клеток экспрессирует различный набор одного или нескольких белков, обладающих функцией иммуномодулятора, при этом по меньшей мере один из белков, обладающих функцией иммуномодулятора или IL-12, находится под контролем функционирующего при определенных условиях промотора, который активируется лигандом; и
(b) введение указанному млекопитающему терапевтически эффективного количества одного или нескольких активирующих лигандов;
вызывая тем самым экспрессию белка, обладающего функциями иммуномодуляторов, и/или белка, обладающего функцией IL-12, и лечение указанного заболевания или расстройства.
[00029] Настоящее изобретение также обеспечивает способ определения эффективности терапии, основанной на сконструированной клетке, например, иммунной клетке или TSC, путем измерения уровня экспрессии или активности IFN-гамма у пациента перед началом терапии, таким образом получая контрольный уровень, затем введения клеток, сконструированных таким образом, что они экспрессируют один или более белков, обладающих функцией иммуномодулятора, и возможно белок, обладающий функцией IL-12, введения эффективного количества активирующего лиганда, а затем измерения уровня экспрессии IFN-гамма, чтобы получить тестовый уровень, и сравнения контрольного уровня с тестовым уровнем, чтобы определить, является ли схема лечения эффективной.
[00030] В одном варианте реализации, настоящее изобретение обеспечивает способ определения эффективности для пациента схемы лечения, основанной на сконструированной in vitro клетке, например, иммунной клетке или TSC, включающий:
(а) измерение уровня экспрессии, или уровня активности, или обоих уровней для интерферона-гамма (IFN-гамма) в первом биологическом образце, полученном из указанного пациента, нуждающегося в лечении, перед введением сконструированных in vitro клеток, таким образом получая контрольный уровень;
(b) введение пациенту, нуждающемуся в этом, сконструированных in vitro клеток, полученных таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора, и возможно белок, обладающий функцией IL-12;
(c) введение указанному пациенту, нуждающемуся в этом, эффективного количества активирующего лиганда;
(d) измерение уровня экспрессии, или уровня активности, или обоих уровней IFN-гамма во втором биологическом образце, полученном от указанного пациента, нуждающегося в лечении, после введения сконструированных in vitro иммунных клеток и активирующего лиганда, таким образом получая тестовый уровень; и
(e) сравнение контрольного уровня с тестовым уровнем IFN-гамма, при этом повышение тестового уровня экспрессии, активности или обоих уровней IFN-гамма относительно контрольного уровня указывает на то, что указанная схема лечения эффективна для указанного нуждающегося в лечении пациента.
ПОДРОБНОЕ ОПИСАНИЕ ФИГУР
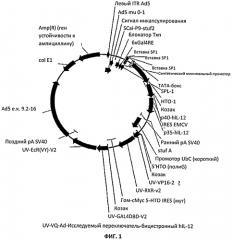
[00031] На Фиг.1 показана карта плазмиды для системы экспрессии с регулируемого промотора для бицистронного транскрипта, кодирующего hIL-12.
[00032] На Фиг.2 показана карта плазмиды для системы экспрессии с регулируемого промотора для бицистронного транскрипта, кодирующего hIL-21 и hIL-15.
[00033] На Фиг.3 показана карта плазмиды для системы экспрессии с регулируемого промотора для бицистронного транскрипта, кодирующего mIL-12.
[00034] На Фиг.4 показана карта плазмиды для системы экспрессии с регулируемого промотора для бицистронного транскрипта, кодирующего mIL-21 и mIL-15.
[00035] На Фиг.5 показана карта плазмиды для системы экспрессии с регулируемого промотора hIL-21.
[00036] На Фиг.6 показана карта плазмиды для системы экспрессии с регулируемого промотора mIL-21.
[00037] На Фиг.7 показана карта плазмиды для системы экспрессии с регулируемого промотора трицистронного транскрипта, кодирующего hIL-12 и hIL-21.
[00038] На Фиг.8 показана карта плазмиды для системы экспрессии с регулируемого промотора трицистронного транскрипта, кодирующего mIL-12 и mIL-21.
[00039] На Фиг.9 показана структура вектора rAd.RheoIL12, в котором участки Е1 и Е3 были удалены и участок Е1 был заменен на компоненты терапевтической системы RheoSwitch® Therapeutic System (RTS)-IL-12. Прямоугольник с надписью "IL12" представляет собой последовательности, кодирующие IL-12p40 и IL-12p35, разделенные участком внутренней посадки рибосомы (IRES).
ПОДРОБНОЕ ОПИСАНИЕ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Иммуномодуляторы
Цитокины
[00040] Полинуклеотидные последовательности интерлейкина 1 (IL-1), который представляет собой цитокин, важный для воспалительного ответа на инфекцию, доступны в открытых базах данных под номерами доступа: М28983 (IL-1α человека); М15330 (IL-1β человека); AF201830 (IL-1δ человека); AF201831 (IL-1ε человека); AF201832 (1L-1ζ человека); AF201833 (IL-1η человека); NM_010554 (IL-1α мыши); NM_008361 (IL-1β мыши); NM_019451 (L-1δ мыши); NM_019450 (IL-1f6 мыши); NM_027163 (IL-1f8 мыши); NM_53511 (IL-1f9 мыши); NM_204524 (IL-1β цыпленка); NM_017019 (IL-1α крысы) и NM_031512 (IL-1β крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00041] Последовательности аминокислот интерлейкина 1 (IL-1) доступны в открытых базах данных под номерами доступа ААА59134 (IL-1α человека); ААА59135 (IL-1β человека); AAF25210 (IL-1δ человека); AAF25211 (IL-1ε человека); AAF25212 (1L-1ζ человека); AAF25213 (IL-1η человека); NP_034684 (IL-1α мыши); NP_032387 (IL-1β мыши); NP_062324 (L-1δ мыши ); NP_062323 (IL-1f6 мыши); NP_081439 (IL-1f8 мыши); NP_705731 (IL-1f9 мыши); NP_989855 (IL-1β цыпленка); NP_058715 (IL-1α крысы) и NP_113700 (IL-1β крысы), перечисленные последовательности включены в настоящее описание посредством ссылки. Laurent и др., Psychiatr. Genet. 7: 103 (1997) обнаружили полиморфные мутации в гене интерлейкина-1-бета человека.
[00042] Полинуклеотидные последовательности интерлейкина 2 (IL-2), который принадлежит к семейству цитокинов, включающему IL-4, IL-7, IL-9, IL-15 и IL-21, доступны в открытых базах данных под номерами доступа U25676 (человека); NM_008366 (мыши); NM_204153 (цыпленка) и NM_053836 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00043] Последовательности аминокислот интерлейкина 2 (IL-2) доступны в открытых базах данных под номерами доступа ААА70092 (человека); NP_032392 (мыши); NP_989484 (цыпленка) и NP_446288 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00044] Liu и др., Appl. Biochem. Biotechnol. 133: 77 (2006) сконструировали мутантный IL-2 человека, a Lorberboum и др., J. Biol. Chem. 265: 16311 (1990) описали конструирование химерного IL-2.
[00045] Полинуклеотидные последовательности интерлейкина 4 (IL-4), который представляет собой цитокин, который вызывает дифференцировку наивных хелперных Т-клеток в клетки Th2, доступны в открытых базах данных под номерами доступа М23442 (человека); NM_021283 (мыши); NM_001007079 (цыпленка) и NM_201270 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00046] Последовательности аминокислот интерлейкина 4 (IL-4) доступны в открытых базах данных под номерами доступа ААА59150 (человека); NP_067258 (мыши); NP_001007080 (цыпленка) и NP_958427 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00047] Kawashima и др., J. Med. Genet. 35: 502 (1998) описывают полиморфизмы в гене IL-4, которые связаны с атопическим дерматитом.
[00048] Интерлейкин 7 (IL-7) представляет собой цитокин, важный для развития В- и Т-клеток. Полинуклеотидные последовательности IL-7 доступны в открытых базах данных под номерами доступа J04156 (человека); NM_008371 (мыши); NM_001037833 (цыпленка) и NM_013110 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00049] Последовательности аминокислот интерлейкина 7 (IL-7) доступны в открытых базах данных под номерами доступа ААА59156 (человека); NP_032397 (мыши); NP_001032922 (цыпленка) и NP_037242 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00050] Feng и др., Genetics 175:545 (2007) обнаружил точечные мутации в IL-7, которые приводят к функциональному дефекту IL-7.
[00051] Интерлейкин 9 (IL-9) представляет собой цитокин, продуцируемый Т-клетками, и является регулятором гематопоэтических клеток. Полинуклеотидные последовательности IL-9 доступны в открытых базах данных под номерами доступа NM_000590 (человека); NM_008373 (мыши); NM_001037825 (цыпленка) и NM_001105747 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00052] Последовательности аминокислот интерлейкина 9 (IL-9) доступны в открытых базах данных под номерами доступа NP_000581 (человека); NP_032399 (мыши); NP_001032914 (цыпленка) и NP_001099217 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00053] IL-12 представляет собой цитокин, который может действовать как фактор роста для активированных Т- и NK-клеток, повышать литическую активность NK/лимфокин- активированных клеток-киллеров и стимулировать продукцию IFN-гамма покоящимися мононуклеарными клетками периферической крови (РВМС). Полинуклеотидные последовательности IL-12 доступны в открытых базах данных под номерами доступа NM_000882 (IL12A человека); NM_002187 (IL12B человека); NM_008351 (IL12a мыши); NM_008352 (IL12b мыши); NM_213588 (IL12A цыпленка); NM_213571 (IL12B цыпленка); NM_053390 (IL12a крысы) и NM_022611 (IL12b крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00054] Последовательности аминокислот интерлейкина 12 (IL-12) доступны в открытых базах данных под номерами доступа NP_000873 (IL12A человека); NP_002178 (IL12B человека); NP_032377 (IL12a мыши); NP_032378 (IL12b мыши); NP_998753 (IL12A цыпленка); NP_998736 (IL12B цыпленка); NP_445842 (IL12a крысы) и NP_072133 (IL12b крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00055] Интерлейкин 15 (IL-15) представляет собой цитокин, который регулирует активацию и пролиферацию Т-клеток и клеток естественных киллеров. Полинуклеотидные последовательности IL-15 доступны в открытых базах данных под номерами доступа U14407 (человека); NM_008357 (мыши); EU334509 (цыпленка) и AF015719 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00056] Последовательности аминокислот интерлейкина 15 (IL-15) доступны в открытых базах данных под номерами доступа ААА21551 (человека); NP_032383 (мыши); ABY55312 (цыпленка) и ААВ94536 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00057] Интерлейкин 18 (IL-18), цитокин, продуцируемый макрофагом, который вместе с интерлейкином 12 вызывает клеточно-опосредованный иммунитет после инфекции микробными продуктами. Полинуклеотидные последовательности IL-18 доступны в открытых базах данных под номерами доступа U90434 (человека); NM_008360 (мыши); EU747333 (цыпленка) и AY258448 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00058] Последовательности аминокислот интерлейкина 18 (IL-18) доступны в открытых базах данных под номерами доступа ААВ50010 (человека); NP_032386 (мыши); АСЕ79188 (цыпленка) и ААР14669 (крысы), перечисленные последовательности включены в настоящее описание