Способы ферментативной переэтерификации/этерификации, в которых использованы липазы, иммобилизованные на гидрофобных смолах, в присутствии водных растворов
Иллюстрации
Показать всеГруппа изобретений относится к ферментативному способу получения сложных алкилэфиров жирных кислот для применения в областях производства биотоплива, продуктов питания и детергентов и системе для осуществления такого способа. В способе используют ферменты, иммобилизированные на гидрофобной смоле, смешанной с источником жирных кислот и спиртом или донором спирта, в присутствии щелочного или слабощелочного водного буфера или в присутствии воды или водного раствора. Способ получения сложных эфиров жирных кислот осуществляют путем переэтерификации или этерификации одновременно или последовательно. Биокаталитическая активность сохраняется без значительных потерь активности при многократных применениях и также без накопления глицерина и водных побочных продуктов или других гидрофильных компонентов на биокатализаторе. Предложенная система включает оборудование и реактивы для осуществления способа с высокой эффективностью. 2 н. и 14 з.п. ф-лы, 23 ил., 16 пр.
Реферат
Область техники, к которой относится изобретение
Раскрыт ферментативный способ получения сложных алкилэфиров жирных кислот для применения в областях производства биотоплива, продуктов питания и детергентов. В этом способе источник жирных кислот и спирт или донор спирта вводят в реакцию в присутствии ферментов, иммобилизированных на гидрофобной смоле, в присутствии щелочного водного буфера или воды. Раскрытый способ можно осуществлять как порционно, так и непрерывно, применяя поточные колоночные реакторы с мешалкой или уплотненным слоем.
Предшествующий уровень техники
Иммобилизация ферментов была описана в огромном количестве методик, в основном направленных на уменьшение доли затрат, связанных с ферментами, в общем ферментативном способе; облегчение выделения ферментов из продуктов и обеспечение непрерывного режима способа.
Методики иммобилизации в основном подразделяются в соответствии со следующим:
1) физическая адсорбция ферментов на твердые подложки, такие как диоксид кремния или нерастворимые полимеры;
2) адсорбция на ионообменных смолах;
3) ковалентное взаимодействие ферментов с материалом твердых подложек, таких как неорганические или полимерные эпоксидные подложки;
4) захват ферментов в растущем полимере;
5) локализация ферментов в мембранном реакторе или в полупроницаемом геле;
6) ферментные кристаллы (CLECS) или агрегаты (CLEAS), образованные при помощи поперечных межмолекулярных связей.
Все вышеупомянутые методики иммобилизации ферментов состоят из следующих этапов:
1) растворение фермента в подходящей буферной системе, что касается рН, температуры, типа буферных солей и ионной силы;
2) добавление твердой подложки в ферментный раствор и перемешивание в течение некоторого времени до тех пор, пока молекулы фермента не иммобилизируются на твердой подложке;
3) отфильтровывание с твердой подложки, которая содержит иммобилизированный фермент;
4) промывка подложки подходящим буфером для удаления слабосвязанных молекул фермента и затем высушивание твердой подложки.
Поверхностные ферменты, в основном липазы, были иммобилизированы посредством вышеупомянутых методов. Эти предложенные препараты иммобилизированных ферментов обладают низкой синтетической активностью и коротким периодом полураспада при эксплуатации. В попытке повысить синтетическую активность и стабильность иммобилизированных липаз и других поверхностных ферментов были применены различные способы. Эти способы включают:
1) связывание поверхностных функциональных групп ферментов с гидрофобными остатками, такими как жирные кислоты или полиэтиленгликоль;
2) покрытие поверхности ферментов поверхностно-активными веществами, такими как сложные полиолэфиры жирных кислот;
3) приведение ферментов в контакт с гидрофобными подложками, обычно полипропиленовыми, которые были предварительно обработаны гидрофильными растворителями, такими как этанол или изопропанол.
Ни один из вышеуказанных способов не давал удовлетворительных результатов в отношении стабилизации и экономической эффективности иммобилизированных поверхностных ферментов для того, чтобы осуществить обратное ферментативное превращение в промышленных масштабах. Также сообщалось, что большинство ферментов, иммобилизированных в соответствии с вышеупомянутыми процедурами, либо теряют значительную часть синтетической активности, либо не проявляют своей полной активности вследствие определенных ограничений, связанных с процедурой иммобилизации, или вследствие присутствия определенных ингибиторов ферментов в реакционной среде.
Еще одним значительным недостатком липаз и фосфолипаз является их низкая устойчивость к гидрофильным субстратам, в частности, к спиртам с короткими цепочками и жирным кислотам с короткими цепочками (до С4). Во многих научных исследованиях было обнаружено, что спирты с короткими цепочками и жирные кислоты с короткими цепочками, как, например, метанол и уксусная кислота, соответственно, ответственны за отщепление присущих им молекул воды от четвертичной структуры этих ферментов, что приводит к их денатурации и последующей утрате их каталитической активности. Этот недостаток препятствовал применению липаз для получения промышленных количеств сложных метилэфиров жирных кислот «биодизель» с применением триглицеридов масел и метанола в качестве субстратов.
Дополнительным недостатком применения иммобилизированных липаз для переэтерификации/этерификации источника жирных кислот со свободным спиртом является накопление образовавшихся побочных продуктов глицерина и воды на биокатализаторе и, вследствие этого, препятствие свободному доступу субстратов к активному центру иммобилизированного фермента. Такие биокатализаторы в основном утрачивают свои каталитические свойства после нескольких циклов при применении одинаковой порции биокатализатора.
Современные изобретатели разработали особые препараты иммобилизированных ферментов, обладающие хорошей стабильностью на протяжении многих производственных циклов с сохранением активности. Примеры таких ферментных препаратов раскрываются в том числе в WO/2008/084470, WO/2008/139455 и WO 2009/069116.
Условия, при которых осуществляется каталитическая реакция, могут отрицательно влиять на стабильность и эффективность препаратов иммобилизированных ферментов. Важно иметь ферментные препараты, которые сохраняют стабильность и активность в реакционных условиях.
Эти и другие объекты настоящего изобретения станут очевидными из следующего далее описания.
Сущность изобретения
В одном варианте осуществления настоящее изобретение относится к способу переэтерификации/этерификации источника жирных кислот со спиртом с образованием сложных алкилэфиров жирных кислот, который включает введение в реакцию источника жирных кислот и спирта или донора спирта в присутствии препарата иммобилизированной липазы, где препарат иммобилизированной липазы включает в себя по меньшей мере одну липазу, иммобилизированную на гидрофобной пористой подложке, и реакционная среда содержит водный щелочной буферный раствор.
Во всех аспектах данного варианта, указанный водный щелочной буферный раствор может быть водным слабощелочным буферным раствором. Указанный водный щелочной буферный раствор может содержаться в реакционной среде в количестве до 99 вес.% источника жирных кислот, например, до 90, 80, 70, 60, 50, 40, 30, 25, 20, 15, 12, 10, 8, 5, 4, 3, 2% и 1%. В ином случае, указанный водный щелочной буферный раствор может содержаться в реакционной смеси в количестве больше, чем 1 вес. % источника жирных кислот, больше, чем 2, 3, 4, 5, 6, 8, 10, 12, 15, 20, 25, 30, 40, 50, 60, 70, 80, 90%, вплоть до 99%. Водный щелочной буферный раствор может иметь рН от 7 до приблизительно 11, например любой из: 7-8,5, 7-9, 7-9,5, 7-10 и 7-11. В способе изобретения рКа добавленного слабощелочного реагента, входящего в состав буферного раствора, может быть выше чем или равно рКа свободных кислот, присутствующих в источнике жирных кислот.
В другом варианте осуществления настоящее изобретение относится к способу переэтерификации/этерификации источника жирных кислот со спиртом с образованием сложных алкилэфиров жирных кислот, который включает введение в реакцию источника жирных кислот и спирта в присутствии препарата иммобилизированной липазы, где препарат иммобилизированной липазы содержит по меньшей мере одну липазу, иммобилизированную на гидрофобной пористой положке, а реакционная среда содержит воду. Вода находится в форме дистиллированной воды или воды, содержащей различные растворенные соли, с рН от 3 до 11. Во всех аспектах данного варианта, реакционная среда может содержать воду или водный раствор в количестве до 99 вес. % источника жирных кислот, например, до 90, 80, 70, 60, 50, 40, 30, 25, 20, 15, 12,10, 8, 5, 4, 3, 2% и 1%. В ином случае, указанный водный щелочной буферный раствор может содержаться в реакционной смеси в количестве больше, чем 1 вес. % источника жирных кислот, больше, чем 2, 3, 4, 5, 6, 8, 10, 12, 15, 20, 25, 30, 40, 50, 60, 70, 80, 90%, вплоть до 99%.
Во всех вариантах осуществления и аспектах настоящего изобретения спирт может быть спиртом с короткой цепью, например C1-С6 алкиловым спиртом, точнее говоря, С1-С4 алкиловым спиртом, в частности, метанолом или этанолом. Если указанным спиртом является метанол, то указанными полученными сложными эфирами жирных кислот являются сложные метилэфиры жирных кислот (FAME - биодизель). Спирт также может быть жирным спиртом с цепью средней длины (С6-С10) или жирными спиртами с длинными цепями (С12-С22). Донор спирта может быть сложным моноалкилэфиром или диалкилкарбонатом, таким как диметилкарбонат или диэтилкарбонат.
Во всех вариантах осуществления и аспектах настоящего изобретения указанная иммобилизированная липаза способна катализировать этерификацию свободных жирных кислот, с образованием сложных алкилэфиров жирных кислот и воды в качестве побочного продукта, и переэтерификацию триглицеридов, частичных глицеридов, восковых эфиров и фосфолипидов с образованием сложных алкилэфиров жирных кислот и глицерина, длинноцепочечных жирных спиртов и глицерофосфолипидов в качестве побочных продуктов, соответственно.
Во всех вариантах осуществления и аспектах настоящего изобретения, связанных с применением щелочного буфера или щелочного раствора, количество указанного щелочного буфера или раствора в реакционной среде составляет больше, чем 0,001 вес. % источника жирных кислот.
Во всех вариантах осуществления и аспектах настоящего изобретения указанная по меньшей мере одна липаза может быть липазой, полученной из любого из Rhizomucor miehei, Pseudomonas sp., Rhizopus niveus, Mucor javanicus, Rhizopus oryzae, Aspergillus niger, Penicillium camembertii, Alcaligenes sp., Acromobacter sp., Burkholderia sp., Thermomyces lanuginosus, Chromobacterium viscosum, Candida antarctica B, Candida rugosa, Candida antarctica А, семян папайи и панкреатина. Препарат липазы может включать по меньшей мере две липазы, которые могут быть каждая отдельно иммобилизированная на гидрофобной подложке или совместно иммобилизированными на одной и той же гидрофобной подложке. Указанные липазы способны одновременно или последовательно катализировать этерификацию свободных жирных кислот, с образованием сложных алкилэфиров жирных кислот и воды в качестве побочного продукта, и переэтерификацию триглицеридов и частичных глицеридов, с образованием сложных алкилэфиров жирных кислот и глицерина в качестве побочного продукта, и/или переэтерификацию фосфолипидов с образованием алкилэфиров жирных кислот, лизофосфолипидов и глицерофосфолипидов в качестве побочных продуктов.
Во всех вариантах осуществления и аспектах настоящего изобретения указанной подложкой может быть любая из подложки на основе гидрофобного алифатического полимера и подложки на основе гидрофобного ароматического полимера. Указанная гидрофобная полимерная подложка может состоять их линейных или разветвленных органических цепей. Указанная подложка может включать макросетчатые органические полимерные или сополимерные цепи. Указанная подложка может быть пористой или непористой неорганической подложкой, которая может быть гидрофобной или покрытой гидрофобным органическим материалом. Указанный органический материал может быть линейной, разветвленной или функционализированной гидрофобной органической цепью.
Во всех вариантах осуществления и аспектах настоящего изобретения, если применяют щелочной буферный раствор, то указанный водный щелочной буферный раствор может быть раствором неорганической щелочной соли или органического основания. Указанный щелочной буферный раствор может быть раствором любого из гидроксида, карбоната, бикарбоната, фосфата, сульфата, ацетата и цитрата щелочных металлов, солей жирных кислот, первичного, вторичного и третичного амина, и любых их смесей. В особых вариантах осуществления указанный щелочной буферный раствор может быть раствором слабого основания, выбранного из бикарбонатов и карбонатов натрия или калия. В некоторых особых вариантах осуществления способа настоящего изобретения указанный щелочной буферный раствор может быть добавлен к указанному источнику жирных кислот на стадии, предшествующей смешиванию, или непосредственно в реакционную среду.
Во всех вариантах осуществления и аспектах настоящего изобретения, если применяют щелочной буферный раствор, содержание указанного щелочного буферного раствора в переэтерификационной/этерификационной реакционной среде может быть в количестве больше чем 0,001 вес. %, от масляного сырья, например, 1-30 вес. %, 1-20 вес. %, 1-10 вес. %, 1-5 вес. %, или 1-2 вес. % от масляного сырья, например, больше, чем 6, 7, 8, 10, 12, 15, 20, 30, 40% и 50 вес.% от масляного сырья.
В некоторых вариантах осуществления настоящего изобретения сначала источник жирных кислот можно смешать с щелочным буферным раствором или с водой или водным раствором, и затем смесь можно обработать указанным препаратом иммобилизированной липазы с последующим добавлением указанного спирта и обеспечения протекания реакции в подходящих условиях до тех пор, пока источник жирных кислот не превратится в сложные эфиры жирных кислот.
Во всех вариантах осуществления и аспектах настоящего изобретения указанным источником жирных кислот может быть любое из растительного масла, животного жира, масла водорослей, рыбьего жира, отработанного масла и любых их смесей. Указанный источник жирных кислот может включать свободные жирные кислоты, моно-, ди- или триглицериды, их смеси в любых соотношениях, в присутствии или отсутствии других минорных производных жирных кислот, таких как фосфолипиды, восковые эфиры и сложные эфиры стеринов. Источник жирных кислот может быть неочищенным, очищенным, обесцвеченным, дезодорированным или любым из их комбинаций.
Во всех вариантах осуществления и аспектах настоящего изобретения реакцию можно осуществлять при температуре от 10 до 100°С, в особенности при 25-30°С.
Во всех вариантах осуществления и аспектах настоящего изобретения указанный источник жирных кислот может быть предварительно смешан с указанным спиртом или донором спирта и с указанной водой или буферным раствором в предреакционном сосуде для приготовления с образованием эмульсии, которая может быть затем подана совместно с указанным препаратом иммобилизированной липазы в реакционный сосуд для переэтерификации/этерификации.
Во всех вариантах осуществления и аспектах настоящего изобретения указанную иммобилизированную липазу можно применять в колоночных реакторах с уплотненным слоем, работающих в порционном или непрерывном режиме.
В соответствии с другим аспектом настоящего изобретения обеспечивается система для переэтерификации/этерификации жирных кислот со спиртом с образованием сложных алкилэфиров жирных кислот, включающая:
реакционный сосуд, сконфигурированный для прохождения реакции в реакционной среде, содержащей жирную кислоту и по меньшей мере один из спирта и донора спирта, в присутствии препарата иммобилизированной липазы, где препарат иммобилизированной липазы включает по меньшей мере одну липазу, иммобилизированную на гидрофобной пористой подложке, и реакционная среда содержит по меньшей мере одно из водного щелочного буферного раствора и воды.
Система может включать один или несколько из следующих признаков в любой желаемой комбинации или перестановке.
A. Реакционный сосуд может включать препарат иммобилизированной липазы, по меньшей мере во время работы указанной системы для получения указанных сложных алкилэфиров жирных кислот.
B. Дополнительно или в качестве альтернативы признаку А реакционный сосуд может содержать жирную кислоту и по меньшей мере один из спирта и донора спирта, по меньшей мере во время работы указанной системы для получения указанных сложных алкилэфиров жирных кислот.
C. Дополнительно или в качестве альтернативы признакам А или В указанная реакционная среда включает смесь, причем указанная система дополнительно включает предреакционный сосуд в избирательном жидкостном взаимодействии с указанным реакционным сосудом, причем указанный предреакционный сосуд сконфигурирован для предварительного смешивания по меньшей мере жирной кислоты и по меньшей мере одного из спирта и донора спирта с образованием указанной смеси, и для избирательной подачи указанной смеси в указанный реакционный сосуд по меньшей мере во время работы указанной системы для получения указанных сложных алкилэфиров жирных кислот. Система может факультативно дополнительно включать источник жирной кислоты в избирательном жидкостном взаимодействии с указанным предреакционным сосудом и сконфигурирована для избирательной подачи жирной кислоты в указанный предреакционный сосуд по меньшей мере во время указанной работы указанной системы, и источник спирта в избирательном жидкостном взаимодействии с указанным предреакционным сосудом и сконфигурирована для избирательной подачи по меньшей мере одного из спирта и донора спирта в указанный предреакционный сосуд по меньшей мере во время указанной работы указанной системы. Система может факультативно дополнительно включать источник буфера в избирательном жидкостном взаимодействии с указанным предреакционным сосудом и сконфигурирована для избирательной подачи по меньшей мере одного из водного щелочного буферного раствора и воды в указанный предреакционный сосуд с включением в указанную смесь по меньшей мере во время указанной работы указанной системы.
D. Дополнительно или в качестве альтернативы признакам А-С система может быть сконфигурирована для избирательной подачи одного или нескольких из жирной кислоты, и/или по меньшей мере одного из спирта и донора спирта, и/или по меньшей мере одного из водного щелочного буферного раствора и воды в указанный предреакционный сосуд, каждый непрерывным образом или отдельными порциями, по меньшей мере во время указанной работы указанной системы.
E. Дополнительно или в качестве альтернативы признакам A-D предреакционный сосуд может быть сконфигурирован для избирательной подачи указанной смеси в указанный реакционный сосуд непрерывным образом или отдельными порциями, по меньшей мере во время указанной работы указанной системы.
F. Дополнительно или в качестве альтернативы признакам А-Е система может быть сконфигурирована для избирательной и непосредственной подачи в указанный реакционный сосуд по меньшей мере одной из жирной кислоты; по меньшей мере одного из спирта и донора спирта; и по меньшей мере одного из водного щелочного буферного раствора и воды.
G. Дополнительно или в качестве альтернативы признакам A-F реакционный сосуд может включать систему терморегулирования, сконфигурированную для поддержания реакционной среды в указанном реакционном сосуде в выбранном диапазоне температур.
H. Дополнительно или в качестве альтернативы признакам A-G система может факультативно включать удерживающее устройство, сконфигурированное для удержания препарата иммобилизированной липазы внутри указанного реакционного сосуда по меньшей мере во время работы указанной системы.
I. Дополнительно или в качестве альтернативы признакам А-Н система дополнительно включает сосуд для отделения продуктов в избирательном жидкостном взаимодействии с указанным реакционным сосудом, причем указанная система сконфигурирована для избирательной подачи реакционной смеси, включающей продукты реакции, из указанного реакционного сосуда в указанный сосуд для отделения продуктов, и где указанный сосуд для отделения продуктов сконфигурирован для избирательного отделения выхода сложных алкилэфиров жирных кислот из поступающей в него реакционной смеси. Например, сосуд для отделения продуктов может быть сосудом из системы центрифужного и гравитационного отделения.
J. Дополнительно или в качестве альтернативы признакам A-I реакционный сосуд сконфигурирован для избирательной подачи указанной реакционной смеси в указанный сосуд для отделения продуктов непрерывным образом и/или отдельными порциями во время указанной работы указанной системы.
К. Дополнительно или в качестве альтернативы признакам I-J система сконфигурирована для избирательной подачи указанного выхода сложных алкилэфиров жирных кислот из указанного сосуда для отделения продуктов. Например, система сконфигурирована для избирательной подачи указанного выхода сложных алкилэфиров жирных кислот из указанного сосуда для отделения продуктов непрерывным образом и/или отдельными порциями.
L. Дополнительно или в качестве альтернативы признакам А-К система сконфигурирована для повышения указанного выхода сложных алкилэфиров жирных кислот из реакционной смеси, подаваемой в указанный сосуд для отделения продуктов. В одной конфигурации системы, имеющей данный признак, система сконфигурирована для избирательного перенаправления указанного выхода сложных алкилэфиров жирных кислот в указанный реакционный сосуд для дополнительного повышения указанного выхода сложных алкилэфиров жирных кислот из реакционной смеси, впоследствии подаваемой в указанный сосуд для отделения продуктов. В другой конфигурации системы, имеющей данный признак, система сконфигурирована для избирательного перенаправления указанного выхода сложных алкилэфиров жирных кислот во вспомогательный реакторный модуль, где указанный вспомогательный реакторный модуль включает вспомогательный реакторный сосуд и вспомогательный сосуд для отделения продуктов, где указанный дополнительно повышенный выход сложных алкилэфиров жирных кислот позже избирательно подают через указанный вспомогательный сосуд для отделения продуктов.
Краткое описание чертежей
Для того чтобы понять настоящее изобретение и увидеть, как оно может быть осуществлено на практике, далее будут описаны варианты осуществления посредством неограничивающих примеров со ссылкой на сопроводительные графические материалы, в которых:
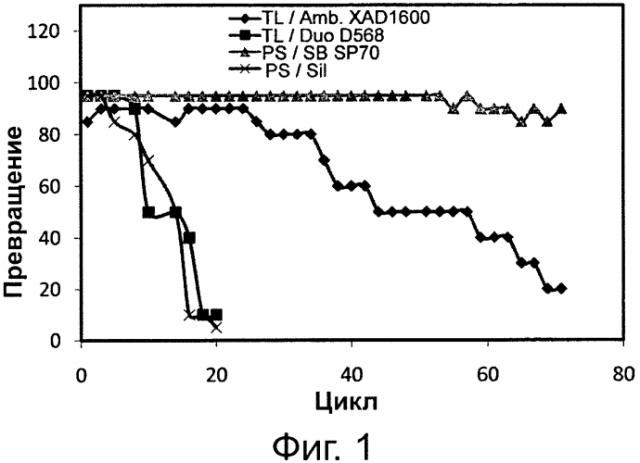
Фигура 1. Переэтерификационная активность липазы Thermomyces lanuginosus (TL), иммобилизированной на Amberlite XAD 1600 (Amb. XAD 1600) в качестве гидрофобной смолы и на Duolite D568 (Duo D568) в качестве гидрофильной смолы, и липазы Pseudomonas sp. (PS), иммобилизированной на Sepabeads SP70 (SB SP70) в качестве гидрофобной смолы на пористом диоксиде кремния (Sil.) в качестве гидрофильной смолы.
Сокращения: Conv. - превращение, Сус. - цикл.
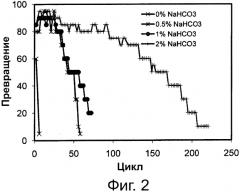
Фигура 2. Превращение соевого масла в биодизель и глицерин через 6 часов реакции при различных уровнях 0,1 М раствора бикарбоната натрия с применением одинаковой порции биокатализатора в многократных периодических экспериментах. Биокатализатором была липаза, полученная из Thermomyces lanuginosus, иммобилизированная на гидрофобной и пористой смоле на основе полистирола и дивинилбензола.
Сокращения: Conv. - превращение; Сус. - цикл.
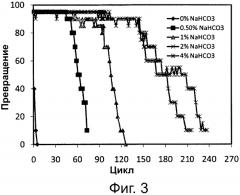
Фигура 3. Превращение соевого масла в биодизель и глицерин через 6 часов реакции при различных уровнях 0,1 М раствора бикарбоната натрия при применении одинаковой порции биокатализатора в многократных периодических экспериментах. Биокатализатором была липаза, полученная из Pseudomonas sp., иммобилизированная на гидрофобной и пористой смоле на основе полистирола и дивинилбензола.
Сокращения: Conv. - превращение; Сус. - цикл.
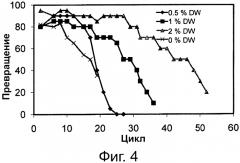
Фигура 4. Превращение соевого масла в биодизель и глицерин через 6 часов реакции без воды и при различных уровнях воды с применением одинаковой порции биокатализатора в многократных периодических экспериментах. Биокатализатором была липаза, полученная из Thermomyces lanuginosus, иммобилизированная на гидрофобной и пористой смоле на основе полистирола и дивинилбензола.
Сокращения: Conv. - превращение; Сус. - цикл; DW - дистиллированная вода.
Фигура 5. Превращение соевого масла в биодизель и глицерин через 6 часов реакции при различных уровнях воды с применением одинаковой порции биокатализатора в многократных периодических экспериментах. Биокатализатором была липаза, полученная из Pseudomonas sp., иммобилизированная на гидрофобной и пористой смоле на основе полистирола и дивинилбензола.
Сокращения: Conv. - превращение; Сус. - цикл; DW - дистиллированная вода.
Фигура 6. Превращение смеси FFA (свободных жирных кислот) и соевого масла в биодизель и глицерин и побочные водные продукты после 4 часов этерификации/переэтерификации при различных уровнях 0,1 М раствора бикарбоната натрия с применением одинаковой порции биокатализатора в многократных периодических экспериментах. Биокатализатором была липаза, полученная из Pseudomonas sp., иммобилизированная на гидрофобной и пористой смоле на основе полистирола и дивинилбензола.
Сокращения: Conv. - превращение; Сус. - цикл; DW - дистиллированная вода.
Фигура 7. Этерификация гидролизата соевого масла в биодизель и воду через 4 часа реакции в присутствии 2% ОД М раствора бикарбоната натрия с применением одинаковой порции биокатализатора в многократных периодических экспериментах. Биокатализатором была липаза, полученная из Pseudomonas sp., иммобилизированная на гидрофобной и пористой смоле на основе полистирола и дивинилбензола.
Сокращения: Ac. Val. - кислотное число; Сус. - цикл.
Фигура 8. Переэтерификация рыбьего жира с этанолом через 6 часов реакции в присутствии 1 вес. % 0,1 М раствора бикарбоната натрия с применением одинаковой порции биокатализатора в многократных периодических экспериментах. Биокатализаторами были липазы, полученные из Thermomyces lanuginosus (TL Lip.) и Pseudomonas sp.(PS Lip.), иммобилизированные на Amberlite XAD 1600.
Сокращения: Conv. - превращение; Сус. - цикл.
Фигура 9. Переэтерификация животного жира с этанолом через 6 часов реакции в присутствии 2 вес. % 0,1 М раствора бикарбоната натрия с применением одинаковой порции биокатализатора в многократных периодических экспериментах. Биокатализаторами были липазы Thermomyces lanuginosus, Pseudomonas sp.(PS Lip.; TL Lip.), иммобилизированные на Amberlite XAD 1600.
Сокращения: Conv. - превращение; Сус. - цикл.
Фигура 10. Обработка реакционной среды переэтерификации/этерификации, полученной после 4 часов и имеющей кислотное число FFA 7 мг КОН/1 г, с применением Pseudomonas sp. или Thermomyces lanuginosus, иммобилизированных на гидрофобных пористых смолах, с Candida antarctica, иммобилизированной на гидрофобной пористой смоле.
Сокращения: Ac. Val. - кислотное число; Сус. - цикл.
Фигура 11. Активность переэтерификации липазы, полученной из Alcaligenes sp. (AL), иммобилизованной на дивинилбензоле/полистироле (DVB-PS) в качестве гидрофобной смолы, на слабой анионообменной гидрофильной смоле (Res.), и на пористом гранулированном силикагеле (Sil) в качестве гидрофобной смолы.
Сокращения: Conv. - превращение; Сус. - цикл.
Фигура 12. Активность переэтерификации липазы Thermomyces lanuginosus (TL), иммобилизованной на дивинилбензоле/полистироле (DVB-PS) в качестве гидрофобной смолы, на слабой анионообменной гидрофильной смоле (Res.), и на пористом гранулированном силикагеле (Sil) в качестве гидрофобной смолы.
Сокращения: Conv. - превращение; Сус. - цикл.
Фигура 13. Активность переэтерификации липазы Pseudomonas sp. (PS), иммобилизованной на дивинилбензоле/полистироле (DVB-PS) в качестве гидрофобной смолы, на слабой анионообменной гидрофильной смоле (Res.), и на пористом гранулированном силикагеле (Sil) в качестве гидрофобной смолы.
Сокращения: Conv. - превращение; Сус. - цикл.
Фигура 14. Преобразование соевого масла в метиловые эфиры жирных кислот и глицерин через 6 часов реакции, с использованием той же партии биокатализатора (Thermomyces lanuginosus (TL), иммобилизованного на подложке DVB-PS) в многократных периодических экспериментах, при различных уровнях 0,1 М раствора бикарбоната натрия. Метанол добавляли в реакционную смесь в одну стадию на основе молярного соотношения масла к метанолу 1:3.
Сокращения: Conv. - превращение; Сус. - цикл; Sol. - раствор.
Фигура 15. Преобразование соевого масла в биодизель и глицерин после 6-часовой реакции, с использованием той же партии биокатализатора (Pseudomonas sp. (SP), иммобилизованного на подложке DVB-PS) в многократных периодических экспериментах, при различных уровнях 0,1 М раствора бикарбоната натрия. Метанол добавляли в реакционную смесь в одну стадию на основе молярного соотношения масла к метанолу 1:3.
Сокращения: Conv. - превращение; Сус. - цикл; Sol. - раствор.
Фигура 16. Преобразование соевого масла в биодизель и глицерин после 6-часовой реакции, с использованием той же партии биокатализатора (Thermomyces lanuginosus (TL), иммобилизованного на подложке DVB-PS) в многократных периодических экспериментах, при различных уровнях 0,1 М раствора бикарбоната натрия. Метанол добавляли в реакционную смесь в одну стадию на основе молярного соотношения масла к метанолу 1:3.
Сокращения: Conv. - превращение; Сус. - цикл; Wat. - вода.
Фигура 17. Преобразование олеиновой кислоты в биодизель и воду после 6-часовой реакции, с использованием той же партии биокатализатора (Thermomyces lanuginosus (TL), иммобилизованного на подложке DVB-PS) в многократных периодических экспериментах, при различных уровнях 0,1 М раствора бикарбоната натрия. Метанол добавляли в реакционную смесь в одну стадию на основе молярного соотношения масла к метанолу.
Сокращения: Conv. - превращение; Сус. - цикл; Sol. - раствор.
Фигура 18. Преобразование различных смесей олеиновой кислоты и триглицеридов соевого масла в биодизель, глицерин и воду после 6-часовой реакции с использованием той же партии биокатализатора (Thermomyces lanuginosus (TL), иммобилизованного на подложке DVB-PS) в многократных периодических экспериментах в присутствии 8 вес. % 0,1 М раствора бикарбоната натрия. Метанол добавляли в реакционную смесь в одну стадию на основе молярного соотношения масла к метанолу.
Сокращения: Conv. - превращение; Сус. - цикл; OA. - Олеиновая кислота.
Фигура 19. Преобразование неочищенных масел, содержащих фосфолипиды, в биодизель и глицерин после 6-часовой реакции с использованием той же партии биокатализатора (Thermomyces lanuginosus (TL), иммобилизованного на подложке DVB-PS) в многократных периодических экспериментах в присутствии 8 вес. % 0,1 М раствора бикарбоната натрия. Метанол добавляли в реакционную смесь в одну стадию на основе молярного соотношения масла к метанолу.
Сокращения: Conv. - превращение; Сус. - цикл; RSBO - очищенное соевое масло; CSBO - неочищенное соевое масло; PL - фосфолипиды; О. - масло.
Фигура 20. Преобразование соевого масла в биодизель и глицерин после 6-часовой реакции, с использованием той же партии биокатализатора (Thermomyces lanuginosus (TL), иммобилизованного на подложке DVB-PS) в многократных периодических экспериментах, при различных значениях рН для 0,1 М раствора бикарбоната натрия. Концентрация буфера в реакционной смеси составляла 8 вес. % масла. Метанол добавляли в реакционную смесь в одну стадию на основе молярного соотношения масла к метанолу.
Сокращения: Conv. - превращение; Сус. - цикл.
Фигура 21. Преобразование соевого масла в биодизель и глицерин после 6-часовой реакции, с использованием той же партии биокатализатор (Thermomyces lanuginosus (TL), иммобилизованного на подложке DVB-PS) в многократных периодических экспериментах, при различных значениях рН для 0,1 М раствора бикарбоната натрия. Концентрация буфера в реакционной смеси составляла 8 вес. % масла. Метанол добавляли в реакционную смесь в одну стадию на основе молярного соотношения масла к метанолу.
Сокращения: Conv. - превращение; Сус. - цикл; Acet. - ацетат.
Фигура 22. Схематически иллюстрирует первый вариант осуществления системы для получения сложных алкилэфиров жирных кислот в соответствии с аспектом настоящего изобретения.
Фигура 23. Схематически иллюстрирует второй вариант осуществления системы для получения сложных алкилэфиров жирных кислот в соответствии с аспектом настоящего изобретения.
Осуществление изобретения
В исследованиях по улучшению ферментативно катализируемых производственных процессов, в частности, способов переэтерификации/этерификации источника жирных кислот со спиртом в присутствии иммобилизированной (иммобилизированных) липазы (липаз), современные изобретатели разработали особые условия, при которых стабильность иммобилизированной (иммобилизированных) липазы (липаз) сохраняется на протяжении многих циклов производства.
В варианте осуществления настоящего изобретения настоящее изобретение относится к способу получения сложных алкилэфиров жирных кислот, а именно сложных алкилэфиров жирных кислот с короткими цепочками, таких как сложные метиловые и этиловые эфиры жирных кислот (биодизель), в щелочной микроводной системе без растворителей. В особых вариантах осуществления, щелочная микроводная система является слабощелочной микроводной системой. Способ включает обеспечение источника жирных кислот и введение его в реакцию со свободным спиртом или донором спирта в присутствии препарата иммобилизированной липазы в указанных щелочных или слабощелочных условиях. Не ограничиваясь теорией, предварительная обработка источника жирных кислот щелочным буферным раствором приведет к нейтрализации кислот, что может иметь ингибирующий эффект на фермент. Количество спирта, необходимое для завершения реакции до 100% превращения, может быть добавлено поэтапно или за одну порцию. Дополнительно, спирт может быть спиртом с короткой цепочкой, например метанолом или этанолом. Можно применять другие доноры спирта в реакции с источником жирных кислот в присутствии гидролазы, и позволяя реакции протекать в подходящих условиях до тех пор, пока указанный источник жирных кислот не превратится в сложные алкилэфиры жирных кислот, а именно в сложные метиловые эфиры жирных кислот (FAME) или сложные этиловые эфиры жирных кислот, где указанный препарат гидролазы содержит одну или несколько липаз, раздельно или совместно иммобилизированных на подходящей подложке на основе пористого макросетчатого гидрофобного полимера.
В дополнительном варианте осуществления реакция переэтерификации/этерификации между источником жирной кислоты и спиртом или донором спирта осуществляют в водной микросреде с добавлением воды в реакционную смесь. В особых вариантах осуществления вода может быть добавлена в количестве больше, чем 0,0001 вес. % (на основе источника жирных кислот). Под водой, используемой здесь, подразумевается чистая или дистиллированная вода, а также «водные растворы» (также называемые водосодержащими растворами), которые могут быть, но без ограничений, водопроводной водой, морской водой или водой из любого другого естественного водного источника или резервуара, опресненной водой, химически или ферментативно очищенной или обработанной водой и любыми иными водными растворами, например, растворами растворенных солей. рН реакционной системы или водного раствора может варьировать и может быть, например, приблизительно 3-11, например 4-10, 5-10, 5-9, 6-10, 6-9 или 7-9.
Способ настоящего изобретения можно осуществлять до тех пор, пока из реакционной смеси постоянно удаляется образующийся глицерин и любая излишняя вода. Превращение ацильных групп жирных кислот или свободных жирных кислот, содержащихся в указанном источнике жирных кислот, в сложные алкилэфиры, а именно сложные метилэфиры, жирных кислот может быть проконтролировано в различные моменты времени в течение реакции. Реакционную среду можно удалить при помощи подходящих средств в любой желаемый момент времени в течение реакции, таким образом останавливая реакцию, и из реакционной среды выделяют образовавшиеся сложные метилэфиры жирных кислот и, факультативно, образовавшийся глицерин. Реакция, в частности, может быть остановлена, когда превращение ацильных групп жирных кислот или свободных жирных кислот, содержащихся в указанном источнике жирных кислот, в сложные метилэфиры жирных кислот достигнет по меньшей мере 70%, например, по меньшей мере 85% или по меньшей мере 90%.
Реакционная система может быть аналогичной описанной в одновременно находящемся на рассмотрении документе WO 2009/069116. Например, в производственной системе можно применять реактор с мешалкой с фильтром из спеченного стекла или нержавеющей стали в нижней части, который удерживает биокатализатор в реакторе, однако позволяет реакционной среде проходить сквозь реактор. Такая конфигурация реактора позволяет побочным продуктам, конкретно глицерину и воде, которые само-десорбируются из иммобилизированного фермента, оседать на дно реактора и проходить сквозь фильтр. Результатом является непрерывное удаление десорбирован