Стабилизация fsh
Иллюстрации
Показать всеГруппа изобретений относится к области стабилизации жидких композиций фолликулостимулирующего гормона (FSH). Предложено применение сернокислого натрия или его комбинации с хлористым натрием для стабилизация жидкой композиции FSH и способ ограничения тенденции FSH к диссоциации в жидкой композиции. FSH теряет биологическую активность при диссоциации нековалентно связанных мономеров. Технический результат состоит в реализации заявленных назначений, что обеспечивает сохранность готовых композиций FSH по меньшей мере 24 месяца при хранении при температуре 5°С или 3-4 месяца при хранении при комнатной температуре. 2 н. и 11 з.п. ф-лы, 6 ил., 30 табл.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение в общем относится к области стабилизации FSH композиций, в частности жидких FSH-композиций. Стабилизация достигается путем добавления соли, в предпочтительных воплощениях путем добавления солей с катионами щелочного металла фармацевтически приемлемых солей, а то есть солей Na или K или их комбинаций.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Гонадотропины представляют собой семейство гормонов, которые по существу вовлечены главным образом в период плодовитости женщин и мужчин. Гонадотропины можно получать из мочи, как для исследовательских, так и для лечебных целей, однако некоторые гонадотропины могут быть получены рекомбинантно.
В частности, гонадотропины можно применять в лечении бесплодия.
Четыре основных гонадотропина, которые рассматриваются здесь и все из которых принадлежат одному и тому же семейству гликопротеинов, представляют собой фолликулостимулирующий гормон (FSH), тиреостимулирующий гормон (TSH), лютеинизирующий гормон (LH) и хорионический гонадотропин (hCG). Все эти гонадотропины состоят из альфа- и бета-субъединицы; альфа-субъединица является общей для всех, то есть одинаковой для всех вышеуказанных четырех гонадотропинов, в то время как бета-субъединицы, соответственно, различаются.
Как указано выше, гонадотропины представляют собой группу гетеродимерных гликопротеиновых гормонов, которые регулируют гонадную функцию у мужчин и женщин. Они включают фолликулостимулирующий гормон (FSH), лютеинизирующий гормон (LH), тиреостимулирующий гормон (TSH) и (человеческий) хорионический гонадотропин (hCG).
FSH естественным образом выделяется передней долей гипофиза и выполняет функцию обеспечения развития фолликула и овуляции. FSH содержит альфа-субъединицу из 92 аминокислот, также общую для других гликопротеиновых гормонов, например LH и hCG, и бета-субъединицу из 111 аминокислот, присущую только FSH, которая обеспечивает биологическую специфичность гормона (Pierce and Parsons, 1981, Glycoprotein hormones: structure and function, Ann Rev Biochem., 50: 465-495). Каждую субъединицу посттрансляционно модифицируют путем добавления остатков сложных углеводов. Обе субъединицы имеют две участка для присоединения N-связанных гликанов, альфа-субъединица на аминокислотах 52 и 78, а бета-субъединица на аминокислотных остатках 7 и 24 (Rathnam и Saxena, (1975) Primary amino acid sequence of follicle stimulating hormone from human pituitary glands. I. alpha subunit, J Biol Chem. 250 (17): 6735-6746; Saxena and Rathnam, (1976) Amino acid sequence of the beta subunit of follicle-stimulating hormone from human pituitary glands, J Biol Chem. 251(4); 993-1005)). FSH гликолизируют таким образом примерно на 30% по массе (Dias and Van Roey, (2001) Structural biology of human follitropin and its receptor. Arch Med Res. 32(6): 510-519; Fox et al. (2001) Three-dimensional structure of human follicle-stimulating hormone. Mol Endocrinol. 15(3), 379-89).
Очищенный FSH из мочи человека после наступления менопаузы применяли в течение многих лет в лечении бесплодия; как для стимулирования овуляции при естественном воспроизводстве, так и для получения ооцитов для вспомогательных репродуктивных технологий. Два рекомбинантных варианта FSH, Gonal-f (Merck Serono) и Puregon (Schering-Plough) появились в продаже в середине 1990-х годов. Оба варианта экспрессировались в клетках яичника китайского хомячка (СНО) cells (Howies, СМ. (1996), Genetic engineering of human FSH (Gonal-f), Hum Reprod. Update, 2: 172-191). CG часто применяют в лечении бесплодия, так как это соединение обладает активностью LH.
Оба человеческих FSH и hCG представляют собой гетеродимеры, состоящие из альфа- и бета-субъединицы. Альфа-субъединица в том и другом гормоне является идентичной. Различия между двумя гормонами обеспечивает бета-субъединица. Зрелая бета-субъединица FSH состоит из 111 аминокислот, в то время как в hCG она состоит из 145 аминокислот, кроме того первичная аминокислотная последовательность бета-субъединицы FSH и hCG отличается на протяжении всей бета-цепи. Бета-цепь как FSH, так и hCG содержит шесть дисульфидных мостиков, однако вследствие их различающейся аминокислотной последовательности они отличаются своей структурой более высокого порядка, что приводит к разному свертыванию и распределению заряженных, полярных и гидрофобных областей (Fox et al. (2001) Three-dimensional structure of human follicle-stimulating hormone. Mol Endocrinol. 15(3), 379-89).
Хотя обе бета-субъединицы FSH и hCG гликолизированы, бета-субъединица FSH содержит только N-гликолизирование (N-7 и N-24), в то время как бета-субъединица hCG содержит как N- так и О-гликолизирование (N-13, N-30, O-121, O-127, O-132 и O-138). Дополнительное гликолизирование в бета-субъединице hCG делает его более гидрофильным, чем FSH. β-субъединицы обеспечивают специфичность взаимодействия с рецептором.
Клетки СНО обычно используют для продуцирования фармацевтических рекомбинантных белков. Структурный анализ показал, что сиаловая кислота присоединяется исключительно посредством α2,3-связи. Многие гликопротеины человека содержат смесь как α2,3-, так и α2,6-связей для остатков сиаловой кислоты. Следовательно, рекомбинантные белки, экспрессированные с применением системы CHO, будут отличаться от своих природных аналогов типом связей концевой сиаловой кислоты.
БЕСПЛОДИЕ
В данном контексте «бесплодие» должно быть определено как пониженная способность или неспособность забеременеть и иметь потомство. Женщин, которые способны забеременеть, но потом имеют неоднократные выкидыши, также называют бесплодными. Бесплодие также определено специальными терминами как неспособность забеременеть после года регулярных половых актов без контрацепции. Бесплодие может быть обусловлено многими причинами. Исследования показали, что чуть более половины случаев бесплодия являются результатом состояния здоровья женщины. Оставшаяся часть вызвана нарушениями сперматозоидов и невыясненными факторами. В настоящее время существует несколько возможностей для лечения бесплодия. Это рассчитанный по времени половой акт, применение вспомогательных репродуктивных технологий (ART), медицинское лечение эндометриоза, фибром и женской половой дисфункции (FSD) и хирургическое вмешательство для коррекции аномалий. Во вспомогательной репродуктивной технологии применяют лекарственные средства для стимулирования овуляции. Наряду с LH и hCG, FSH является одним из соединений, которые применяют в этом случае.
Жидкие композиции этих соединений являются подходящими для введения. К сожалению, ранее было доказано, что консерванты, добавленные к жидким композициям, в частности бензиловый спирт (ВА), фенол и м-крезол, оказывают дестабилизирующее действие на белок (Маа, Y.F. и Chung, С.Н. 1996, Aggregation of recombinant human growth hormone induced by phenolic compounds. Int. J. Pharm. 140:155-168; Lam, X.M., Patapoff, T.W., and Nguyen, Т.Н. 1997, The effect of benzyl alcohol on recombinant human interferon-gamma. Pharm. Res. 14:725-729; Hoffmann, J.A. and Lu, J. 2002, FSH and FSH variant formulations comprising benzyl alcohol as preservative. EP 0974359B1, 1-50).
Следовательно, важно предложить стабилизированную композицию, в частности ввиду того, что дозировка FSH, подлежащая введению, должна снижать риск побочных эффектов диссоциированных или агрегированных форм, подобных иммуногенным реакциям, если присутствует ненативный FSH. Однако дестабилизирующие явления, обусловленные консервантами, снижают фактический уровень активного гонадотропина, то есть FSH, в жидкой композиции. Таким образом, целью настоящего изобретения является предложение композиций, в частности жидких композиций FSH, которые являются стабильными, а также способа их стабилизации.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к применению солей, содержащих фармацевтически приемлемые катионы щелочных металлов, для стабилизации жидкой композиции FSH так, чтобы стабилизировать жидкую композицию FSH. Жидкая композиция, которую нужно стабилизировать, может представлять собой композицию с консервантом или без него.
Следующие воплощения являются предпочтительными:
1. Применение солей, содержащих фармацевтически приемлемые катионы щелочных металлов для стабилизации жидкой композиции FSH, где соль выбрана из группы, состоящей из фармацевтически приемлемых солей Na+ и солей K+ или их комбинации.
2. Применение согласно аспекту 1, где соли представляют собой соли Na+.
3. Применение согласно любому из аспектов 1 или 2, где соль представляет собой NaCl или Na2SO4.
4. Применение согласно любому из аспектов 1 или 2, где соль представляет собой Na2SO4.
5. Применение согласно любому из аспектов 1 или 2, где соль представляет собой комбинацию NaCl и Na2SO4.
6. Применение согласно любому из аспектов 1-5, где соль содержится в количестве от 20 до 500 мм, или в количестве 30-300 мм, или в количестве 50-200 мм.
7. Применение согласно любому из аспектов 1-6, где композиция FSH представляет собой композицию rFSH.
8. Применение согласно любому из аспектов 1-7, где композиция дополнительно содержит консервант.
9. Применение согласно аспекту 8, где композиция содержит бензиловый спирт, фенол и/или м-крезол.
10. Применение согласно любому из аспектов 1-9, где композиция представляет собой инъекционную композицию.
11. Способ стабилизации жидкой композиции FSH, включающий стадию добавления солей, содержащих фармацевтически приемлемые катионы щелочного металла, в указанную композицию, где указанные соли выбраны из группы, состоящей из солей Na+- и солей K+ или их комбинации.
12. Способ согласно аспекту 11, где соли определены как в аспектах 2-6 выше.
13. Способ согласно аспектам 11 и/или 12, где FSH, который нужно стабилизировать, представляет собой rFSH.
14. Способ согласно любому из аспектов 11-13, где композиция дополнительно содержит консервант.
15. Способ согласно аспекту 14, где консервант выбран из группы, состоящей из бензилового спирта, фенола и м-крезола.
16. Применение согласно любому из аспектов 1-10, где жидкая композиция представляет собой восстановленную жидкую композицию, которая была получена из лиофилизированной композиции.
17. Способ согласно любому из аспектов 11-15, где стадию добавления соли осуществляют до стадии лиофилизации.
18. Способ согласно аспекту 17, где стадию восстановления осуществляют после стадии лиофилизации.
19. Способ согласно аспекту 17 и/или 18, где соль содержится в лиофилизированной композиции, или где соль содержится в жидкости для восстановления.
Композиция, которая снабжена стабилизирующей солью, входит, таким образом, в альтернативное воплощение, хранящееся в лиофилизированном состоянии. Лиофилизацию осуществляют как общеизвестно специалисту в данной области техники. Затем лиофилизированную композицию можно хранить до окончательного применения пациентом. Затем перед введением лиофилизированную композицию восстанавливают любой из известных сред для восстановления, например стерилизованной водой. Соль содержится или в лиофилизированной композиции или в жидкости для восстановления.
20. Применение или способ согласно любому из аспектов 1-19, где жидкая композиция представляет собой композицию для однократного применения или многодозовую композицию, предпочтительно для инъекции.
В предпочтительном воплощении соль содержится непосредственно в жидкой композиции самой по себе, которая не лиофилизирована, а хранится в виде жидкости на складе.
В частности, в предпочтительном воплощении настоящее изобретение относится к стабилизации жидкой композиции FSH, где катион щелочного металла выбран из группы, состоящей из Na+ и K+. Особенно предпочтительно соль представляет собой NaCl или Na2SO4.
Как описано выше, жидкие композиции FSH пригодны для лечения бесплодия. В связи с этим становится ясно, что жидкие композиции FSH могут быть нестабильными; это верно для всех жидких композиций FSH, включая композиции, предназначенные для однократного применения. Нестабильность может быть еще более выраженной, если жидкие композиции FSH содержат консервант, который является необходимым, например, для всех многодозовых композиций. Данный консервант может представлять собой любой консервант, полезный для консервирования композиции FSH; таким образом, консервантом может являться консервант, который одобрен FDA (Управление по контролю за продуктами и лекарствами (США)) для композиций FSH, в частности, например, одобренный FDA консервант, одобренный для парентеральных композиций FSH, такой как, например, бензиловый спирт, фенол и/или м-крезол; консервант, однако, не ограничен данными примерами. Стабильность FSH снижается, например, бензиловым спиртом, фенолом и/или м-крезолом.
Таким образом, заявленные и описанные сейчас соли, содержащие фармацевтически приемлемые катионы, применяют для стабилизации композиций FSH однократного применения.
Кроме того, заявленные и описанные сейчас соли, содержащие фармацевтически приемлемые катионы, применяют для стабилизации многодозовых композиций FSH; такие композиции не нуждаются во включении консерванта, но могут также содержать консервант.
Добавление заявленных и описанных в данном описании изобретения солей, содержащих фармацевтически приемлемые катионы, то есть солей Na+- и K+-, стабилизирует жидкую композицию FSH. В особенно предпочтительном воплощении соли представляют собой фармацевтически приемлемые соли. Стабилизация достигается в композициях для однократного применения или многодозовых композициях, в частности в течение более продолжительного периода хранения, и может в еще одном возможном воплощении быть полезной в качестве меры противодействия дестабилизирующему эффекту консервантов, таких как бензиловый спирт, фенол и/или м-крезол.
Соли, которые можно применять согласно настоящему изобретению, включают в предпочтительном воплощении NaCl или Na2SO4.
Соль предпочтительно содержится в количестве от 20 до 500 мм, еще более предпочтительно она содержится в количестве 30-300 мм; в конкретном предпочтительном воплощении она содержится в количестве 50-200 мм.
Максимальное количество добавленной соли ограничено осмоляльностью раствора. Для минимизации боли при инъекции раствор предпочтительно должен быть изотоническим или по меньшей мере не гипертоническим. Так как все эксципиенты в растворе вносят вклад в осмоляльность, максимальное количество соли, которое может быть добавлено в раствор, зависит от количества других присутствующих компонентов.
Соль предпочтительно содержится в количестве, приводящем к максимальной осмоляльности 350 миллиосмоль/кг, еще более предпочтительно в количестве, приводящем к максимальной осмоляльности 320 миллиосмоль/кг; в конкретном предпочтительном воплощении она содержится в количестве, приводящем к максимальной осмоляльности 300 миллиосмоль/кг.
Теория осмоляльности
Осмоляльность представляет собой практическое средство для общей оценки вклада различных растворенных веществ, присутствующих в растворе, в осмотическое давление раствора. Осмоляльность может быть измерена в соответствии с Ph. Eur. (Европейская фармакопея) 2.2.35, 7-е издание, Приложение 2011 (7.2), раздел "Osmolality", 01/2008: 20235.
«Соль» в контексте настоящего изобретения представляет собой химической соединение, полученное из кислоты путем замены водорода, полностью или частично, металлом или электроположительным радикалом.
Определение «солей с (или содержащих) катионами(ы) фармацевтически приемлемых солей» относится ко всем солям, которые образованы с катионами, одобренными для в/м (внутримышечной) или п/к (подкожной) доставки, согласно перечню инертных ингредиентов FDA; катионами щелочных металлов в данной группе являются натрий (Na+) и калий (K+).
Авторы изобретения неожиданно обнаружили, что два очень конкретных катиона являются особенно подходящими для стабилизации композиции FSH. Таким образом, соли могут быть образованы следующими фармацевтически приемлемыми катионами: калия (моно-, двух- или трехосновные) или натрия (моно- или двух- или трехосновные). Предпочтительно соли представляют собой соли натрия. Особенно предпочтительными являются NaCl и Na2SO4.
Гонадотропин, который можно стабилизировать согласно настоящему изобретению, представляет собой FSH, то есть фолликулостимулирующий гормон, возможно в комбинации с дополнительными активными ингредиентами.
FSH представляет собой полученный из мочи или плазмы или рекомбинантный FSH (rFSH). В предпочтительном воплощении FSH представляет собой FSH из мочи или rFSH; особенно предпочтительно он представляет собой rFSH.
Как указано выше, сейчас является возможно получать FSH рекомбинантно. Таким образом, ссылка здесь на FSH в общем всегда включает как полученный из мочи, так и рекомбинантный (r) гонадотропин. Таким образом, ссылка на FSH также включает rFSH.
В предпочтительном воплощении изобретения композиция представляет собой жидкую композицию rFSH, наиболее предпочтительно инъекционную, которая стабилизирована Na2SO4 или NaCl.
В предпочтительном воплощении изобретения композиция представляет собой жидкую композицию rFSH, наиболее предпочтительно инъекционную, которая стабилизирована Na2SO4 или NaCl.
В альтернативном воплощении rFSH во всех воплощениях представляет собой FSH длительного действия. Композиции FSH длительного действия могут быть получены, как общеизвестно специалисту в данной области техники, например путем модифицирования молекулы FSH или путем модифицирования композиции.
Таким образом, в данном изобретении FSH охватывает все возможные полученные из мочи или рекомбинантные формы вышеуказанного FSH, а также все возможные комбинации форм FSH. Также охвачена композиция для однократного применения и одна или более других композиций (одного и того же или другого гонадотропина) для многодозового применения.
Одним возможным продуктом может быть композиция, включающая FSH (возможно с CG, LH, LH-активностью и так далее), все в разных флаконах. LH-Активность, если присутствует, может возникать от LH или CG. LH можно замещать эквивалентной дозой CG и наоборот; «эквивалентную дозу» в данном контексте можно вычислить на основании того, что 1 ME (международная единица) CG эквивалентна 5-7 ME LH в Pharmacopeia Van Hell Bioassay (Van Hell, H et al, Acta Endocrin. 47, 409-418, 1964).
Предпочтительная комбинация представляет собой комбинацию (r)FSH, (r)LH и (r)hCG, все в разных флаконах.
Возможные комбинации в разных флаконах также включают: мочевой (и) FSH и uhCG или uFSH и uLH; кроме того (rhCG или rLH или rFSH) и (uhCG или uLH или rhCG или rLH) и все возможные их перестановки.
Другая предпочтительная комбинация представляет собой комбинацию (r)FSH и (r)hCG в разных флаконах соответственно.
Другая предпочтительная комбинация представляет собой комбинацию (r)FSH и (r)LH в разных флаконах соответственно.
Препарат FSH по настоящему изобретению представляет собой жидкий препарат. Предпочтительно препарат является инъекционным. Препараты могут поставляться в виде продукта, содержащего одну, две или более фармацевтическую(их) композицию(й), включающую(их) FSH или FSH/hCG, для введения раздельно или вместе. При раздельном введении, введение может быть последовательным. Продукт может поставляться в любой подходящей упаковке. Например, продукт может содержать несколько предварительно заполненных шприцев, каждый из которых включает FSH (композицию FSH), или дополнительно hCG (композицию hCG), например, где шприцы могут быть упакованы в блистерную упаковку или другие средства для сохранения стерильности. Продукт, возможно, может содержать инструкции для применения композиций FSH. Согласно еще одному аспекту препарат FSH по изобретению предлагается в виде многодозового препарата. Настоящее изобретение, однако, также прямо направлено на препараты, предназначенные для однократного применения. Настоящее изобретение также относится к стабилизации композиций как части набора. Такой набор будет включать по меньшей мере один контейнер, содержащий одну или более суточных доз FSH, или например два контейнера (например флакон), каждый из которых содержит другой гонадотропин и, например, дополнительные инструкции (например по введению) и, например, дополнительные устройства для инъекции. В предпочтительном воплощении применяют шприц-ручку для многократных инъекций, при помощи которого раствор FSH заполняют в соответствующие картриджи.
В предпочтительном воплощении FSH содержится в количестве 35-850 МЕ/мл, предпочтительно 50-800 МЕ/мл, еще более предпочтительных 100-600 МЕ/мл.
Особенно предпочтительный препарат, например, 600 МЕ/мл rFSH, имеет следующую композицию: 600 МЕ/мл rFSH.
От 0,001-0,05, предпочтительно 0,005 мг/мл Полисорбата 20 От 0,1 до 10, предпочтительно 1,0 мг/мл L-метионина От 0,5 до 50, предпочтительно 5,0 мг/мл фенола.
От 1 до 100, предпочтительно 14 мг/мл двухосновного сульфата натрия (то есть 0,1 М).
От 0,1 до 10, предпочтительно 1 мМ натрий-фосфатного буфера (pH от 6 до 8, предпочтительно pH 6,5).
Осмоляльность раствора предпочтительно равна 300 миллиосмоль/кг (pH относится к pH всего раствора).
Инъекционные депо-формы могут быть изготовлены путем формирования микрокапсульных матриц FSH (и других агентов, если они присутствуют) в биоразлагаемых полимерах. Депо-формы/системы замедленного высвобождения на основе полимера могут, в зависимости от их химической природы, представлять собой, например, микро- или наночастицы, гидрогели, мицеллы, эмульсии или импланты. В зависимости от соотношения FSH и полимера и природы конкретного используемого полимера, можно контролировать скорость высвобождения FSH. Примеры биоразлагаемых полимеров включают системы сополимеров полилактид/полигликолид, поливинилпирролидон, поли(ортоэфиры), поли(ангидриды), поли(этиленгликоль), полиаминокислоты, полисахариды, например гиалуронат натрия (NaHA) или другие его соли, желатин, хитозан и так далее. Все указанные полимеры могут быть получены или модифицированы для оптимизации доставки белкового лекарственного средства или его стабильности. Инъекционные депо-препараты также получают посредством захвата FSH в липидные системы или полимер-липидные смеси, такие как мицеллы, липосомы или микроэмульсии, которые совместимы с тканями организма.
Инъекционные препараты можно стерилизовать, например посредством фильтрации через фильтр, удерживающий бактерии, или путем включения стерилизующих агентов в форме стерильных твердых композиций, которые могут быть растворены или диспергированы в стерильной воде или другой стерильной инъекционной среде непосредственно перед применением. Инъекционные композиции могут поставляться в любом подходящем контейнере, например флаконе, предварительно заполненном шприце, инъекционных картриджах и подобном, как описано выше.
pH и точную концентрацию разных компонентов фармацевтической композиции регулируют в соответствии с установившейся в этой области практикой. Смотри GOODMAN and GILMAN's THE PHARMACOLOGICAL BASIS FOR THERAPEUTICES, 7th edition. В предпочтительном воплощении композиции по изобретению поставляют в виде композиций для парентерального введения. Основные способы получения парентеральных композиций известны в данной области техники и описаны в REMINGTON; THE SCIENCE AND PRACTICE OF PHARMACY, см. выше, на с.780-820. Парентеральные композиции могут поставляться в жидком препарате или в виде твердого вещества, которое смешивают со стерильной инъекционной средой непосредственно перед введением. В особенно предпочтительном воплощении парентеральные композиции поставляют в форме дозированных единиц для облегчения введения и обеспечения однородности дозирования.
FSH по настоящему изобретению можно получать обычными способами из мочи или можно получить рекомбинантно. Возможные способы получения также указаны, например, в WO 2009/127826.
hCG может быть получен любыми способами, известными в данной области техники. hCG, при использовании в данном описании изобретения, включает человеческий и рекомбинантный hCG. Человеческий hCG может быть очищен от любого соответствующего источника (например мочи и плаценты) любым способом, известным в данной области техники. Способы экспрессирования и очистки рекомбинантного hCG хорошо известны в данной области техники.
LH может быть получен любыми способами, известными в данной области техники. LH, при использовании в данном описании изобретения, включает человеческий и рекомбинантный LH. Человеческий LH может быть очищен от любого соответствующего источника (например мочи) любым способом, известным в данной области техники. Способы экспрессирования и очистки рекомбинантного LH известны в данной области техники.
Фармацевтическая композиция может быть предназначена для лечения бесплодия, например для применения, например, во вспомогательных репродуктивных технологиях (ART), индукции овуляции (OI) или внутриматочном оплодотворении (IUI). Фармацевтическую композицию можно применять, например, при медицинских показаниях, когда применяются известные препараты FSH. В настоящем изобретении также предлагается применение стабилизированного препарата FSH, описанного в данном описании изобретения (согласно аспектам изобретения) для, или в изготовлении лекарственного средства для лечения бесплодия. Фармацевтические композиции могут быть изготовлены в виде хорошо известных композиций для любого пути введения лекарственного средства, например перорального, ректального, парентерального, чрескожного (например, пластырная технология), внутривенного, внутримышечного, подкожного, интрацистернального, внутривагинального, внутрибрюшинного, местного (порошки, мази или капли) или в виде букального или назального спрея. Типичная композиция содержит фармацевтически приемлемый носитель, такой как водный раствор, нетоксичные эксципиенты, включая соли и консерванты, буферы и тому подобное, как описано, наряду с прочими, в пятнадцатом издании Remington's Pharmaceutical Science (Matt Publishing Company, 1975) на страницах 1405-1412 и 1461-87, и в четырнадцатом издании Национального формуляра XIV (American Pharmaceutical Association, 1975).
Примеры подходящих водных и неводных фармацевтических носителей, разбавителей, растворителей или средств доставки включают воду, этанол, полиолы (такие как глицерин, пропиленгликоль, полиэтиленгликоль и тому подобные), карбоксиметилцеллюлозу и подходящие их смеси, растительные масла (такие как оливковое масло) и инъекционные органические сложные эфиры, такие как этилолеат.
Композиции могут также содержать добавки, такие как, но без ограничения ими, консерванты, увлажнители, эмульгаторы, буферные агенты и диспергирующие агенты. Антибактериальные и противогрибковые агенты могут быть включены для предупреждения роста микробов и включают, например, парабены, хлорбутанол, фенолы, сорбиновую кислоту и тому подобное. Кроме того, может быть желательно включать агенты, регулирующие тоничность.
В некоторых случаях для продолжительного действия желательно замедлить абсорбцию FSH (и других активных ингредиентов, если они присутствуют) при подкожной или внутримышечной инъекции. Этого можно достичь применением жидкой суспензии кристаллического или аморфного вещества с плохой растворимостью в воде. Скорость поглощения, например, FSH тогда зависит от скорости его растворения, которая, в свою очередь, может зависеть от размера кристаллов и кристаллической формы. Альтернативно, отложенное поглощение парентерально введенной комбинированной формы FSH достигается путем растворения или суспендирования комбинации FSH в масляном носителе.
Согласно настоящему изобретению, авторами изобретения была сделана попытка изучить влияние некоторых соединений на стабильность жидкой композиции гонадотропина; в данном изобретении изучался стабилизирующий, а также дестабилизирующий эффект некоторых соединений.
Термин «стабильность» может относиться к химической стабильности, включающей ковалентную модификацию аминокислотной последовательности, но в контексте стабильности белка он также может относиться к физической стабильности, которая включает изменения свернутого состояния белка (то есть нативное состояние), не включая расщепление ковалентной связи.
В настоящем изобретении термин «стабильность» относится к физической стабильности композиций гонадотропинов, в частности FSH по настоящему изобретению. Физическая нестабильность белковой композиции может быть вызвана агрегацией молекул белка с образованием агрегатов более высокого порядка, диссоциацией гетеродимеров на мономеры, или любым другим конформационным изменением, которое снижает по меньшей мере одну биологическую активность FSH-белков, включенных в настоящее изобретение.
«Стабильный» раствор или препарат представляет собой такой раствор или препарат, где степень агрегации, диссоциации, конформационной модификации, потери биологической активности и подобного белков в нем контролируется удовлетворительным образом и не увеличивается неприемлемо со временем. Стабильность можно оценить способами, хорошо известными в данной области техники, включающими измерение светорассеяния образца, визуальный контроль прозрачности и/или окрашивания, поглощения или оптической плотности, определения размера молекул (например посредством эксклюзионной хроматографии или фракционирования в потоке при наличии поля), биологической активности in vitro или in vivo и/или посредством дифференциальной сканирующей калориметрии (DSC). Другие способы оценки стабильности хорошо известны в данной области техники и также могут применяться согласно настоящему изобретению.
Известно, что некоторые консерванты обладают выраженным дестабилизирующим влиянием на препараты гонадотропина, и в данном изобретении неожиданно было обнаружено, что соли, в частности соли, содержащие фармацевтически приемлемые катионы щелочных металлов, которые, как было показано здесь, являются подходящими для стабилизации жидкой композиции FSH, в частности Na+ или K+, такие как NaCl или Na2SO4, дополнительно полезны для противодействия дестабилизирующим эффектам консерванта, такого как бензиловый спирт, фенол и м-крезол, который должен содержаться в жидкой многодозовой композиции FSH для медицинского применения. Заявленные здесь соли обладают стабилизирующим воздействием на жидкую композицию FSH, которое выгодным и неожиданным образом даже более выражено, чем стабилизирующие эффекты известных стабилизаторов, таких как, например, сахароза. Улучшенный стабилизационный эффект по сравнению с известными стабилизаторами, такими как сахароза, особенно удивителен. Кроме того, совершенно неожиданно стабилизирующие эффекты солей по изобретению могут быть продемонстрированы для композиций FSH, хотя для очень похожего hCG не может быть показано никакого стабилизирующего эффекта. Также было неожиданным то, что наблюдаемые стабилизирующие эффекты не подчиняются так называемому ряду Гофмейстера (смотри также ниже), а фактически действуют вопреки ему.
Из предшествующего уровня техники было известно, что в фармацевтических композициях FSH происходит разложение FSH, и это было подтверждено первой серией примеров в данной заявке.
FSH будет разлагаться и в зависимости от времени, и в зависимости от температуры. В частности, при температурах выше комнатной температуры будут изменяться вторичная, третичная и четвертичная структуры.
Очевидно, что конформационное развертывание третичной и вторичной структур FSH, происходящее при нагревании, представляет собой переход между двумя состояниями (когда агрегации белка ограничена). Это развертывание может быть независимым от диссоциации субъединиц (изменений в четвертичной структуре).
Кроме того, из настоящего изобретения становится ясно, что FSH, содержащий консервант, подобный бензиловому спирту или фенолу, когда такие консерванты необходимы, например, в качестве противомикробных агентов в жидких препаратах FSH, очевидным образом влияет на стабильность многодозовых композиций FSH негативным образом. При этом долговременная стабильность FSH понижается, температура денатурации FSH становится ниже, и уже денатурированные формы имеют более низкий уровень вторичных структур, чем препараты FSH, не содержащие консерванты.
В настоящем изобретении также впервые показано, что соли, содержащие фармацевтически приемлемые катионы щелочных металлов для стабилизации жидкого препарата FSH, а именно Na и K, оказывают значительное влияние на стабильность жидких препаратов FSH. Можно видеть, что вторичная структура FSH в жидких препаратах FSH, содержащих эти соли, не будет значительно меняться при нагревании до 76,5°C. Денатурированная форма является относительно структурированной в присутствие, например, Na2SO4, что делает денатурацию более обратимой и, таким образом, значительно увеличивает кинетическую стабильность белка. Это подтверждается приведенными сейчас данными по стабильности в реальном времени, показывающими выраженный стабилизирующий эффект на гетеродимерную структуру FSH.
Результаты ясно показывают, что заявленные сейчас соли, например сульфат натрия и хлорид натрия, могут ограничивать тенденцию молекул FSH к диссоциации и таким образом значительно увеличивают стабильность при хранении.
Настоящее изобретение также относится к способу стабилизации жидкой композиции FSH, включающему стадию добавления указанных выше солей к указанной композиции.
Все исследования были подтверждены дополнительно осуществленными данными в реальном времени.
Краткое описание графических материалов
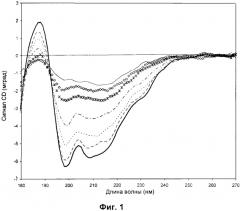
Фиг.1:
Сигнал CD (кругового дихроизма, смотри ниже) (мградус) в зависимости от длины волны (нм) показан для rFSH при разных температурах. Не наблюдалось значительного различия между спектрами 24,0°C→45,9°C, но наблюдалось зависимое от температуры уменьшение CD-сигнала выше 50°C. Белок rFSH (0,93 мг/мл) растворяли в 3,57 мМ фосфатном буфере pH 6,3, содержащем 0,0036 мг/мл Полисорбата 20. Сканирование при 24,0°C (сплошная жирная линия), 50,3°C (штриховая линия), 54,7°C (пунктирная линия), 59,0°C (штрихпунктирная линия), 63,4°C (звездочки), 67,8°C (ромбы) и 76,5°C (сплошная линия).
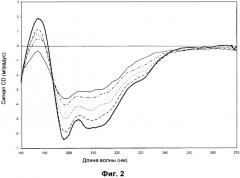
Фиг.2:
Сигнал CD (мградус) в зависимости от длины волны (нм) показан для rFSH, содержащего Na2SO4, при различных температурах. Не наблюдалось значительного различия между спектрами 24,0°C→45,9°C. Белок rFSH растворяли в 3,57 мМ фосфатном буфере pH 6,3, содержащем 0,0036 мг/мл Полисорбата 20 и 8,6 мг/мл сульфата натрия (Na2SO4). Сканирование при 2,0°C (сплошная жирная линия), 50,3°C (штриховая линия), 54,7°C (пунктирная линия), 59,0°C (штрихпунктирная линия) и 76,5°C (сплошная линия).
Фиг.3:
Сигнал CD (мградус) в зависимости от длины волны (нм) показан для rFSH, содержащего бензиловый спирт, при различных температурах. Не наблюдалось значительного различия между спектрами 24,0°C→45,9°C. Белок rFSH (0,93 мг/мл) растворяли в 3,57 мМ фосфатном буфере pH 6,3, содержащем 0,0036 мг/мл Полисорбата 20 и 0,17 мг/мл бензилового спирта. Сканирование при 24,0°C (сплошная жирная линия), 45,9°C (кружки), 50,3°C (штриховая линия), 54,7°C (пунктирная линия), S9,0°C (штрихпунктирная линия), 63,4°C (звездочки), 67,8°C (ромбы) и 76,5°C (сплошная линия).
Фиг.4
Последовательные DSC-термограммы hCG и rFSH. Данные DSC для 5 мг/мл hCG в смеси 0,005 мг/мл Полисорбата 20, 0,5 мг/мл L-метионина, 1 мМ фосфатного буфера, pH 6,5 и 2,4 мг/мл rFSH в смеси 0,005 мг/мл Полисорбата 20, 0,5 мг/мл L-метионина, 0,24 М NaCl, 1 мМ фосфатного буфера, pH 6,5. Скорость сканирования 2,0°C/мин. Первое сканирование rFSH (сплошная линия), второе сканирование rFSH (штрихпунктирная линия), первое сканирование hCG (штриховая линия) и второе сканирование hCG (пунктирная линия). После первого сканирования образец охлаждали до 20°C перед вторым сканированием.
Фиг.5:
DSC-термограммы hCG с разными сахарами или солями. Данные DSC для 5 мг/мл hCG в смеси 0,005 мг/мл Полисорбата 20, 0,5 мг/мл L-метионина и 1 мМ фосфатного буфера, pH 6,5. Без добавления сахара или соли (сплошная жирная линия), 0,1 М Na2SO4 (сплошная линия), 0,1 М NaCl (пунктирная линия), 0,1 M NaClО4 (штриховая линия) и 0,1 М сахароза (штрихпунктирная линия). Скорость сканирования 2,0°C/мин.
Фиг.6:
DSC-термограммы rFSH с разными сахарами и солями. Данные DSC для 2,4 мг/мл rFSH в смеси 0,005 мг/мл Полисорбата 20, 0,5 мг/мл L-метионина и 1 мМ фосфатного буфера, pH 6,5. Без добавления сахара или соли (сплошная жирная линия), 0,1 М Na2SO4 (сплошная линия), 0,1 М NaCl (пунктирная линия), 0,1 М NaClО4 (штриховая линия) и 0,1 М сахароза (штрихпунктирная линия). Скорость сканирования 1,0°C/мин.
Настоящее изобретение дополнительно пояснено посредством следующих примеров, которые, однако, никоим образом не следует истолковывать, как ограничение объема изобретения.
ПРИМЕРЫ
Пример 1 - Спектроскопия кругового дихроизма с использованием синхротронного излучения (SRCD) СПОСОБ
Спектроскопию кругового дихроизма выполняли, используя синхротронное оборудование в Орхуском Университете, Дания. Все спект