Квантовые точки сульфида серебра, излучающие в ближней инфракрасной области спектра, способ их получения и применение в биологии
Иллюстрации
Показать всеИзобретение относится к квантовым точкам сульфида серебра, излучающим в ближней инфракрасной области спектра, и их применению в биологии. Квантовые точки сульфида серебра содержат присоединенные к поверхности гидрофильные группы из меркаптосодержащего гидрофильного реагента. Гидрофильный реагент выбран из меркаптоуксусной кислоты, меркаптопропионовой кислоты, цистеина, цистеамина, тиоктовой кислоты и меркаптоацетата аммония или любых их комбинаций. Способ получения указанных квантовых точек включает реакцию гидрофобных квантовых точек сульфида серебра со стехиометрическим или избыточным количеством меркаптосодержащего гидрофильного реагента в полярном органическом растворителе. Квантовые точки сульфида серебра имеют высокий выход флуоресценции, хорошую стабильность флуоресценции, хорошую биосовместимость, единообразные размеры и могут быть использованы для визуализации клеток и для визуализации биологических тканей. 3 н. и 4 з.п. ф-лы, 5 ил., 6 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к областям техники «химия материалов» и «биология». В частности, настоящее изобретение относится к квантовым точкам сульфида серебра, излучающим в ближней инфракрасной области спектра, к способу их получения и к применению в биологии.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
В качестве фундаментального способа биомедицинских исследований технологии флуоресцентного мечения и детектирования играют важную роль в исследованиях на субклеточном уровне, клеточном уровне и на уровне in vivo. При визуализации in vivo технология флуоресцентной визуализации с использованием квантовых точек, излучающих в ближней инфракрасной области спектра, имеет много уникальных преимуществ. Например, она обеспечивает более глубокое проникновение в ткани и может преодолеть дефект, состоящий в том, что визуализация глубоких тканей с использованием квантовых точек, излучающих в видимой области спектра, чувствительна к фоновой флуоресценции. Поэтому она привлекает большое внимание в медицинской диагностике, молекулярной биологии, клеточной биологии и т.п. В настоящее время все стандартные квантовые точки, излучающие в ближней инфракрасной области спектра, содержат токсичные элементы, такие как Cd, Hg, Pb и т.п. Описаны квантовые точки сульфида серебра (Ag2S) с низкой токсичностью или вообще не токсичные, излучающие флуоресценцию в ближней инфракрасной области спектра (Near-infrared photoluminescent Ag2S quantum dots from single source precursor. J. Am. Chem. Soc, 2010, 132, 1470), но частицы являются относительно крупными, а интенсивность флуоресценции в ближней инфракрасной области спектра - недостаточно сильной. В других публикациях, касающихся Ag2S, нет информации о флуоресценции. Более того, Ag2S, описанный в этих публикациях, обладает плохой гомогенностью и дисперсностью и получен сложным способом. Кроме того, во многих публикациях описана функционализация поверхности квантовых точек, то есть преобразование из гидрофобной формы в гидрофильную форму, для обеспечения пригодности квантовых точек для использования в биомедицинских исследованиях. Однако описанные способы функционализации поверхности квантовых точек по существу не пригодны для квантовых точек Ag2S, поскольку все квантовые точки Ag2S обладают структурой сверхрешетки, и трудно модифицировать сверхрешетку традиционными способами. Кроме того, реагенты с сильной окисляемостью не пригодны для преобразования Ag2S в гидрофильную форму. Поэтому большое значение имеет разработка способа получения и функционализации поверхности квантовых точек Ag2S, который был бы простым и мог бы обеспечить высокое качество квантовых точек Ag2S с однородным размером частиц, хорошей дисперсностью частиц, высокой интенсивностью флуоресценции и хорошей воспроизводимостью, для того чтобы квантовые точки Ag2S можно было использовать в области биологии.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Для преодоления вышеуказанных проблем задачей настоящего изобретения является обеспечение квантовых точек сульфида серебра, излучающих в ближней инфракрасной области спектра. Квантовые точки сульфида серебра, излучающие в ближней инфракрасной области спектра, обладают такими преимуществами, как высокий выход флуоресценции, стабильность флуоресценции, единообразные размеры, легкий способ получения и т.п., и могут также обладать хорошей биосовместимостью после функционализации поверхности, которая делает их пригодными для биологической визуализации.
Квантовые точки сульфида серебра, излучающие в ближней инфракрасной области спектра, согласно настоящему изобретению содержат гидрофильные группы, присоединенные к их поверхности, которые получают из меркаптосодержащего гидрофильного реагента. Гидрофильный реагент выбран из меркаптоуксусной кислоты, меркаптопропионовой кислоты, цистеина, цистеамина, тиоктовой кислоты и аммония меркаптоацетата или любых их комбинаций.
Для преодоления вышеуказанных проблем еще одной задачей настоящего изобретения является обеспечение способа получения квантовых точек сульфида серебра, излучающих в ближней инфракрасной области спектра, который включает следующие стадии:
1) получение гидрофобных квантовых точек сульфида серебра; и
2) проведение реакции гидрофобных квантовых точек сульфида серебра, полученных на стадии 1), с эквивалентным или избыточным количеством меркаптосодержащего гидрофильного реагента в полярном органическом растворителе, так что к поверхности квантовых точек сульфида серебра присоединяют гидрофильные группы для получения гидрофильных квантовых точек сульфида серебра, излучающих в ближней инфракрасной области спектра. Гидрофильные квантовые точки сульфида серебра, полученные согласно настоящему изобретению, обладают хорошими рабочими характеристиками, при условии, что число молей меркаптосодержащего гидрофильного реагента больше или равно числу молей гидрофобных квантовых точек сульфида серебра. Отношение числа молей меркаптосодержащего гидрофильного реагента к числу молей гидрофобных квантовых точек сульфида серебра можно регулировать в зависимости от фактической потребности во время процесса получения, для того чтобы можно было решить задачи настоящего изобретения.
Гидрофильный реагент выбран из меркаптоуксусной кислоты, меркаптопропионовой кислоты, цистеина, цистеамина, тиоктовой кислоты и аммония меркаптоацетата или любых их комбинаций.
В способе получения квантовых точек сульфида серебра, излучающих в ближней инфракрасной области спектра, согласно настоящему изобретению полярный органический растворитель на стадии 2) содержит, но не ограничивается этим, этанол, метанол, ацетон или 1-метил-2-пирролидон, или любую их комбинацию. Значение pH смешанной системы, состоящей из гидрофобных квантовых точек сульфида серебра и меркаптосодержащего гидрофильного реагента, на стадии 2) регулируют так, чтобы оно лежало в диапазоне от 7 до 14, и проводят реакцию смешанной системы в полярном органическом растворителе при 2-80°C в течение 3 или более часов. Гидрофильные квантовые точки сульфида серебра, полученные согласно настоящему изобретению, обладают хорошими рабочими характеристиками, при условии, что время реакции больше или равно 3 часам. Время реакции можно регулировать в зависимости от фактической потребности во время процесса получения, для того чтобы можно было решить задачи настоящего изобретения.
Предпочтительно, способ получения гидрофобных квантовых точек сульфида серебра на стадии 1) включает следующие стадии:
1-1) нагревание смешанной реакционной системы, содержащей источник серебра и длинноцепочечный тиол, до 80-350°C в замкнутом пространстве до тех пор, пока не пройдет достаточная реакция; и
1-2) естественное охлаждение смешанной реакционной системы до комнатной температуры, последующее добавление полярного растворителя, центрифугирование и промывание с получением гидрофобных квантовых точек сульфида серебра, излучающих в ближней инфракрасной области спектра,
причем источник серебра содержит одно или более соединений, выбранных из нитрата серебра, диэтилдитиокарбамата серебра, дигидрокарбилдитиофосфата серебра, диоктилсульфосукцината серебра, тиобензоата серебра, ацетата серебра, додеканоата серебра, тетрадеканоата серебра и октадеканоата серебра;
а длинноцепочечный тиол содержит одно или более соединений, выбранных из октантиола, ундекантиола, додекантиола, тридекантиола, тетрадекантиола, пентадекантиола, гексадекантиола, октадекантиола, эйкозантиола, гексантиола, 1,6-гександитиола и 1,8-октандитиола.
В способе получения квантовых точек сульфида серебра, излучающих в ближней инфракрасной области спектра, согласно настоящему изобретению предпочтительно, чтобы смешанная реакционная система на стадии 1-2) дополнительно содержала поверхностно-активное вещество с координационной способностью, которое выбрано из длинноцепочечной алкилкислоты, алкиламина, длинноцепочечного спирта и длинноцепочечного тиола и простого эфира или любой их комбинации; и чтобы смешанная реакционная система была помещена для реакции в замкнутое пространство. Более предпочтительно, чтобы на стадии 2) гидрофобные квантовые точки сульфида серебра реагировали с меркаптосодержащим гидрофильным реагентом в условиях непрерывного перемешивания, и/или вибрации, и/или обработки ультразвуком в полярном органическом растворителе при 2-80°C в течение 3 или более часов.
В способе получения квантовых точек сульфида серебра, излучающих в ближней инфракрасной области спектра, согласно настоящему изобретению квантовые точки сульфида серебра, излучающие в ближней инфракрасной области спектра, полученные способом согласно настоящему изобретению, имеют моноклинную структуру, а размер их частиц меньше 8 нм.
Предусмотрено применение квантовых точек сульфида серебра, излучающих в ближней инфракрасной области спектра, согласно настоящему изобретению для визуализации биологических тканей.
В настоящем изобретении источник серебра и длинноцепочечный тиол используют в качестве реагентов, а нуклеация и рост гидрофобных квантовых точек сульфида серебра происходят в реакционных системах в присутствии поверхностно-активного вещества с другими координационными свойствами для получения гидрофобных квантовых точек сульфида серебра, причем длинноцепочечный тиол обеспечивает источник серы и может быть использован в качестве растворителя и поверхностно-активного вещества. Затем проводят функционализацию полученных гидрофобных квантовых точек сульфида серебра с использованием меркаптосодержащего гидрофильного реагента. Поскольку меркаптогруппы обладают превосходной способностью к связыванию с серебром, они могут заменять другие группы на поверхности квантовых точек сульфида серебра, что приводит к получению квантовых точек сульфида серебра, излучающих в ближней инфракрасной области, с низкой токсичностью, хорошей биосовместимостью и высоким выходом флуоресценции. Отличием от преобразования гидрофобного материала в гидрофильный материал согласно предшествующему уровню техники является то, что вначале согласно настоящему изобретению получают квантовые точки Ag2S, которые обладают структурой сверхрешетки, и которые не могут быть преобразованы в гидрофильные квантовые точки Ag2S в экспериментальных условиях, используемых для модификации на предшествующем уровне техники, из-за этой особой структуры. В многочисленных экспериментах, результаты которых совпадают с опытом авторов настоящего изобретения, было обнаружено, что время модификации, которое оказывает значительное влияние на эффект модификации, является ключевым условием эксперимента, если производится модификация квантовых точек Ag2S с особой структурой. Кроме того, было обнаружено, что лучшего эффекта модификации можно добиться, если время модификации равно или больше 3 часов. Чем дольше это время, тем лучше эффект модификации. Поэтому время можно регулировать в зависимости от фактической потребности во время процесса получения. Однако задачи настоящего изобретения могут быть решены при условии, что время равно или больше 3 часов. Кроме того, гидрофильные квантовые точки Ag2S после модификации являются монодисперсными, не агрегируют, обладают хорошей гидрофильностью и стабильностью и могут быть использованы для визуализации клеток, и в частности - для визуализации in vivo.
Более конкретно, способ согласно настоящему изобретению включает следующие стадии:
смешивание источника серебра, длинноцепочечного тиола и подходящего поверхностно-активного вещества; помещение смеси в замкнутое устройство и нагревание до соответствующей температуры в течение определенного времени для проведения нуклеации и роста квантовых точек; последующее естественное охлаждение и добавление избыточного количества этанола; центрифугирование и промывание с получением гидрофобных квантовых точек сульфида серебра; последующее смешивание полученных гидрофобных квантовых точек сульфида серебра, некоторого количества меркаптосодержащего гидрофильного реагента и этанола; перемешивание, вибрационная обработка или обработка ультразвуком смеси до полной реакции; центрифугирование и промывание водой с получением низкотоксичных квантовых точек сульфида серебра, излучающих в ближней инфракрасной области спектра, с хорошей биосовместимостью и высоким выходом флуоресценции, которые можно использовать для визуализации клеток.
Кроме того, описанное выше техническое решение может дополнительно включать следующие варианты осуществления:
1. Различные источники серебра, различные длинноцепочечные тиолы, различные поверхностно-активные вещества, различные температуры реакции и различное время реакции могут быть использованы в реакции для регулирования размера наночастиц сульфида серебра. Например, можно увеличить размер частиц посредством повышения температуры или увеличения времени реакции.
2. Дисперсность функционализированных квантовых точек Ag2S в водном растворе может быть изменена посредством регулирования значения pH (лучшую дисперсность получают при значении pH, лежащем в диапазоне от 7 до 14). Можно также отрегулировать пик эмиссии в зависимости от различной модификации различными меркаптосодержащими гидрофильными реагентами в реакции.
По сравнению с предшествующим уровнем техники, преимущества технического решения согласно настоящему изобретению состоят в том, что для способа согласно настоящему изобретению характерны умеренные условия реакции, простота осуществления, короткий производственный цикл, хорошая воспроизводимость и легкость управления. Полученные квантовые точки Ag2S имеют высокий выход флуоресценции, хорошую стабильность флуоресценции, превосходную биосовместимость и единообразные размеры, и они могут быть использованы для визуализации клеток in vitro и для визуализации in vivo.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
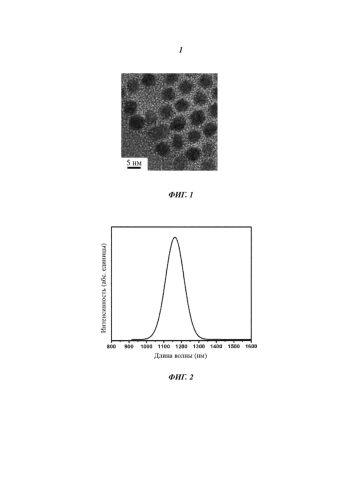
Фиг. 1 является полученным с помощью трансмиссионной электронной микроскопии (ТЭМ) изображением гидрофобных квантовых точек Ag2S из Примера 1;
Фиг. 2 является спектром флуоресценции в ближней инфракрасной области гидрофобных квантовых точек Ag2S из Примера 1;
Фиг. 3 является спектром флуоресценции в ближней инфракрасной области гидрофильных квантовых точек Ag2S из Примера 1;
Фиг. 4 является флуоресцентным фотоснимком клеток, специфически помеченных квантовыми точками сульфида серебра, излучающими в ближней инфракрасной области спектра, из Примера 1; и
Фиг. 5 является флуоресцентным фотоснимком опухоли живой мыши, специфически помеченной квантовыми точками сульфида серебра, излучающими в ближней инфракрасной области спектра.
ОПИСАНИЕ ПРИМЕРОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Способ получения согласно настоящему изобретению далее будет подробно описан на основании конкретных примеров его осуществления.
Пример 1
0,1 ммоля диэтилдитиокарбамата серебра и 10 г додекантиола смешали в колбе и нагревали до 200°C в атмосфере N2 в течение часа. После естественного охлаждения раствора до комнатной температуры к нему добавили 50 мл безводного этанола, затем полученную смесь центрифугировали, промыли и диспергировали в циклогексане. Полученный образец посредством дифракции рентгеновского излучения и трансмиссионной электронной микроскопии был идентифицирован как моноклинные квантовые точки Ag2S (размер частиц был равен примерно 5 нм, как показано на Фиг. 1), которые имели хороший эмиссионный спектр флуоресценции, как показано на Фиг. 2. К полученной дисперсии в циклогексане добавили 0,15 г тиоктовой кислоты и равный объем безводного этанола, после чего полученную смесь обработали ультразвуком в аппарате для звуковой очистки в течение 4 часов, центрифугировали и промыли деионизированной водой с получением водорастворимых квантовых точек Ag2S с размером частиц около 5 нм, которые сохранили очень сильную эмиссию флуоресценции, как показано на Фиг. 3. 0,25 мг этих квантовых точек Ag2S диспергировали в 100 мкл диметилсульфоксида (ДМСО) и 50 мкл раствора ДМСО, содержащего 0,01 ммоль нормальной сыворотки крови человека (NHS; от англ. Normal Human Serum), смешали с этим раствором. После этого к смешанному раствору добавили 50 мкл раствора ДМСО, содержавшего 0,01 ммоль хлористого этилена (EDC; от англ. ethylene dichloride), и полученную смесь герметично закрыли алюминиевой фольгой, перемешивали в течение 1 часа, центрифугировали и снова диспергировали в 100 мкл ДМСО. Смешанный раствор 0,15 мкл раствора Erbitux с концентрацией 2 мг/мл и 185 мкл 1× фосфатно-солевого буферного раствора (PBS; от англ. phosphate buffered saline) добавили к 100 мкл смешанного раствора Ag2S/ДMCO, полученную смесь оставили для протекания реакции в темноте при 4°C на 12 часов, затем центрифугировали при 400g в течение 4 минут, после чего отделили супернатант. Клетки MDA-MB-468 добавили к смешанному раствору 100 мкл супернатанта и 100 мкл 1×PBS, окрасили при 4°C в течение 2 часов, после чего 3 раза промыли 1× раствором PBS. Можно ясно видеть, что квантовые точки Ag2S излучают люминесценцию в клетках при возбуждении лазером с длиной волны 658 нм, при использовании фильтра на 1100 нм и фотографировании 2D InGaAs камерой (см. Фиг. 4).
Пример 2
0,1 ммоль нитрата серебра, 8 г додекантиола и 5,4 г олеиламина смешали в трехгорлой колбе и нагревали до 180°C в атмосфере воздуха в течение 1 часа. После того как раствор естественным образом охладился до комнатной температуры, было добавлено 50 мл безводного этанола. Полученную смесь центрифугировали, промыли и диспергировали в циклогексане. Полученный образец посредством дифракции рентгеновского излучения и трансмиссионной электронной микроскопии был идентифицирован как моноклинные квантовые точки Ag2S с размером частиц менее 8 нм, которые имели хороший эмиссионный спектр флуоресценции в ближней инфракрасной области спектра. К полученной дисперсии в циклогексане добавили 0,2 г L-цистеина, затем добавили равный объем безводного этанола. Полученную смесь перемешивали в течение 24 часов, затем центрифугировали и промыли деионизированной водой с получением водорастворимых квантовых точек Ag2S с размером частиц около 8 нм, которые сохраняли очень сильную эмиссию флуоресценции. 0,25 мг полученных квантовых точек Ag2S диспергировали в 100 мкл ДМСО и 50 мкл раствора ДМСО, содержавшего 0,01 ммоль NHS, смешали с этим раствором. Затем к смешанному раствору добавили 50 мкл раствора ДМСО, содержавшего 0,01 ммоль EDC. Полученную смесь герметично закрыли алюминиевой фольгой, перемешивали в течение 1 часа, центрифугировали и снова диспергировали в 100 мкл ДМСО. Смешанный раствор 15 мкл раствора Erbitux с концентрацией 2 мг/мл и 185 мкл 1×PBS добавили к 100 мкл смешанного раствора Ag2S/ДMCO. Полученную смесь оставили для протекания реакции в темноте при 4°C на 12 часов, затем центрифугировали при 400g в течение 4 минут, после чего отделили супернатант. Клетки MDA-MB-468 добавили к смешанному раствору 100 мкл супернатанта и 100 мкл 1×PBS, окрасили при 4°C в течение 2 часов, после чего 3 раза промыли 1× раствором PBS. Можно ясно видеть, что квантовые точки Ag2S излучают люминесценцию в клетках при возбуждении лазером с длиной волны 658 нм, при использовании фильтра на 1100 нм и фотографировании 2D InGaAs камерой.
Пример 3
0,1 ммоль тиобензоата серебра, 8 г гексадекантиола и 2 г триоктиофосфина оксида смешали в трехгорлой колбе и нагревали до 160°C в течение 4 часов. После того как раствор естественным образом охладился до комнатной температуры, было добавлено 50 мл безводного этанола. Полученную смесь центрифугировали, промыли и диспергировали в циклогексане. К дисперсии в циклогексане добавили 0,1 г меркаптопропионовой кислоты, затем добавили равный объем безводного этанола. Полученную смесь обрабатывали в вибраторе в течение 8 часов, центрифугировали и промыли деионизированной водой с получением водорастворимых квантовых точек Ag2S с размером частиц около 6 нм, которые сохраняли очень сильную эмиссию флуоресценции. 0,25 мг полученных квантовых точек Ag2S диспергировали в 100 мкл ДМСО и 50 мкл раствора ДМСО, содержавшего 0,01 ммоль NHS, смешали с этим раствором. Затем к смешанному раствору добавили 50 мкл раствора ДМСО, содержавшего 0,01 ммоль EDC. Полученную смесь герметично закрыли алюминиевой фольгой, перемешивали в течение 1 часа, центрифугировали и снова диспергировали в 100 мкл ДМСО. Смешанный раствор 15 мкл раствора Erbitux с концентрацией 2 мг/мл и 185 мкл 1× PBS добавили к 100 мкл смешанного раствора Ag2S/ДMCO. Полученную смесь оставили для протекания реакции в темноте при 4°C на 12 часов, затем центрифугировали при 400g в течение 4 минут, после чего отделили супернатант. Клетки MDA-MB-468 добавили к смешанному раствору 100 мкл супернатанта и 100 мкл 1×PBS, окрасили при 4°C в течение 2 часов, после чего 3 раза промыли 1× раствором PBS. Можно ясно видеть, что квантовые точки Ag2S излучают люминесценцию в клетках при возбуждении лазером с длиной волны 658 нм, при использовании фильтра на 1100 нм и фотографировании 2D InGaAs камерой.
Пример 4
0,1 ммоль гексадеканоата серебра, 5 г гексадекантиола и 4 г октадециламина смешали в трехгорлой колбе и нагревали до 200°C в атмосфере Аr в течение 1 часа. После того как раствор естественным образом охладился до комнатной температуры, было добавлено 50 мл безводного этанола. Полученную смесь центрифугировали, промыли и диспергировали в циклогексане. К дисперсии в циклогексане добавили 0,12 г меркаптопропионовой кислоты, затем добавили равный объем безводного этанола. Полученную смесь перемешивали в течение 24 часов, центрифугировали и промыли деионизированной водой с получением водорастворимых квантовых точек Ag2S с размером частиц около 6 нм, которые сохраняли очень сильную эмиссию флуоресценции. 0,25 мг полученных квантовых точек Ag2S диспергировали в 100 мкл ДМСО и 50 мкл раствора ДМСО, содержавшего 0,01 ммоль NHS, смешали с этим раствором. Затем к смешанному раствору добавили 50 мкл раствора ДМСО, содержавшего 0,01 ммоль EDC. Полученную смесь герметично закрыли алюминиевой фольгой, перемешивали в течение 1 часа, центрифугировали и снова диспергировали в 100 мкл ДМСО. Смешанный раствор 15 мкл раствора Erbitux с концентрацией 2 мг/мл и 185 мкл 1×PBS добавили к 100 мкл смешанного раствора Ag2S/ДMCO и оставили полученную смесь для протекания реакции в темноте при 4°C на 12 часов, затем центрифугировали при 400g в течение 4 минут, после чего отделили супернатант. Клетки MDA-MB-468 добавили к смешанному раствору 100 мкл супернатанта и 100 мкл 1×PBS, окрасили при 4°C в течение 2 часов, после чего 3 раза промыли 1× раствором PBS. Можно ясно видеть, что квантовые точки Ag2S излучают люминесценцию в клетках при возбуждении лазером с длиной волны 658 нм, при использовании фильтра на 1100 нм и фотографировании 2D InGaAs камерой.
Пример 5
0,1 ммоль дигидрокарбилдитиофосфата серебра, 10 г эйкозантиола и 4 г гексадециламина смешали в трехгорлой колбе и нагревали до 230°C в атмосфере Аr в течение 0,5 часа. После того как раствор естественным образом охладился до комнатной температуры, было добавлено 50 мл безводного этанола. Полученную смесь центрифугировали, промыли и диспергировали в циклогексане. К дисперсии в циклогексане добавили 0,1 г цистеамина, затем добавили равный объем безводного этанола. Полученную смесь перемешивали в течение 24 часов, затем центрифугировали и промыли деионизированной водой с получением водорастворимых квантовых точек Ag2S с размером частиц около 5 нм, которые сохраняли очень сильную эмиссию флуоресценции. 0,25 мг полученных квантовых точек Ag2S диспергировали в 100 мкл ДМСО и 50 мкл раствора ДМСО, содержавшего 0,01 ммоль NHS, смешали с этим раствором. Затем к смешанному раствору добавили 50 мкл раствора ДМСО, содержавшего 0,01 ммоль EDC. Полученную смесь герметично закрыли алюминиевой фольгой, перемешивали в течение 1 часа, центрифугировали и снова диспергировали в 100 мкл ДМСО. Смешанный раствор 15 мкл раствора Erbitux с концентрацией 2 мг/мл и 185 мкл 1×PBS добавили к 100 мкл смешанного раствора Ag2S/ДMCO и оставили полученную смесь для протекания реакции в темноте при 4°C на 12 часов, затем центрифугировали при 400g в течение 4 минут, после чего отделили супернатант. Клетки MDA-MB-468 добавили к смешанному раствору 100 мкл супернатанта и 100 мкл 1×PBS, окрасили при 4°C в течение 2 часов, после чего 3 раза промыли 1× раствором PBS. Можно ясно видеть, что квантовые точки Ag2S излучают люминесценцию в клетках при возбуждении лазером с длиной волны 658 нм, при использовании фильтра на 1100 нм и фотографировании 2D InGaAs камерой.
Пример 6
0,1 ммоль додеканоата серебра, 8 г октантиола и 4 г додециламина смешали в трехгорлой колбе и нагревали до 200°C в атмосфере Аr в течение 0,5 часа. После того как раствор естественным образом охладился до комнатной температуры, было добавлено 50 мл безводного этанола. Полученную смесь центрифугировали, промыли и диспергировали в циклогексане. К дисперсии в циклогексане добавили 0,12 г меркаптоуксусной кислоты, затем добавили равный объем безводного этанола, полученную смесь перемешивали в течение 24 часов, затем полученную смесь центрифугировали и промыли деионизированной водой с получением водорастворимых квантовых точек Ag2S с размером частиц около 5 нм, которые сохраняли очень сильную эмиссию флуоресценции. 0,25 мг полученных квантовых точек Ag2S диспергировали в 100 мкл ДМСО и 50 мкл раствора ДМСО, содержавшего 0,01 ммоль NHS, смешали с этим раствором. Затем к смешанному раствору добавили 50 мкл раствора ДМСО, содержавшего 0,01 ммоль EDC, полученную смесь герметично закрыли алюминиевой фольгой, перемешивали в течение 1 часа, центрифугировали и снова диспергировали в 100 мкл ДМСО. Смешанный раствор 15 мкл раствора Erbitux с концентрацией 2 мг/мл и 185 мкл 1×PBS добавили к 100 мкл смешанного раствора Ag2S/ДMCO и оставили полученную смесь для протекания реакции в темноте при 4°C на 12 часов, затем центрифугировали при 400g в течение 4 минут, после чего отделили супернатант. Клетки MDA-MB-468 добавили к смешанному раствору 100 мкл супернатанта и 100 мкл 1×PBS, окрасили при 4°C в течение 2 часов, после чего 3 раза промыли 1× раствором PBS. Можно ясно видеть, что квантовые точки Ag2S излучают люминесценцию в клетках при возбуждении лазером с длиной волны 658 нм, при использовании фильтра на 1100 нм и фотографировании 2D InGaAs камерой.
В заключение следует отметить, что для способа согласно настоящему изобретению характерны умеренные условия реакции, простота осуществления, короткий производственный цикл, хорошая воспроизводимость и легкость управления. Полученные квантовые точки Ag2S имеют высокий выход флуоресценции, хорошую стабильность флуоресценции, превосходную биосовместимость и единообразные размеры, и они могут быть использованы для визуализации клеток in vitro и для визуализации животных тканей in vivo. Кроме того, способ согласно настоящему изобретению легко осуществить в большом масштабе, поэтому его можно использовать для промышленного производства.
Приведенные выше примеры являются лишь представителями многочисленных примеров осуществления настоящего изобретения и не ограничивают объем правовой охраны настоящего изобретения. Все технические решения, имеющие эквивалентные варианты или эквивалентные замены, входят в объем правовой охраны настоящего изобретения.
1. Способ получения квантовых точек сульфида серебра, излучающих в ближней инфракрасной области спектра, характеризующийся тем, что он включает следующие стадии:1) получение гидрофобных квантовых точек сульфида серебра; и2) проведение реакции гидрофобных квантовых точек сульфида серебра из стадии 1) со стехиометрическим или избыточным количеством меркаптосодержащего гидрофильного реагента в полярном органическом растворителе для обеспечения присоединения гидрофильных групп к поверхности квантовых точек с получением гидрофильных квантовых точек сульфида серебра, излучающих в ближней инфракрасной области спектра, причем число молей меркаптосодержащего гидрофильного реагента больше или равно числу молей гидрофобных квантовых точек сульфида серебра;причем гидрофильный реагент выбран из меркаптоуксусной кислоты, меркаптопропионовой кислоты, цистеина, цистеамина, тиоктовой кислоты и меркаптоацетата аммония или любых их комбинаций,отличающийся тем, что стадия 1) включает следующие стадии:1-1) нагревание смешанной реакционной системы, содержащей источник серебра и длинноцепочечный тиол, до температуры, лежащей в диапазоне от 80°C до 350°C, в замкнутом пространстве до тех пор, пока не пройдет достаточная реакция; и1-2) естественное охлаждение смешанной реакционной системы до комнатной температуры, последующее добавление полярного растворителя, центрифугирование и промывание с получением гидрофобных квантовых точек сульфида серебра, излучающих в ближней инфракрасной области спектра,причем источник серебра содержит одно или более соединений, выбранных из нитрата серебра, диэтилдитиокарбамата серебра, дигидрокарбилдитиофосфата серебра, диоктилсульфосукцината серебра, тиобензоата серебра, ацетата серебра, додеканоата серебра, тетрадеканоата серебра и октадеканоата серебра; идлинноцепочечный тиол содержит одно или более соединений, выбранных из октантиола, ундекантиола, додекантиола, тридекантиола, тетрадекантиола,пентадекантиола, гексадекантиола, октадекантиола, эйкозантиола, гексантиола, 1,6-гександитиола и 1,8-октандитиола,и на стадии 2) гидрофобные квантовые точки сульфида серебра реагируют с меркаптосодержащим гидрофильным реагентом в полярном органическом растворителе при температуре, лежащей в диапазоне от 2°C до 80°C, в течение 3 или более часов.
2. Способ получения квантовых точек сульфида серебра, излучающих в ближней инфракрасной области спектра, по п. 1, отличающийся тем, что на стадии 2) значение pH реакционной системы регулируют так, чтобы оно лежало в диапазоне от 7 до 14.
3. Способ получения квантовых точек сульфида серебра, излучающих в ближней инфракрасной области спектра, по п. 1, отличающийся тем, что на стадии 2) полярный органический растворитель содержит одно или более веществ, выбранных из этанола, метанола, ацетона и 1-метил-2-пирролидона.
4. Способ получения квантовых точек сульфида серебра, излучающих в ближней инфракрасной области спектра, по п. 1, отличающийся тем, что на стадии 1-2) смешанная реакционная система дополнительно содержит поверхностно-активное вещество с координационной способностью, которое выбрано из длинноцепочечной алкилкислоты, алкиламина, длинноцепочечного спирта, длинноцепочечного тиола и простого эфира или любой их комбинации; и смешанная реакционная система помещена для реакции в замкнутое пространство.
5. Способ получения квантовых точек сульфида серебра, излучающих в ближней инфракрасной области спектра, по п. 1, отличающийся тем, что на стадии 2) гидрофобные квантовые точки сульфида серебра реагируют с меркаптосодержащим гидрофильным реагентом в условиях непрерывного перемешивания и/или вибрации и/или обработки ультразвуком в полярном органическом растворителе при температуре, лежащей в диапазоне от 2°C до 80°C, в течение 3 или более часов.
6. Квантовые точки сульфида серебра, излучающие в ближней инфракрасной области спектра, полученные способом по любому из пп. 1-5, отличающиеся тем, что квантовые точки сульфида серебра содержат гидрофильные группы, присоединенные к их поверхности, причем гидрофильные группы получены из меркаптосодержащего гидрофильного реагента, а гидрофильный реагент выбран из меркаптоуксусной кислоты, меркаптопропионовой кислоты, цистеина, цистеамина, тиоктовой кислоты и меркаптоацетата аммония или любых их комбинаций, причем указанные квантовые точки сульфида серебра, излучающие в ближней инфракрасной области спектра, имеют моноклинную структуру и размер частиц меньше 8 нм.
7. Применение квантовых точек сульфида серебра, излучающих в ближней инфракрасной области спектра, по п. 6 для визуализации клеток и визуализации биологических тканей.