Способ получения наноразмерного порошка алюмоиттриевого граната
Иллюстрации
Показать всеИзобретение относится к технологии получения соединений сложных оксидов со структурой граната, которые могут быть использованы для изготовления активных элементов твердотельных лазеров ближнего и среднего ИК-диапазонов, для разработки сцинтилляторов и люминофоров, а также в производстве термостойкой керамики. Способ получения наноразмерного порошка алюмоиттриевого граната включает приготовление исходных реакционных водных растворов, содержащих соли иттрия (III) и алюминия (III) в молярном отношении 3:5. Сначала реагент-осадитель, в качестве которого используют сильноосновный гелевый анионит АВ-17-8 в гидроксидной форме, приводят в контакт с раствором солей иттрия (III) при комнатной температуре в течение 20 мин, затем добавляют раствор солей алюминия (III). Из полученного раствора осаждают продукт-прекурсор, отделяют его от раствора, промывают водой, сушат и обжигают при температуре 900°С. Ионообменный способ обеспечивает получение наноразмерного порошка алюмоиттриевого граната, не содержащего катионов осадителя, без применения агрессивных сред и давлений. 3 ил., 2 пр.
Реферат
Изобретение относится к способу получения соединений сложных оксидов со структурой граната, которые могут быть использованы для изготовления активных элементов твердотельных лазеров ближнего и среднего ИК-диапазонов, для разработки сцинтилляторов и люминофоров, а также в производстве термостойкой керамики.
Алюмоиттриевый гранат представляет собой сложный оксид иттрия и алюминия с химической формулой Y3Al5O12 и структурой граната.
Известен способ получения алюмоиттриевого граната [Авторское свидетельство 544614, C01F 17/00, УДК 546.641, опубл. 30.01.77, Бюлл. №4], в котором в качестве исходных компонентов использовали безводные хлориды алюминия и иттрия и хлориды щелочных металлов, которые предварительно расплавляли при температуре 750-950°С. Для приготовления алюмоиттриевого граната состава Y3Al5O12 плавы 46 г хлоралюминатов KAlCl4 (NaAlCl4) щелочных металлов и 54 г хлориттратов K3YCl6 (NaYCl6) смешивали и нагревали в корундовом реакторе до температуры 750-950°С и в полученный расплав подавали газообразный кислород, скорость подачи которого составляет 10-15 л/ч на 100 г расплава. В ходе реакции в расплаве образовывались тонкодисперсные частицы алюмоиттриевого граната и выделялось большое количество газообразного хлора. Затем расплав охлаждали, промывали водой от солей, отфильтровывали и просушивали при температуре 120°С. Получали тонкодисперсный порошок алюмоиттриевого граната белого цвета высокой степени чистоты.
К недостаткам данного способа можно отнести использование дополнительной стадии расплавления исходных веществ, а также выделение газообразного хлора в ходе реакции.
Известен способ получения алюмоиттриевого граната [патент RU №2137715, C01F 17/00, С01В 13/32, C01G 49/00, С30В 29/22, С30В 29/28, опубл. 20.09.1999], в соответствии с которым оксиды иттрия Y2O3 и железа Al2O3, взятые в молярном отношении (3:5), перемешивали в изопропаноле в течение 10 мин под действием ультразвука и после удаления изопропанола с помощью испарителя и вакуумной сушилки обжигали в кварцевом муфеле при температуре 1100°С в течение 60 минут в атмосфере хлористого водорода. Полученный продукт, по данным РФА, представлял собой чистую фазу иттрий-алюминиевого граната с размером частиц 52 мкм.
К недостаткам данного способа можно отнести использование органического растворителя, который далее нужно отгонять; необходимость применения кварцевого муфеля из-за использования хлороводорода на стадии обжига, а также высокие температуры обжига.
Известен также способ получения алюмоиттриевого граната золь-гель методом [Ramanujam P.A comparative study of the synthesis of nanocrystalline yttrium aluminium garnet using sol-gel and co-precipitation methods / P. Ramanujam, B. Vaidhynatan, J. Binner, A. Anshuman, C. Spacie // Ceramics International. - 2014. - №40. - P. 4179-4186]. Синтез проводили следующим образом: смешали нитратные водные растворы иттрия (0,6 М), алюминия (1 М) и лимонную кислоту (1 М) и нагревали на масляной бане при температуре 90°С в течение 24 ч. Полученный гель высушивали при 100°С 24 ч и обжигали при 900-1000°С 1 ч. Размер частиц составил 30-60 нм. Согласно данным рентгенофазного анализа чистая фаза граната Y3Al5O12 получается при 1000°С.
Недостатком данного способа является длительное время контакта фаз, а также необходимость отмывки конечного продукта от анионов и катионов.
Наиболее близким техническим решением, выбранным в качестве прототипа, является способ получения алюмоиттриевого граната, легированного редкоземельными элементами, методом соосаждения [патент RU №2503754, С30В 29/28, C09K 11/80]. В качестве исходных веществ используют нитраты алюминия, иттрия и редкоземельных элементов (с общей концентрацией ионов металла 1 моль/л), а в качестве осадителя - гидрокарбонат аммония (2 моль/л), содержащий фторид аммония (в количестве 0,1-5% атомов фтора относительно количества осадителя). Смесь водных растворов нитратов алюминия, иттрия и редкоземельного элемента заливают в капельную воронку и приливают ее к осадителю со скоростью 60 мл/мин при перемешивании 300-500 об/мин. Полученный осадок отфильтровывают, промывают водой, сушат при температуре 100-150°С в течение 8-12 часов, обжигают при температуре 1100°С 5 часов.
К недостаткам данного способа можно отнести загрязнение полученного осадка анионами исходной соли и катионами осадителя.
Техническим результатом заявляемого изобретения является разработка анионообменного способа получения алюмоиттриевого граната, являющегося достаточно простым, не предполагающего применения агрессивных сред и давлений.
Технический результат достигается тем, что в способе получения наноразмерного порошка алюмоиттриевого граната, включающем приготовление исходных реакционных водных растворов, содержащих соли иттрия (III) и алюминия (III) в молярном отношении 3:5, осаждение из раствора продукта-прекурсора, отделение от раствора, промывку водой, сушку и обжиг, новым является то, что в качестве реагента-осадителя используют сильноосновный гелевый анионит АВ-17-8 в гидроксидной форме, который приводят сначала в контакт с раствором иттрия (III), а затем с раствором алюминия (III), обжиг проводят при температуре не менее 900°С.
Эти отличия позволяют сделать вывод о соответствии заявляемого технического решения критерию «новизна». Признаки, отличающие заявляемый способ от прототипа, не выявлены в других технических решениях при изучении данной и смежных областей химии и, следовательно, обеспечивают заявляемому решению соответствие критерию «изобретательский уровень».
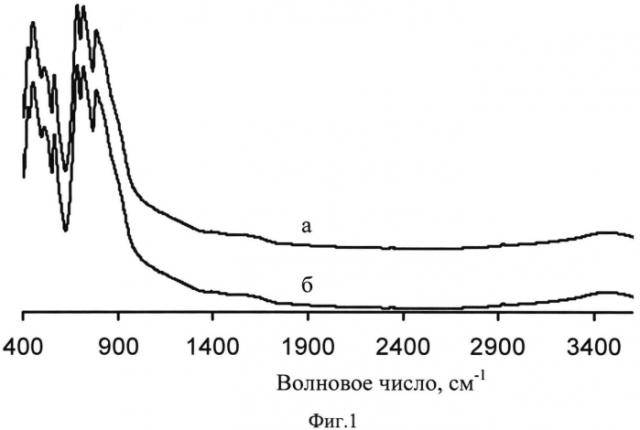
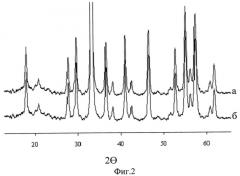
Изобретение поясняется чертежами. На фиг. 1 представлен ИК-спектр алюмоиттриевого граната: а - полученного из хлоридного раствора; б - полученного из нитратного раствора. На фиг. 2 показаны рентгеновские спектры алюмоиттриевого граната: а - полученного из хлоридного раствора; б - полученного из нитратного раствора. На фиг. 3 представлена микрофотография алюмоиттриевого граната, полученного из хлоридного раствора (а) и нитратного раствора (б).
Необходимость создания настоящего изобретения обусловлена тем, что при анионообменном синтезе, проводимом из смеси солей, образуются прекурсоры, обладающие высокой активностью, поэтому формирование сложных оксидов протекает при более низкой температуре. Поскольку данный способ позволяет получать прекурсоры состава, близкого к стехиометрическому, при термообработке формируется однофазный материал с узким распределением частиц по размерам.
При создании заявленного изобретения были использованы гелевые и пористые сильноосновные аниониты в ОН-форме. Полученные данные свидетельствуют, что использование пористых анионитов нецелесообразно, так как значительная доля осадка (более 50%) удерживается анионитом. Поэтому выбор сильноосновного анионита АВ-17-8 является предпочтительным.
Заявляемый способ осуществляется следующим образом.
Переводят анионит АВ-17-8 (сильноосновной анионит с полистирольной матрицей, содержащий четвертичные аммониевые основания - N+(СН3)3 (ГОСТ 20301-74)) в ОН-форму, осуществляют контакт анионита с раствором солей иттрия (III) и алюминия (III), отделение и промывку осадка, прокаливание.
Перевод анионита в ОН-форму проводят, заливая исходный АВ-17-8 в хлоридной форме 1 М раствором NaOH (т:ж=1:3), затем 2 М раствором NaOH 3 раз, выдерживая каждую порцию в течение часа. После чего анионит промывают дистиллированной водой до отрицательной реакции на хлорид-ион. Полученный анионит высушивают при температуре около 60°С.
Массу анионита, необходимую для синтеза, рассчитывают по формуле:
где CY, CAl - концентрация исходных растворов иттрия (III) и алюминия (III), М; VY, VAl - объем исходных растворов, мл; СОЕ - статическая обменная емкость анионита в OH-форме, ммоль-экв·г-1.
Рассчитанное количество анионита, выступающего в качестве реагента-осадителя, приводят в контакт с 19 мл 0,24 М раствора иттрия (III). Систему перемешивают на шейкере со скоростью 120 мин-1 при комнатной температуре в течение 20 мин, затем в систему добавляют 31 мл 0,24 М раствора алюминия (III) и перемешивают еще 40 мин. После чего анионит отделяют, пропуская смесь через сито с диаметром отверстий 0,25 мм. Для отделения осадка проводят фильтрование на воронке Бюхнера под вакуумом. Осадок (прекурсор) после промывания водой сушат при температуре 100°С. Далее прекурсор обжигают при температуре 900°С в течение 60 мин для получения чистой фазы алюмоиттриевого граната.
Пример 1. Получение наноразмерного порошка алюмоиттриевого граната из хлоридных растворов иттрия (III) и железа (III) при температуре обжига 900°С.
Навеску анионита массой 34 г приводят в контакт с 19 мл 0,24 М раствора YCl3. Систему перемешивают на шейкере со скоростью 120 мин-1 при комнатной температуре в течение 20 мин, затем в систему добавляют 31 мл 0,24 М раствора AlCl3 и оставляют контактировать еще 40 мин при перемешивание на шейкере. После чего анионит отделяют, пропуская смесь через сито с диаметром отверстий 0,25 мм. Для отделения осадка проводят фильтрование на воронке Бюхнера под вакуумом. Полученный осадок (прекурсор) промывают водой, высушивают при 100°С в сушильном шкафу. Далее прекурсор обжигают при температуре 900°С в течение 60 мин для получения чистой фазы алюмоиттриевого граната.
На фиг. 1а представлен ИК-спектр продукта. В спектре активны семь колебательных мод при 788, 722, 689, 567, 532, 522, 463 и 432 см-1, относящиеся к связям Al-O и Y-O и подтверждающие формирование структуры алюмоиттриевого граната. Также на спектре отсутствуют полосы поглощения, характерные для анионов исходной соли.
На фиг. 2а представлен рентгеновский спектр продукта, обожженного при 900°С. Основные пики на рентгенограмме 4,88, 4,254, 3,22, 2,90, 2,69, 2,39, 1,663 характерны для кубической структуры граната.
На фиг. 3а представлена электронная микрофотография алюмоиттриевого граната, полученного при 900°С. Видны крупные агломераты, близкие к сферической форме, порядка 326 нм.
Пример 2. Получение алюмоиттриевого граната из нитратных растворов иттрия (III) и алюминия (III) при температуре обжига 900°С.
Навеску анионита массой 34 г приводят в контакт с 19 мл 0,24 М раствора Y(NO3)3. Систему перемешивают на шейкере со скоростью 120 мин-1 при комнатной температуре в течение 20 мин, затем добавляют 31 мл 0,24 М раствора Al(NO3)3 и оставляют контактировать еще 40 мин при перемешивание на шейкере. После чего анионит отделяют, пропуская смесь через сито с диаметром отверстий 0,25 мм. Для отделения осадка проводят фильтрование на воронке Бюхнера под вакуумом. Полученный осадок (прекурсор) промывают водой, высушивают при 100°С в сушильном шкафу. Далее прекурсор обжигают при температуре 900°С в течение 60 мин для получения чистой фазы алюмоиттриевого граната.
На фиг. 1б представлен ИК-спектр продукта. В спектре активны семь колебательных мод при 788, 722, 689, 567, 532, 522, 463 и 432 см-1, относящиеся к связям Al-O и Y-O и подтверждающие формирование структуры алюмоиттриевого граната. Также на спектре отсутствуют полосы поглощения, характерные для анионов исходной соли.
На фиг. 2б представлен рентгеновский спектр продукта, обожженного при 900°С. Основные пики на рентгенограмме 4,88, 4,254, 3,22, 2,90, 2,69, 2,39, 1,663 характерны для кубической структуры граната.
На фиг. 3б представлена электронная микрофотография алюмоиттриевого граната, полученного при 900°С. Видны крупные агломераты, близкие к сферической форме, порядка 300 нм.
Преимущества предлагаемого способа заключаются в том, что он достаточно прост, не предполагает применения агрессивных сред и давлений. Используя данное техническое решение, можно добиться получения продукта, не содержащего катионов осадителя, что освобождает в дальнейшем от необходимости длительной промывки полученного осадка. Кроме того, формирование структуры граната происходит при более низкой температуре. Также, предложенный анионообменный метод синтеза алюмоиттриевого граната приводит к образованию высокодисперсного продукта с воспроизводимыми физико-химическими свойствами.
Способ получения наноразмерного порошка алюмоиттриевого граната, включающий приготовление исходных реакционных водных растворов, содержащих соли иттрия (III) и алюминия (III) в молярном отношении 3:5, приведение растворов в контакт, осаждение из полученного раствора продукта-прекурсора, отделение его от раствора, промывку водой, сушку и обжиг, отличающийся тем, что реагент-осадитель, в качестве которого используют сильноосновный гелевый анионит АВ-17-8 в гидроксидной форме, предварительно приводят в контакт с раствором солей иттрия (III) при комнатной температуре в течение 20 мин, а затем в систему добавляют раствор солей алюминия (III), при этом обжиг проводят при температуре не менее 900°С.