Способ получения полиорганосилоксанов
Иллюстрации
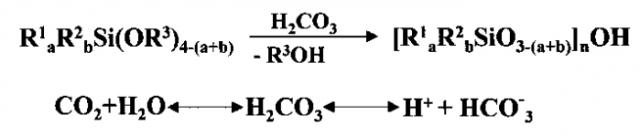
Показать всеИзобретение относится к химической технологии кремнийорганических соединений. Предложен способ получения полиорганосилоксанов путем поликонденсации алкоксисиланов, которую проводят в водной среде, насыщенной диоксидом углерода, под давлением от 150 до 350 атм в температурном интервале от 20 до 110°C. В качестве исходного алкоксисилана используют соединение, выбранное из алкоксисиланов общей формулы R1 aR2 bSi(OR3)4-(a+b), где R1=С1-С4 алкил или С6Н5; R2=С1-С4 алкил; R3=C1-C4 алкил; а=0, или 1, или 2; b=0 или 1. Технический результат - предложенный способ технологичен, позволяет получить целевой полиорганосилоксан с количественным выходом при малой продолжительности процесса и при отсутствии органического растворителя. 4 ил., 1 табл., 8 пр.
Реферат
Изобретение относится к химической технологии высокомолекулярных кремнийорганических соединений, а именно к способу получения полиорганосилоксанов гидролитической поликонденсацией алкоксисиланов.
Изобретение может быть использовано в химической промышленности для производства полиорганосилоксанов, которые составляют основу полимерных композиционных материалов для получения герметиков, компаундов, адгезивов, разнообразных покрытий и т.п., применяемых в машиностроении, радиоэлектронике и других областях техники.
Способ по изобретению позволяет получать полиорганосилоксаны различного строения, в частности линейные или циклические полидиметилсилоксаны, без растворителя и добавления катализаторов.
Известно, что полиорганосилоксаны различного строения получают гидролитической поликонденсацией функционально замещенных силанов. Гидролитическая поликонденсация - это совокупность процессов гидролиза функциональных групп исходного мономера водой с последующей гомо- и гетерофункциональной поликонденсацией, образующихся при гидролизе интермедиатов.
Известны способы получения полиорганосилоксанов гидролизом органохлорсиланов [Андрианов, К.А. Методы элементоорганической химии. Кремний / К.А. Андрианов. - М.: Наука, 1968. - 699 с.; Соколов, Н.Н. Методы синтеза полиорганосилоксанов / Н.Н. Соколов. - М.: Госхимиздат, 1959. - 197 с.; Гидролитическая поликонденсация органохлорсиланов (обзор) / В.М. Копылов, Л.М. Хананашвили, О.В. Школьник, А.Г. Иванов // ВМС (А) - 1995. - Т. 37, №3. - С. 394-416; Хананашвили, Л.М. Химия и технология элементоорганических мономеров и полимеров / Л.М. Хананашвили. - М.: Химия, 1998. - 528 с.].
Процессы с использованием органохлорсиланов протекают быстро, но характеризуются сложностью управления и технологического оформления, наличием промежуточных стадий фильтрации и нейтрализации продуктов, образованием большого количества солянокислых отходов, в том числе промывных вод, которые сложно утилизировать.
Известны способы получения полиорганосилоксанов гидролитической поликонденсацией алкоксисиланов [Hook, R.J. A 29Si NMR study of the sol-gel polymerization rates of substituted ethoxysilanes / R.J. Hook // J. of Non-Cryst. Sol. - 1996. - V. 195. - P. 1-15; Schmidt, H. Principles of Hydrolysis and Condensation Reaction of Alkoxysilanes / H. Schmidt, H. Scholze, A. Kaiser. // J. Non-Cryst. Sol. - 1984. - V. 63. - P. 1-11; Chemical modification of TEOS with acetic acid / А. Campero, R. Arroyo, C. Sanchez, J. Livage. // Utrastructure processing of advanced ceramics. Edit. J.D. Mackenzie, D.R. Ulrich. - John Wyley&Sons, 1988. - P. 327-332; Tsai, M.T. Hydrolysis and condensation of forsterite precursor alkoxides: modification of the molecular gel structure by acetic acid / M.T. Tsai // J. of Non-Cryst. Sol. - 2002. - V. 298. - P. 116-130; Поликонденсация алкоксисиланов в активной среде - универсальный метод получения полиорганосилоксанов / Е.В. Егорова, Н.Г. Василенко, Н.В. Демченко [и др.] // ДАН. - 2009. - Т. 424, №2. - С. 200-204].
Способы, использующие алкоксисиланы в качестве мономеров, обладают рядом преимуществ: снижается экологическая нагрузка благодаря отсутствию большого количества солянокислых отходов, нет необходимости использовать дорогостоящее коррозионно-стойкое оборудование.
Однако гидролиз алкоксисилильных групп происходит значительно медленнее гидролиза хлорсилильных групп, поэтому для ускорения таких процессов необходимо использование катализаторов.
Известны способы получения полиорганосилоксанов гидролизом алкоксисиланов в присутствии кислот и оснований, однако для этих способов характерны неполная конверсия мономера и алкоксисилильных групп, необходимость использования растворителей, отсутствие селективной направленности процессов для образования продуктов заданной структуры в случае гидролиза диорганодиалкоксисиланов, наличие дополнительных стадий очистки продуктов от катализаторов (нейтрализация, фильтрация, отмывка), что приводит к снижению выхода и качества целевого продукта [Rankin, S. 29Si NMR study of base-catalyzed polymerization of dimethyldiethoxysilane / S. Rankin, A.V. McCormick // Magn. Reson. Chem. - 1999. - V. 37. - P. s27-s37; Sanchez, J. 29Si NMR Kinetic Study of Tetraethoxysilane and Ethyl-Substituted Ethoxysilane Polymerization in Acidic Conditions / J. Sanchez, S.E. Rankin, A.V. McCormick // Ind. Eng. Chem. Res. - 1996. - V. 35. - P. 117-129; Zhang, Z. Hydrolysis and Polymerization of Dimethyldiethoxysilane, Methyltrimethoxysilane and Tetramethoxysilane in Presence of Aluminum Acetylacetonate. A Complex Catalyst for the Formation of Siloxanes / Z. Zhang, S. Sakka. // J. Sol-Gel Sci. Technol. - 1999. - V. 16. - P. 209-220; Perfomance enhancement of polybenzoxazine by hybridization with polysiloxane / H. Ardhyananta, M. Wahid, M. Sasaki, T. Agag // Polymer. - 2008. - V. 49. - P. 4585-4591].
Известен способ получения линейных органополисилоксанов с концевыми гидроксильными группами гидролизом диалкоксисилана в присутствии соляной кислоты в течение 1 часа с последующим добавлением оксидов металла для нейтрализации катализатора, сушкой продукта над сульфатом магния и удалением спирта из продукта (патент Японии JP 2652307).
Недостатками способа является многостадийность, наличие отходов, неполная конверсия мономера, отсутствие селективности процесса.
Известен двухстадийный способ получения полиорганосилоксанов с концевыми гидроксисилильными группами (патент Японии JP 3079939), где на первой стадии проводят гидролитическую поликонденсацию органоалкоксисиланов в присутствии сульфокатионита в течение 4 часов и получают продукты с концевыми этоксисилильными группами, на второй стадии проводят гидролиз этих продуктов, прибавляя дополнительное количество воды.
Недостатками способа являются неполная конверсия мономера, низкая молекулярная масса продукта, наличие дополнительных стадий очистки и выделения продукта.
Известен способ получения полиорганосилоксанов, заключающийся в проведении поликонденсации органоалкоксисиланов в муравьиной кислоте с использованием ионообменной смолы в качестве катализатора (Европейский патент ЕР 0431409).
Недостатками данного способа являются: низкая молекулярная масса продукта, отсутствие полной конверсии алкоксигрупп, продолжительность процесса в течение 3-4 дней, отсутствие возможности управления строением и составом продукта.
Известны способы гидролиза тетраалкоксисиланов в условиях сверхкритического CO2 в присутствии катализаторов - неорганических и органических кислот, где сверхкритический CO2 выступает в роли растворителя, что является преимуществом этих способов, так как после сброса давления газообразный CO2 улетучивается, и не требуется дополнительных стадий удаления растворителей в отличие от вышеописанных способов (Moner-Girona, М.; Roig, A.; Molins, E.J. Sol-Gel Route to Direct Formation of Silica Aerogel Microparticles Using Supercritical Solvents Sol-Gel Sci. Technol. 2003, 26, 645.; A. Rao, D. Bhagat Solid State Sciences 6 (2004) 945-952; патент США US 6670402). Однако CO2 в указанных способах не является реагентом и не участвует в процессе поликонденсации, его ключевая роль заключается в осушке геля, образовавшегося при взаимодействии тетраалкоксисилана и катализатора, и получении так называемого аэрогеля. Способы, в которых применяют сверхкритический CO2, не использовались для получения замещенных полиорганосилоксанов.
Известен способ получения полиорганосилоксанов путем гидролитической поликонденсации алкоксисиланов в активной среде, представляющей собой карбоновую кислоту, которая выступает одновременно в роли реагента, катализатора и растворителя, или смесь карбоновой кислоты и растворителя (RU 2006113775; Е.В. Егорова, Н.Г. Василенко, Н.В. Демченко [и др.] // ДАН. - 2009. - Т. 424, №2. - С. 200-204). При этом количество карбоновой кислоты составляет от 3 до 20 моль на 1 моль алкоксисилана, а количество используемого растворителя в реакционной смеси - от 10 до 90 объемн. %. Продолжительность процесса варьируется от 5 до 20 часов в зависимости от числа алкокси-групп мономера. Выделение продукта в указанном способе осуществляют отгонкой легколетучих компонентов. Этот способ наиболее близок к предлагаемому способу по технической сущности и может рассматриваться как прототип.
Недостатками данного способа являются: наличие побочных продуктов - спирт, вода, сложный эфир карбоновой кислоты, что осложняет и замедляет выделение целевого полиорганосилоксана, необходимость использования больших объемов карбоновой кислоты, растворителя и большая продолжительность процесса по сравнению с продолжительностью гидролитической поликонденсации органохлорсиланов, которая протекает в непрерывном режиме.
Задачей заявляемого изобретения является создание эффективного технологичного способа получения полиорганосилоксанов из алкоксисиланов, который обеспечивал бы полную конверсию мономера при малой продолжительности процесса и в отсутствие органического растворителя.
Задача решается заявляемым способом получения полиорганосилоксанов путем поликонденсации алкоксисилана, причем поликонденсацию проводят в водной среде, насыщенной диоксидом углерода, под давлением от 150 до 350 атм в температурном интервале от 20 до 110°C. В качестве исходного алкоксисилана используют алкоксисилан, выбранный из соединений общей формулы R1 aR2 bSi(OR3)4-(a+b), где
R1 обозначает С1-С4 алкил или С6Н5;
R2 обозначает С1-С4 алкил;
R3 обозначает С1-С4 алкил;
а равно 0, или 1, или 2;
b равно 0 или 1.
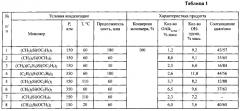
Время проведения поликонденсации зависит от структуры исходного алкоксисилана и составляет от 10 мин до 3 часов (Таблица 1).
В отличие от способа-прототипа, где гидролитическую поликонденсацию алкоксисиланов проводят в избытке карбоновой кислоты (RU 2006113775), в заявленном способе поликонденсацию алкоксисилана проводят в водной среде, насыщенной диоксидом углерода, под давлением от 150 до 350 атм и температуре от 20 до 110°C. Раствор диоксида углерода в воде при таких значениях температуры и давления характеризуется значением pH в диапазоне от 2,8 до 3,9, то есть представляет собой угольную кислоту, которая выступает в роли катализатора гидролитической поликонденсации мономера.
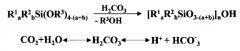
В общем виде гидролитическая поликонденсация алкоксисиланов в угольной кислоте может быть представлена следующей суммарной схемой:
где: R1 обозначает С1-С4 алкил или С6Н5; R2 обозначает С1-С4 алкил; R3 обозначает С1-С4 алкил; а равно 0, или 1, или 2; b равно 0 или 1; n обозначает количество элементарных звеньев цепи.
Продолжительность гидролитической поликонденсации алкоксисилана в таких условиях составляет не более трех часов, тогда как в прототипе - от 5 до 20 часов. Конечный продукт поликонденсации состоит из полиорганосилоксана, спирта, воды и диоксида углерода, что упрощает выделение целевого продукта. Диоксид углерода самопроизвольно удаляется из реактора при сбросе давления, оставшиеся компоненты представляют собой гетерофазную систему, состоящую из целевого полиорганосилоксана и водно-спиртового слоя. После отделения водно-спиртового слоя силоксановый слой анализируют с помощью ГЖХ, ГПХ, ИК- и ЯМР-спектроскопии. Таким образом, выделение целевого продукта не требует операций, связанных с удалением растворителя и большого избытка кислоты (как в прототипе). Целевой полиорганосилоксан получают с количественным выходом. На примере дифункциональных алкоксисиланов показана возможность управления структурой продукта. Так, повышение температуры поликонденсации диметилдиэтоксисилана от 60°C (пример 1, Таблица 1) до 110°C (пример 5, Таблица 1) приводит к увеличению выхода линейных полиорганосилоксанов от 57 до 88%.
Технический результат, достигаемый в заявленном изобретении, заключается в значительном сокращении длительности процесса при полной конверсии мономера; проведении поликонденсации без использования органического растворителя; в менее трудоемком выделении целевого продукта и возможности управления строением образующегося продукта.
Анализ продукта после сброса давления и отделения водно-спиртового слоя проводили методами ГЖХ, ГПХ, ИК- и 1Н ЯМР-спектроскопии.
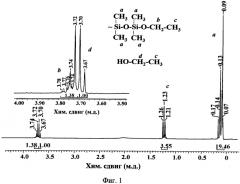
На Фиг. 1 приведен 1Н ЯМР-спектр реакционной смеси, полученной в примере 1 после сброса давления. Для определения количества концевых гидроксильных групп проводили блокирование полученного продукта диметилвинилхлорсиланом в условиях, обеспечивающих их полную конверсию.
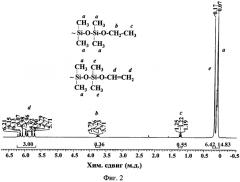
На Фиг. 2 приведен 1Н ЯМР спектр блокированного полидиметилсилоксана из примера 4. Содержание винилдиметилсилильных групп и, соответственно, гидроксильных групп определяют по соотношению интегральных интенсивностей сигналов протонов метальных групп у атомов кремния в области δ=0,06 м.д. и протонов винильных групп в области δ=5,9 м.д.
Молекулярно-массовое распределение полученных образцов определяли ГПХ-анализом образцов, а состав летучих полиорганосилоксанов определяли методом ГЖХ. В качестве примера на Фиг. 3 приведена ГЖХ-кривая для примера 3, которая типична для примеров 1-6. На Фиг. 4 представлены ГПХ-кривые продуктов, полученных в примерах 4 и 5.
Условия получения и результаты исследования полученных полиорганосилоксанов представлены в Таблице 1.
Изобретение иллюстрируется приведенными ниже примерами его осуществления.
Пример 1. Поликонденсация (CH3)2Si(OC2H5)2 в среде угольной кислоты.
В автоклав объемом 20 мл помещают 10 мл диметилдиэтоксисилана и 5 мл воды Milli-Q. Затем в автоклав подают СО2 при давлении 150 атм. С помощью электронного термостата задают температуру внутри автоклава, равную 60°C. Процесс проводят в течение 3 часов. Затем давление сбрасывают, отделяют водно-спиртовой слой. Силоксановый слой анализируют с помощью ГЖХ, ГПХ, ИК- и ЯМР-спектроскопии. Выход полидиметилсилоксана количественный. ГЖХ: [(CH3)2SiO]3 - 3%, [(CH3)2SiO]4 - 33%, [(CH3)2SiO]5 - 7%, HO-[(CH3)2SiO]n-H - 57%. ГПХ: Mp=500. По данным 1Н ЯМР продукт содержит 1,2 масс. % остаточных EtO-групп (по соотношению сигналов CH3CH 2OSi- и CH3Si- групп). ИК-спектр (CCl4), v/см-1: 3300 (SiOH). Количество гидроксильных групп, определенное после блокирования диметилвинилхлорсиланом, составляет 9,2 масс. %.
Примеры 2-8. Поликонденсацию алкоксиланов в примерах 2-8 осуществляют по методике, аналогичной описанной в Примере 1. Условия получения и результаты исследования полученных полиорганосилоксанов представлены в Таблице 1.
Таким образом, предлагаемый способ обладает следующими преимуществами:
- он позволяет получать полиорганосилоксаны различного строения, в частности линейные или циклические полидиметилсилоксаны и регулировать строение образующегося продукта;
- при этом значительно сокращается время поликонденсации;
- нет необходимости добавлять органический растворитель и катализатор;
- менее трудоемкое выделение целевого продукта;
- способ более технологичен, чем прототип.
Способ получения полиорганосилоксанов путем поликонденсации алкоксисилана, выбранного из алкоксисиланов общей формулы R1 aR2 bSi(OR3)4-(a+b), гдеR1 обозначает С1-С4 алкил или С6Н5;R2 обозначает С1-С4 алкил;R3 обозначает С1-С4 алкил;а равно 0, или 1, или 2;b равно 0 или 1,отличающийся тем, что поликонденсацию проводят в водной среде, насыщенной диоксидом углерода, под давлением от 150 до 350 атм в температурном интервале от 20 до 110°C.