Фармацевтическая композиция для профилактики или лечения макулярной дегенерации
Иллюстрации
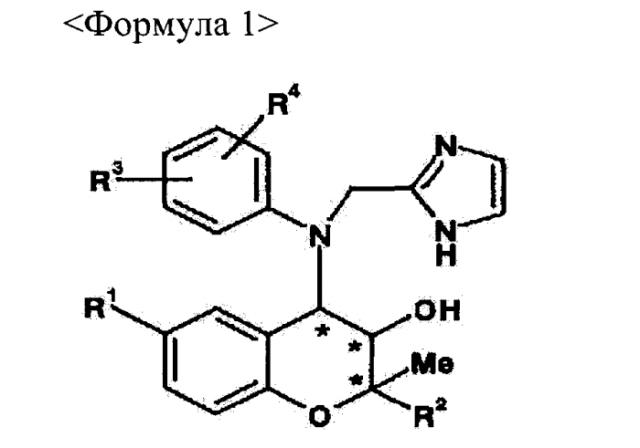
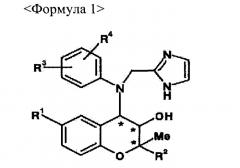
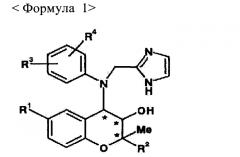
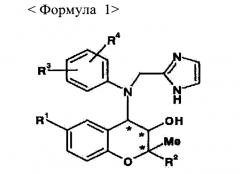
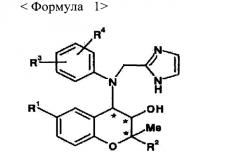
Показать всеИзобретение относится к фармацевтической композиции для профилактики или лечения макулярной дегенерации, содержащее бензопирановые производные формулы 1 или их фармацевтически приемлемые соли в качестве активного компонента, где R1 соответствует H, CN, NO2 или NH2, R2 соответствует , R3 и R4 независимы друг от друга и соответствуют H, Cl, Br, F, C1~C3 алкильному радикалу с линейной или разветвленной цепью, ORb, CF3, OCF3, NO2 или CO2Rb, Ra соответствует C1~C4 алкильному радикалу с линейной или разветвленной цепью, Rb соответствует H или C1~C3 алкильному радикалу, и * соответствует хиральному центру. Также изобретение относится к препарату глазных капель на основе соединения формулы 1. Технический результат: получена фармацевтическая композиция на основе бензопирана, полезная при лечении макулярной дегенерации. 4 н. и 5 з.п. ф-лы, 12 ил., 3 табл., 10 пр.
<Формула 1>
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к фармацевтической композиции для профилактики или лечения макулярной дегенерации, которая содержит бензопирановые производные, замещенные вторичными аминами, включающими имидазол, либо к его фармацевтически приемлемым солям в качестве активного компонента.
УРОВЕНЬ ТЕХНИКИ
Нервная ткань, расположенная в центральной части сетчатки глаза, называется макулой (желтым пятном). Желтое пятно содержит большинство фоторецепторных клеток, реагирующих на световую стимуляцию, и изображение объекта фокусируется в центре желтого пятна. Таким образом, макула играет важную роль в поддержании зрительного восприятия. Возрастная макулярная дегенерация (ВМД) - хроническое заболевание, которое проявляется в дегенерации пигментного эпителия и мембраны Бруха в области желтого пятна, а также капиллярной сетки сосудистой оболочки глаза. С анатомической точки зрения сенсорный отдел сетчатки расположен перед пигментным эпителием. Трофика, опорная функция, преобразование и переработка отходов сенсорного отдела сетчатки зависят от пигментного эпителия. Мембрана Бруха, имеющая пятислойную структуру, размещена между сосудистой оболочкой и пигментным эпителием. Внутренний слой является базальной мембраной пигментного эпителия, внешний слой - базальной мембраной сосудистой оболочки. Таким образом, макулярная дегенерация - дегенеративное заболевание, проявляющееся в комплексе пигментного эпителия сетчатки, мембраны Бруха и капиллярной сетки сосудистой оболочки.
Заболевание, которое развивается преимущественно у пациентов старше 50 лет, является основной причиной слепоты у населения в возрасте 60 и более лет в западных странах; также наблюдается тенденция к увеличению заболеваемости в Южной Корее. Хотя причина возрастной макулярной дегенерации все еще не выяснена, в число факторов риска входит возраст (особенно резкое увеличение заболеваемости наблюдается среди пациентов 75 лет и старше), курение (наиболее значимый экзогенный фактор риска), повышенное артериальное давление, ожирение, генетическая предрасположенность, избыточное воздействие ультрафиолета, низкая концентрация антиоксидантных веществ в крови и т.п.
Выделяют два типа макулярной дегенерации: сухая (неэкссудативная) и влажная (экссудативная) макулярная дегенерация. Сухая макулярная дегенерация (сухая ВМД, неэкссудативная ВМД или не-неоваскулярная ВМД) связана с образованием под сетчаткой желтых отложений (друз). Избыточное образование друз приводит к нарушениям поступления крови к сетчатке, в особенности к области желтого пятна, что приводит к затуманиванию зрения и снижению остроты зрения. Хотя сухая макулярная дегенерация не приводит к внезапной потере зрения, не исключена возможность последующего развития влажной макулярной дегенерации. Под слоем сетчатки расположена сосудистая оболочка, содержащая капиллярную сеть, скрытую внутри волокнистой соединительной ткани, и пигментный эпителий, покрывающий сосудистую оболочку. Влажная макулярная дегенерация (влажная ВМД, экссудативная ВМД или неоваскулярная ВМД) связана с ангиогенезом в области сосудистой оболочки под сетчаткой. Рост таких некрепких молодых сосудов приводит к кровоизлияниям и экссудации с последующей дегенерацией в области желтого пятна сетчатки и, как следствие, к снижению остроты зрения. По причине крайне быстрого развития влажной макулярной дегенерации зрение может ухудшиться через несколько недель; или такая потеря зрения может происходить от 2 месяцев до 3 лет.
Для лечения макулярной дегенерации в настоящее время применяется фотодинамическая терапия (ФДТ) и инъекционное введение антител к ангиогенному фактору роста. Фотодинамическая терапия - это метод, при котором в кровеносные сосуды вводят фотосенсибилизатор визидин с последующим облучением глазного яблока специальным лазерным лучом, воздействующим только на фотосенсибилизатор, во время его поступления к новообразованным сосудам сетчатки, чтобы добиться селективного разрушения новообразованных сосудов. Однако фотодинамическая терапия не позволяет избежать рецидивов, требующих проведения повторных терапевтических сеансов. Кроме того, недостатком таких повторных терапевтических сеансов является то, что они приводят к повреждению сетчатки самой по себе. Терапия с применением антител - это метод лечения, который заключается в прямом введении в сетчатку антител к фактору роста эндотелия сосудов (ФРЭС), которые селективно связываются с ФРЭС, необходимом для формирования и роста новых сосудов, и ингибируют их образование и пролиферацию. В качестве белковых препаратов в методе лечения с введением антител используются Люсентис и Авастин. Люсентис был одобрен FDA в качестве лекарственного средства для лечения влажной макулярной дегенерации. Помимо того, что Авастин одобрен в качестве противоопухолевого препарата, в клинической практике его также используют для лечения влажной ВМД.
Метод лечения с введением антител имеет некоторые недостатки, например, высокую стоимость лечения, местный характер применения (в особенности непосредственное введение в глазное яблоко) и необходимость в повторном введении. Таким образом, с точки зрения комплаентности пациента к лекарству, стоимости лечения и т.д., существует необходимость в разработке (неинъекционного) препарата глазных капель на основе низкомолекулярных синтетических соединений.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ТЕХНИЧЕСКАЯ ЗАДАЧА
В настоящее время учеными проведен ряд исследований в целях разработки эффективных соединений для профилактики и лечения макулярной дегенерации. В результате ученые выяснили, что определенные бензопирановые производные, известные ранее, эффективные при лечении опухолевых заболеваний, ревматоидного артрита и пр., могут быть использованы для приготовления препарата глазных капель на основе низкомолекулярных соединений и успешно применены в целях профилактики и лечения макулярной дегенерации, не требуя при этом непосредственного введения в очаг поражения, как при терапии с применением антител.
Таким образом, задачей настоящего изобретения являлось получение фармацевтической композиции для профилактики или лечения макулярной дегенерации, содержащей определенное бензопирановое производное в качестве активного компонента.
РЕШЕНИЕ ТЕХНИЧЕСКОЙ ЗАДАЧИ
В контексте заявленного изобретения разработана фармацевтическая композиция для профилактики или лечения макулярной дегенерации, которая представлена соединением Формулы 1 или его фармацевтически приемлемой соли в качестве активного вещества:
где
R1 соответствует H, CN, NO2 или NH2,
R2 соответствует
R3 и R4 независимы друг от друга и соответствуют H, Cl, Br, F, C1~C3 алкильному радикалу с линейной или разветвленной цепью, ORb, CF3, OCF3, NO2 или CO2Rb,
Ra соответствует C1~C4 алкильному радикалу с линейной или разветвленной цепью,
Rb соответствует H или C1~C3 алкильному радикалу, и
* соответствует хиральному центру.
В одном из вариантов осуществления заявляемого изобретения предложена фармацевтическая композиция для профилактики или лечения макулярной дегенерации, включающая (2R,3R,4S)-6-амино-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2Н-1-бензопиран или его фармацевтически приемлемую соль в качестве активного компонента.
В качестве другого варианта осуществления заявляемого изобретения предложен препарат глазных капель для профилактики или лечения макулярной дегенерации, включающий (2R,3R,4S)-6-амино-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран или его фармацевтически приемлемую соль в качестве активного компонента. Препарат глазных капель может быть представлен в виде раствора или суспензии.
ДОСТИГАЕМЫЙ РЕЗУЛЬТАТ
В ходе работы над представленным изобретением выяснилось, что соединение Формулы 1 или его фармацевтически приемлемая соль может успешно применяться в целях профилактики и лечения макулярной дегенерации, дегенеративного заболевания сосудистой оболочки сетчатки глаза. В частности обнаружено, что при нанесении (2R,3R,4S)-6-амино-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопирана или его фармацевтически приемлемой соли на роговицу глаза в виде глазных капель он поступает в сетчатку, не приводя к ингибированию естественной регенерации эпителиоцитов роговицы. Таким образом, соединение Формулы 1, включающее (2R,3R,4S)-6-амино-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран или его фармацевтически приемлемую соль, может эффективно применяться в виде глазных капель в целях профилактики или лечения макулярной дегенерации.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На ФИГ.1 представлены результаты (фотографии), полученные при оценке ингибирующего воздействия на ангиогенез роговицы в моделях поражения роговицы у животных.
На ФИГ.2 и 3 представлены результаты (диаграммы), полученные при оценке ингибирующего воздействия на ангиогенез роговицы в моделях поражения роговицы у животных.
На ФИГ.4 представлены результаты, полученные при измерении ингибирующего воздействия на экспрессию рецептора 2 ФРЭС (FLK-1).
На ФИГ.5 представлены результаты (фотографии), полученные при оценке воздействия на естественную регенерацию эпителиоцитов роговицы.
На ФИГ.6 представлены результаты (диаграммы), полученные при оценке воздействия на естественную регенерацию эпителиоцитов роговицы.
На ФИГ.7 представлены результаты (фотографии), полученные при изучении ингибирующего воздействия на ангиогенез в сетчатке серых крыс.
На ФИГ.8 представлены результаты (диаграммы), полученные при изучении ингибирующего воздействия на ангиогенез в сетчатке серых крыс.
На ФИГ.9 представлены результаты (фотографии), полученные при измерении ингибирующего воздействия на ангиогенез в сетчатке карликовых свиней.
На ФИГ.10 представлены результаты (диаграммы), полученные при измерении ингибирующего воздействия на ангиогенез в сетчатке карликовых свиней.
На ФИГ.11 представлены результаты (фотографии), полученные при измерении ингибирующего воздействия глазных капель в виде раствора и в виде суспензии на ангиогенез в сетчатке.
На ФИГ.12 представлены результаты (диаграммы), полученные при измерении ингибирующего воздействия глазных капель в виде раствора и в виде суспензии на ангиогенез в сетчатке.
ПРЕДПОЧТИТЕЛЬНЫЙ СПОСОБ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Разработана лекарственная форма для профилактики или лечения макулярной дегенерации, которая представлена соединением Формулы 1 или его фармацевтически приемлемой соли в качестве активного вещества:
где
R1 соответствует H, CN, NO2 или NH2,
R2 соответствует
R3 и R4 независимы друг от друга и соответствуют H, Cl, Br, F, C1~C3 алкильному радикалу с линейной или разветвленной цепью, ORb, CF3, OCF3, NO2 или CO2Rb,
Ra соответствует C1~C4 алкильному радикалу с линейной или разветвленной цепью,
Rb соответствует H или C1~C3 алкильному радикалу, и
* соответствует хиральному центру.
В соответствии с представленным изобретением, соединение Формулы 1 может быть выбрано из следующей группы:
(2S,3S,4R)-6-нитро-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3R,4S)-6-нитро-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2R,3R,4S)-6-нитро-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2R,3S,4R)-6-нитро-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-нитро-4-[N-(4-трифторметилфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-нитро-4-[N-(4-метоксифенил)-N-(1Н-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-нитро-4-[N-(4-трифторметоксифенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-нитро-4-[N-(4-бромфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-нитро-4-[N-(2,4-диметилфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-нитро-4-[N-(2-изопропилфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-нитро-4-[N-(2,3-диметилфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2R,3R,4S)-6-нитро-4-[N-(2,3-диметилфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2R,3R,4S)-6-нитро-4-[N-(4-бромфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2R,3R,4S)-6-нитро-4-[N-(4-метоксифенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-нитро-4-[N-(4-фторфенил)-N-(1Н-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-нитро-4-[N-(2-метоксифенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2R,3R,4S)-6-нитро-4-[N-(2-изопропилфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2R,3R,4S)-6-нитро-4-[N-(2-метоксифенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2R,3R,4S)-6-нитро-4-[N-(3-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-нитро-4-[N-(3-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2R,3R,4S)-6-нитро-4-[N-(4-трифторметоксифенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-циано-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2R,3R,4S)-6-амино-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-амино-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-амино-4-[N-(4-трифторметилфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2R,3R,4S)-6-амино-4-[N-(4-трифторметоксифенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2R,3R,4S)-6-амино-4-[N-(2,3-диметилфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2R,3R,4S)-6-амино-4-[N-(4-метоксифенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2R,3R,4S)-6-амино-4-[N(4-бромфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-амино-4-[N-(2,3-диметилфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-амино-4-[N-(2-метоксифенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-амино-4-[N-(4-метоксифенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-амино-4-[N-(2,4-диметилфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-амино-4-[N-(2-изопропилфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-амино-4-[N-(4-трифторметоксифенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
(2S,3S,4R)-6-амино-4-[N-(4-бромфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран; и
(2S,3S,4R)-6-амино-4-[N-(4-фторфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран;
Среди соединений Формулы 1 наиболее предпочтительным является (2R,3R,4S)-6-амино-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран или его фармацевтически приемлемая соль. Таким образом, в качестве одного из вариантов осуществления заявляемого изобретения предложена фармацевтическая композиция для профилактики или лечения макулярной дегенерации, включающая (2R,3R,4S)-6-амино-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран или его фармацевтически приемлемую соль в качестве активного компонента.
Соединение Формулы 1 может использоваться как фармацевтически приемлемая соль, включая, например, кислотно-аддитивную соль, полученную на основе фармацевтически приемлемых свободных кислот, соль щелочных металлов (натриевая соль, калиевая соль и пр.) и соль щелочноземельных металлов (кальциевая соль, магниевая соль и пр.). Свободная кислота включает неорганическую кислоту и органическую кислоту. Неорганическая кислота включает хлорводородную кислоту, бромводородную кислоту, азотную кислоту, серную кислоту, перхлорную кислоту, фосфорную кислоту и пр. Органическая кислота включает лимонную кислоту, уксусную кислоту, молочную кислоту, малеиновую кислоту, фумаровую кислоту, глюконовую кислоту, метансульфоновую кислоту, гликолевую кислоту, янтарную кислоту, винную кислоту, галактуроновую кислоту, эмбоновую кислоту, глутаминовую кислоту, аспарагиновую кислоту, щавелевую кислоту, (Д)- или (L)- яблочную кислоту, малеиновую кислоту, метансульфоновую кислоту, этансульфоновую кислоту, 4-толуолсульфоновую кислоту, салициловую кислоту, лимонную кислоту, бензойную кислоту, малоновую кислоту и пр. Примеры фармацевтически приемлемой соли Формулы 1 включают ацетат, аспартат, бензоат, безилат, бикарбонат/карбонат, бисульфат/сульфат, борат, камсилат, цитрат, эдизилат, эзилат, формиат, фумарат, глуцептат, глюконат, глюкуронат, гексафторфосфат, гибензат, гидрохлорид/хлорид, гидробромид/бромид, гидроиодид/иодид, изетионат, лактат, малат, малеат, малонат, мезилат, метилсульфат, нафтилат, 2-напсилат, никотинат, нитрат, оротат, оксалат, пальмитат, фамоат, фосфат/гидрофосфат, фосфат/дигидрофосфат, фосфат, сахарат, стеарат, сукцинат, тартрат, тозилат, трифторацетат, алюминиевую соль, аргининовую соль, бензатиновую соль, кальциевую соль, холиновую соль, диэтиламиновую соль, диоламиновую соль, глициновую соль, лизиновую соль, магниевую соль, меглуминовую соль, оламиновую соль, калиевую соль, натриевую соль, трометаминовую соль, цинковую соль и пр. Среди них предпочтительны соляная кислота и/или трифторацетат.
Фармацевтически приемлемая соль соединения Формулы 1 может быть приготовлена традиционными методами. Например, кислотно-аддитивная соль может быть подготовлена посредством растворения соединения Формулы 1 в смешиваемом с водой органическом растворителе, например, ацетоне, метаноле, этаноле или ацетонитриле, с последующим добавлением избытка органической кислоты или водного раствора неорганической кислоты, чтобы выделить в осадок или кристаллизовать конечную соль. Соответственно, кислотно-аддитивную соль можно выделить с помощью испарения растворителя или избытка кислоты и последующим высушиванием конечного остатка, а также с использованием вакуумной фильтрации осажденной соли.
Кроме того, соединение Формулы 1 или его фармацевтически приемлемая соль включает его изомеры, гидраты и сольваты.
Соединение Формулы 1 или его фармацевтически приемлемая соль проявляет ингибирующее действие в отношении ангиогенеза в роговице и ингибирующее действие в отношении экспрессии маркера ангиогенеза в роговице FLK-1 (ФИГ.1-4). Естественная способность к заживлению (регенерации) эпителиоцитов роговицы не угнетается под действием лекарственного средства, представленного в настоящем изобретении (ФИГ.5, 6). Также соединение Формулы 1 или его фармацевтически приемлемая соль проявляет высокую активность при профилактике или лечении макулярной дегенерации - заболевания, вызванного дегенерацией капиллярной сетки сосудистой оболочки сетчатки (ФИГ.7-10). В частности, в ходе разработки изобретения выяснилось, что соединение Формулы 1 или его фармацевтически приемлемая соль могут быть приготовлены в виде препарата глазных капель для наружного местного применения, которые проявляют высокую активность при профилактике или лечении макулярной дегенерации без необходимости введения в пораженную область (ФИГ.11, 12). Кроме того, в ходе разработки изобретения выяснилось, что при нанесении препарата глазных капель на роговицу активный ингредиент эффективно проникает в сетчатку при поступлении в кровь его незначительной доли (Таблица 1).
Таким образом, представленное изобретение включает в свой объем препарат глазных капель для профилактики или лечения макулярной дегенерации, который содержит соединение Формулы 1 или его фармацевтически приемлемую соль в качестве активного вещества. В качестве варианта осуществления заявляемого изобретения предложен препарат глазных капель для профилактики или лечения макулярной дегенерации, включающий (2R,3R,4S)-6-амино-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран или его фармацевтически приемлемую соль в качестве активного компонента. Препарат глазных капель может быть в виде раствора или суспензии.
Например, препарат глазных капель в виде раствора может включать солюбилизатор, например, полиэтиленгликоль 400, глицерин и пр.; стабилизатор, например, ЭДТА и пр.; буферную систему, например, борную кислоту и пр.; регулятор pH, например, соляную кислоту, гидроксид натрия и пр., в дополнение к соединению Формулы 1 или его фармацевтически приемлемой соли (например, (2R,3R,4S)-6-амино-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран или его соль). Также препарат глазных капель в виде суспензии может включать регулятор вязкости, например, поливинилпирролидон с поперечными связями (например, повидон К-25) и пр.; регулятор изотонии, например, хлорид натрия и пр.; стабилизатор, например, ЭДТА и пр.; буферную систему, например, борную кислоту, боракс и пр.; регулятор pH, например, соляную кислоту, гидроксид натрия и пр., в дополнение к соединению Формулы 1 или его фармацевтически приемлемой соли (например, (2R,3R,4S)-6-амино-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран или его соль). При необходимости фармацевтическую композицию в виде препарата глазных капель можно стерилизовать с помощью традиционных методов либо добавлять вспомогательные вещества, например, консервант, гидратирующую добавку, эмульгатор, солюбилизатор, соль для регулировки осмотического давления и/или буферную систему.
В фармацевтической композиции согласно настоящему изобретению соединение Формулы 1 или его фармацевтически приемлемой соли можно вводить в количестве, составляющем в среднем от приблизительно 0,01 мг/сутки до приблизительно 100 мг/сутки, предпочтительно 0,03-80 мг/сутки (для взрослого пациента массой 70 кг), хотя объем вводимого различается в зависимости от возраста, массы тела, пола, лекарственной формы, состояния здоровья, тяжести заболевания и пр. Применение композиции может проводиться с различной периодичностью, например, в виде разового введения или несколько раз в сутки, на основании указаний врача или фармацевта.
Представленное изобретение включает в свой объем соединение Формулы 1 или его фармацевтически приемлемой соли, необходимое для производства лекарственного вещества для профилактики или лечения макулярной дегенерации.
где R1, R2, R3 и R4 такие же, как описанные выше; и * обозначает хиральный центр.
В использовании представленного изобретения предпочтительным вариантом соединения Формулы 1 является (2R,3R,4S)-6-амино-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран. Лекарственное средство может быть представлено раствором или суспензией. При использовании представленного изобретения соединение Формулы 1 или его фармацевтически приемлемую соль можно вводить в количестве, составляющем в среднем от приблизительно 0,01 мг/сутки до приблизительно 100 мг/сутки, предпочтительно 0,03-80 мг/сутки (для взрослого пациента массой 70 кг), хотя объем вводимого различается в зависимости от возраста, массы тела, пола, лекарственной формы, состояния здоровья, тяжести заболевания и пр. Применение композиции может проводиться с различной периодичностью, например, в виде разового введения или несколько раз в сутки, на основании указаний врача или фармацевта.
Представленное изобретение также включает в свой объем метод профилактики или лечения макулярной дегенерации у пациентов, предусматривающий введение пациенту терапевтически эффективного количества следующего соединения Формулы 1 или его фармацевтически приемлемой соли:
где, R1, R2, R3 и R4 такие же, как описанные выше; и * обозначает хиральный центр.
В методе профилактики или лечения макулярной дегенерации согласно представленному изобретениию предпочтительным вариантом соединения Формулы 1 является (2R,3R,4S)-6-амино-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопиран. Соединение может вводиться в виде препарата глазных капель, представленного раствором или суспензией. В методе профилактики или лечения макулярной дегенерации согласно представленному изобретениию соединение Формулы 1 или его фармацевтически приемлемую соль можно вводить в количестве, составляющем в среднем от приблизительно 0,01 мг/сутки до приблизительно 100 мг/сутки, предпочтительно 0,03-80 мг/сутки (для взрослого пациента массой 70 кг), хотя объем вводимого различается в зависимости от возраста, массы тела, пола, лекарственной формы, состояния здоровья, тяжести заболевания и пр. Введение препарата может проводиться с различной периодичностью, например, в виде разового введения или несколько раз в сутки, на основании указаний врача или фармацевта.
Ниже приведено подробное описание представленного изобретения со ссылкой на следующие примеры приготовления соединений и примеры. Примеры приготовления соединений и примеры приведены только в иллюстративных целях и не призваны ограничить объем представленного изобретения.
Пример приготовления 1: Приготовление (2S,3S,4R)-6-нитро-4-[N-(4-хлорфенил)-N-(1H-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2H-1-бензопирана
Эпоксидное соединение (2S,3S,4S)-6-нитро-2-метил-2-диметоксиметил-3,4-эпокси-3,4-дигидро-2H-1-бензопиран (437 мг, 1,55 ммоль) и (4-хлорфенил)(1H-имидазол-2-илметил)амин (323 мг, 1,55 ммоль) растворяли в ацетонитриле (2 мл). К полученному раствору добавляли безводный хлорид кобальта (CoCl2) (202 мг, 1,55 ммоль). Реакционную смесь перемешивали при 60°C в течение 10 часов, затем добавляли насыщенный водный раствор NaHCO3 (5 мл) с последующей экстракцией с использованием этилацетата (30 мл). Слой органических соединений промывали солевым раствором, сушили с использованием безводного Na2SO4 и затем концентрировали при низком давлении. Полученный остаток очищали, используя метод колоночной хроматографии на силикагеле (гексан : этилацетат = 2:1) для получения указанного в заголовке соединения (304 мг, 40%).
1Н ЯМР (200 МГц, CDCl3) δ 1,49 (с, 3H), 3,60 (с, 3H), 3,63 (с, 3H), 4,32 (м, 1Н), 4,57 (с, 1Н), 5,14(ушир. с, 1Н), 6,75 (ушир. с, 2Н), 6,97 (м, 4Н), 7,27 (м, 2Н), 7,93 (с, 1Н), 8,08 (д, 1Н).
Пример приготовления 2: Приготовление (2S,3R,4S)-6-нитро-4-[N-(4-хлорфенил)-N-(1Н-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2Н-1-бензопирана
Указанное в заголовке соединение (76 мг, 34%) было приготовлено в соответствии с теми же процедурами, как в Примере приготовления 1, но с использованием эпоксидного соединения (2S,3R,4R)-6-нитро-2-метил-2-диметоксиметил-3,4-эпокси-3,4-дигидро-2Н-1-бензопирана (129 мг, 0,46 ммоль) и (4-хлорфенил)(1Н-имидазол-2-илметил)амина (95 мг, 0,46 ммоль).
1Н ЯМР (200 МГц, CDCl3) δ 1,66 (с, 3Н), 3,60 (с, 3Н), 3,69 (с, 3Н), 3,87 (ушир. с, 1Н), 4,13 (м, 1Н), 4,29 (д, 1Н), 4,43 (д, 1Н), 4,64 (с, 1Н), 5,64 (д, 1Н), 6,83 (д, 2Н), 6,95 (м, 4Н), 7,15 (д, 2Н), 7,86 (с, 1Н), 8,06 (м, 2Н), 8,41 (с, 1Н).
Пример приготовления 3: Приготовление (2R,3R,4S)-6-нитро-4-[N-(4-хлорфенил)-N-(1Н-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2Н-1-бензопирана
Указанное в заголовке соединение (2,13 г, 64%) было приготовлено в соответствии с теми же процедурами, как в Примере приготовления 1, но с использованием эпоксидного соединения (2R,3R,4R)-6-нитро-2-метил-2-диметоксиметил-3,4-эпокси-3,4-дигидро-2Н-1-бензопирана (1,038 г, 3,7 ммоль) и (4-хлорфенил)(1Н-имидазол-2-илметил)амина (766 мг, 3,7 ммоль).
1H ЯМР (200 МГц, CDCl3) δ 1,49 (с, 3Н), 3,60 (с, 3Н), 4,32 (м, 1Н), 4,57 (с, 1Н), 5,14 (ушир. с, 1Н), 6,75 (ушир. с, 2Н), 6,97 (м, 4Н), 7,27 (м, 2Н), 7,93 (с, 1Н), 8,08 (д, 1Н).
Пример приготовления 4: Приготовление (2R,3S,4R)-6-нитро-4-[N-(4-хлорфенил)-N-(1Н-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2Н-1-бензопирана
Указанное в заголовке соединение (269 мг, 63%) было приготовлено в соответствии с теми же процедурами, как в Примере приготовления 1, но с использованием эпоксидного соединения (2R,3S,4S)-6-нитро-2-метил-2-диметоксиметил-3,4-эпокси-3,4-дигидро-2Н-1-бензопирана (250 мг, 0,88 ммоль) и (4-хлорфенил)(1Н-имидазол-2-илметил)амина (183 мг, 0,88 ммоль).
1Н ЯМР (200 МГц, CDCl3) δ 1,66 (с, 3Н), 3,60 (с, 3Н), 3,69 (с, 3Н), 3,87 (ушир. с, 1Н), 4,13 (м, 1Н), 4,29 (д, 1Н), 4,43 (д, 1Н), 4,64 (с, 1Н), 5,64 (д, 1Н), 6,83 (д, 2Н), 6,95 (м, 4Н), 7,15 (д, 2Н), 7,86 (с, 1Н), 8,06 (м, 2Н), 8,41 (с, 1Н).
Пример приготовления 5: Приготовление (2S,3S,4R)-6-нитро-4-[N-(4-трифторметилфенил)-N-(1Н-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2Н-1-бензопирана
Указанное в заголовке соединение (146 г, 22%) было приготовлено в соответствии с теми же процедурами, как в Примере приготовления 1, но с использованием эпоксидного соединения (2S,3S,4S)-6-нитро-2-метил-2-диметоксиметил-3,4-эпокси-3,4-дигидро-2Н-1-бензопирана (356 мг, 1,26 ммоль) и (4-трифторметилфенил)(1Н-имидазол-2-илметил)амина(305 мг, 1,26 ммоль).
1Н ЯМР (200 МГц, CDCl3) δ 1,51 (с, 3Н), 3,60 (с, 3Н), 3,61 (с, 3Н), 4,32 (м, 3Н), 4,57 (с, 1Н), 5,14 (ушир. с, 1Н), 6,85 (м, 2Н), 6,95 (м, 4Н), 7,38 (д, 2Н), 7,91 (с, 1Н), 8,05 (дд, 2Н), 8,42 (м, 1Н).
Пример приготовления 6: Приготовление (2S,3S,4R)-6-нитро-4-[N-(4-метоксифенил)-N-(1Н-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2Н-1-бензопирана
Указанное в заголовке соединение (280 г, 28%) было приготовлено в соответствии с теми же процедурами, как в Примере приготовления 1, но с использованием эпоксидного соединения (2S,3S,4S)-6-нитро-2-метил-2-диметоксиметил-3,4-эпокси-3,4-дигидро-2Н-1-бензопирана (591 мг, 2,10 ммоль) и (4-метоксифенил)(1Н-имидазол-2-илметил)амина (427 мг, 2,10 ммоль).
1H ЯМР (200 МГц, CDCl3) δ 1,47 (с, 3Н), 3,59 (д, 6Н), 3,68 (с, 3Н), 4,30 (м, 2Н), 4,54 (м, 2Н), 5,02 (д, 1Н), 6,67-6,78 (м, 4Н), 6,89-7,26 (м, 3Н), 8,04 (м, 2Н).
Пример приготовления 7: Приготовление (2S,3S,4R)-6-нитро-4-[N-(4-трифторметоксифенил)-N-(1Н-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2Н-1-бензопирана
Указанное в заголовке соединение (181 мг, 47%) было приготовлено в соответствии с теми же процедурами, как в Примере приготовления 1, но с использованием эпоксидного соединения (2S,3S,4S)-6-нитро-2-метил-2-диметоксиметил-3,4-эпокси-3,4-дигидро-2Н-1-бензопирана (200 мг, 0,71 ммоль) и (4-трифторметоксифенил)(1Н-имидазол-2-илметил) амина (183 мг, 0,71 ммоль).
1H ЯМР (200 МГц, CDCl3) δ 1,50 (с, 3Н), 3,60 (д, 6Н), 4,2-4,50 (м, 2Н), 4,58-5,65 (м, 2Н), 5,18 (с, 1Н), 6,91-6,95 (м, 7Н), 8,00 (с, 1Н), 8,05 (дд, 1Н).
Пример приготовления 8: Приготовление (2S,3S,4R)-6-нитро-4-[N-(4-бромфенил)-N-(1Н-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2Н-1-бензопирана
Указанное в заголовке соединение (310 г, 41%) было приготовлено в соответствии с теми же процедурами, как в Примере приготовления 1, но с использованием эпоксидного соединения (2S,3S,4S)-6-нитро-2-метил-2-диметоксиметил-3,4-эпокси-3,4-дигидро-2Н-1-бензопирана (400 мг, 1,42 ммоль) и (4-бромфенил)(1Н-имидазол-2-илметил)амина (359 мг, 1,42 ммоль).
1Н ЯМР (200 МГц, CDCl3) δ 1,48 (с, 3Н), 3,61 (д, 6Н), 4,10-4,19 (м, 2Н), 4,20-4,40 (м, 2Н), 5,13 (с, 1Н), 6,70-7,01 (м, 6Н), 7,21 (с, 1Н), 7,94 (с, 1Н), 8,06 (дд, 1Н).
Пример приготовления 9: Приготовление (2S,3S,4R)-6-нитро-4-[N-(2,4-диметилфенил)-N-(1Н-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2Н-1-бензопирана
Указанное в заголовке соединение (231 мг, 33%) было приготовлено в соответствии с теми же процедурами, как в Примере приготовления 1, но с использованием эпоксидного соединения (2S,3S,4S)-6-нитро-2-метил-2-диметоксиметил-3,4-эпокси-3,4-дигидро-2Н-1-бензопирана (400 мг, 1,42 ммоль) и (2,4-диметилфенил)(1Н-имидазол-2-илметил)амина (287 мг, 1,42 ммоль).
1H ЯМР (200 МГц, CDCl3) δ 1,39 (с, 3Н), 2,19 (с, 3Н), 2,47 (с, 3Н), 3,59 (д, 6Н), 4,15-4,82 (м, 5Н), 6,80-6,89 (м, 5Н), 7,58 (д, 1Н), 7,94-7,99 (дд, 1Н), 8,62 (м, 1Н).
Пример приготовления 10: Приготовление (2S,3S,4R)-6-нитро-4-[N-(2-изопропилфенил)-N-(1Н-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2Н-1-бензопирана
Указанное в заголовке соединение (140 мг, 20%) было приготовлено в соответствии с теми же процедурами, как в Примере приготовления 1, но с использованием эпоксидного соединения (2S,3S,4S)-6-нитро-2-метил-2-диметоксиметил-3,4-эпокси-3,4-дигидро-2Н-1-бензопирана (400 мг, 1,42 ммоль) и (2-изопропилфенил)(1Н-имидазол-2-илметил)амина (306 мг, 1,42 ммоль).
1Н ЯМР (200 МГц, CDCl3) δ 1,22-1,29 (м, 10Н), 3,60 (д, 6Н), 4,07-4,63 (м, 5Н), 6,79-7,35 (м, 6Н), 7,78 (м, 1Н), 7,99 (дд, 1Н), 8,61 (м, 1Н)
Пример приготовления 11: Приготовление (2S,3S,4R)-6-нитро-4-[N-(2,3-диметилфенил)-N-(1Н-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2Н-1-бензопирана
Указанное в заголовке соединение (253 мг, 37%) было приготовлено в соответствии с теми же процедурами, как в Примере приготовления 1, но с использованием эпоксидного соединения (2S,3S,4S)-6-нитро-2-метил-2-диметоксиметил-3,4-эпокси-3,4-дигидро-2Н-1-бензопирана (400 мг, 1,42 ммоль) и (2,3-диметилфенил)(1Н-имидазол-2-илметил)амина (287 мг, 1,42 ммоль).
1Н ЯМР (200 МГц, CDCl3) δ 1,39 (с, 3Н), 2,17 (с, 3Н), 2,41 (с, 3Н), 3,61 (д, 6Н), 4,26-4,74 (м, 5Н), 6,76-6,95 (м, 4Н), 6,98 (м, 1Н), 7,58 (д, 1Н), 7,95 (дд, 1Н), 8,63 (д, 1Н).
Пример приготовления 12: Приготовление (2R,3R,4S)-6-нитро-4-[N-(2,3-диметилфенил)-N-(1Н-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2Н-1-бензопирана
Указанное в заголовке соединение (416 мг, 49%) было приготовлено в соответствии с теми же процедурами, как в Примере приготовления 1, но с использованием эпоксидного соединения (2R,3R,4R)-6-нитро-2-метил-2-диметоксиметил-3,4-эпокси-3,4-дигидро-2Н-1-бензопирана (500 мг, 1,77 ммоль) и (2,3-диметилфенил)(1Н-имидазол-2-илметил)амина (358 мг, 1,77 ммоль).
1H ЯМР (200 МГц, CDCl3) δ 1,39 (с, 3Н), 2,17 (с, 3Н), 2,41 (с, 3Н), 3,61 (д, 6Н), 4,26-4,74 (м, 5Н), 6,76-6,95 (м, 4Н), 6,98 (м, 1Н), 7,58 (д, 1Н), 7,95 (дд, 1Н), 8,63 (д, 1Н).
Пример приготовления 13: Приготовление (2R,3R,4S)-6-нитро-4-[N-(4-бромфенил)-N-(1Н-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2Н-1-бензопирана
Указанное в заголовке соединение (570 мг, 60%) было приготовлено в соответствии с теми же процедурами, как в Примере приготовления 1, но с использованием эпоксидного соединения (2R,3R,4R)-6-нитро-2-метил-2-диметоксиметил-3,4-эпокси-3,4-дигидро-2Н-1-бензопирана (500 мг, 1,78 ммоль) и (4-бромфенил)(1Н-имидазол-2-илметил)амина (450 мг, 1,78 ммоль).
1H ЯМР (200 МГц, CDCl3) δ 1,48 (с, 3Н), 3,61 (д, 6Н), 4,10-4,19 (м, 2Н), 4,20-4,40 (м, 2Н), 5,13 (с, 1Н), 6,70-7,01 (м, 6Н), 7,21 (с, 1Н), 7,94 (с, 1Н), 8,06 (дд, 1Н).
Пример приготовления 14: Приготовление (2R,3R,4S)-6-нитро-4-[N-(4-метоксифенил)-N-(1Н-имидазол-2-илметил)амино]-3-гидрокси-2-метил-2-диметоксиметил-3,4-дигидро-2Н-1-бензопирана
Указанное в заголовке соединение (446 мг, 86%) было приготовлено в соответствии с теми же процедурами, как в Примере приготовления 1, но с использованием эпоксидного соединения (2R,3R,4R)-6-нитро-2-метил-2-диметоксиметил-3,4-эпокси-3,4-дигидро-2Н-1-бензопирана (300 мг, 1,06 ммоль) и (4-метоксифенил)(1Н-имидазол-2-илметил)амина (216 мг, 1,06 ммоль).
1Н ЯМР (200 МГц, CDCl3) δ 1,47 (с, 3Н), 3,59 (д, 6Н), 3,68 (с, 3Н), 4,30 (м, 2Н), 4,54 (м, 2Н), 5,02 (д, 1Н), 6,67-6,78 (м, 4Н), 6,89-7,26 (м, 3Н), 8,04 (м, 2Н).
Пример приготовления 15: П